Olaparib retrasa el avance de cáncer de ovario después del tratamiento inicial
, por Equipo del NCI
El fármaco olaparib (Lynparza) pronto será una opción de tratamiento más temprano para algunas mujeres con cáncer de ovario, de acuerdo con los nuevos hallazgos de un estudio clínico grande. Olaparib ya está aprobado como terapia de mantenimiento y tratamiento para mujeres con cáncer de ovario avanzado que ya han recibido varias líneas de quimioterapia. Al presente, los resultados del estudio SOLO-1 muestran que el fármaco puede retrasar el regreso del cáncer en forma considerable después de la primera línea de quimioterapia.
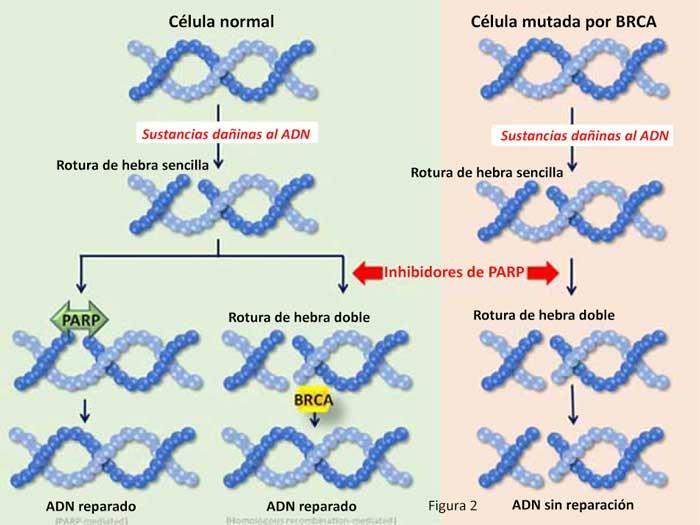
Olaparib es un inhibidor de PARP, un fármaco que bloquea las proteínas (denominadas PARP) que ayudan a reparar el ADN dañado. Debido a que las mutaciones en BRCA pueden también dificultar la reparación del ADN, la inhibición ulterior de este proceso con olaparib puede causar la muerte de las células cancerosas que portan una mutación en BRCA.
El estudio SOLO-1 es el primer estudio en fase 3 que evalúa un inhibidor de PARP como terapia de mantenimiento en mujeres con diagnóstico reciente de cáncer de ovario avanzado que contiene una mutación en los genes BRCA1 o BRCA2, o ambos.
El tratamiento con olaparib demostró beneficios duraderos en algunas mujeres y fue bien tolerado, notificó la investigadora principal del estudio, doctora Kathleen Moore, del Centro Oncológico Stephenson de la Universidad de Oklahoma.
Los investigadores estimaron que las mujeres que recibieron olaparib vivirían una mediana de 3 años más sin avance del cáncer, en comparación con las mujeres que recibieron un placebo. Es necesario realizar un seguimiento más prolongado para verificar esta estimación y determinar si olaparib ayuda a que las pacientes vivan más.
Los hallazgos del estudio se presentaron el 21 de octubre en la Conferencia de la Sociedad Europea de Oncología Médica 2018 en Munich, Alemania y, al mismo tiempo, se publicaron en el New England Journal of Medicine.
"Estos datos respaldan la incorporación de olaparib como parte del tratamiento convencional para mujeres con diagnóstico reciente de cáncer de ovario que contiene una mutación en BRCA", dijo la doctora Moore.
Los hallazgos del estudio SOLO-1 generarán cambios en la práctica clínica, dijo la doctora Isabelle Ray-Coquard, de la Universidad Claude Bernard de Lyon, Francia, en un comunicado de prensa.
Terapia de mantenimiento para el cáncer de ovario
La terapia de primera línea con una combinación de cirugía y quimioterapia con platino es el tratamiento convencional para mujeres con diagnóstico reciente de cáncer avanzado de ovario. No obstante, en la mayoría de las mujeres, el cáncer regresa dentro de los 3 años siguientes a este tratamiento inicial.
Bevacizumab (Avastin) es la única terapia de mantenimiento actualmente aprobada por la Administración de Alimentos y Medicamentos (FDA) de los EE. UU. para mujeres con diagnóstico reciente de cáncer avanzado de ovario. En el estudio patrocinado por el NCI que llevó a la aprobación, bevacizumab más quimioterapia seguido únicamente de bevacizumab, prolongó alrededor de 6 meses la mediana de supervivencia sin avance (esto es, el tiempo que la mitad de los participantes vivieron sin avance del cáncer), comparado con quimioterapia sola.
En el estudio SOLO-1 se inscribieron cerca de 400 mujeres con cáncer de ovario seroso o endometrioide, peritoneal primario y/o de las trompas de Falopio, que habían respondido al menos en forma parcial al tratamiento de primera línea de quimioterapia con platino. Las mujeres fueron asignadas al azar para recibir olaparib o un placebo durante 2 años o hasta que el cáncer avanzara. La mediana de duración del seguimiento fue de 41 meses y el criterio de valoració primario criterio de valoración primario fue la supervivencia sin avance.
El estudio fue financiado por AstraZeneca y Merck, las compañías farmacéuticas que formularon en conjunto a olaparib.
Tres años después de la asignación al azar, la supervivencia sin avance fue 60 % en el grupo que recibió olaparib y 27 % en el grupo que recibió el placebo. El tratamiento con olaparib redujo en 70 % el riesgo de muerte o de avance de la enfermedad, según lo determinaron los investigadores.
La mediana de la supervivencia sin avance fue de alrededor de 14 meses en el grupo que recibió el placebo. Es necesario realizar un seguimiento más prolongado para determinar la mediana de supervivencia sin avance en el grupo que recibió olaparib, pero el análisis actual permite suponer que es probable que sea de más de 4 años.
Estudios previos indicaron que un subgrupo pequeño de pacientes cuyo cáncer empeoró con el tratamiento con olaparib, no respondió al tratamiento subsiguiente de quimioterapia con platino. Esto plantea interrogantes sobre cómo el uso de inhibidores de PARP para la terapia de mantenimiento inicial quizá altere la eficacia de los tratamientos posteriores, explicó la doctora Elise Kohn, directora de Terapéutica de Cánceres Ginecológicos de la División de Tratamiento y Diagnóstico Oncológico del NCI, quien no participó en el estudio.
Pero 3 años después de la asignación al azar, hubo menos mujeres en el grupo que recibió olaparib que presentaron avance del cáncer después de la siguiente ronda de tratamiento, en comparación con las del grupo que recibió el placebo (25 % frente a 40 %). La doctora Moore explicó que esto permite suponer que el tratamiento con olaparib no disminuyó el posible beneficio de otras terapias.
La FDA ha otorgado revisión prioritaria a la nueva aplicación del fármaco olaparib como terapia de mantenimiento para mujeres con diagnóstico reciente de cáncer de ovario con mutación en BRCA.
Inquietudes sobre la seguridad de olaparib
El perfil de seguridad de olaparib fue similar al observado en otros estudios clínicos.
La mayoría de los efectos secundarios de olaparib fueron de bajo grado, los más comunes fueron anemia y neutropenia. Solo 12 % de las participantes en el estudio dejaron el tratamiento con olaparib debido a los efectos secundarios. Dos años después del inicio del estudio, el cambio en la calidad de vida no fue considerablemente diferente entre los grupos de tratamiento.
No obstante, después de dejar de recibir olaparib, tres mujeres (1 %) presentaron leucemia mieloide aguda (LMA), un tipo de cáncer de la sangre. Se ha observado una frecuencia similar de síndrome mielodisplásico (SMD) y/o LMA en otros estudios clínicos de olaparib.
En su aprobación previa de olaparib, la FDA recomendó que los doctores controlen la concentración de células sanguíneas en pacientes que reciben tratamiento con olaparib para detectar la formación de SMD o LMA (en particular, en las pacientes que padecen cáncer de ovario y mutaciones heredadas en BRCA).
En búsqueda del tratamiento óptimo
Si bien estos hallazgos muestran que la terapia de mantenimiento con olaparib ofrece un claro beneficio para mujeres con diagnóstico reciente de cáncer de ovario, aún existen dudas.
Por ejemplo, la doctora Kohn dijo que es una cuestión de "aplicabilidad [de los resultados del estudio] a la población general con cáncer de ovario" porque algunas mujeres no responden al tratamiento inicial tan bien como lo hizo el grupo del estudio, en el cual la mayoría de dichas participantes tuvo una respuesta completa.
Además, la doctora agregó que "dado que olaparib y otros inhibidores de PARP ya tienen varias indicaciones aprobadas, la interrogante clave es: ¿cuándo es mejor usar estos fármacos?" Tanto olaparib como otros dos inhibidores de PARP (niraparib (Zejula) y rucaparib (Rubraca)) están aprobados como terapia de mantenimiento para mujeres con cáncer recurrente de ovario, independientemente de la presencia o no de mutaciones en BRCA.
De la misma manera, la doctora Ray-Coquard cuestionó si se debe combinar olaparib con bevacizumab para la terapia de mantenimiento del cáncer de ovario de diagnóstico reciente.
Es fundamental que en el futuro logremos comprender mejor los efectos de olaparib en la supervivencia general y resistencia a otras terapias de las pacientes, señaló la doctora Kohn.
Evaluación de la sensibilidad a los inhibidores de PARP
Otra cuestión que todavía se desconoce es si la terapia de mantenimiento con olaparib puede beneficiar a mujeres con diagnóstico reciente de cáncer de ovario sin la mutación en BRCA. Los resultados de otros estudios de olaparib y de otros inhibidores de PARP ofrecen algunas explicaciones.
Además de BRCA, "hay otros genes que pueden contener mutaciones en el cáncer de ovario que hacen que los tumores sean susceptibles a olaparib", explicó la doctora Kohn. De manera similar a las mutaciones en BRCA, estas otras mutaciones genéticas invalidan el proceso de reparación del ADN. Las pruebas genéticas que analizan si los tumores tienen deficiencias en la reparación del ADN pueden identificar a las personas que más probablemente respondan a los inhibidores de PARP, agregó la doctora.
Un estudio clínico de 2016 mostró que la terapia de mantenimiento con el inhibidor de PARP niraparib proveyó algunos beneficios a las mujeres con cáncer recurrente de ovario independientemente de si tenían o no mutaciones en BRCA. Sin embargo, las mujeres que tenían mutaciones en BRCA u otras deficiencias en la reparación del ADN tuvieron una supervivencia sin avance más prolongada que quienes no tenían dichas mutaciones.
En un estudio en curso, los investigadores están estudiando a niraparib como terapia de mantenimiento para mujeres con cáncer avanzado de ovario después de la quimioterapia inicial. Dado que para participar no se requería tener las mutaciones en BRCA u otras deficiencias en la reparación del ADN, este estudio puede ayudar a contestar si la terapia de mantenimiento con un inhibidor de PARP podría beneficiar a mujeres con diagnóstico reciente de cáncer de ovario sin la mutación en BRCA, dijo la doctora Kohn.