Tratamiento de los tumores de células germinativas del ovario (PDQ®)–Versión para profesionales de salud
Información general sobre los tumores de células germinativas del ovario
Incidencia y mortalidad
Los tumores de células germinativas del ovario son poco comunes pero de gran malignidad, y se observan con mayor frecuencia en mujeres jóvenes y adolescentes. Estos tumores suelen ser unilaterales y por lo general se curan si se detectan y se tratan temprano. El uso de la quimioterapia combinada después de cirugía inicial mejora bastante el pronóstico para muchas mujeres con estos tumores.[1-3]
Disgerminomas
En una serie se notificó una tasa de supervivencia a 10 años del 88,6 % luego de una cirugía conservadora para pacientes con disgerminoma confinado al ovario menor de 10 cm, con una cápsula intacta y lisa separada de otros órganos, y sin ascitis.[4] Algunas pacientes presentaron uno o más embarazos exitosos después de una salpingooforectomía unilateral.[4] Incluso aquellas pacientes con una resección incompleta del disgerminoma se pueden considerar sin enfermedad, luego de recibir quimioterapia con bleomicina, etopósido y cisplatino (BEP) o una combinación de cisplatino, vinblastina y bleomicina.[5]
Otros tumores de células germinativas
En un informe sobre 35 casos de tumores de células germinativas, la mitad con enfermedad en estadio avanzado, recidivante o progresivo, se notificó una remisión sostenida del 97 % después de 10 a 54 meses de comenzar una combinación de BEP.[1] En 2 ensayos del Gynecologic Oncology Group se informó que 89 de 93 pacientes con enfermedad en estadios I, II o III que se sometieron a resección completa del tumor, no presentaron enfermedad luego de 3 ciclos de BEP.[1,3]
Los tumores de seno endodérmico del ovario son, en especial, muy malignos. Un análisis de la literatura en 1979, previo a la diseminación del uso de la quimioterapia combinada, encontró que solo el 27 % de 96 pacientes con tumor de seno endodérmico en estadio I sobrevivieron 2 años después del diagnóstico. Más del 50 % de las pacientes murieron en un plazo de 1 año a partir del diagnóstico.
Las pacientes con teratomas maduros, por lo general sobreviven a largo plazo, pero la supervivencia en pacientes con teratomas inmaduros después de una cirugía sola, se relaciona con el grado del tumor, sobre todo sus elementos neurales. En una serie de 58 pacientes con teratoma inmaduro que se trataron antes de la era quimioterapéutica moderna, se informó que la recidiva fue del 18 % en las pacientes con enfermedad en grado 1, del 37 % en las pacientes con enfermedad de grado 2 y del 70 % en las pacientes con enfermedad de grado 3.[6] Otros informaron hallazgos similares.[7]
En algunos estudios se encontró que el tamaño y el tipo histológico eran los factores principales que determinaban el pronóstico en pacientes con tumores malignos mixtos de células germinativas del ovario.[6,8] El pronóstico fue precario en las pacientes con tumores grandes cuando más de un tercio del tumor estaba compuesto de elementos del seno endodérmico, coriocarcinoma o teratoma inmaduro de grado 3. Cuando el tumor tenía menos de 10 cm de diámetro, el pronóstico era favorable, independientemente de su composición.[8,9]
Bibliografía
- Gershenson DM: Update on malignant ovarian germ cell tumors. Cancer 71 (4 Suppl): 1581-90, 1993. [PUBMED Abstract]
- Segelov E, Campbell J, Ng M, et al.: Cisplatin-based chemotherapy for ovarian germ cell malignancies: the Australian experience. J Clin Oncol 12 (2): 378-84, 1994. [PUBMED Abstract]
- Williams S, Blessing JA, Liao SY, et al.: Adjuvant therapy of ovarian germ cell tumors with cisplatin, etoposide, and bleomycin: a trial of the Gynecologic Oncology Group. J Clin Oncol 12 (4): 701-6, 1994. [PUBMED Abstract]
- Thomas GM, Dembo AJ, Hacker NF, et al.: Current therapy for dysgerminoma of the ovary. Obstet Gynecol 70 (2): 268-75, 1987. [PUBMED Abstract]
- Williams SD, Blessing JA, Hatch KD, et al.: Chemotherapy of advanced dysgerminoma: trials of the Gynecologic Oncology Group. J Clin Oncol 9 (11): 1950-5, 1991. [PUBMED Abstract]
- Norris HJ, Zirkin HJ, Benson WL: Immature (malignant) teratoma of the ovary: a clinical and pathologic study of 58 cases. Cancer 37 (5): 2359-72, 1976. [PUBMED Abstract]
- Gallion H, van Nagell JR, Powell DF, et al.: Therapy of endodermal sinus tumor of the ovary. Am J Obstet Gynecol 135 (4): 447-51, 1979. [PUBMED Abstract]
- Kurman RJ, Norris HJ: Malignant germ cell tumors of the ovary. Hum Pathol 8 (5): 551-64, 1977. [PUBMED Abstract]
- Murugaesu N, Schmid P, Dancey G, et al.: Malignant ovarian germ cell tumors: identification of novel prognostic markers and long-term outcome after multimodality treatment. J Clin Oncol 24 (30): 4862-6, 2006. [PUBMED Abstract]
Clasificación celular de los tumores de células germinativas del ovario
Se han descrito los siguientes subtipos histológicos de los tumores de células germinativas del ovario.[1,2]
- Disgerminoma.
- Otros tumores de células germinativas:
- Tumor de seno endodérmico (subtipos raros son el hepatoide y el intestinal).[1]
- Carcinoma embrionario.
- Poliembrioma.
- Coriocarcinoma.
- Teratoma:
- Inmaduro.
- Maduro:
- Sólido.
- Quístico:
- Quiste dermoide (teratoma quístico maduro).
- Quiste dermoide con transformación maligna.
- Monodérmico y muy especializado:
- Estroma ovárico.
- Carcinoide.
- Estroma ovárico y carcinoide.
- Otros (por ejemplo, neuroectodérmicos y ependimomas malignos).
- Formas mixtas.
Bibliografía
- Gershenson DM: Update on malignant ovarian germ cell tumors. Cancer 71 (4 Suppl): 1581-90, 1993. [PUBMED Abstract]
- Serov SF, Scully RE, Robin IH: International Histologic Classification of Tumours: No. 9. Histological Typing of Ovarian Tumours. World Health Organization, 1973.
Información sobre los estadios de los tumores de células germinativas del ovario
En la ausencia de enfermedad metastásica obvia, la clasificación exacta de los tumores de células germinativas del ovario requiere que se efectúe una laparotomía con un examen cuidadoso de los siguientes órganos:
- Diafragma completo.
- Ambos espacios paracólicos.
- Ganglios linfáticos pélvicos del mismo lado del tumor de ovario.
- Ganglios linfáticos paraórticos.
- Epiplón.
Se deberá examinar el ovario contralateral con cuidado y, si fuera necesario, se obtiene una biopsia. El líquido ascítico se deberá examinar citológicamente. Si no hay ascitis, es importante obtener lavados peritoneales antes de manipular el tumor. En pacientes con disgerminoma, se indica una linfangiografía o tomografía computarizada si no se examinaron con cuidado los ganglios linfáticos pélvicos y paraórticos en el momento de la cirugía.
Es conveniente obtener las concentraciones séricas de la α-fetoproteína y la gonadotropina coriónica humana tan pronto se establezca el diagnóstico, aunque no son necesarias para una clasificación formal, ya que la persistencia de estos marcadores en el suero después de la cirugía indica que quedó tumor no resecado.
Estadificación FIGO
La Federación Internacional de Ginecología y Obstetricia (FIGO) y el American Joint Committee on Cancer (AJCC) han creado estadificaciones para definir los tumores limítrofes de ovario; el sistema FIGO se usa con mayor frecuencia.[1,2]
| Estadio | Definición | Ilustración |
|---|---|---|
| FIGO = Federación Internacional de Ginecología y Obstetricia. | ||
| aAdaptación de FIGO Committee for Gynecologic Oncology.[1] | ||
| I | Tumor confinado en los ovarios o las trompas de Falopio. |
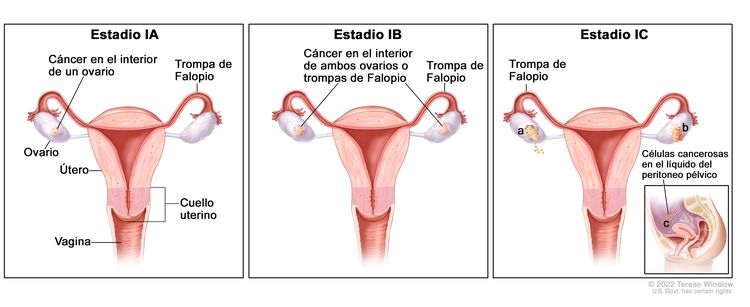 |
| IA | Tumor limitado a un ovario (cápsula intacta) o una trompa de Falopio; no hay tumor en la superficie del ovario o la trompa de Falopio; no hay células malignas en el líquido de la ascitis o los lavados peritoneales. | |
| IB | Tumor limitado a ambos ovarios (cápsulas intactas) o a las trompas de Falopio; no hay tumor en la superficie del ovario o las trompas de Falopio; no hay células malignas en el líquido de la ascitis o los lavados peritoneales. | |
| IC | Tumor limitado a uno o ambos ovarios, o a las trompas de Falopio y se presenta cualquiera de las siguientes situaciones: | |
| IC1: Derrame quirúrgico. | ||
| IC2: Ruptura de la cápsula antes de la cirugía, o tumor en la superficie del ovario o la trompa de Falopio. | ||
| IC3: Células malignas en el líquido de la ascitis o los lavados peritoneales. | ||
| Estadio | Definición | Ilustración |
|---|---|---|
| FIGO = Federación Internacional de Ginecología y Obstetricia. | ||
| aAdaptación de FIGO Committee for Gynecologic Oncology.[1] | ||
| II | El tumor compromete uno o ambos ovarios o trompas de Falopio con extensión pélvica (debajo del borde de la pelvis) o cáncer primario de peritoneo. |
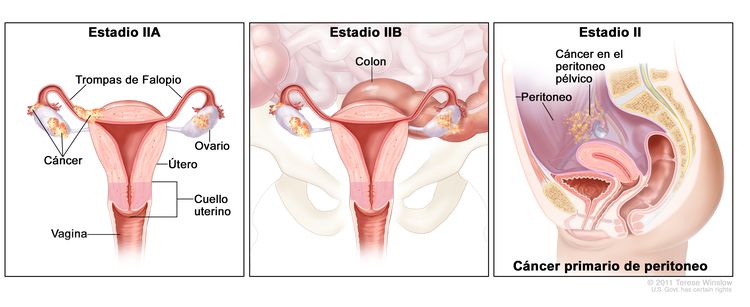 |
| IIA | Diseminación o implantes en el útero, las trompas de Falopio o los ovarios. | |
| IIB | Diseminación a otros tejidos pélvicos intraperitoneales. | |
| Estadio | Definición | Ilustración |
|---|---|---|
| FIGO = Federación Internacional de Ginecología y Obstetricia. | ||
| aAdaptación de FIGO Committee for Gynecologic Oncology.[1] | ||
| III | El tumor compromete uno o ambos ovarios o trompas de Falopio, o hay un cáncer primario de peritoneo, con diseminación al peritoneo fuera de la pelvis confirmada por pruebas citológicas o histológicas, o metástasis en los ganglios linfáticos retroperitoneales. | |
| IIIA1 | Solo hay compromiso tumoral de ganglios linfáticos retroperitoneales (confirmado por pruebas citológicas o histológicas): |
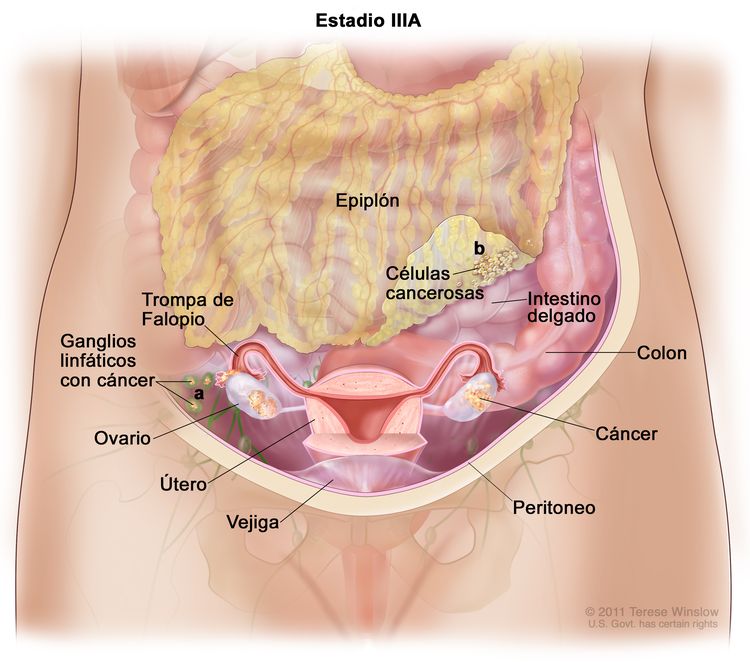 |
| IIIA1(i): Metástasis ≤ 10 mm en su mayor dimensión. | ||
| IIIA1(ii): Metástasis >10 mm en su mayor dimensión. | ||
| IIIA2 | Compromiso peritoneal extrapélvico microscópico (encima del borde de la pelvis), con compromiso de los ganglios linfáticos retroperitoneales o sin este. | |
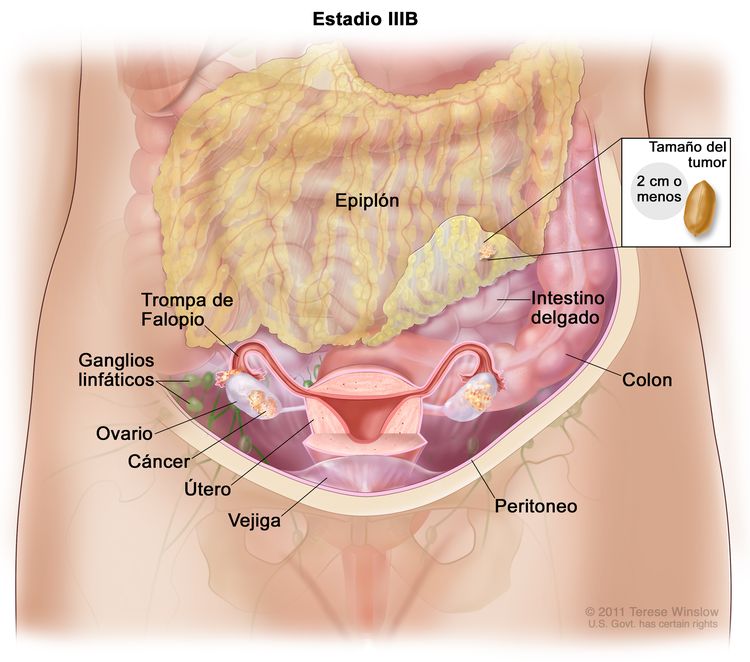
| IIIB | Metástasis peritoneales macroscópicas fuera de la pelvis de ≤2 cm en su mayor dimensión, con metástasis en los ganglios linfáticos retroperitoneales o sin estas. |
 |
| IIIC | Metástasis peritoneales macroscópicas fuera de la pelvis de >2 cm en su mayor dimensión, con metástasis en los ganglios linfáticos retroperitoneales o sin estas (incluye extensión del tumor a la cápsula del hígado y el bazo sin compromiso parenquimatoso en ninguno de los dos órganos). |
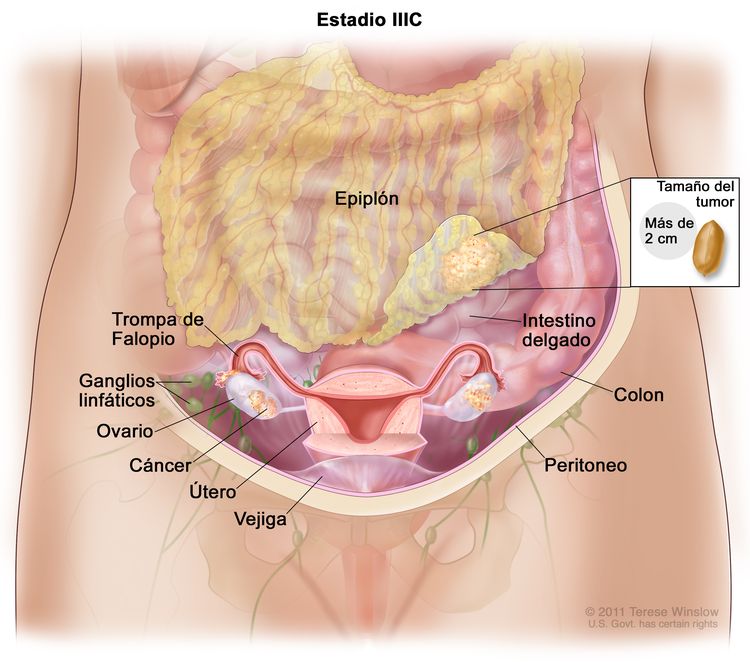 |
| Estadio | Definición | Ilustración |
|---|---|---|
| FIGO = Federación Internacional de Ginecología y Obstetricia. | ||
| aAdaptación de FIGO Committee for Gynecologic Oncology.[1] | ||
| IV | Metástasis a distancia con exclusión de metástasis peritoneales. |
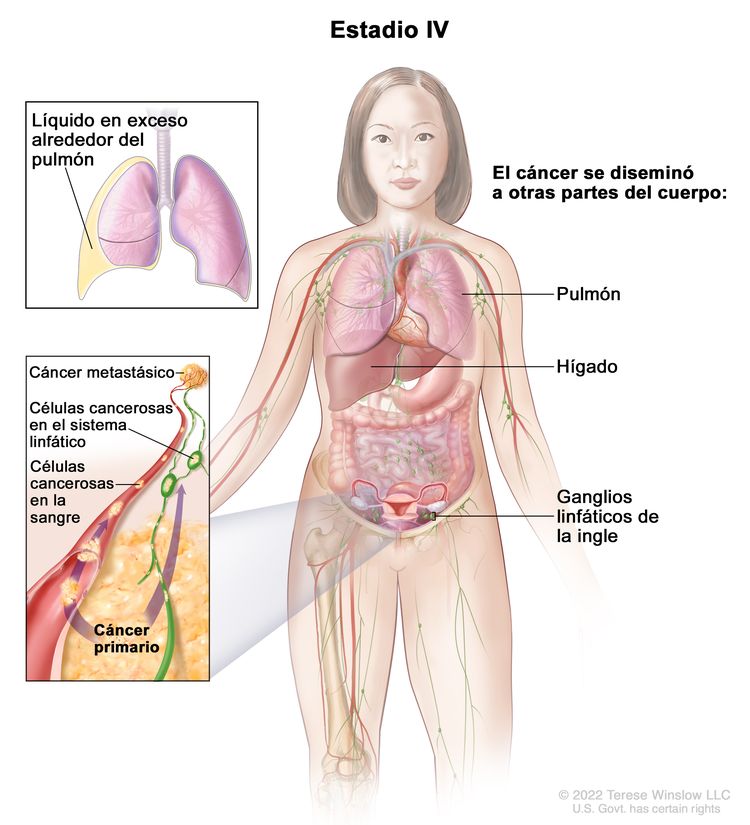 |
| IVA | Derrame pleural con prueba citológica positiva para compromiso tumoral. | |
| IVB | Metástasis parenquimatosas y metástasis en órganos extraabdominales (incluso en los ganglios linfáticos inguinales y los ganglios linfáticos fuera de la cavidad abdominal). | |
Bibliografía
- Berek JS, Renz M, Kehoe S, et al.: Cancer of the ovary, fallopian tube, and peritoneum: 2021 update. Int J Gynaecol Obstet 155 (Suppl 1): 61-85, 2021. [PUBMED Abstract]
- Ovary, fallopian tube, and primary peritoneal carcinoma. In: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. Springer; 2017, pp 681-90.
Aspectos generales de las opciones de tratamiento de los tumores de células germinativas del ovario
Las opciones de tratamiento para las pacientes con tumores de células germinativas del ovario son las siguientes:
- Cirugía.
- Quimioterapia.
- Radioterapia.
- Dosis altas de quimioterapia con trasplante de médula ósea (en evaluación clínica).
Las pacientes se pueden tratar con salpingooforectomía unilateral, o histerectomía abdominal total y salpingooforectomía bilateral.
Todas las pacientes necesitan quimioterapia postoperatoria (excepto aquellas con teratoma inmaduro en estadio I y grado I y con disgerminoma en estadio IA). Con la quimioterapia combinada a base de derivados del platino, el pronóstico para pacientes con tumores de seno endodérmico, teratomas inmaduros, carcinomas embrionarios, coriocarcinomas y tumores mixtos que contienen uno o más de estos elementos ha mejorado de forma significativa.[1] A medida que se desarrollan fármacos nuevos y más eficaces, muchas de estas pacientes son aptas para nuevos ensayos clínicos.
Bibliografía
- Gershenson DM, Morris M, Cangir A, et al.: Treatment of malignant germ cell tumors of the ovary with bleomycin, etoposide, and cisplatin. J Clin Oncol 8 (4): 715-20, 1990. [PUBMED Abstract]
Tratamiento de los tumores de células germinativas del ovario en estadio I
Disgerminomas
Las opciones de tratamiento para pacientes con disgerminomas en estadio I son las siguientes:
- Salpingooforectomía unilateral con linfangiografía o tomografía computarizada (TC) o sin estas.
- Salpingooforectomía unilateral seguida de observación.
- Salpingooforectomía unilateral con radioterapia adyuvante o quimioterapia.
En el caso de pacientes de disgerminoma en estadio I, la salpingooforectomía unilateral que conserva el útero y el ovario opuesto es el tratamiento aceptado para las pacientes jóvenes, interesadas en preservar su fertilidad o un embarazo. Se indica efectuar una linfangiografía postoperatoria o TC antes de decidir sobre el tratamiento para pacientes que no tuvieron un examen quirúrgico y patológico cuidadoso de los ganglios linfáticos pélvicos y paraórticos durante la cirugía.
Las pacientes que se estadificaron en forma completa y que presentan tumores en estadio IA se pueden observar de cerca después de una cirugía sin terapia adyuvante. Cerca del 15 % al 25 % de estas pacientes presentarán recaídas, pero es posible tratarlas con éxito en el momento de la recidiva, con una gran probabilidad de curación.
Es probable que las pacientes estadificadas en forma incompleta, o aquellas con tumores en estadios más avanzados deban recibir tratamiento adyuvante. Las opciones incluyen radioterapia o quimioterapia. Una desventaja de la primera es la esterilidad debido a la insuficiencia ovárica. La experiencia con la quimioterapia adyuvante es limitada, pero considerando la eficacia de la quimioterapia en los tumores que no son disgerminomas y en disgerminomas de estadios avanzados, es probable que sea muy eficaz y que permita la recuperación del potencial reproductivo en las pacientes con un ovario, trompa de Falopio y útero intactos.[1]
Otros tumores de células germinativas
Las opciones de tratamiento para pacientes con otros tumores de células germinativas en estadio I son las siguientes:
- Salpingooforectomía unilateral con quimioterapia adyuvante.
- Salpingooforectomía unilateral seguida de observación.
En el caso de pacientes con tumores de células germinativas en estadio I, se deberá efectuar una salpingooforectomía unilateral cuando se deba preservar la fertilidad. Para todos los tumores que no sean disgerminomas puros y teratomas inmaduros de grado bajo (grado I), la quimioterapia se suele administrar después de la cirugía, aunque en unas series se observó una supervivencia excelente para todos los tipos de tumores de estadio I controlados mediante vigilancia, lo que permitió reservar la quimioterapia para casos en donde se documentó una recidiva posquirúrgica.[2][Nivel de evidencia C1]
Se tiene bastante experiencia con una combinación de vincristina, dactinomicina y ciclofosfamida (VAC) administrada en un entorno adyuvante. Sin embargo, en la actualidad se prefieren combinaciones que contengan cisplatino, etopósido y bleomicina (BEP), debido a una tasa de recidiva más baja y a un tratamiento más corto.[3] A pesar de que no se efectuó una comparación de VAC y BEP, se deberá notar que en las pacientes bien clasificadas con resección completa de los tumores, es infrecuente que se presenten recaídas después de la quimioterapia a base de derivados del platino.[3] Sin embargo, la enfermedad recidivará en cerca del 25 % de las pacientes bien clasificadas y tratadas por 6 meses con VAC.[4]
La evidencia indica que una laparotomía de revisión no es beneficiosa en pacientes con resección tumoral completa inicial que reciben tratamiento adyuvante con derivados del cisplatino.[5,6]
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Thomas GM, Dembo AJ, Hacker NF, et al.: Current therapy for dysgerminoma of the ovary. Obstet Gynecol 70 (2): 268-75, 1987. [PUBMED Abstract]
- Dark GG, Bower M, Newlands ES, et al.: Surveillance policy for stage I ovarian germ cell tumors. J Clin Oncol 15 (2): 620-4, 1997. [PUBMED Abstract]
- Williams S, Blessing JA, Liao SY, et al.: Adjuvant therapy of ovarian germ cell tumors with cisplatin, etoposide, and bleomycin: a trial of the Gynecologic Oncology Group. J Clin Oncol 12 (4): 701-6, 1994. [PUBMED Abstract]
- Slayton RE, Park RC, Silverberg SG, et al.: Vincristine, dactinomycin, and cyclophosphamide in the treatment of malignant germ cell tumors of the ovary. A Gynecologic Oncology Group Study (a final report). Cancer 56 (2): 243-8, 1985. [PUBMED Abstract]
- Williams SD, Blessing JA, DiSaia PJ, et al.: Second-look laparotomy in ovarian germ cell tumors: the gynecologic oncology group experience. Gynecol Oncol 52 (3): 287-91, 1994. [PUBMED Abstract]
- Gershenson DM: The obsolescence of second-look laparotomy in the management of malignant ovarian germ cell tumors. Gynecol Oncol 52 (3): 283-5, 1994. [PUBMED Abstract]
Tratamiento de los tumores de células germinativas del ovario en estadio II
Disgerminomas
Las opciones de tratamiento para pacientes con disgerminomas en estadio II son las siguientes:
- Histerectomía abdominal total y salpingooforectomía bilateral con radioterapia adyuvante o quimioterapia.
- Salpingooforectomía unilateral con quimioterapia adyuvante.
- Participación en ensayos clínicos.
En el caso de pacientes de disgerminoma en estadio II, por lo general se realiza una histerectomía abdominal total y una salpingooforectomía bilateral. En las pacientes jóvenes con interés de preservar su fertilidad, es posible considerar el uso de la salpingooforectomía unilateral como terapia estándar dependiendo de la edad de la paciente, y se deberá administrar quimioterapia adyuvante.
Estas pacientes deberán recibir tratamiento adyuvante. Las opciones son la radioterapia o la quimioterapia. Una desventaja de la primera es la esterilidad debido a la insuficiencia ovárica. La experiencia con la quimioterapia adyuvante es limitada, pero considerando la eficacia de la quimioterapia en los tumores que no son disgerminomas y su eficacia en disgerminomas de estadio avanzado, es probable que sea muy eficaz y que permita la recuperación del potencial reproductivo en pacientes con ovario, trompa de Falopio y útero intactos. Por tanto, la quimioterapia adyuvante junto a la combinación de bleomicina, etopósido y cisplatino (BEP) reemplazan la radioterapia, excepto en la paciente ocasional para quien la quimioterapia no se considera apropiada.
Otros tumores de células germinativas
Las opciones de tratamiento para pacientes con otros tumores de células germinativas en estadio II son las siguientes:
- Salpingooforectomía unilateral con quimioterapia adyuvante.
- Laparotomía de revisión.
- Participación en ensayos clínicos.
En el caso de pacientes con tumores de células germinativas en estadio II que no son disgerminomas puros, se deberá efectuar una salpingooforectomía unilateral cuando se deba preservar la fertilidad. A pesar de que existe experiencia considerable con vincristina, dactinomicina y ciclofosfamida (VAC), en especial cuando se administran en un entorno adyuvante, BEP es más eficaz.[1-3] Las pacientes que no responden a una combinación a base de cisplatino aún pueden lograr una remisión duradera con VAC como terapia de rescate.[4] La recidiva después de 3 ciclos de BEP como terapia adyuvante es poco común.[4] Todas las pacientes que no responden a la terapia estándar son aptas para participar en ensayos clínicos. Cuando se presenta enfermedad residual o concentraciones elevadas de α-fetoproteína o gonadotropina coriónica humana después de efectuar una citorreducción quirúrgica máxima, se indica administrar 3 o 4 ciclos de quimioterapia combinada BEP.[5]
La evidencia indica que una laparotomía de revisión no es beneficiosa en pacientes con resección tumoral completa inicial que reciben tratamiento adyuvante a base de derivados del cisplatino.[6] La revisión quirúrgica puede ser beneficiosa para una minoría de pacientes cuyo tumor no se resecó por completo en el procedimiento quirúrgico inicial y quienes tuvieron elementos de teratoma en su tumor primario.[6,7] Se deberá llevar a cabo la resección quirúrgica de masas residuales localizadas por examen clínico, por procedimientos radiográficos, o al hacer la revisión quirúrgica, ya que se reseñó que hay una reversión hacia un tumor de células germinativas.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Williams S, Blessing JA, Liao SY, et al.: Adjuvant therapy of ovarian germ cell tumors with cisplatin, etoposide, and bleomycin: a trial of the Gynecologic Oncology Group. J Clin Oncol 12 (4): 701-6, 1994. [PUBMED Abstract]
- Pinkerton CR, Pritchard J, Spitz L: High complete response rate in children with advanced germ cell tumors using cisplatin-containing combination chemotherapy. J Clin Oncol 4 (2): 194-9, 1986. [PUBMED Abstract]
- Gershenson DM, Morris M, Cangir A, et al.: Treatment of malignant germ cell tumors of the ovary with bleomycin, etoposide, and cisplatin. J Clin Oncol 8 (4): 715-20, 1990. [PUBMED Abstract]
- Williams SD, Blessing JA, Moore DH, et al.: Cisplatin, vinblastine, and bleomycin in advanced and recurrent ovarian germ-cell tumors. A trial of the Gynecologic Oncology Group. Ann Intern Med 111 (1): 22-7, 1989. [PUBMED Abstract]
- Williams SD, Birch R, Einhorn LH, et al.: Treatment of disseminated germ-cell tumors with cisplatin, bleomycin, and either vinblastine or etoposide. N Engl J Med 316 (23): 1435-40, 1987. [PUBMED Abstract]
- Williams SD, Blessing JA, DiSaia PJ, et al.: Second-look laparotomy in ovarian germ cell tumors: the gynecologic oncology group experience. Gynecol Oncol 52 (3): 287-91, 1994. [PUBMED Abstract]
- Gershenson DM: The obsolescence of second-look laparotomy in the management of malignant ovarian germ cell tumors. Gynecol Oncol 52 (3): 283-5, 1994. [PUBMED Abstract]
Tratamiento de los tumores de células germinativas del ovario en estadio III
Disgerminomas
Las opciones de tratamiento para pacientes con disgerminomas en estadio III son las siguientes:
- Histerectomía abdominal total y salpingooforectomía bilateral.
- Salpingooforectomía unilateral con quimioterapia adyuvante.
- Participación en ensayos clínicos.
En el caso de pacientes de disgerminoma en estadio III, se recomienda efectuar una histerectomía abdominal total y salpingooforectomía bilateral con extirpación de la mayor cantidad de tumor que se pueda hacer de forma inocua, sin resección de segmentos del tracto urinario o segmentos largos del intestino delgado o grueso. Las pacientes que desean preservar su fertilidad se pueden tratar con salpingooforectomía unilateral si van a someterse a quimioterapia.[1-5]
La quimioterapia combinada con bleomicina, etopósido, cisplatino (BEP) puede curar a la mayoría de estas pacientes. En un informe de los resultados de 2 ensayos del Gynecologic Oncology Group (GOG), 19 pacientes de 20 con resección tumoral incompleta que fueron tratadas con BEP o cisplatino, vinblastina y bleomicina (PVB) permanecieron sin enfermedad durante una mediana de seguimiento de 26 meses.[1] Es cada vez más común administrar de 3 a 4 ciclos de una combinación que contenga cisplatino, como PVB o BEP, cuando hay enfermedad residual voluminosa.[6-8] Un estudio aleatorizado de cáncer testicular mostró que la bleomicina es un componente esencial del régimen BEP, cuando solo se administran 3 ciclos.[9] Ya que la quimioterapia con BEP parece tener un efecto menos esterilizante que la radiación de campo amplio, la quimioterapia combinada es el tratamiento preferido en la paciente que todavía desea preservar la fertilidad.[1]
Otros tumores de células germinativas
Las opciones de tratamiento para pacientes con otros tumores de células germinativas en estadio III son las siguientes:
- Histerectomía abdominal total y salpingooforectomía bilateral con quimioterapia adyuvante, con quimioterapia neoadyuvante o sin esta.
- Salpingooforectomía unilateral con quimioterapia adyuvante, con quimioterapia neoadyuvante o sin esta.
- Laparotomía de revisión.
- Participación en ensayos clínicos.
En el caso de pacientes con tumores de células germinativas en estadio III con excepción de los disgerminomas puros, se recomienda efectuar una histerectomía abdominal total y una salpingooforectomía bilateral, extirpando el tumor del abdomen y pelvis tanto como sea posible sin daño y sin resecar porciones del tracto urinario o grandes segmentos del intestino delgado o grueso. Las pacientes que desean preservar la fertilidad se pueden tratar con salpingooforectomía unilateral.[1,3,4] En las pacientes con enfermedad intraabdominal extensa, cuya condición clínica excluye la cirugía de citorreducción, se puede considerar la quimioterapia antes de la cirugía. Después de una cirugía de citorreducción máxima, se indica administrar de 3 a 4 ciclos de quimioterapia combinada que contenga cisplatino.[2,6,10]
La evidencia indica que una laparotomía de revisión no es beneficiosa en pacientes con resección tumoral completa inicial que reciben tratamiento adyuvante a base de derivados del cisplatino.[11] Las pacientes que no responden con una combinación a base de cisplatino y etopósido pueden obtener una remisión durable con una combinación de vincristina, dactinomicina y ciclofosfamida o cisplatino, vinblastina e ifosfamida como terapia de rescate.[6] La revisión quirúrgica puede ser beneficiosa en una minoría de pacientes cuyo tumor no se resecó por completo en el procedimiento quirúrgico inicial, y quienes tuvieron elementos de teratoma en el tumor primario.[11] Se deberá llevar a cabo la resección quirúrgica de las masas residuales localizadas por examen clínico, por procedimientos radiográficos o en la revisión quirúrgica, ya que se reseñó la posibilidad de reversión a tumor de células germinativas o teratoma evolutivo.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Williams SD, Blessing JA, Hatch KD, et al.: Chemotherapy of advanced dysgerminoma: trials of the Gynecologic Oncology Group. J Clin Oncol 9 (11): 1950-5, 1991. [PUBMED Abstract]
- Gershenson DM, Morris M, Cangir A, et al.: Treatment of malignant germ cell tumors of the ovary with bleomycin, etoposide, and cisplatin. J Clin Oncol 8 (4): 715-20, 1990. [PUBMED Abstract]
- Wu PC, Huang RL, Lang JH, et al.: Treatment of malignant ovarian germ cell tumors with preservation of fertility: a report of 28 cases. Gynecol Oncol 40 (1): 2-6, 1991. [PUBMED Abstract]
- Schwartz PE, Chambers SK, Chambers JT, et al.: Ovarian germ cell malignancies: the Yale University experience. Gynecol Oncol 45 (1): 26-31, 1992. [PUBMED Abstract]
- Low JJ, Perrin LC, Crandon AJ, et al.: Conservative surgery to preserve ovarian function in patients with malignant ovarian germ cell tumors. A review of 74 cases. Cancer 89 (2): 391-8, 2000. [PUBMED Abstract]
- Williams SD, Blessing JA, Moore DH, et al.: Cisplatin, vinblastine, and bleomycin in advanced and recurrent ovarian germ-cell tumors. A trial of the Gynecologic Oncology Group. Ann Intern Med 111 (1): 22-7, 1989. [PUBMED Abstract]
- Williams SD, Birch R, Einhorn LH, et al.: Treatment of disseminated germ-cell tumors with cisplatin, bleomycin, and either vinblastine or etoposide. N Engl J Med 316 (23): 1435-40, 1987. [PUBMED Abstract]
- Taylor MH, Depetrillo AD, Turner AR: Vinblastine, bleomycin, and cisplatin in malignant germ cell tumors of the ovary. Cancer 56 (6): 1341-9, 1985. [PUBMED Abstract]
- Williams S, Blessing JA, Liao SY, et al.: Adjuvant therapy of ovarian germ cell tumors with cisplatin, etoposide, and bleomycin: a trial of the Gynecologic Oncology Group. J Clin Oncol 12 (4): 701-6, 1994. [PUBMED Abstract]
- Williams SD, Blessing JA, DiSaia PJ, et al.: Second-look laparotomy in ovarian germ cell tumors: the gynecologic oncology group experience. Gynecol Oncol 52 (3): 287-91, 1994. [PUBMED Abstract]
- Gershenson DM: The obsolescence of second-look laparotomy in the management of malignant ovarian germ cell tumors. Gynecol Oncol 52 (3): 283-5, 1994. [PUBMED Abstract]
Tratamiento de los tumores de células germinativas del ovario en estadio IV
Disgerminoma
Las opciones de tratamiento para pacientes con disgerminomas en estadio IV son las siguientes:
- Histerectomía abdominal total y salpingooforectomía bilateral con quimioterapia adyuvante.
- Salpingooforectomía unilateral con quimioterapia adyuvante.
- Participación en ensayos clínicos.
En las pacientes de disgerminoma en estadio IV, se recomienda la histerectomía abdominal total y la salpingooforectomía bilateral con la extirpación del tumor macroscópico del abdomen y pelvis tanto como sea posible, sin daño y sin resección de porciones del tracto urinario o de grandes segmentos de intestino delgado o grueso, aunque se deberá considerar la salpingooforectomía unilateral en pacientes que desean preservar la fertilidad.[1,2] La quimioterapia con bleomicina, etopósido y cisplatino (BEP) puede curar a la mayoría de estas pacientes. El disgerminoma en estadio IV no se trata con radioterapia, sino más bien con quimioterapia, de preferencia con 3 o 4 ciclos de quimioterapia combinada que contenga cisplatino, como BEP.[1] Una revisión quirúrgica después de tratamiento muy pocas veces es beneficiosa.
Otros tumores de células germinativas
Las opciones de tratamiento para pacientes con otros tumores de células germinativas en estadio IV son las siguientes:
- Histerectomía abdominal total y salpingooforectomía bilateral con quimioterapia adyuvante con quimioterapia neoadyuvante o sin esta.
- Salpingooforectomía unilateral con quimioterapia adyuvante con quimioterapia neoadyuvante o sin esta.
- Participación en ensayos clínicos.
En las pacientes con tumores de células germinativas en estadio IV con excepción de disgerminomas puros, se recomienda una histerectomía abdominal total y una salpingooforectomía bilateral con extirpación, sin daño de tanto tumor del abdomen y pelvis como sea posible, y sin resección de riñón o de grandes segmentos de intestino delgado o grueso. Las pacientes que desean preservar la fertilidad se pueden tratar con salpingooforectomía unilateral. Después de la citorreducción quirúrgica máxima, se indica administrar 3 a 4 ciclos de quimioterapia que contenga cisplatino.[3,4] En las pacientes con enfermedad intraabdominal extensa, cuya condición clínica descarta la cirugía citorreductora, se puede tomar en consideración la quimioterapia antes de la cirugía. Las pacientes que no responden a una combinación a base de cisplatino y etopósido pueden obtener una remisión durable con vincristina, dactinomicina y ciclofosfamida, o cisplatino, vinblastina e ifosfamida como terapia de rescate.[4]
La revisión quirúrgica puede ser beneficiosa en una minoría de pacientes cuyo tumor no se resecó por completo en el procedimiento quirúrgico inicial y quienes tuvieron elementos de teratoma en el tumor primario.[5,6] Se deberá llevar a cabo la resección quirúrgica de las masas residuales detectadas por examen clínico, por procedimientos radiográficos o en la revisión quirúrgica, ya que se reseñó la posibilidad de reversión a tumor de células germinativas o teratoma progresivo.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Williams SD, Blessing JA, Hatch KD, et al.: Chemotherapy of advanced dysgerminoma: trials of the Gynecologic Oncology Group. J Clin Oncol 9 (11): 1950-5, 1991. [PUBMED Abstract]
- Low JJ, Perrin LC, Crandon AJ, et al.: Conservative surgery to preserve ovarian function in patients with malignant ovarian germ cell tumors. A review of 74 cases. Cancer 89 (2): 391-8, 2000. [PUBMED Abstract]
- Gershenson DM, Morris M, Cangir A, et al.: Treatment of malignant germ cell tumors of the ovary with bleomycin, etoposide, and cisplatin. J Clin Oncol 8 (4): 715-20, 1990. [PUBMED Abstract]
- Williams SD, Blessing JA, Moore DH, et al.: Cisplatin, vinblastine, and bleomycin in advanced and recurrent ovarian germ-cell tumors. A trial of the Gynecologic Oncology Group. Ann Intern Med 111 (1): 22-7, 1989. [PUBMED Abstract]
- Williams SD, Blessing JA, DiSaia PJ, et al.: Second-look laparotomy in ovarian germ cell tumors: the gynecologic oncology group experience. Gynecol Oncol 52 (3): 287-91, 1994. [PUBMED Abstract]
- Gershenson DM: The obsolescence of second-look laparotomy in the management of malignant ovarian germ cell tumors. Gynecol Oncol 52 (3): 283-5, 1994. [PUBMED Abstract]
Tratamiento de los tumores de células germinativas del ovario recidivantes
Disgerminomas
Las opciones de tratamiento para pacientes con disgerminomas recidivantes son las siguientes:
- La quimioterapia a base de cisplatino se usa con eficacia en pacientes con disgerminoma recidivante con radioterapia adyuvante y sin esta.[1]
- Las pacientes de disgerminomas puros recidivantes de ovario son aptas para participar en ensayos clínicos. Se debe tener en cuenta el uso de regímenes de dosis altas con rescate.
Otros tumores de células germinativas
Las opciones de tratamiento para pacientes con otros tumores de células germinativas recidivantes son las siguientes:
- Las pacientes con tumores recidivantes de células germinativas del ovario, a excepción de disgerminoma puro, se deberán tratar con quimioterapia. El tipo de quimioterapia se determina por el tratamiento administrado antes.[2] La radioterapia no es eficaz en estos casos, en cambio, la quimioterapia combinada a base de cisplatino lo es.[1,3,4] Las pacientes que no responden a una combinación a base de cisplatino aún pueden alcanzar una remisión duradera con vincristina, dactinomicina y ciclofosfamida o ifosfamida y cisplatino como terapia de rescate.[1] Nuevos tratamientos potenciales incluyen una combinación de ifosfamida [5] o quimioterapia de dosis elevada y rescate con médula autógena.[6-8] A pesar de que la función de la cirugía secundaria citorreductora en pacientes con tumores de las células germinativas del ovario, progresivo o recidivantes, todavía es polémica, puede traer beneficios para un grupo reducido de pacientes, en especial, aquellas con teratoma inmaduro.[9] Después de un esfuerzo máximo hacia la citorreducción quirúrgica, se debe considerar la quimioterapia.
- Las pacientes con tumores recidivantes de células germinativas del ovario son aptas para participar en ensayos clínicos. Se debe tener en cuenta el uso de regímenes de dosis altas con rescate.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Williams SD, Blessing JA, Moore DH, et al.: Cisplatin, vinblastine, and bleomycin in advanced and recurrent ovarian germ-cell tumors. A trial of the Gynecologic Oncology Group. Ann Intern Med 111 (1): 22-7, 1989. [PUBMED Abstract]
- Williams SD, Blessing JA, Hatch KD, et al.: Chemotherapy of advanced dysgerminoma: trials of the Gynecologic Oncology Group. J Clin Oncol 9 (11): 1950-5, 1991. [PUBMED Abstract]
- Williams SD, Birch R, Einhorn LH, et al.: Treatment of disseminated germ-cell tumors with cisplatin, bleomycin, and either vinblastine or etoposide. N Engl J Med 316 (23): 1435-40, 1987. [PUBMED Abstract]
- Taylor MH, Depetrillo AD, Turner AR: Vinblastine, bleomycin, and cisplatin in malignant germ cell tumors of the ovary. Cancer 56 (6): 1341-9, 1985. [PUBMED Abstract]
- Munshi NC, Loehrer PJ, Roth BJ, et al.: Vinblastine, ifosfamide and cisplatin (VeIP) as second line chemotherapy in metastatic germ cell tumors (GCT). [Abstract] Proceedings of the American Society of Clinical Oncology 9: A-520, 134, 1990.
- Broun ER, Nichols CR, Kneebone P, et al.: Long-term outcome of patients with relapsed and refractory germ cell tumors treated with high-dose chemotherapy and autologous bone marrow rescue. Ann Intern Med 117 (2): 124-8, 1992. [PUBMED Abstract]
- Motzer RJ, Bosl GJ: High-dose chemotherapy for resistant germ cell tumors: recent advances and future directions. J Natl Cancer Inst 84 (22): 1703-9, 1992. [PUBMED Abstract]
- Mandanas RA, Saez RA, Epstein RB, et al.: Long-term results of autologous marrow transplantation for relapsed or refractory male or female germ cell tumors. Bone Marrow Transplant 21 (6): 569-76, 1998. [PUBMED Abstract]
- Munkarah A, Gershenson DM, Levenback C, et al.: Salvage surgery for chemorefractory ovarian germ cell tumors. Gynecol Oncol 55 (2): 217-23, 1994. [PUBMED Abstract]
Actualizaciones más recientes a este resumen (02/14/2025)
Los resúmenes del PDQ con información sobre el cáncer se revisan con regularidad y se actualizan a medida que se obtiene nueva información. Esta sección describe los cambios más recientes hechos a este resumen a partir de la fecha arriba indicada.
Se incorporaron cambios editoriales en este resumen.
El Consejo editorial del PDQ sobre el tratamiento para adultos es responsable de la redacción y actualización de este resumen y mantiene independencia editorial respecto del NCI. El resumen refleja una revisión independiente de la bibliografía médica y no representa las políticas del NCI ni de los NIH. Para obtener más información sobre las políticas relativas a los resúmenes y la función de los consejos editoriales del PDQ responsables de su actualización, consultar Información sobre este resumen del PDQ e Información del PDQ® sobre el cáncer dirigida a profesionales de la salud.
Información sobre este resumen del PDQ
Propósito de este resumen
Este resumen de información del PDQ sobre el cáncer dirigido a profesionales de la salud proporciona información integral revisada por expertos y basada en la evidencia sobre el tratamiento de los tumores de células germinativas del ovario. El objetivo es servir como fuente de información y ayuda para los profesionales clínicos durante la atención de pacientes. No ofrece pautas ni recomendaciones formales para tomar decisiones relacionadas con la atención sanitaria.
Revisores y actualizaciones
El consejo editorial del PDQ sobre el tratamiento para adultos, que mantiene independencia editorial respecto del Instituto Nacional del Cáncer (NCI), revisa este resumen de manera periódica y, en caso necesario, lo actualiza. Este resumen es el resultado de una revisión bibliográfica independiente y no constituye una declaración de política del NCI ni de los Institutos Nacionales de la Salud (NIH).
Cada mes, los integrantes de este consejo revisan los artículos publicados recientemente para determinar lo siguiente:
- Si el artículo se debe analizar en una reunión del consejo.
- Si conviene añadir texto acerca del artículo.
- Si se debe reemplazar o actualizar un artículo que ya se citó.
Los cambios en los resúmenes se deciden mediante consenso de los integrantes del consejo después de evaluar la solidez de la evidencia de los artículos publicados y determinar la forma de incorporar el artículo en el resumen.
Los revisores principales del sumario sobre Tratamiento de los tumores de células germinativas del ovario son:
- Olga T. Filippova, MD (Lenox Hill Hospital)
- Marina Stasenko, MD (New York University Medical Center)
Cualquier comentario o pregunta sobre el contenido de este resumen se debe enviar al Servicio de Información de Cáncer del Instituto Nacional del Cáncer. Por favor, no enviar preguntas o comentarios directamente a los integrantes del consejo, ya que no responderán consultas de manera individual.
Niveles de evidencia
Algunas de las referencias bibliográficas de este resumen se acompañan del nivel de evidencia. El propósito de esto es ayudar al lector a evaluar la solidez de la evidencia que respalda el uso de ciertas intervenciones o abordajes. El consejo editorial del PDQ sobre el tratamiento para adultos emplea un sistema de jerarquización formal para asignar los niveles de evidencia científica.
Permisos para el uso de este resumen
PDQ (Physician Data Query) es una marca registrada. Se autoriza el uso del texto de los documentos del PDQ; sin embargo, no se podrá identificar como un resumen de información sobre cáncer del PDQ del NCI, salvo que el resumen se reproduzca en su totalidad y se actualice de manera periódica. Por otra parte, se permitirá que un autor escriba una oración como “En el resumen del PDQ del NCI de información sobre la prevención del cáncer de mama se describen, de manera concisa, los siguientes riesgos: [incluir fragmento del resumen]”.
Se sugiere citar la referencia bibliográfica de este resumen del PDQ de la siguiente forma:
PDQ® sobre el tratamiento para adultos. PDQ Tratamiento de los tumores de células germinativas del ovario. Bethesda, MD: National Cancer Institute. Actualización: <MM/DD/YYYY>. Disponible en: https://www.cancer.gov/espanol/tipos/ovario/pro/tratamiento-celulas-germinativas-ovario-pdq. Fecha de acceso: <MM/DD/YYYY>.
Las imágenes en este resumen se reproducen con autorización del autor, el artista o la editorial para uso exclusivo en los resúmenes del PDQ. La utilización de las imágenes fuera del PDQ requiere la autorización del propietario, que el Instituto Nacional del Cáncer no puede otorgar. Para obtener más información sobre el uso de las ilustraciones de este resumen o de otras imágenes relacionadas con el cáncer, consultar Visuals Online, una colección de más de 2000 imágenes científicas.
Cláusula sobre el descargo de responsabilidad
Según la solidez de la evidencia, las opciones de tratamiento se clasifican como “estándar” o “en evaluación clínica”. Estas clasificaciones no se deben utilizar para justificar decisiones sobre reembolsos de seguros. Para obtener más información sobre la cobertura de seguros, consultar la página Manejo de la atención del cáncer en Cancer.gov/espanol.
Comuníquese con el Instituto Nacional del Cáncer
Para obtener más información sobre las opciones para comunicarse con el NCI, incluso la dirección de correo electrónico, el número telefónico o el chat, consultar la página del Servicio de Información de Cáncer del Instituto Nacional del Cáncer.