Tratamiento del cáncer de vejiga (PDQ®)–Versión para profesionales de salud
Información general sobre el cáncer de vejiga
Incidencia y mortalidad
El cáncer de vejiga es el sexto tipo de cáncer más común en los Estados Unidos, después del cáncer de mama, el cáncer de próstata, el cáncer de pulmón, el cáncer de colon y el melanoma. Es el cuarto tipo de cáncer más común en hombres y el duodécimo cáncer más común en mujeres. De los cerca de 84 000 casos nuevos por año, alrededor de 65 000 corresponden a hombres y alrededor de 19 000 a mujeres. De cerca de 17 000 defunciones por año, más de 12 000 corresponden a hombres y menos de 5000 a mujeres. No se entienden bien las razones de esta disparidad entre los sexos.[1,2]
Número estimado de casos nuevos y defunciones por cáncer de vejiga en los Estados Unidos para 2025:[2]
- Casos nuevos: 84 870.
- Defunciones: 17 420.
Características anatómicas
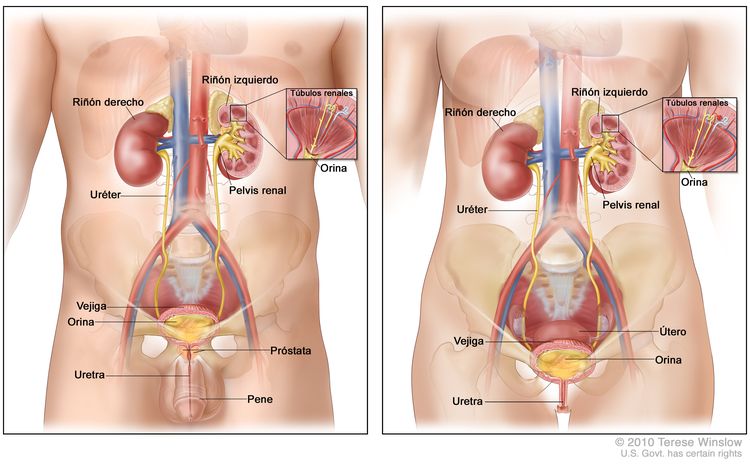
Las vías urinarias están formadas por los riñones, los uréteres, la vejiga y la uretra. Las vías urinarias están revestidas de urotelio de células transicionales desde la pelvis renal hasta la uretra proximal. Es posible que se presente un carcinoma de células de transición (también conocido como carcinoma urotelial) en cualquier parte a lo largo de estas vías.
Características histopatológicas
En condiciones normales, la vejiga, la parte inferior de los riñones (pelvis renal), los uréteres y la uretra proximal están revestidos con una membrana mucosa especializada conocida como epitelio de transición (también llamado urotelio). La mayoría de los cánceres que se forman en estos tejidos son carcinomas de células de transición (también llamados carcinomas uroteliales) que se derivan del epitelio de transición. Para obtener más información, consultar Tratamiento del cáncer de células renales y Tratamiento del cáncer de células de transición de pelvis renal y de uréter.
El carcinoma de células de transición de vejiga puede ser de grado bajo o de grado alto:
- El cáncer de vejiga de grado bajo a menudo recidiva en la vejiga después del tratamiento, pero rara vez invade la pared muscular de la vejiga o se disemina a otras partes del cuerpo. Los pacientes muy pocas veces mueren por cáncer de vejiga de grado bajo.
- El cáncer de vejiga de grado alto, por lo general, recidiva en la vejiga y tiene una fuerte tendencia a invadir la pared muscular de la vejiga y diseminarse a otras partes del cuerpo. El cáncer de vejiga de grado alto se trata de forma más intensiva que el de grado bajo y es mucho más probable que cause la muerte. Casi todas las muertes por cáncer de vejiga se deben a una enfermedad de grado alto.
El cáncer de vejiga se divide también en enfermedad con invasión muscular y enfermedad sin invasión muscular de acuerdo con el grado de invasión de la capa muscular (también llamado músculo detrusor), que es el músculo grueso y profundo de la pared de la vejiga.
- Es mucho más probable que la enfermedad con invasión muscular se disemine a otras partes del cuerpo y, en general, se trata con extirpación de la vejiga o con radiación y quimioterapia. Como se señaló antes, los cánceres de grado alto son mucho más propensos a invadir el músculo que los de grado bajo. Por lo tanto, los cánceres con invasión del músculo a menudo se tratan con mayor intensidad que los cánceres sin invasión muscular.
- La enfermedad sin invasión muscular se trata a menudo extirpando uno o más tumores con un abordaje transuretral. A veces, se introduce quimioterapia u otros tratamientos en la vejiga usando un catéter como medio para ayudar a combatir el cáncer.
En condiciones de inflamación crónica, como cuando hay una infestación de la vejiga por el parásito Schistosoma haematobium, es posible que se presente una metaplasia escamosa en la vejiga. La incidencia de carcinomas de células escamosas de vejiga es más alta en condiciones de inflamación crónica que la que se observa en otros casos. Además de los carcinomas de células de transición y los carcinomas de células escamosas, en la vejiga se pueden formar adenocarcinomas, carcinomas de células pequeñas y sarcomas. En los Estados Unidos, los carcinomas de células de transición representan la mayoría (>90 %) de los cánceres de vejiga. Sin embargo, un número significativo de carcinomas de células de transición tiene áreas de diferenciación de células escamosas o de otro tipo.
Carcinogénesis y factores de riesgo
El envejecimiento es el factor de riesgo más importante para la mayoría de los cánceres. Otros factores de riesgo para el cáncer de vejiga son los siguientes:
- Consumo de tabaco, en especial, de cigarrillos.[3]
- Antecedentes familiares de cáncer de vejiga.[4]
- Variantes genéticas.[5-7]
- Variante de HRAS (síndrome de Costello, síndrome osteo-facio-cutáneo).
- Variante de RB1.
- Variante de PTEN/MMAC1 (síndrome de Cowden).
- Fenotipo de acetilador lento de NAT2.
- Fenotipo anulador de GSTM1.
- Exposiciones ocupacionales a sustancias químicas presentes en pinturas, colorantes, metales y derivados del petróleo, como los siguientes:
- Tratamiento con ciclofosfamida, ifosfamida o radiación dirigida a la pelvis para otras neoplasias malignas.[10-12]
- Uso de productos de hierbas chinas como el ácido aristolóquico que se extrae de la especie Aristolochia fangchi.[13]
- Exposición al arsénico.
- Exposición a los hidrocarburos alifáticos clorados y subproductos de la cloración en agua tratada.[16]
- Infestaciones de la vejiga por Schistosoma haematobium (cáncer de vejiga por esquistosomas o bilharzias).[17]
- Vejiga neurógena y el uso de sondas vesicales permanentes para esta afección.[18]
Se cuenta con evidencia sólida que relacionan la exposición a carcinógenos con el cáncer de vejiga. El factor de riesgo más común para el cáncer de vejiga en los Estados Unidos es el consumo de cigarrillos. Se calcula que hasta la mitad de todos los cánceres de vejiga se presentan por el consumo de cigarrillos y que este aumenta el riesgo del cáncer de vejiga entre 2 y 4 veces por encima del riesgo inicial de una persona.[19,20] Los fumadores con menos polimorfismos funcionales de la N-acetiltransferasa 2 (conocidos como acetiladores lentos) tienen un riesgo más alto de cáncer de vejiga que otros fumadores, supuestamente debido a su reducida capacidad para desintoxicarse de los carcinógenos.
Ciertas exposiciones ocupacionales también se relacionaron con el cáncer de vejiga; se notificaron tasas más altas de cáncer de vejiga en las industrias de tinturas textiles y de caucho para neumáticos, y entre los pintores, los trabajadores del cuero, calzado y aluminio, hierro y siderurgia. Las sustancias químicas específicas relacionadas con la carcinogénesis vesical incluyen la beta-naftilamina, el 4-aminobifenilo y la bencidina. Aunque estas sustancias químicas por lo general están prohibidas en los países occidentales, se sospecha que muchas otras sustancias químicas en uso también causan cáncer de vejiga.[20]
La exposición al fármaco quimioterapéutico ciclofosfamida también se relacionó con un aumento del riesgo del cáncer de vejiga.
Las infecciones crónicas de las vías urinarias y la infestación por el parásito S. haematobium también se relacionaron con un aumento del riesgo del cáncer de vejiga, que a menudo se presenta como carcinoma de células escamosas. Se piensa que la inflamación crónica desempeña una función importante en la carcinogénesis en estos casos.
Características clínicas
El cáncer de vejiga se suele presentar con hematuria macroscópica o microscópica. Es menos común que los pacientes se quejen de frecuencia urinaria, nocturia y disuria, síntomas que son más comunes en los pacientes de carcinoma in situ. Los pacientes con carcinomas uroteliales de vías urinarias superiores a veces presentan dolor debido a la obstrucción que causa el tumor.
Los carcinomas uroteliales son a menudo multifocales; se debe evaluar todo el urotelio si se encuentra un tumor. En pacientes de cáncer de vejiga, las imágenes de las vías urinarias superiores son esenciales para la estadificación y la vigilancia. Esto es posible de lograr con ureteroscopia, pielografía retrógrada durante la cistoscopia, pielografía intravenosa o urogramas con tomografía computarizada (TC). Del mismo modo, los pacientes de carcinoma de células de transición de vías urinarias superiores tienen un riesgo alto de cáncer de vejiga; es necesario que estos pacientes se sometan a cistoscopia y vigilancia periódica de la vía urinaria superior contralateral.
Diagnóstico
Cuando se sospecha que hay un cáncer de vejiga, la prueba de diagnóstico más útil es la cistoscopia. Los estudios radiológicos, como las TC o las ecografías, no tienen la sensibilidad suficiente para detectar cánceres de vejiga. La cistoscopia se puede realizar en un consultorio de urología.
Si se observa un cáncer de grado alto en la cistoscopia, se suele citar al paciente para una exploración bimanual con anestesia y una repetición de la cistoscopia en un quirófano, de modo que se pueda realizar la biopsia o la resección transuretral de uno o más tumores. Si se observa un cáncer de grado alto (incluso un carcinoma in situ) o cáncer invasivo, el paciente se estadifica con una TC del abdomen y la pelvis (o un urograma con TC), o bien una radiografía o una TC del tórax. Los pacientes con una elevación de la fosfatasa alcalina no hepática o síntomas que indican metástasis óseas se someten a una gammagrafía ósea.
Factores pronósticos
Los factores pronósticos más importantes de un carcinoma de vejiga son los siguientes:
- Invasión profunda de la pared de la vejiga.
- Grado patológico del tumor.
- Presencia versus ausencia de un carcinoma in situ.
Entre los cánceres sin invasión muscular, también son pronósticos los siguientes factores:[21]
- Número de tumores.
- Tamaño del tumor (por ejemplo, >3 cm o <3 cm).
- Invasión de la lámina propia (Ta vs. T1).
- Si el tumor es primario o recidivante.
La mayoría de los tumores superficiales son bien diferenciados. Los pacientes con tumores superficiales menos diferenciados, grandes, múltiples o relacionados con un carcinoma in situ (Tis) en otras áreas de la mucosa vesical tienen el mayor riesgo de recidiva y de cáncer invasivo. Se considera que estos pacientes tienen riesgo de cáncer en toda la superficie endotelial.
Supervivencia
Los pacientes que mueren por cáncer de vejiga casi siempre tienen enfermedad que se metastatizó desde la vejiga hasta otros órganos. Como los cánceres de vejiga de grado bajo rara vez crecen en la pared muscular de la vejiga y hacen metástasis con poca frecuencia, los pacientes de cáncer de vejiga de grado bajo (grado I) casi nunca mueren por el cáncer. No obstante, sufren recaídas múltiples y la resección es necesaria.
Casi todas las muertes por cáncer de vejiga ocurren en pacientes con enfermedad de grado alto, que tiene un potencial mucho mayor de invadir profundamente la pared muscular de la vejiga y diseminarse a otros órganos.
Alrededor del 70 % al 80 % de los pacientes con cáncer de vejiga recién diagnosticado presentan tumores superficiales de la vejiga (es decir, estadio Ta, Tis o T1). El pronóstico de estos pacientes depende en gran medida del grado tumoral. Los pacientes con tumores de grado alto tienen un riesgo significativo de morir por su cáncer, incluso si no invaden el músculo.[22] Entre los pacientes con tumores de grado alto, quienes presentan cáncer de vejiga superficial y sin invasión muscular, a menudo se curan; aquellos con enfermedad con invasión muscular, a veces se curan.[23-25] En estudios se demostró que algunos pacientes con metástasis a distancia lograron una respuesta completa a largo plazo después de haber sido tratados con regímenes de quimioterapia combinada, aunque la mayoría de estos pacientes tienen metástasis limitadas a sus ganglios linfáticos y un estado funcional casi normal.[26,27]
Hay ensayos clínicos apropiados para los pacientes de cáncer de vejiga en todos los estadios. Siempre que sea posible, los pacientes deben considerar la participación en los ensayos clínicos diseñados para mejorar el tratamiento estándar.
También se dispone de información general sobre ensayos clínicos en el portal de Internet del NCI.
Seguimiento
El cáncer de vejiga tiende a recidivar, incluso cuando no es invasivo en el momento del diagnóstico; por lo tanto, es una práctica estándar realizar la vigilancia de las vías urinarias después de un diagnóstico de este tipo de cáncer. Sin embargo, no se han realizado estudios para evaluar si la vigilancia afecta las tasas de progresión, supervivencia o calidad de vida; los ensayos clínicos tampoco definen un cronograma óptimo de vigilancia. Se piensa que los carcinomas uroteliales reflejan un llamado defecto de campo según el que se presenta un cáncer debido a variantes genéticas que están presentes en toda la vejiga o en todo el urotelio del paciente. En consecuencia, las personas a quienes se les resecó un tumor vesical a menudo presentan después tumores recidivantes en la vejiga; con frecuencia, en sitios diferentes a los del tumor inicial. Del mismo modo, pero con menos frecuencia, pueden tener tumores que aparecen en las vías urinarias superiores (es decir, en la pelvis renal o los uréteres).
Una explicación alternativa de estos patrones de recidiva es que las células cancerosas que se desorganizan cuando se extirpa un tumor se pueden reimplantar en otros sitios del urotelio. En favor de esta segunda teoría es que es más probable que los tumores recidiven de modo anterógrado que retrógrado con respecto al cáncer inicial. Es más probable que los cánceres de vías urinarias superiores recidiven en la vejiga que los cánceres de vejiga recidiven en las vías urinarias superiores.[28-31]
Bibliografía
- National Cancer Institute: SEER Cancer Stat Facts: Bladder Cancer. Bethesda, Md: National Cancer Institute. Available online. Last accessed January 31, 2025.
- American Cancer Society: Cancer Facts and Figures 2025. American Cancer Society, 2025. Available online. Last accessed January 16, 2025.
- Burger M, Catto JW, Dalbagni G, et al.: Epidemiology and risk factors of urothelial bladder cancer. Eur Urol 63 (2): 234-41, 2013. [PUBMED Abstract]
- Fraumeni JF Jr, Thomas LB: Malignant bladder tumors in a man and his three sons. JAMA 201 (7): 97-9, 1967.
- Marees T, Moll AC, Imhof SM, et al.: Risk of second malignancies in survivors of retinoblastoma: more than 40 years of follow-up. J Natl Cancer Inst 100 (24): 1771-9, 2008. [PUBMED Abstract]
- Gallagher DJ, Feifer A, Coleman JA: Genitourinary cancer predisposition syndromes. Hematol Oncol Clin North Am 24 (5): 861-83, 2010. [PUBMED Abstract]
- Lindor NM, McMaster ML, Lindor CJ, et al.: Concise handbook of familial cancer susceptibility syndromes - second edition. J Natl Cancer Inst Monogr (38): 1-93, 2008. [PUBMED Abstract]
- Stadler WM: Molecular events in the initiation and progression of bladder cancer (review). Int J Oncol 3: 549-557, 1993.
- Brown T, Slack R, Rushton L, et al.: Occupational cancer in Britain. Urinary tract cancers: bladder and kidney. Br J Cancer 107 (Suppl 1): S76-84, 2012. [PUBMED Abstract]
- Nieder AM, Porter MP, Soloway MS: Radiation therapy for prostate cancer increases subsequent risk of bladder and rectal cancer: a population based cohort study. J Urol 180 (5): 2005-9; discussion 2009-10, 2008. [PUBMED Abstract]
- Abern MR, Dude AM, Tsivian M, et al.: The characteristics of bladder cancer after radiotherapy for prostate cancer. Urol Oncol 31 (8): 1628-34, 2013. [PUBMED Abstract]
- Monach PA, Arnold LM, Merkel PA: Incidence and prevention of bladder toxicity from cyclophosphamide in the treatment of rheumatic diseases: a data-driven review. Arthritis Rheum 62 (1): 9-21, 2010. [PUBMED Abstract]
- Cosyns JP: Aristolochic acid and 'Chinese herbs nephropathy': a review of the evidence to date. Drug Saf 26 (1): 33-48, 2003. [PUBMED Abstract]
- Letašiová S, Medve'ová A, Šovčíková A, et al.: Bladder cancer, a review of the environmental risk factors. Environ Health 11 (Suppl 1): S11, 2012. [PUBMED Abstract]
- Fernández MI, López JF, Vivaldi B, et al.: Long-term impact of arsenic in drinking water on bladder cancer health care and mortality rates 20 years after end of exposure. J Urol 187 (3): 856-61, 2012. [PUBMED Abstract]
- Villanueva CM, Cantor KP, Grimalt JO, et al.: Bladder cancer and exposure to water disinfection by-products through ingestion, bathing, showering, and swimming in pools. Am J Epidemiol 165 (2): 148-56, 2007. [PUBMED Abstract]
- Kantor AF, Hartge P, Hoover RN, et al.: Urinary tract infection and risk of bladder cancer. Am J Epidemiol 119 (4): 510-5, 1984. [PUBMED Abstract]
- Locke JR, Hill DE, Walzer Y: Incidence of squamous cell carcinoma in patients with long-term catheter drainage. J Urol 133 (6): 1034-5, 1985. [PUBMED Abstract]
- Brennan P, Bogillot O, Greiser E, et al.: The contribution of cigarette smoking to bladder cancer in women (pooled European data). Cancer Causes Control 12 (5): 411-7, 2001. [PUBMED Abstract]
- Kirkali Z, Chan T, Manoharan M, et al.: Bladder cancer: epidemiology, staging and grading, and diagnosis. Urology 66 (6 Suppl 1): 4-34, 2005. [PUBMED Abstract]
- Sylvester RJ, van der Meijden AP, Oosterlinck W, et al.: Predicting recurrence and progression in individual patients with stage Ta T1 bladder cancer using EORTC risk tables: a combined analysis of 2596 patients from seven EORTC trials. Eur Urol 49 (3): 466-5; discussion 475-7, 2006. [PUBMED Abstract]
- Herr HW: Tumor progression and survival of patients with high grade, noninvasive papillary (TaG3) bladder tumors: 15-year outcome. J Urol 163 (1): 60-1; discussion 61-2, 2000. [PUBMED Abstract]
- Stein JP, Lieskovsky G, Cote R, et al.: Radical cystectomy in the treatment of invasive bladder cancer: long-term results in 1,054 patients. J Clin Oncol 19 (3): 666-75, 2001. [PUBMED Abstract]
- Madersbacher S, Hochreiter W, Burkhard F, et al.: Radical cystectomy for bladder cancer today--a homogeneous series without neoadjuvant therapy. J Clin Oncol 21 (4): 690-6, 2003. [PUBMED Abstract]
- Manoharan M, Ayyathurai R, Soloway MS: Radical cystectomy for urothelial carcinoma of the bladder: an analysis of perioperative and survival outcome. BJU Int 104 (9): 1227-32, 2009. [PUBMED Abstract]
- Loehrer PJ, Einhorn LH, Elson PJ, et al.: A randomized comparison of cisplatin alone or in combination with methotrexate, vinblastine, and doxorubicin in patients with metastatic urothelial carcinoma: a cooperative group study. J Clin Oncol 10 (7): 1066-73, 1992. [PUBMED Abstract]
- von der Maase H, Sengelov L, Roberts JT, et al.: Long-term survival results of a randomized trial comparing gemcitabine plus cisplatin, with methotrexate, vinblastine, doxorubicin, plus cisplatin in patients with bladder cancer. J Clin Oncol 23 (21): 4602-8, 2005. [PUBMED Abstract]
- Millán-Rodríguez F, Chéchile-Toniolo G, Salvador-Bayarri J, et al.: Primary superficial bladder cancer risk groups according to progression, mortality and recurrence. J Urol 164 (3 Pt 1): 680-4, 2000. [PUBMED Abstract]
- Nieder AM, Brausi M, Lamm D, et al.: Management of stage T1 tumors of the bladder: International Consensus Panel. Urology 66 (6 Suppl 1): 108-25, 2005. [PUBMED Abstract]
- Babjuk M, Oosterlinck W, Sylvester R, et al.: EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder. Eur Urol 54 (2): 303-14, 2008. [PUBMED Abstract]
- Babjuk M, Oosterlinck W, Sylvester R, et al.: EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder, the 2011 update. Eur Urol 59 (6): 997-1008, 2011. [PUBMED Abstract]
Clasificación celular del cáncer de vejiga
Más del 90 % de los cánceres de vejiga son carcinomas de células de transición derivadas del uroepitelio. Entre el 2 % y el 7 % son carcinomas de células escamosas y el 2 % son adenocarcinomas.[1] Los adenocarcinomas pueden ser de origen uracal o no uracal; se piensa que este último tipo surge, por lo general, de la metaplasia del epitelio transicional con irritación crónica. También se pueden presentar en la vejiga carcinomas de células pequeñas.[2,3] Los sarcomas de vejiga son muy poco frecuentes.
El grado patológico de los carcinomas de células de transición, que se basa en la atipia celular, las anomalías nucleares y el número de figuras mitóticas es de gran importancia pronóstica.
Bibliografía
- Al-Ahmadie H, Lin O, Reuter VE: Pathology and cytology of tumors of the urinary tract. In: Scardino PT, Linehan WM, Zelefsky MJ, et al., eds.: Comprehensive Textbook of Genitourinary Oncology. 4th ed. Lippincott Williams & Wilkins, 2011, pp 295-316.
- Koay EJ, Teh BS, Paulino AC, et al.: A Surveillance, Epidemiology, and End Results analysis of small cell carcinoma of the bladder: epidemiology, prognostic variables, and treatment trends. Cancer 117 (23): 5325-33, 2011. [PUBMED Abstract]
- Fahed E, Hansel DE, Raghavan D, et al.: Small cell bladder cancer: biology and management. Semin Oncol 39 (5): 615-8, 2012. [PUBMED Abstract]
Información sobre los estadios del cáncer de vejiga
La estadificación clínica del carcinoma de vejiga se determina por la profundidad de la invasión tumoral en la pared vesical. Esta determinación exige un examen cistoscópico que incluye una biopsia y un examen con anestesia, para evaluar los siguientes aspectos:
- Tamaño y movilidad de las masas palpables.
- Grado de induración de la pared vesical.
- Presencia de extensión extravesical o invasión de los órganos adyacentes.
La estadificación clínica, incluso cuando se utilizan tomografías computarizadas (TC) o imágenes por resonancia magnética (IRM) así como otras modalidades de imágenes, a menudo subestima el grado tumoral; en particular, de cánceres menos diferenciados y de mayor profundidad invasiva. Las imágenes con TC son la modalidad estándar de estadificación. No se ha demostrado un beneficio clínico de las IRM o las tomografías por emisión de positrones en lugar de las imágenes con TC.[1,2]
Agrupamiento por estadios y definiciones TNM del American Joint Committee on Cancer
El American Joint Committee on Cancer (AJCC) designó la estadificación según la clasificación TNM (tumor, ganglio linfático y metástasis) para definir el cáncer de vejiga.[3]
| Estadio | TNM | Descripción | Imagen |
|---|---|---|---|
| T = tumor primario; N = ganglio linfático regional; M = metástasis a distancia. | |||
| aReproducción autorizada por el AJCC: Urinary bladder. En: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 757–65. | |||
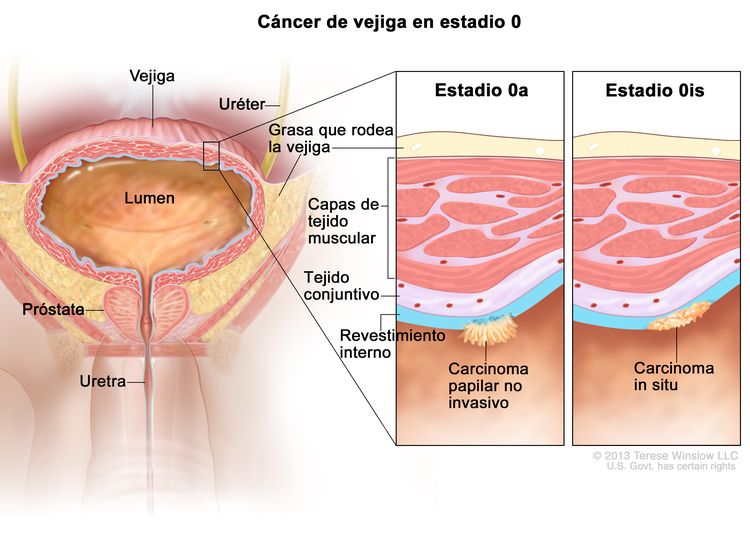
| 0a | Ta, N0, M0 | Ta = carcinoma papilar no invasivo. |
 |
| N0 = sin metástasis en ganglios linfáticos. | |||
| M0 = sin metástasis a distancia. | |||
| 0is | Tis, N0, M0 | Tis = carcinoma urotelial in situ: tumor plano. | |
| N0 = sin metástasis en ganglios linfáticos. | |||
| M0 = sin metástasis a distancia. | |||
| Estadio | TNM | Descripción | Imagen |
|---|---|---|---|
| T = tumor primario; N = ganglio linfático regional; M = metástasis a distancia. | |||
| aReproducción autorizada por el AJCC: Urinary bladder. En: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 757–65. | |||
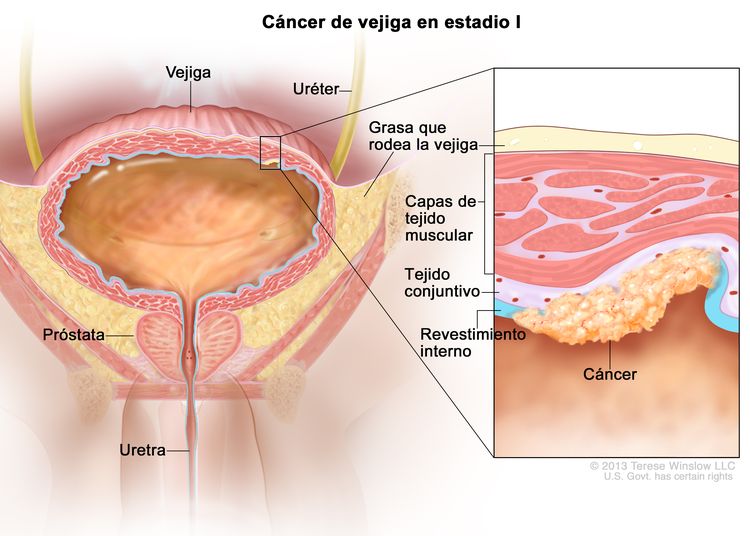
| I | T1, N0, M0 | T1 = tumor con invasión de la lámina propia (tejido conjuntivo subepitelial). |
 |
| N0 = sin metástasis en ganglios linfáticos | |||
| M0 = sin metástasis a distancia. | |||
| Estadio | TNM | Descripción | Imagen | |
|---|---|---|---|---|
| T = tumor primario; N = ganglio linfático regional; M = metástasis a distancia; p = patológico. | ||||
| aReproducción autorizada por el AJCC: Urinary bladder. En: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 757–65. | ||||
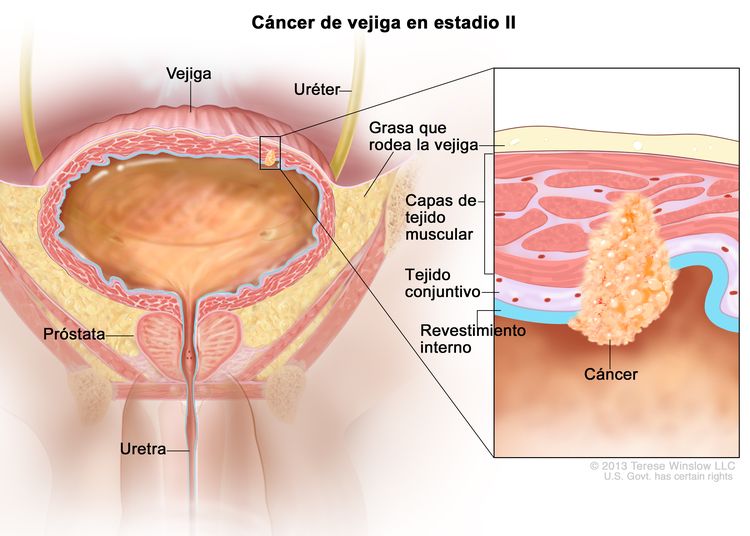
| II | T2a, N0, M0 | pT2a = tumor con invasión superficial de la capa muscular propia (mitad interna). |
 |
|
| N0 = sin metástasis en ganglios linfáticos. | ||||
| M0 = sin metástasis a distancia. | ||||
| T2b, N0, M0 | pT2b = tumor con invasión profunda de la capa muscular propia (mitad externa). | |||
| N0 = sin metástasis en ganglios linfáticos. | ||||
| M0 = sin metástasis a distancia. | ||||
| Estadio | TNM | Descripción | Imagen |
|---|---|---|---|
| T = tumor primario; N = ganglio linfático regional; M = metástasis a distancia; p = patológico. | |||
| aReproducción autorizada por el AJCC: Urinary bladder. En: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 757–65. | |||
| IIIA | T3a, T3b, T4a, N0, M0 | –pT3a = microscópico. |
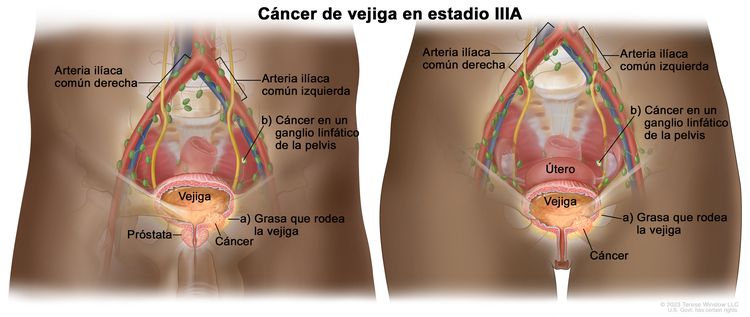 |
| –pT3b = macroscópico (masa extravesical). | |||
| –T4a = tumor extravesical con invasión directa del estroma prostático, el útero o la vagina. | |||
| N0 = sin metástasis en ganglios linfáticos. | |||
| M0 = sin metástasis a distancia. | |||
| T1–T4a, N1, M0 | T1 = tumor con invasión de la lámina propia (tejido conjuntivo subepitelial). | ||
| T2 = tumor con invasión de la capa muscular propia. | |||
| –pT2a = tumor con invasión superficial de la capa muscular propia (mitad interna). | |||
| –pT2b = tumor con invasión profunda de la capa muscular propia (mitad externa). | |||
| T3 = tumor con invasión del tejido blando perivesical. | |||
| –pT3a = microscópico. | |||
| –pT3b = macroscópico (masa extravesical). | |||
| T4 = tumor extravesical con invasión directa en cualquiera de los siguientes sitios: el estroma prostático, las vesículas seminales, el útero, la vagina, la pared pélvica o la pared abdominal. | |||
| –T4a = tumor extravesical con invasión directa del estroma prostático, el útero o la vagina. | |||
| N1 = metástasis en un solo ganglio linfático regional de la pelvis menor (ganglio linfático perivesical, del obturador, ilíaco interno o externo o sacro). | |||
| M0 = sin metástasis a distancia. | |||
| IIIB | T1–4a, N2, N3, M0 | T1 = tumor con invasión de la lámina propia (tejido conjuntivo subepitelial). |
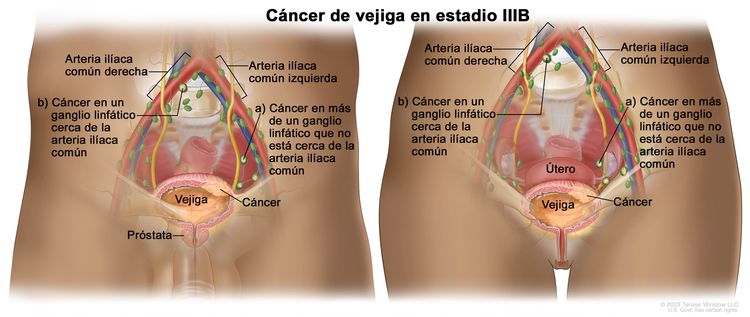 |
| T2 = tumor con invasión de la capa muscular propia. | |||
| –pT2a = tumor con invasión superficial de la capa muscular propia (mitad interna). | |||
| –pT2b = tumor con invasión profunda de la capa muscular propia (mitad externa). | |||
| T3 = tumor con invasión del tejido blando perivesical. | |||
| –pT3a = microscópico. | |||
| pT3b = macroscópico (masa extravesical). | |||
| T4 = tumor extravesical con invasión directa en cualquiera de los siguientes sitios: el estroma prostático, las vesículas seminales, el útero, la vagina, la pared pélvica o la pared abdominal. | |||
| –T4a = tumor extravesical con invasión directa del estroma prostático, el útero o la vagina. | |||
| N2 = múltiples metástasis en ganglios linfáticos regionales de la pelvis menor (metástasis en ganglio linfático perivesical, del obturador, ilíaco interno o externo o sacro). | |||
| N3 = metástasis en ganglios linfáticos de la ilíaca común. | |||
| M0 = sin metástasis a distancia. | |||
| Estadio | TNM | Descripción | Imagen | |
|---|---|---|---|---|
| T = tumor primario; N = ganglio linfático regional; M = metástasis a distancia; p = patológico. | ||||
| aReproducción autorizada por el AJCC: Urinary bladder. En: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 757–65. | ||||
| IVA | T4b, N0, M0 | T4b = tumor extravesical con invasión de la pared pélvica o la pared abdominal. |
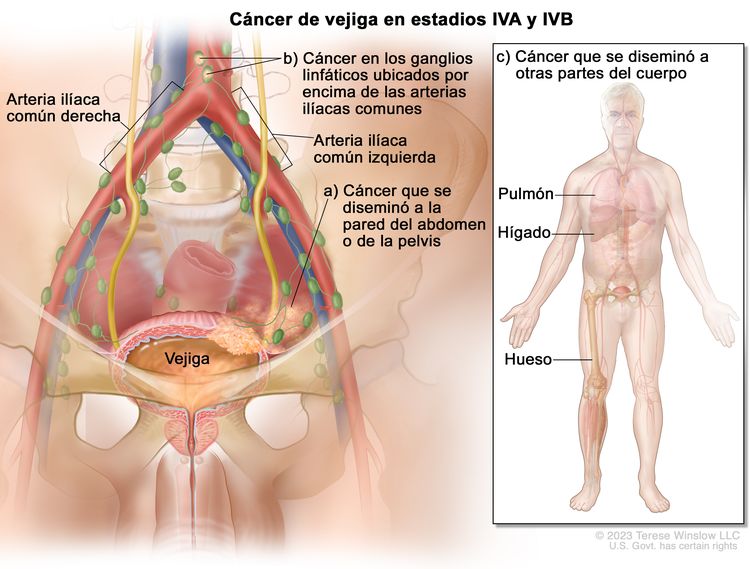 |
|
| N0 = sin metástasis en ganglios linfáticos. | ||||
| M0 = sin metástasis a distancia. | ||||
| Cualquier T, cualquier N, M1a | TX = tumor primario no evaluable. | |||
| T0 = sin indicios de tumor primario. | ||||
| Ta = carcinoma papilar no invasivo. | ||||
| Tis = carcinoma urotelial in situ: tumor plano. | ||||
| T1 = tumor con invasión de la lámina propia (tejido conjuntivo subepitelial). | ||||
| T2 = tumor con invasión de la capa muscular propia. | ||||
| –pT2a = tumor con invasión superficial de la capa muscular propia (mitad interna). | ||||
| –pT2b = tumor con invasión profunda de la capa muscular propia (mitad externa). | ||||
| T3 = tumor con invasión del tejido blando perivesical. | ||||
| –pT3a = microscópico. | ||||
| –pT3b = macroscópico (masa extravesical). | ||||
| T4 = tumor extravesical con invasión directa en cualquiera de los siguientes sitios: el estroma prostático, las vesículas seminales, el útero, la vagina, la pared pélvica o la pared abdominal. | ||||
| –T4a = tumor extravesical con invasión directa del estroma prostático, el útero o la vagina. | ||||
| T4b = tumor extravesical con invasión de la pared pélvica o la pared abdominal. | ||||
| NX = ganglios linfáticos no evaluables. | ||||
| N0 = sin metástasis en ganglios linfáticos. | ||||
| N1 = metástasis en un solo ganglio linfático regional de la pelvis menor (ganglio linfático perivesical, del obturador, ilíaco interno o externo o sacro). | ||||
| N2 = múltiples metástasis en ganglios linfáticos regionales de la pelvis menor (metástasis en ganglio linfático perivesical, del obturador, ilíaco interno o externo o sacro). | ||||
| N3 = metástasis en ganglios linfáticos de la ilíaca común. | ||||
| M0 = sin metástasis a distancia. | ||||
| M1a = metástasis a distancia limitadas a ganglios linfáticos ubicados fuera de las ilíacas comunes. | ||||
| IVB | Cualquier T, cualquier N, M1b | TX = tumor primario no evaluable. | ||
| T0 = sin indicios de tumor primario. | ||||
| Ta = carcinoma papilar no invasivo. | ||||
| Tis = carcinoma urotelial in situ: tumor plano. | ||||
| T1 = tumor con invasión de la lámina propia (tejido conjuntivo subepitelial). | ||||
| T2 = tumor con invasión de la capa muscular propia. | ||||
| –pT2a = tumor con invasión superficial de la capa muscular propia (mitad interna). | ||||
| –pT2b = tumor con invasión profunda de la capa muscular propia (mitad externa). | ||||
| T3 = tumor con invasión del tejido blando perivesical. | ||||
| –pT3a = microscópico. | ||||
| –pT3b = macroscópico (masa extravesical). | ||||
| T4 = tumor extravesical con invasión directa en cualquiera de los siguientes sitios: el estroma prostático, las vesículas seminales, el útero, la vagina, la pared pélvica o la pared abdominal. | ||||
| –T4a = tumor extravesical con invasión directa del estroma prostático, el útero o la vagina. | ||||
| –T4b = tumor extravesical con invasión de la pared pélvica o la pared abdominal. | ||||
| NX = ganglios linfáticos no evaluables. | ||||
| N0 = sin metástasis en ganglios linfáticos. | ||||
| N1 = metástasis en un solo ganglio linfático regional de la pelvis menor (ganglio linfático perivesical, del obturador, ilíaco interno o externo o sacro). | ||||
| N2 = múltiples metástasis en ganglios linfáticos regionales de la pelvis menor (metástasis en ganglio linfático perivesical, del obturador, ilíaco interno o externo o sacro). | ||||
| N3 = metástasis en ganglios linfáticos de la ilíaca común. | ||||
| M1b = sin metástasis a distancia en ganglios linfáticos. | ||||
Para los tipos histológicos uroteliales se usa una designación de grado bajo y alto para coincidir con el sistema de clasificación recomendado por la Organización Mundial de la Salud/International Society of Urologic Pathology.[3]
Para el carcinoma de células escamosas y el adenocarcinoma, se recomienda usar el modelo de grados del Cuadro 6.[3]
| G | Definición G |
|---|---|
| aReproducción autorizada por el AJCC: Urinary bladder. En: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 757–65. | |
| GX | Grado no evaluable. |
| G1 | Bien diferenciado. |
| G2 | Moderadamente diferenciado. |
| G3 | Precariamente diferenciado. |
Bibliografía
- Cowan NC, Crew JP: Imaging bladder cancer. Curr Opin Urol 20 (5): 409-13, 2010. [PUBMED Abstract]
- Green DA, Durand M, Gumpeni N, et al.: Role of magnetic resonance imaging in bladder cancer: current status and emerging techniques. BJU Int 110 (10): 1463-70, 2012. [PUBMED Abstract]
- Bochner BH, Hansel DE, Efstathiou JA, et al.: Urinary Bladder. In: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. Springer; 2017, pp 757-65.
Aspectos generales de las opciones de tratamiento del cáncer de vejiga
Cáncer de vejiga sin invasión muscular
El tratamiento de los cánceres de vejiga sin invasión muscular (Ta, Tis, T1) se basa en la estratificación del riesgo. Esencialmente, todos los pacientes se tratan al inicio con una resección transuretral (RTU) del tumor de vejiga seguida de una sola instilación inmediata de quimioterapia intravesical (en los Estados Unidos se suele usar mitomicina).[1-7]
La terapia posterior se basa en el riesgo y, por lo general, incluye uno de los siguientes procedimientos:[6-9]
- Vigilancia de la recaída o recidiva (por lo general, se utiliza para los tumores con riesgo bajo de recidiva o progresión).
- Mínimo 1 año de tratamiento intravesical con el bacilo de Calmette-Guérin (BCG), además de vigilancia de la recidiva (por lo general, se utiliza para los tumores con riesgo intermedio o alto de progresión a enfermedad con invasión muscular).
- Quimioterapia intravesical adicional (por lo general, se utiliza para los tumores con riesgo alto de recidiva, pero riesgo bajo de progresión a enfermedad con invasión muscular).
Cáncer de vejiga con invasión muscular
El tratamiento estándar para los pacientes de cáncer de vejiga con invasión muscular cuyo objetivo es la curación consiste en quimioterapia multifarmacológica neoadyuvante a base de cisplatino, seguida de cistectomía radical y derivación urinaria o radioterapia con quimioterapia simultánea.[10-13] Los siguientes son otros abordajes de tratamiento:
Muchos pacientes con diagnóstico reciente de cáncer de vejiga son aptos para participar en ensayos clínicos.
Las técnicas de reconstrucción con depósitos de almacenamiento de baja presión usando la reconfiguración del intestino delgado y grueso, eliminan la necesidad de dispositivos externos de drenaje y, en muchos pacientes, permiten el vaciado por la uretra. Estas técnicas están diseñadas para mejorar la calidad de vida de los pacientes que necesitan una cistectomía.[19]
| Estadio (criterios de estadificación TNM) | Opciones de tratamiento | |
|---|---|---|
| BCG = bacilo de Calmette-Guérin; RHE = radioterapia de haz externo; TNM = T, tamaño del tumor y cualquier diseminación del cáncer al tejido adyacente; N, diseminación del cáncer a ganglios linfáticos adyacentes; M, metástasis o diseminación del cáncer a otras partes del cuerpo; RTU = resección transuretral. | ||
| Cáncer de vejiga en estadio 0 | RTU con fulguración, seguida de una instilación inmediata de quimioterapia intravesical posoperatoria | |
| RTU con fulguración | ||
| RTU con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de instilaciones intravesicales periódicas con el BCG | ||
| RTU con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de quimioterapia intravesical | ||
| Cistectomía segmentaria (indicada con poca frecuencia) | ||
| Cistectomía radical (poco frecuente, para pacientes muy seleccionados con tumores superficiales extensos de grado alto resistentes al tratamiento) | ||
| Cáncer de vejiga en estadio I | RTU con fulguración, seguida de una instilación inmediata de quimioterapia intravesical posoperatoria | |
| RTU con fulguración | ||
| RTU con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de instilaciones intravesicales periódicas con el BCG | ||
| RTU con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de quimioterapia intravesical | ||
| Cistectomía segmentaria (indicada con poca frecuencia) | ||
| Cistectomía radical para pacientes muy seleccionados con tumores superficiales extensos o resistentes al tratamiento | ||
| Cáncer de vejiga en estadios II y III | Cistectomía radical | |
| Quimioterapia combinada neoadyuvante seguida de cistectomía radical | ||
| Cistectomía radical seguida de quimioterapia adyuvante o inmunoterapia | ||
| RHE con quimioterapia simultánea o sin esta | ||
| Cistectomía segmentaria (para pacientes seleccionados) | ||
| RTU con fulguración (para pacientes seleccionados) | ||
| Cáncer de vejiga en estadio IV | T4b, N0, M0 | Enfortumab vedotina con pembrolizumab |
| Quimioterapia con inmunoterapia | ||
| Quimioterapia sola | ||
| Terapia sistémica seguida de cistectomía radical | ||
| RHE con quimioterapia simultánea o sin esta | ||
| Derivación urinaria o cistectomía para la paliación | ||
| Cualquier T, cualquier N, M1 | Enfortumab vedotina con pembrolizumab | |
| Quimioterapia con inmunoterapia | ||
| Quimioterapia sola o adjunta al tratamiento local | ||
| Inmunoterapia | ||
| RHE para la paliación | ||
| Derivación urinaria o cistectomía para la paliación | ||
| Otros fármacos quimioterapéuticos eficaces para el tratamiento del cáncer de vejiga metastásico, como paclitaxel, docetaxel, ifosfamida, nitrato de galio y pemetrexed (en evaluación clínica) | ||
| Participación en ensayos clínicos | ||
| Cáncer de vejiga recidivante | Quimioterapia combinada | |
| Inmunoterapia | ||
| Terapia dirigida | ||
| Cirugía para tumores superficiales nuevos o localizados | ||
| Terapia paliativa | ||
| Participación en ensayos clínicos | ||
Dosificación de fluorouracilo
El gen DPYD codifica la enzima que cataboliza las pirimidinas y las fluoropirimidinas, como la capecitabina y el fluorouracilo. Se estima que entre el 1 % y el 2 % de la población tiene variantes defectuosas de DPYD que reducen la función de la proteína DPD y la acumulación de pirimidinas y fluoropirimidinas en el cuerpo.[20,21] Los pacientes con la variante DPYD*2A que reciben fluoropirimidinas quizás presenten efectos tóxicos graves que ponen en riesgo la salud, y a veces son mortales. Se han identificado muchas otras variantes de DPYD, con diferentes efectos clínicos.[20-22] Es posible que se recomiende evitar la fluoropirimidina o reducir la dosis al 50 % según el genotipo DPYD del paciente y el número de alelos funcionales de DPYD.[23-25] Las pruebas genéticas para DPYD cuestan menos de $200, pero la cobertura del seguro varía debido a la falta de directrices nacionales.[26] Además, es posible que las pruebas retrasen el tratamiento por 2 semanas, lo que no sería aconsejable en casos de urgencia. Este tema es objeto de controversia y requiere evaluación adicional.[27]
Bibliografía
- Sylvester RJ, Oosterlinck W, van der Meijden AP: A single immediate postoperative instillation of chemotherapy decreases the risk of recurrence in patients with stage Ta T1 bladder cancer: a meta-analysis of published results of randomized clinical trials. J Urol 171 (6 Pt 1): 2186-90, quiz 2435, 2004. [PUBMED Abstract]
- Mariappan P, Smith G: A surveillance schedule for G1Ta bladder cancer allowing efficient use of check cystoscopy and safe discharge at 5 years based on a 25-year prospective database. J Urol 173 (4): 1108-11, 2005. [PUBMED Abstract]
- Nieder AM, Brausi M, Lamm D, et al.: Management of stage T1 tumors of the bladder: International Consensus Panel. Urology 66 (6 Suppl 1): 108-25, 2005. [PUBMED Abstract]
- Oosterlinck W, Solsona E, Akaza H, et al.: Low-grade Ta (noninvasive) urothelial carcinoma of the bladder. Urology 66 (6 Suppl 1): 75-89, 2005. [PUBMED Abstract]
- Sylvester RJ, van der Meijden A, Witjes JA, et al.: High-grade Ta urothelial carcinoma and carcinoma in situ of the bladder. Urology 66 (6 Suppl 1): 90-107, 2005. [PUBMED Abstract]
- Babjuk M, Oosterlinck W, Sylvester R, et al.: EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder. Eur Urol 54 (2): 303-14, 2008. [PUBMED Abstract]
- Babjuk M, Oosterlinck W, Sylvester R, et al.: EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder, the 2011 update. Eur Urol 59 (6): 997-1008, 2011. [PUBMED Abstract]
- Millán-Rodríguez F, Chéchile-Toniolo G, Salvador-Bayarri J, et al.: Upper urinary tract tumors after primary superficial bladder tumors: prognostic factors and risk groups. J Urol 164 (4): 1183-7, 2000. [PUBMED Abstract]
- Millán-Rodríguez F, Chéchile-Toniolo G, Salvador-Bayarri J, et al.: Multivariate analysis of the prognostic factors of primary superficial bladder cancer. J Urol 163 (1): 73-8, 2000. [PUBMED Abstract]
- Sauer R, Birkenhake S, Kühn R, et al.: Efficacy of radiochemotherapy with platin derivatives compared to radiotherapy alone in organ-sparing treatment of bladder cancer. Int J Radiat Oncol Biol Phys 40 (1): 121-7, 1998. [PUBMED Abstract]
- Advanced Bladder Cancer Meta-analysis Collaboration: Neoadjuvant chemotherapy in invasive bladder cancer: a systematic review and meta-analysis. Lancet 361 (9373): 1927-34, 2003. [PUBMED Abstract]
- Winquist E, Kirchner TS, Segal R, et al.: Neoadjuvant chemotherapy for transitional cell carcinoma of the bladder: a systematic review and meta-analysis. J Urol 171 (2 Pt 1): 561-9, 2004. [PUBMED Abstract]
- James ND, Hussain SA, Hall E, et al.: Radiotherapy with or without chemotherapy in muscle-invasive bladder cancer. N Engl J Med 366 (16): 1477-88, 2012. [PUBMED Abstract]
- Madersbacher S, Hochreiter W, Burkhard F, et al.: Radical cystectomy for bladder cancer today--a homogeneous series without neoadjuvant therapy. J Clin Oncol 21 (4): 690-6, 2003. [PUBMED Abstract]
- Stein JP, Dunn MD, Quek ML, et al.: The orthotopic T pouch ileal neobladder: experience with 209 patients. J Urol 172 (2): 584-7, 2004. [PUBMED Abstract]
- Manoharan M, Ayyathurai R, Soloway MS: Radical cystectomy for urothelial carcinoma of the bladder: an analysis of perioperative and survival outcome. BJU Int 104 (9): 1227-32, 2009. [PUBMED Abstract]
- Widmark A, Flodgren P, Damber JE, et al.: A systematic overview of radiation therapy effects in urinary bladder cancer. Acta Oncol 42 (5-6): 567-81, 2003. [PUBMED Abstract]
- Holzbeierlein JM, Lopez-Corona E, Bochner BH, et al.: Partial cystectomy: a contemporary review of the Memorial Sloan-Kettering Cancer Center experience and recommendations for patient selection. J Urol 172 (3): 878-81, 2004. [PUBMED Abstract]
- Hautmann RE, Miller K, Steiner U, et al.: The ileal neobladder: 6 years of experience with more than 200 patients. J Urol 150 (1): 40-5, 1993. [PUBMED Abstract]
- Sharma BB, Rai K, Blunt H, et al.: Pathogenic DPYD Variants and Treatment-Related Mortality in Patients Receiving Fluoropyrimidine Chemotherapy: A Systematic Review and Meta-Analysis. Oncologist 26 (12): 1008-1016, 2021. [PUBMED Abstract]
- Lam SW, Guchelaar HJ, Boven E: The role of pharmacogenetics in capecitabine efficacy and toxicity. Cancer Treat Rev 50: 9-22, 2016. [PUBMED Abstract]
- Shakeel F, Fang F, Kwon JW, et al.: Patients carrying DPYD variant alleles have increased risk of severe toxicity and related treatment modifications during fluoropyrimidine chemotherapy. Pharmacogenomics 22 (3): 145-155, 2021. [PUBMED Abstract]
- Amstutz U, Henricks LM, Offer SM, et al.: Clinical Pharmacogenetics Implementation Consortium (CPIC) Guideline for Dihydropyrimidine Dehydrogenase Genotype and Fluoropyrimidine Dosing: 2017 Update. Clin Pharmacol Ther 103 (2): 210-216, 2018. [PUBMED Abstract]
- Henricks LM, Lunenburg CATC, de Man FM, et al.: DPYD genotype-guided dose individualisation of fluoropyrimidine therapy in patients with cancer: a prospective safety analysis. Lancet Oncol 19 (11): 1459-1467, 2018. [PUBMED Abstract]
- Lau-Min KS, Varughese LA, Nelson MN, et al.: Preemptive pharmacogenetic testing to guide chemotherapy dosing in patients with gastrointestinal malignancies: a qualitative study of barriers to implementation. BMC Cancer 22 (1): 47, 2022. [PUBMED Abstract]
- Brooks GA, Tapp S, Daly AT, et al.: Cost-effectiveness of DPYD Genotyping Prior to Fluoropyrimidine-based Adjuvant Chemotherapy for Colon Cancer. Clin Colorectal Cancer 21 (3): e189-e195, 2022. [PUBMED Abstract]
- Baker SD, Bates SE, Brooks GA, et al.: DPYD Testing: Time to Put Patient Safety First. J Clin Oncol 41 (15): 2701-2705, 2023. [PUBMED Abstract]
Tratamiento del cáncer de vejiga en estadio 0
Opciones de tratamiento para el cáncer de vejiga en estadio 0
Los pacientes con tumores de vejiga en estadio 0 se pueden curar mediante una variedad de tratamientos, aun cuando hay una tendencia alta a la formación de tumores nuevos. En una serie de pacientes con tumores Ta o T1 a quienes se les dio un seguimiento por un mínimo de 20 años o hasta que fallecieron, el riesgo de recidiva de cáncer de vejiga luego de la resección inicial fue del 80 %.[1] De mayor preocupación que la recidiva es el riesgo de progresión a una enfermedad con invasión muscular, localmente avanzada o cáncer de vejiga metastásico. Mientras que la progresión es poco frecuente en los pacientes con tumores de grado bajo, es común entre los pacientes de cánceres de grado alto.
En una serie de 125 pacientes de cáncer TaG3 seguidos durante 15 a 20 años, se notificó que el 39 % progresó a una enfermedad en estadio más avanzado, mientras que el 26 % murió por cáncer urotelial. En comparación, de 23 pacientes con tumores TaG1, ninguno murió y el 5 % progresó.[2] Los factores de riesgo para la recidiva y la progresión son los siguientes:[2-6]
- Enfermedad de grado alto.
- Carcinoma in situ.
- Tumor que mide más de 3 cm.
- Tumores múltiples.
- Antecedentes de cáncer de vejiga.
Las opciones de tratamiento para el cáncer de vejiga en estadio 0 son las siguientes:
- Resección transuretral con fulguración, seguida de una instilación inmediata de quimioterapia intravesical posoperatoria.
- Resección transuretral con fulguración.
- Resección transuretral con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de instilaciones intravesicales periódicas con el bacilo de Calmette-Guérin.
- Resección transuretral con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de quimioterapia intravesical.
- Cistectomía segmentaria (indicada con poca frecuencia).
- Cistectomía radical (poco frecuente, para pacientes muy seleccionados con tumores de grado alto superficiales extensos o resistentes al tratamiento).
Resección transuretral con fulguración, seguida de una instilación inmediata de quimioterapia intravesical posoperatoria
La resección transuretral (RTU) y la fulguración son las formas de tratamiento más comunes y conservadoras. Es importante la vigilancia cuidadosa de la progresión posterior de un tumor vesical. Debido a que la mayoría de los cánceres de vejiga recidivan después de la RTU, a menudo se administra una instilación inmediata de quimioterapia intravesical luego de una RTU. Esta práctica se evaluó en numerosos ensayos controlados aleatorizados y en un metanálisis de 7 ensayos se notificó que un tratamiento único con quimioterapia intravesical reduce las probabilidades de recidiva en el 39 % (oportunidad relativa [OR] = 0,61; P <0,0001).[7,8] Sin embargo, aunque una sola instilación de quimioterapia reduce la tasa de recaída en pacientes con tumores múltiples, la mayoría todavía recae. En consecuencia, tal tratamiento es insuficiente por sí solo para estos pacientes.
En una serie retrospectiva se subrayó la utilidad de realizar una segunda RTU después de 2 a 6 semanas de la primera.[9][Nivel de evidencia C3] Una segunda RTU realizada en 38 pacientes con enfermedad Tis o Ta reveló que 9 pacientes (24 %) tenían invasión de la lámina propia (T1) y 3 pacientes (8 %) tenían invasión muscular (T2).[9]
Dicha información puede cambiar las opciones de tratamiento definitivo para estas personas. Los pacientes con enfermedad recidivante multifocal extensa u otras características pronósticas desfavorables necesitan formas más intensivas de tratamiento.
Evidencia (resección transuretral con fulguración, seguida de una instilación inmediata de quimioterapia intravesical posoperatoria):
- En un metanálisis de 7 ensayos controlados aleatorizados realizado en 2004 (1476 pacientes con cáncer de vejiga en estadio Ta o estadio T1), se comparó la RTU sola con la RTU seguida de una única instilación inmediata de quimioterapia intravesical.[7]
- La tasa de recaída fue del 48 % en los pacientes que recibieron RTU sola y del 37 % en los pacientes que recibieron RTU con quimioterapia intravesical (OR = 0,61, P < 0,0001). El riesgo de recidiva se redujo en los pacientes con un solo tumor (OR, 0,61) o tumores múltiples (OR, 0,44), pero el 65 % de aquellos con tumores múltiples sufrieron recaídas pese a la quimioterapia intravesical.
- Los fármacos en estudio fueron la epirrubicina, la mitomicina (MMC), la tiotepa y la pirarrubicina.
- En un ensayo controlado aleatorizado multicéntrico posterior, se confirmó la reducción del riesgo de recidiva. En un estudio en el que se incluyeron 404 pacientes se notificó una tasa de recaída del 51 % en los pacientes que recibieron epirrubicina administrada inmediatamente después de la RTU y del 63 % en los pacientes que recibieron placebo administrado inmediatamente después de la RTU (P = 0,04). Sin embargo, como solo se previnieron pequeñas recidivas en este estudio, se pone en tela de juicio la magnitud del beneficio.[10]
- Del mismo modo, en otro ensayo controlado aleatorizado multicéntrico se confirmó la reducción del riesgo de recidiva. En un estudio, los pacientes (N = 305) se asignaron al azar a una instilación de epirrubicina o a ningún tratamiento adicional después de la RTU.[8]
- Las tasas de recaída fueron del 62 % en los pacientes con epirrubicina y del 77 % en el grupo control (P = 0,016).
- El cociente de riesgos instantáneos de recidiva fue de 0,56 (P = 0,002) con epirrubicina. Sin embargo, el principal beneficio se observó en pacientes con riesgo bajo de recaída. Entre los pacientes con riesgo intermedio o alto de recaída, las tasas de recaída fueron del 81 % con epirrubicina versus el 85 % sin tratamiento adicional (P = 0,35).
Resección transuretral con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de instilaciones vesicales periódicas del bacilo de Calmette-Guérin
El bacilo de Calmette-Guérin (BCG) intravesical es el tratamiento preferido para reducir el riesgo de progresión del cáncer y se utiliza principalmente para cánceres con riesgo intermedio o alto de progresión.[6,11-13] En un metanálisis con datos individuales de pacientes se comparó el uso del BCG intravesical con la MMC intravesical. En los resultados del metanálisis se observó una reducción del 32 % del riesgo de recidiva con el BCG, pero solo cuando el tratamiento con el BCG incluyó una fase de mantenimiento en la que se administró el BCG periódicamente durante 1 año como mínimo (por lo general, una fase de inducción de 6 tratamientos semanales seguida de 3 tratamientos semanales cada 3 meses).[12] La quimioterapia intravesical se tolera mejor que el BCG intravesical.[14-18] Aunque el BCG quizás no prolongue la supervivencia general para la enfermedad Tis, alcanza tasas de respuesta completa de casi el 70 %, lo que disminuye de ese modo la necesidad de una cistectomía de último recurso.[17] En los estudios se observa que el BCG intravesical demora la recidiva y la progresión tumorales.[18,19]
La terapia intravesical con tiotepa, MMC, doxorrubicina o BCG se utiliza con mayor frecuencia para pacientes con tumores múltiples o recidivantes, o como medida profiláctica para pacientes de riesgo alto después de la resección transuretral (RTU).[20-22]
Evidencia (RTU con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de instilaciones intravesicales periódicas con el BCG):
Quimioterapia intravesical
- En tres metanálisis de ensayos controlados aleatorizados en los que se comparó la RTU sola con la RTU seguida de quimioterapia intravesical, se notificó que la terapia adyuvante se relacionó con un aumento estadísticamente significativo del tiempo hasta la recidiva.[23-25] No se ha demostrado ventaja con respecto a la supervivencia o la prevención de la progresión a enfermedad invasiva o metástasis.
BCG intravesical con tratamientos de mantenimiento con el BCG
- Se publicó un metanálisis con datos individuales de pacientes de 9 ensayos aleatorizados (2820 pacientes de cáncer de vejiga Ta o T1) en los que se comparó el BCG intravesical con la MMC intravesical.[12]
- Entre los ensayos en los que el tratamiento con el BCG incluyó un componente de mantenimiento, hubo una reducción del 32 % del riesgo de recidiva (P < 0,0001) en comparación con la MMC; el BCG se relacionó con un aumento del 28 % del riesgo de recidiva cuando no se administró mantenimiento con el BCG en comparación con la MMC.
- No hubo diferencias en la progresión o el número de muertes.[12]
- Se publicó un metanálisis de nueve ensayos controlados aleatorizados (2410 pacientes) en los que se comparó el BCG intravesical con la MMC.[26]
- Se observó progresión en el 7,67 % de los pacientes que recibieron el BCG y en el 9,44 % de los pacientes que recibieron MMC en el momento de una mediana de seguimiento de 26 meses (P = 0,08).
- Cuando el análisis se limitó a los ensayos en los que el grupo del BCG incluyó un componente de mantenimiento, la tasa de progresión fue significativamente más baja en los pacientes que recibieron el BCG (OR: 0,66, intervalo de confianza 95 %, 0,47–0,94; P = 0,02).
- Se publicó un metanálisis de los resultados publicados de 9 ensayos controlados aleatorizados en los que se comparó el BCG intravesical con quimioterapia intravesical en 700 pacientes de carcinoma de vejiga in situ.[11]
- Con una mediana de seguimiento de 3,6 años, el 47 % del grupo del BCG y el 26 % del grupo de quimioterapia no presentaron indicios de la enfermedad.
- El BCG fue superior a la MMC para prevenir la recidiva solo cuando el mantenimiento con el BCG formó parte del tratamiento.
- En un ensayo controlado se evaluó a 384 pacientes asignados al azar a inducción con el BCG intravesical o a inducción intravesical con el BCG seguida de mantenimiento con el BCG intravesical.[27]
- La mediana de supervivencia sin recidiva fue de 36 meses sin mantenimiento con el BCG y de 77 meses en el grupo de mantenimiento (P < 0,0001). El riesgo de empeoramiento de la enfermedad (progresión a T2 o mayor, uso de cistectomía, quimioterapia sistémica o radioterapia) fue mayor en el grupo de inducción que en el grupo de mantenimiento (P = 0,04).
- La tasa de supervivencia general a 5 años fue del 78 % en el grupo de inducción versus el 83 % en el grupo de mantenimiento, pero esta diferencia no fue estadísticamente significativa.
El BCG se relaciona con un riesgo importante de toxicidad, que incluye muertes poco frecuentes por sepsis del BCG. En comparación con la MMC, el BCG produce más toxicidad local (44 % con el BCG vs. 30 % con la MMC) y efectos secundarios sistémicos (19 % con el BCG vs. 12 % con la MMC). Debido a la preocupación por los efectos secundarios y la toxicidad, el BCG en general no se usa para pacientes con riesgo bajo de progresión de la enfermedad a un estadio más avanzado.[6,26]
Cistectomía segmentaria (indicada con poca frecuencia)
La cistectomía segmentaria se indica con poca frecuencia.[22] Solo está indicada en unos pocos pacientes debido a la tendencia del cáncer de vejiga a comprometer múltiples regiones de la mucosa vesical y presentarse en áreas que no se pueden resecar por segmentos. Es más, la cistectomía (ya sea segmentaria o radical) por lo general no está indicada para el cáncer de vejiga T0 (ver cistectomía radical más adelante).[28,29]
Cistectomía radical (poco frecuente, para pacientes muy seleccionados con tumores de grado alto superficiales extensos o resistentes al tratamiento)
La cistectomía radical se utiliza en pacientes seleccionados con un tumor superficial extendido o resistente al tratamiento,[2,30,31] de acuerdo con informes que indican que hasta el 20 % de los pacientes con tumores Tis morirán por cáncer de vejiga. Sin embargo, la cistectomía (segmentaria o radical) a menudo no está indicada para los pacientes con cáncer de vejiga Ta o Tis. Los pacientes con riesgo alto de progresión, por lo general aquellos con tumores de grado alto recidivantes con carcinoma in situ después de la terapia intravesical con el bacilo de Calmette-Guérin (BCG), deben considerar la cistectomía radical.[32-35]
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Holmäng S, Hedelin H, Anderström C, et al.: The relationship among multiple recurrences, progression and prognosis of patients with stages Ta and T1 transitional cell cancer of the bladder followed for at least 20 years. J Urol 153 (6): 1823-6; discussion 1826-7, 1995. [PUBMED Abstract]
- Herr HW: Tumor progression and survival of patients with high grade, noninvasive papillary (TaG3) bladder tumors: 15-year outcome. J Urol 163 (1): 60-1; discussion 61-2, 2000. [PUBMED Abstract]
- Millán-Rodríguez F, Chéchile-Toniolo G, Salvador-Bayarri J, et al.: Upper urinary tract tumors after primary superficial bladder tumors: prognostic factors and risk groups. J Urol 164 (4): 1183-7, 2000. [PUBMED Abstract]
- Millán-Rodríguez F, Chéchile-Toniolo G, Salvador-Bayarri J, et al.: Multivariate analysis of the prognostic factors of primary superficial bladder cancer. J Urol 163 (1): 73-8, 2000. [PUBMED Abstract]
- Babjuk M, Oosterlinck W, Sylvester R, et al.: EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder. Eur Urol 54 (2): 303-14, 2008. [PUBMED Abstract]
- Babjuk M, Oosterlinck W, Sylvester R, et al.: EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder, the 2011 update. Eur Urol 59 (6): 997-1008, 2011. [PUBMED Abstract]
- Sylvester RJ, Oosterlinck W, van der Meijden AP: A single immediate postoperative instillation of chemotherapy decreases the risk of recurrence in patients with stage Ta T1 bladder cancer: a meta-analysis of published results of randomized clinical trials. J Urol 171 (6 Pt 1): 2186-90, quiz 2435, 2004. [PUBMED Abstract]
- Gudjónsson S, Adell L, Merdasa F, et al.: Should all patients with non-muscle-invasive bladder cancer receive early intravesical chemotherapy after transurethral resection? The results of a prospective randomised multicentre study. Eur Urol 55 (4): 773-80, 2009. [PUBMED Abstract]
- Herr HW: The value of a second transurethral resection in evaluating patients with bladder tumors. J Urol 162 (1): 74-6, 1999. [PUBMED Abstract]
- Berrum-Svennung I, Granfors T, Jahnson S, et al.: A single instillation of epirubicin after transurethral resection of bladder tumors prevents only small recurrences. J Urol 179 (1): 101-5; discussion 105-6, 2008. [PUBMED Abstract]
- Sylvester RJ, van der Meijden AP, Witjes JA, et al.: Bacillus calmette-guerin versus chemotherapy for the intravesical treatment of patients with carcinoma in situ of the bladder: a meta-analysis of the published results of randomized clinical trials. J Urol 174 (1): 86-91; discussion 91-2, 2005. [PUBMED Abstract]
- Malmström PU, Sylvester RJ, Crawford DE, et al.: An individual patient data meta-analysis of the long-term outcome of randomised studies comparing intravesical mitomycin C versus bacillus Calmette-Guérin for non-muscle-invasive bladder cancer. Eur Urol 56 (2): 247-56, 2009. [PUBMED Abstract]
- Stenzl A, Cowan NC, De Santis M, et al.: Treatment of muscle-invasive and metastatic bladder cancer: update of the EAU guidelines. Eur Urol 59 (6): 1009-18, 2011. [PUBMED Abstract]
- Herr HW, Schwalb DM, Zhang ZF, et al.: Intravesical bacillus Calmette-Guérin therapy prevents tumor progression and death from superficial bladder cancer: ten-year follow-up of a prospective randomized trial. J Clin Oncol 13 (6): 1404-8, 1995. [PUBMED Abstract]
- Sarosdy MF, Lamm DL: Long-term results of intravesical bacillus Calmette-Guerin therapy for superficial bladder cancer. J Urol 142 (3): 719-22, 1989. [PUBMED Abstract]
- Catalona WJ, Hudson MA, Gillen DP, et al.: Risks and benefits of repeated courses of intravesical bacillus Calmette-Guerin therapy for superficial bladder cancer. J Urol 137 (2): 220-4, 1987. [PUBMED Abstract]
- De Jager R, Guinan P, Lamm D, et al.: Long-term complete remission in bladder carcinoma in situ with intravesical TICE bacillus Calmette Guerin. Overview analysis of six phase II clinical trials. Urology 38 (6): 507-13, 1991. [PUBMED Abstract]
- Herr HW, Wartinger DD, Fair WR, et al.: Bacillus Calmette-Guerin therapy for superficial bladder cancer: a 10-year followup. J Urol 147 (4): 1020-3, 1992. [PUBMED Abstract]
- Lamm DL, Griffith JG: Intravesical therapy: does it affect the natural history of superficial bladder cancer? Semin Urol 10 (1): 39-44, 1992. [PUBMED Abstract]
- Igawa M, Urakami S, Shirakawa H, et al.: Intravesical instillation of epirubicin: effect on tumour recurrence in patients with dysplastic epithelium after transurethral resection of superficial bladder tumour. Br J Urol 77 (3): 358-62, 1996. [PUBMED Abstract]
- Lamm DL, Blumenstein BA, Crawford ED, et al.: A randomized trial of intravesical doxorubicin and immunotherapy with bacille Calmette-Guérin for transitional-cell carcinoma of the bladder. N Engl J Med 325 (17): 1205-9, 1991. [PUBMED Abstract]
- Soloway MS: The management of superficial bladder cancer. In: Javadpour N, ed.: Principles and Management of Urologic Cancer. 2nd ed. Williams and Wilkins, 1983, pp 446-467.
- Pawinski A, Sylvester R, Kurth KH, et al.: A combined analysis of European Organization for Research and Treatment of Cancer, and Medical Research Council randomized clinical trials for the prophylactic treatment of stage TaT1 bladder cancer. European Organization for Research and Treatment of Cancer Genitourinary Tract Cancer Cooperative Group and the Medical Research Council Working Party on Superficial Bladder Cancer. J Urol 156 (6): 1934-40, discussion 1940-1, 1996. [PUBMED Abstract]
- Huncharek M, Geschwind JF, Witherspoon B, et al.: Intravesical chemotherapy prophylaxis in primary superficial bladder cancer: a meta-analysis of 3703 patients from 11 randomized trials. J Clin Epidemiol 53 (7): 676-80, 2000. [PUBMED Abstract]
- Huncharek M, McGarry R, Kupelnick B: Impact of intravesical chemotherapy on recurrence rate of recurrent superficial transitional cell carcinoma of the bladder: results of a meta-analysis. Anticancer Res 21 (1B): 765-9, 2001 Jan-Feb. [PUBMED Abstract]
- Böhle A, Bock PR: Intravesical bacille Calmette-Guérin versus mitomycin C in superficial bladder cancer: formal meta-analysis of comparative studies on tumor progression. Urology 63 (4): 682-6; discussion 686-7, 2004. [PUBMED Abstract]
- Lamm DL, Blumenstein BA, Crissman JD, et al.: Maintenance bacillus Calmette-Guerin immunotherapy for recurrent TA, T1 and carcinoma in situ transitional cell carcinoma of the bladder: a randomized Southwest Oncology Group Study. J Urol 163 (4): 1124-9, 2000. [PUBMED Abstract]
- Holzbeierlein JM, Lopez-Corona E, Bochner BH, et al.: Partial cystectomy: a contemporary review of the Memorial Sloan-Kettering Cancer Center experience and recommendations for patient selection. J Urol 172 (3): 878-81, 2004. [PUBMED Abstract]
- Fahmy N, Aprikian A, Tanguay S, et al.: Practice patterns and recurrence after partial cystectomy for bladder cancer. World J Urol 28 (4): 419-23, 2010. [PUBMED Abstract]
- Amling CL, Thrasher JB, Frazier HA, et al.: Radical cystectomy for stages Ta, Tis and T1 transitional cell carcinoma of the bladder. J Urol 151 (1): 31-5; discussion 35-6, 1994. [PUBMED Abstract]
- Sylvester RJ, van der Meijden A, Witjes JA, et al.: High-grade Ta urothelial carcinoma and carcinoma in situ of the bladder. Urology 66 (6 Suppl 1): 90-107, 2005. [PUBMED Abstract]
- Madersbacher S, Hochreiter W, Burkhard F, et al.: Radical cystectomy for bladder cancer today--a homogeneous series without neoadjuvant therapy. J Clin Oncol 21 (4): 690-6, 2003. [PUBMED Abstract]
- Stein JP, Dunn MD, Quek ML, et al.: The orthotopic T pouch ileal neobladder: experience with 209 patients. J Urol 172 (2): 584-7, 2004. [PUBMED Abstract]
- Lerner SP, Tangen CM, Sucharew H, et al.: Failure to achieve a complete response to induction BCG therapy is associated with increased risk of disease worsening and death in patients with high risk non-muscle invasive bladder cancer. Urol Oncol 27 (2): 155-9, 2009 Mar-Apr. [PUBMED Abstract]
- Manoharan M, Ayyathurai R, Soloway MS: Radical cystectomy for urothelial carcinoma of the bladder: an analysis of perioperative and survival outcome. BJU Int 104 (9): 1227-32, 2009. [PUBMED Abstract]
Tratamiento del cáncer de vejiga en estadio I
Opciones de tratamiento para el cáncer de vejiga en estadio I
Los pacientes con tumores de vejiga en estadio I no son propensos a morir por este tipo de cáncer, pero la tendencia de formación de tumores nuevos es alta. En una serie de pacientes con tumores Ta o T1 a los que se les hizo seguimiento durante por lo menos 20 años o hasta que murieron, el riesgo de recidiva en la vejiga después la resección inicial fue del 80 %.[1] De mayor preocupación que la recidiva es el riesgo de progresión a cáncer de vejiga con invasión muscular, localmente avanzado o metastásico. Mientras que la progresión es poco frecuente en los pacientes con tumores de grado bajo, es común en los pacientes de cánceres de grado alto.
En una serie con 125 pacientes de cáncer TaG3 seguidos durante 15 a 20 años, se notificó que el 39 % progresaron a una enfermedad en estadio más avanzado, mientras que el 26 % murieron por cáncer urotelial. En comparación, de 23 pacientes con tumores TaG1, ninguno murió y el 5 % progresó.[2] Los factores de riesgo de recidiva y progresión son los siguientes:[2-6]
- Enfermedad de grado alto.
- Carcinoma in situ.
- Tumor que mide más de 3 cm.
- Tumores múltiples.
- Antecedentes de cáncer de vejiga.
Las opciones de tratamiento para el cáncer de vejiga en estadio I son las siguientes:
- Resección transuretral con fulguración, seguida de una instilación inmediata de quimioterapia intravesical posoperatoria.
- Resección transuretral con fulguración.
- Resección transuretral con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de instilaciones intravesicales periódicas con el bacilo de Calmette-Guérin.
- Resección transuretral con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de quimioterapia intravesical.
- Cistectomía segmentaria (se indica con poca frecuencia).
- Cistectomía radical (para pacientes muy seleccionados con tumores superficiales extensos o resistentes al tratamiento).
Resección transuretral con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria
La resección transuretral (RTU) y la fulguración son las formas de tratamiento más comunes y conservadoras. Es importante la vigilancia cuidadosa de la progresión posterior de un tumor vesical. Debido a que la mayoría de los cánceres de vejiga recidivan después de la RTU, a menudo se administra una instilación inmediata de quimioterapia intravesical después de una RTU. Esta práctica se evaluó en numerosos ensayos controlados aleatorizados y en un metanálisis de 7 ensayos se notificó que un tratamiento único con quimioterapia intravesical reduce las probabilidades de recidiva en el 39 % (oportunidad relativa [OR] = 0,61, P <0,0001).[7,8]
Resección transuretral con fulguración
La estadificación de un cáncer de vejiga mediante resección transuretral (RTU) se basa en la extensión de la invasión. Para evaluar si el cáncer invadió el músculo, la capa muscular propia debe estar presente en el tejido resecado. Mientras que una repetición de la RTU por lo general se considera obligatoria para cánceres de vejiga no invasivos T1 y de grado alto si no hay capa muscular propia en el tejido resecado en la primera RTU, muchos expertos recomiendan que se realice una segunda RTU de rutina dentro de las 2 a 6 semanas de la primera RTU para confirmar la estadificación y lograr una resección más completa. Esto se fundamenta en numerosos hallazgos, incluso los siguientes:
- El riesgo de recidiva local después de la RTU es alto.
- A menudo se encuentra cáncer residual cuando se repite la RTU.
- A veces, se encuentra cáncer en estadio más avanzado con la repetición de la RTU.
- Con frecuencia, se encuentra que los pacientes sometidos a cistectomía radical por un cáncer de vejiga sin invasión muscular tienen enfermedad T2 o más avanzada cuando se examina la muestra de la cistectomía.
- Un número importante de pacientes con cáncer de vejiga de grado alto sin invasión muscular, luego muere por la enfermedad.
Evidencia (repetición rutinaria de la resección transuretral):
- En una revisión de más de 2400 pacientes de más de 60 instituciones diferentes, se notificó una tasa de recidiva a 3 meses de alrededor del 14 % al 20 % después de la RTU, mientras que en una revisión de la bibliografía se notificó que hasta el 10 % de los pacientes que se sometieron a una segunda RTU por cánceres Ta a T1 se sobrestadificaron a T2.[9] La probabilidad de ser sobrestadificado a T2 es mucho mayor cuando no hay capa muscular propia en el tejido de la RTU inicial.[10]
- En una serie retrospectiva de 38 pacientes con enfermedad Tis o Ta sometidos a una segunda RTU, se encontró que 9 pacientes (24 %) tenían invasión de la lámina propia (T1) y 3 pacientes (8 %) tenían invasión muscular (T2).[11]
- En un estudio posterior de otra institución, se informó que, de 214 pacientes con cánceres Ta a T1 sometidos a una segunda RTU, se detectó cáncer residual en el 27 % de los pacientes con Ta y el 37 % de los pacientes con T1.[12]
- En una revisión de otros artículos publicados, se informó que se encontró tumor residual en el 27 al 62 % de los casos y se descubrió enfermedad con invasión muscular en el 1 al 10 % de las series de casos con 50 pacientes como mínimo.[10]
Se observó que la repetición de la RTU no reduce las tasas de recaída ni prolonga la supervivencia, pero hay una justificación clara de usarla para determinar la información precisa de la estadificación con el fin de fundamentar las decisiones de tratamiento. Es posible que dicha información cambie las opciones de tratamiento definitivo de los pacientes y permita identificar a los pacientes con más probabilidades de beneficiarse de un tratamiento más intensivo.
Resección transuretral con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de instilaciones intravesicales periódicas con el bacilo de Calmette-Guérin
El bacilo de Calmette-Guérin (BCG) intravesical es el tratamiento preferido para reducir el riesgo de progresión del cáncer y se utiliza principalmente para cánceres con riesgo intermedio o alto de progresión.[6,13-15] En un metanálisis con datos individuales de pacientes de ensayos aleatorizados en los que se comparó el uso del BCG intravesical con la mitomicina (MMC) intravesical, se notificó que hubo una reducción del 32 % del riesgo de recidiva con el BCG, pero solo cuando el tratamiento con el BCG incluyó una fase de mantenimiento en la que se administró el BCG periódicamente durante 1 año como mínimo (por lo general, una fase de inducción de 6 tratamientos semanales seguida de 3 tratamientos semanales cada 3 meses).[14] La quimioterapia intravesical se tolera mejor que el BCG intravesical.[16-20] Aunque el BCG quizás no prolongue la supervivencia general para la enfermedad Tis, alcanza tasas de respuesta completa de casi el 70 %, lo que disminuye de ese modo la necesidad de una cistectomía de último recurso.[19] En los estudios se observa que el BCG intravesical demora la recidiva y progresión tumorales.[20,21]
Evidencia (quimioterapia intravesical inmediata después de una resección transuretral):
- En un metanálisis de 7 ensayos controlados aleatorizados realizado en 2004 (1476 pacientes con cáncer de vejiga en estadio Ta o estadio T1), se comparó la resección transuretral (RTU) sola con la RTU seguida de una sola instilación inmediata de quimioterapia intravesical. Los fármacos que se estudiaron fueron epirrubicina, MMC, tiotepa y pirarrubicina.[7]
- Las tasas de recaída fueron del 48 % en los pacientes que recibieron la RTU sola y del 37 % en los pacientes que recibieron la RTU con quimioterapia intravesical (OR = 0,61, P < 0,0001). El riesgo de recidiva se redujo en los pacientes con un solo tumor (OR, 0,61) o tumores múltiples (OR, 0,44), pero el 65 % de aquellos con tumores múltiples sufrieron recaídas pese a la quimioterapia intravesical.
- En un ensayo controlado aleatorizado multicéntrico posterior, se confirmó la reducción del riesgo de recidiva. En un estudio en el que se incluyeron 404 pacientes se notificó una tasa de recaída del 51 % en los pacientes que recibieron epirrubicina administrada inmediatamente después de la RTU y del 63 % en los pacientes que recibieron placebo administrado inmediatamente después de la RTU (P = 0,04). Sin embargo, como solo se previnieron pequeñas recidivas en este estudio, se pone en tela de juicio la magnitud del beneficio.[22]
- Del mismo modo, en otro ensayo controlado aleatorizado multicéntrico se confirmó la reducción del riesgo de recidiva. En un estudio, los pacientes (N = 305) se asignaron al azar a una instilación de epirrubicina o ningún tratamiento adicional después de la RTU.[8]
- Las tasas de recaída fueron del 62 % en los pacientes que recibieron epirrubicina y del 77 % en los pacientes del grupo control (P = 0,016).
- El cociente de riesgos instantáneos de recidiva fue de 0,56 (P = 0,002) con epirrubicina. No obstante, el principal beneficio se observó en pacientes con riesgo bajo de recaída. Entre los pacientes con riesgo intermedio o alto de recaída, las tasas de recaída fueron del 81 % con epirrubicina versus el 85 % sin tratamiento adicional (P = 0,35).
Evidencia (BCG intravesical con tratamientos de mantenimiento con BCG):
- Se publicó un metanálisis con datos individuales de pacientes de 9 ensayos aleatorizados (2820 pacientes de cáncer de vejiga Ta o T1) en los que se comparó el BCG intravesical con la MMC intravesical.[14]
- Entre los ensayos en los que el tratamiento con el BCG incluyó un componente de mantenimiento, hubo una reducción del 32 % del riesgo de recidiva (P < 0,0001) en comparación con la MMC; el BCG se relacionó con un aumento del 28 % del riesgo de recidiva cuando no se administró mantenimiento con el BCG en comparación con la MMC.
- No hubo diferencias en la progresión o el número de defunciones.
- Se publicó un metanálisis de 9 ensayos controlados aleatorizados (2410 pacientes) en los que se comparó el BCG intravesical con la MMC.[23]
- Se observó progresión en el 7,67 % de los pacientes que recibieron el BCG y el 9,44 % de los pacientes que recibieron la MMC en el momento de una mediana de seguimiento de 26 meses (P = 0,08).
- Cuando el análisis se limitó a los ensayos en los que el grupo del BCG incluyó un componente de mantenimiento, la tasa de progresión fue significativamente más baja en los pacientes que recibieron el BCG (OR: 0,66, intervalo de confianza 95 %, 0,47-0,94; P = 0,02).
- Se publicó un metanálisis de los resultados publicados de 9 ensayos controlados aleatorizados en los que se comparó el BCG intravesical con quimioterapia intravesical en 700 pacientes de carcinoma de vejiga in situ.[13]
- Con una mediana de seguimiento de 3,6 años, el 47 % del grupo del BCG y el 26 % del grupo de quimioterapia no presentaron indicios de la enfermedad.
- En este metanálisis, el BCG solo fue superior a la MMC para prevenir la recidiva cuando el mantenimiento con el BCG formó parte del tratamiento.
- En un ensayo controlado se evaluó a 384 pacientes asignados al azar a inducción con el BCG intravesical o a inducción intravesical con el BCG seguida de mantenimiento con el BCG intravesical.[24]
- La mediana de supervivencia sin recidiva fue de 36 meses sin mantenimiento con el BCG y de 77 meses en el grupo de mantenimiento (P < 0,0001). El riesgo de empeoramiento de la enfermedad (progresión a T2 o mayor, uso de cistectomía, quimioterapia sistémica o radioterapia) fue mayor en el grupo de inducción que en el grupo de mantenimiento (P = 0,04).
- La supervivencia general a 5 años fue del 78 % en el grupo de inducción sola versus el 83 % en el grupo de mantenimiento, pero esta diferencia no fue estadísticamente significativa.
El BCG se relaciona con un riesgo importante de toxicidad, que incluye muertes poco frecuentes por sepsis del BCG. En comparación con la MMC, el BCG produce más toxicidad local (44 % con el BCG vs. 30 % con la MMC) y efectos secundarios sistémicos (19 % con el BCG vs. 12 % con la MMC). Debido a la preocupación por los efectos secundarios y la toxicidad, el BCG en general no se usa para pacientes con riesgo bajo de progresión de la enfermedad a un estadio más avanzado.[6,23]
Evidencia (2 ciclos de tratamiento con el BCG intravesical):
- Es posible que se necesiten 2 ciclos no consecutivos de 6 semanas con el BCG para obtener un respuesta óptima.[25] Los pacientes con un tumor T1 en la evaluación realizada 3 meses después de un ciclo de 6 semanas del BCG y los pacientes con Tis que persiste después del segundo ciclo de 3 semanas del BCG tienen una probabilidad alta de presentar una enfermedad con invasión muscular y se deben considerar para una cistectomía.[18,25,26]
Resección transuretral con fulguración seguida de una instilación inmediata de quimioterapia intravesical posoperatoria, seguida de quimioterapia intravesical
La terapia intravesical con tiotepa, mitomicina, doxorrubicina o el BCG se utiliza con mayor frecuencia para pacientes con tumores múltiples o recidivantes, o como medida profiláctica para pacientes de riesgo alto después de la resección transuretral (RTU).[27,28]
Evidencia (quimioterapia intravesical):
- En tres metanálisis de ensayos controlados aleatorizados en los que se comparó la RTU sola con la RTU seguida de quimioterapia intravesical, se notificó que la terapia adyuvante se relacionó con un aumento estadísticamente significativo del tiempo hasta la recidiva. No se ha demostrado ventaja con respecto a la supervivencia o la prevención de la progresión de la enfermedad invasiva o las metástasis.[29-31]
- En un análisis de 8 estudios con 1609 pacientes, se informó que la quimioterapia intravesical redujo el riesgo de recaída a 1 año en el 38 % y hasta el 70 % a los 3 años, según los fármacos utilizados.[30]
- En otro análisis de 11 estudios con 3703 pacientes, se notificó una reducción del 44 % en las tasas de recidiva a 1 año.[30]
- En un estudio anterior de 2535 pacientes que participaron en 6 ensayos controlados aleatorizados diferentes, se notificó una disminución del riesgo de recidiva, pero no un beneficio significativo en relación con el riesgo de progresión de la enfermedad a un estadio más avanzado o la supervivencia.[29]
Cistectomía segmentaria (indicada con poca frecuencia)
La cistectomía segmentaria se indica con poca frecuencia.[32] Solo está indicada para relativamente pocos pacientes debido a la tendencia del carcinoma de vejiga a comprometer múltiples regiones de la mucosa vesical y presentarse en áreas que no se pueden resecar por segmentos. Es más, la cistectomía (segmentaria o radical) por lo general no está indicada para los pacientes con cáncer de vejiga T0.[33,34]
Cistectomía radical para pacientes seleccionados con tumores superficiales extensos o resistentes al tratamiento
La cistectomía radical se utiliza para pacientes seleccionados con tumores superficiales extensos o resistentes al tratamiento.[35-43] Los pacientes con riesgo alto de progresión, por lo general aquellos con tumores recidivantes de grado alto con carcinoma in situ después de la terapia intravesical con el BCG, deben considerar la cistectomía radical. Otros factores de riesgo son los tumores múltiples y los tumores mayores de 3 cm.
Ciertos pacientes de cáncer de vejiga sin invasión muscular enfrentan un riesgo sustancial de progresión y muerte por sus cánceres.
Evidencia (cistectomía radical):
- En un análisis de 307 pacientes inscritos en los estudios del BCG intravesical en la década de 1980, se informó que, de 85 pacientes con recidiva T1, 60 progresaron por lo menos a enfermedad en estadio II. A los 5 años de la recidiva T1, el 71 % progresaron y el 48 % murieron por su cáncer.[44]
- En comparación, en otra cohorte de 589 pacientes tratados con el BCG entre 1992 y 2004, 65 de los 120 pacientes con recidiva T1 se sometieron a una cistectomía inmediata. De todos los pacientes con recidiva T1, el 28 % progresó a enfermedad en estadio más alto y el 31 % murió por su cáncer. Si bien estos datos confirman que los pacientes con cáncer recidivante después del tratamiento con el BCG intravesical enfrentan un riesgo considerable de morir por su enfermedad, no proporcionan evidencia sólida de que una cistectomía inmediata produzca un riesgo más bajo de muerte o progresión.[44]
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Holmäng S, Hedelin H, Anderström C, et al.: The relationship among multiple recurrences, progression and prognosis of patients with stages Ta and T1 transitional cell cancer of the bladder followed for at least 20 years. J Urol 153 (6): 1823-6; discussion 1826-7, 1995. [PUBMED Abstract]
- Herr HW: Tumor progression and survival of patients with high grade, noninvasive papillary (TaG3) bladder tumors: 15-year outcome. J Urol 163 (1): 60-1; discussion 61-2, 2000. [PUBMED Abstract]
- Millán-Rodríguez F, Chéchile-Toniolo G, Salvador-Bayarri J, et al.: Upper urinary tract tumors after primary superficial bladder tumors: prognostic factors and risk groups. J Urol 164 (4): 1183-7, 2000. [PUBMED Abstract]
- Millán-Rodríguez F, Chéchile-Toniolo G, Salvador-Bayarri J, et al.: Multivariate analysis of the prognostic factors of primary superficial bladder cancer. J Urol 163 (1): 73-8, 2000. [PUBMED Abstract]
- Babjuk M, Oosterlinck W, Sylvester R, et al.: EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder. Eur Urol 54 (2): 303-14, 2008. [PUBMED Abstract]
- Babjuk M, Oosterlinck W, Sylvester R, et al.: EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder, the 2011 update. Eur Urol 59 (6): 997-1008, 2011. [PUBMED Abstract]
- Sylvester RJ, Oosterlinck W, van der Meijden AP: A single immediate postoperative instillation of chemotherapy decreases the risk of recurrence in patients with stage Ta T1 bladder cancer: a meta-analysis of published results of randomized clinical trials. J Urol 171 (6 Pt 1): 2186-90, quiz 2435, 2004. [PUBMED Abstract]
- Gudjónsson S, Adell L, Merdasa F, et al.: Should all patients with non-muscle-invasive bladder cancer receive early intravesical chemotherapy after transurethral resection? The results of a prospective randomised multicentre study. Eur Urol 55 (4): 773-80, 2009. [PUBMED Abstract]
- Brausi M, Collette L, Kurth K, et al.: Variability in the recurrence rate at first follow-up cystoscopy after TUR in stage Ta T1 transitional cell carcinoma of the bladder: a combined analysis of seven EORTC studies. Eur Urol 41 (5): 523-31, 2002. [PUBMED Abstract]
- Jakse G, Algaba F, Malmström PU, et al.: A second-look TUR in T1 transitional cell carcinoma: why? Eur Urol 45 (5): 539-46; discussion 546, 2004. [PUBMED Abstract]
- Herr HW: The value of a second transurethral resection in evaluating patients with bladder tumors. J Urol 162 (1): 74-6, 1999. [PUBMED Abstract]
- Zurkirchen MA, Sulser T, Gaspert A, et al.: Second transurethral resection of superficial transitional cell carcinoma of the bladder: a must even for experienced urologists. Urol Int 72 (2): 99-102, 2004. [PUBMED Abstract]
- Sylvester RJ, van der Meijden AP, Witjes JA, et al.: Bacillus calmette-guerin versus chemotherapy for the intravesical treatment of patients with carcinoma in situ of the bladder: a meta-analysis of the published results of randomized clinical trials. J Urol 174 (1): 86-91; discussion 91-2, 2005. [PUBMED Abstract]
- Malmström PU, Sylvester RJ, Crawford DE, et al.: An individual patient data meta-analysis of the long-term outcome of randomised studies comparing intravesical mitomycin C versus bacillus Calmette-Guérin for non-muscle-invasive bladder cancer. Eur Urol 56 (2): 247-56, 2009. [PUBMED Abstract]
- Stenzl A, Cowan NC, De Santis M, et al.: Treatment of muscle-invasive and metastatic bladder cancer: update of the EAU guidelines. Eur Urol 59 (6): 1009-18, 2011. [PUBMED Abstract]
- Herr HW, Schwalb DM, Zhang ZF, et al.: Intravesical bacillus Calmette-Guérin therapy prevents tumor progression and death from superficial bladder cancer: ten-year follow-up of a prospective randomized trial. J Clin Oncol 13 (6): 1404-8, 1995. [PUBMED Abstract]
- Sarosdy MF, Lamm DL: Long-term results of intravesical bacillus Calmette-Guerin therapy for superficial bladder cancer. J Urol 142 (3): 719-22, 1989. [PUBMED Abstract]
- Catalona WJ, Hudson MA, Gillen DP, et al.: Risks and benefits of repeated courses of intravesical bacillus Calmette-Guerin therapy for superficial bladder cancer. J Urol 137 (2): 220-4, 1987. [PUBMED Abstract]
- De Jager R, Guinan P, Lamm D, et al.: Long-term complete remission in bladder carcinoma in situ with intravesical TICE bacillus Calmette Guerin. Overview analysis of six phase II clinical trials. Urology 38 (6): 507-13, 1991. [PUBMED Abstract]
- Herr HW, Wartinger DD, Fair WR, et al.: Bacillus Calmette-Guerin therapy for superficial bladder cancer: a 10-year followup. J Urol 147 (4): 1020-3, 1992. [PUBMED Abstract]
- Lamm DL, Griffith JG: Intravesical therapy: does it affect the natural history of superficial bladder cancer? Semin Urol 10 (1): 39-44, 1992. [PUBMED Abstract]
- Berrum-Svennung I, Granfors T, Jahnson S, et al.: A single instillation of epirubicin after transurethral resection of bladder tumors prevents only small recurrences. J Urol 179 (1): 101-5; discussion 105-6, 2008. [PUBMED Abstract]
- Böhle A, Bock PR: Intravesical bacille Calmette-Guérin versus mitomycin C in superficial bladder cancer: formal meta-analysis of comparative studies on tumor progression. Urology 63 (4): 682-6; discussion 686-7, 2004. [PUBMED Abstract]
- Lamm DL, Blumenstein BA, Crissman JD, et al.: Maintenance bacillus Calmette-Guerin immunotherapy for recurrent TA, T1 and carcinoma in situ transitional cell carcinoma of the bladder: a randomized Southwest Oncology Group Study. J Urol 163 (4): 1124-9, 2000. [PUBMED Abstract]
- Coplen DE, Marcus MD, Myers JA, et al.: Long-term followup of patients treated with 1 or 2, 6-week courses of intravesical bacillus Calmette-Guerin: analysis of possible predictors of response free of tumor. J Urol 144 (3): 652-7, 1990. [PUBMED Abstract]
- Herr HW: Progression of stage T1 bladder tumors after intravesical bacillus Calmette-Guerin. J Urol 145 (1): 40-3; discussion 43-4, 1991. [PUBMED Abstract]
- Igawa M, Urakami S, Shirakawa H, et al.: Intravesical instillation of epirubicin: effect on tumour recurrence in patients with dysplastic epithelium after transurethral resection of superficial bladder tumour. Br J Urol 77 (3): 358-62, 1996. [PUBMED Abstract]
- Rintala E, Jauhiainen K, Kaasinen E, et al.: Alternating mitomycin C and bacillus Calmette-Guerin instillation prophylaxis for recurrent papillary (stages Ta to T1) superficial bladder cancer. Finnbladder Group. J Urol 156 (1): 56-9; discussion 59-60, 1996. [PUBMED Abstract]
- Pawinski A, Sylvester R, Kurth KH, et al.: A combined analysis of European Organization for Research and Treatment of Cancer, and Medical Research Council randomized clinical trials for the prophylactic treatment of stage TaT1 bladder cancer. European Organization for Research and Treatment of Cancer Genitourinary Tract Cancer Cooperative Group and the Medical Research Council Working Party on Superficial Bladder Cancer. J Urol 156 (6): 1934-40, discussion 1940-1, 1996. [PUBMED Abstract]
- Huncharek M, Geschwind JF, Witherspoon B, et al.: Intravesical chemotherapy prophylaxis in primary superficial bladder cancer: a meta-analysis of 3703 patients from 11 randomized trials. J Clin Epidemiol 53 (7): 676-80, 2000. [PUBMED Abstract]
- Huncharek M, McGarry R, Kupelnick B: Impact of intravesical chemotherapy on recurrence rate of recurrent superficial transitional cell carcinoma of the bladder: results of a meta-analysis. Anticancer Res 21 (1B): 765-9, 2001 Jan-Feb. [PUBMED Abstract]
- Soloway MS: The management of superficial bladder cancer. In: Javadpour N, ed.: Principles and Management of Urologic Cancer. 2nd ed. Williams and Wilkins, 1983, pp 446-467.
- Holzbeierlein JM, Lopez-Corona E, Bochner BH, et al.: Partial cystectomy: a contemporary review of the Memorial Sloan-Kettering Cancer Center experience and recommendations for patient selection. J Urol 172 (3): 878-81, 2004. [PUBMED Abstract]
- Fahmy N, Aprikian A, Tanguay S, et al.: Practice patterns and recurrence after partial cystectomy for bladder cancer. World J Urol 28 (4): 419-23, 2010. [PUBMED Abstract]
- Lambert EH, Pierorazio PM, Olsson CA, et al.: The increasing use of intravesical therapies for stage T1 bladder cancer coincides with decreasing survival after cystectomy. BJU Int 100 (1): 33-6, 2007. [PUBMED Abstract]
- Skinner EC: The best treatment for high-grade T1 bladder cancer is cystectomy. Urol Oncol 25 (6): 523-5, 2007 Nov-Dec. [PUBMED Abstract]
- Stein JP, Penson DF: Invasive T1 bladder cancer: indications and rationale for radical cystectomy. BJU Int 102 (3): 270-5, 2008. [PUBMED Abstract]
- Boström PJ, Alkhateeb S, van Rhijn BW, et al.: Optimal timing of radical cystectomy in T1 high-grade bladder cancer. Expert Rev Anticancer Ther 10 (12): 1891-902, 2010. [PUBMED Abstract]
- Fritsche HM, Burger M, Svatek RS, et al.: Characteristics and outcomes of patients with clinical T1 grade 3 urothelial carcinoma treated with radical cystectomy: results from an international cohort. Eur Urol 57 (2): 300-9, 2010. [PUBMED Abstract]
- Ali-El-Dein B, Al-Marhoon MS, Abdel-Latif M, et al.: Survival after primary and deferred cystectomy for stage T1 transitional cell carcinoma of the bladder. Urol Ann 3 (3): 127-32, 2011. [PUBMED Abstract]
- Canter D, Egleston B, Wong YN, et al.: Use of radical cystectomy as initial therapy for the treatment of high-grade T1 urothelial carcinoma of the bladder: a SEER database analysis. Urol Oncol 31 (6): 866-70, 2013. [PUBMED Abstract]
- Chalasani V, Kassouf W, Chin JL, et al.: Radical cystectomy for the treatment of T1 bladder cancer: the Canadian Bladder Cancer Network experience. Can Urol Assoc J 5 (2): 83-7, 2011. [PUBMED Abstract]
- Segal R, Yafi FA, Brimo F, et al.: Prognostic factors and outcome in patients with T1 high-grade bladder cancer: can we identify patients for early cystectomy? BJU Int 109 (7): 1026-30, 2012. [PUBMED Abstract]
- Raj GV, Herr H, Serio AM, et al.: Treatment paradigm shift may improve survival of patients with high risk superficial bladder cancer. J Urol 177 (4): 1283-6; discussion 1286, 2007. [PUBMED Abstract]
Tratamiento del cáncer de vejiga en estadios II y III
Opciones de tratamiento para el cáncer de vejiga en estadios II y III
Las opciones de tratamiento para el cáncer de vejiga en estadio II y cáncer de vejiga en estadio III son las siguientes:
- Cistectomía radical.
- Quimioterapia combinada neoadyuvante seguida de cistectomía radical.
- Cistectomía radical seguida de quimioterapia adyuvante o inmunoterapia.
- Radioterapia de haz externo con terapia hormonal o sin esta.
- Cistectomía segmentaria (para pacientes seleccionados).
- Resección transuretral con fulguración (para pacientes seleccionados).
Los tratamientos más comunes para el cáncer de vejiga con invasión muscular son la cistectomía radical y la radioterapia. No hay evidencia sólida de ensayos controlados aleatorizados para determinar si la cirugía o la radioterapia son más eficaces. Hay evidencia sólida de que ambos tratamientos son más eficaces cuando se combinan con quimioterapia. Los tratamientos con el mayor nivel de evidencia científica que apoyan su eficacia son la cistectomía radical precedida de quimioterapia multifarmacológica a base de cisplatino y radioterapia con quimioterapia simultánea.
Cistectomía radical
La cistectomía radical es una opción de tratamiento estándar para el cáncer de vejiga en estadio II y estadio III; su eficacia para prolongar la supervivencia aumenta si va precedida de quimioterapia multifarmacológica a base de cisplatino.[1-4] La cistectomía radical se acompaña de disección de los ganglios linfáticos pélvicos e incluye la extirpación de la vejiga, los tejidos perivesicales, la próstata y las vesículas seminales en los hombres y la extirpación del útero, las trompas de Falopio, los ovarios, la pared vaginal anterior y la uretra en las mujeres.[5-8] En los estudios de los desenlaces después de una cistectomía radical, se notifica un aumento de la supervivencia en los pacientes que tenían más, en vez que menos, ganglios linfáticos resecados; no se sabe si esto representa un beneficio terapéutico de la resección de ganglios adicionales o una migración de estadio.[9] No hay ensayos controlados aleatorizados para evaluar el beneficio terapéutico de la disección de ganglios linfáticos en este entorno.
La cistectomía radical es una operación mayor con una tasa de mortalidad perioperatoria del 2 % al 3 % cuando se lleva a cabo en centros de excelencia.[6-8] Las complicaciones posoperatorias incluyen el íleo. La mayoría de los hombres sufren de disfunción eréctil después de la cistectomía radical; la disfunción sexual después de esta operación también es común en las mujeres.[10-12]
En un estudio de 27 mujeres sometidas a cistectomía radical, se notificó disminución de la capacidad de tener un orgasmo en el 45 %, disminución de la lubricación en el 41 %, disminución del deseo sexual en el 37 % y dolor durante el coito vaginal en el 22 %. Menos de la mitad logró tener relaciones sexuales vaginales exitosas y la mayoría informó una disminución de la satisfacción en su vida sexual después de la cirugía.[12] Los estudios indican que se puede realizar una cistectomía radical con preservación del funcionamiento sexual en algunos hombres. Además, las nuevas formas de derivación urinaria pueden obviar la necesidad de un artefacto urinario externo.[13-16]
En un análisis retrospectivo de una sola institución, se encontró que los pacientes de edad avanzada (≥ 70 años) en buen estado de salud obtienen resultados clínicos y funcionales después de la cistectomía radical similares a los de los pacientes más jóvenes.[17]
Sin embargo, después de una cistectomía radical todavía hay alrededor del 30 % al 40 % de riesgo de recidiva para los pacientes con enfermedad invasiva del músculo, incluso en centros de excelencia.[6-8] Se informó que las tasas de supervivencia general (SG) a 5 años están entre el 50 % y el 60 %, pero estas tasas varían según el estadio del cáncer.[4] En un ensayo aleatorizado prospectivo, la adición de radioterapia preoperatoria a la cistectomía radical no aportó ventaja alguna para la supervivencia cuando se comparó con la cistectomía radical sola.[18]
Quimioterapia combinada neoadyuvante seguida de cistectomía radical
Dado que el cáncer de vejiga recidiva por lo común con metástasis a distancia, se evaluó la administración de quimioterapia sistémica antes o después de la cistectomía como un medio para mejorar los desenlaces. La administración de quimioterapia antes de la cistectomía (es decir, quimioterapia neoadyuvante) tal vez se prefiera al tratamiento posoperatorio porque la subestadificación del tumor mediante quimioterapia puede aumentar la resecabilidad; la enfermedad metastásica oculta se trata tan pronto como sea posible y es probable que se tolere mejor la quimioterapia. En la actualidad, el conjunto de pruebas que respalda la quimioterapia preoperatoria es mucho más fuerte que la evidencia que respalda la quimioterapia posoperatoria.
Evidencia (quimioterapia combinada neoadyuvante seguida de cistectomía radical):
- En un ensayo controlado de quimioterapia preoperatoria realizado por el Medical Research Council y la European Organisation for Research and Treatment of Cancer, se asignó al azar a 976 pacientes con cáncer de vejiga localmente avanzado (T3 o T4a) o de grado alto con invasión muscular (T2) a someterse de inmediato a tratamiento definitivo o después de 3 ciclos de cisplatino, vinblastina y metotrexato neoadyuvantes.[19,20] En este estudio, el tratamiento definitivo consistió en cistectomía radical (n = 428), radioterapia (n = 403) o radioterapia preoperatoria seguida de cistectomía radical (n = 66).
- Con una mediana de seguimiento de 8,0 años para los pacientes todavía vivos, la SG fue significativamente mayor en el grupo asignado al azar para recibir quimioterapia neoadyuvante (coeficiente de riesgos instantáneos [CRI], 0,84; intervalo de confianza [IC] 95 %, 0,72–0,99; P = 0,037). El beneficio para la supervivencia de la quimioterapia neoadyuvante en comparación con el tratamiento definitivo solo confiere un aumento absoluto del 6 % de la verosimilitud de estar vivo a los 3 años (56 vs. 50 %), a los 5 años (49 vs. 43 %) y a los 10 años (36 vs. 30 %).[20][Nivel de evidencia A1]
- En un estudio aleatorizado llevado a cabo por el Southwest Oncology Group, se compararon tres ciclos de cisplatino, metotrexato, vinblastina y doxorrubicina neoadyuvantes administrados antes de la cistectomía con la cistectomía sola en 317 pacientes de cáncer de vejiga en estadios T2 a T4a.[21]
- En el estudio se observó que la tasa de supervivencia a 5 años fue del 57 % para el grupo que recibió quimioterapia adyuvante y del 43 % para el grupo tratado con cistectomía sola, que es una diferencia con significación estadística marginal (valor bilateral de P = 0,06 mediante prueba del orden logarítmico).
- No hubo muertes relacionadas con la quimioterapia neoadyuvante y no hubo diferencia en la tasa o la gravedad de las complicaciones posoperatorias en los pacientes que recibieron cirugía inmediata y en aquellos que recibieron quimioterapia preoperatoria. Como estaba previsto, se sometió a cistectomía al 82 % de los pacientes asignados a quimioterapia preoperatoria y el 81 % de los asignados a cistectomía sola. Este estudio proporciona evidencia de que la quimioterapia preoperatoria no impide que los pacientes se sometan a una cistectomía y no aumenta el riesgo de complicaciones perioperatorias.
- De los pacientes que recibieron quimioterapia neoadyuvante, el 38 % tuvieron una respuesta patológica completa en el momento de la cirugía y el 85 % de quienes lograron una respuesta patológica completa estaban vivos a los 5 años.
- En un metanálisis de 10 ensayos aleatorizados con quimioterapia neoadyuvante, que incluyó datos actualizados de 2688 pacientes, se observó que la quimioterapia combinada a base de cisplatino se relacionó con una reducción relativa significativa del 13 % del riesgo de muerte y mejoró las tasas de supervivencia a 5 años del 45 % al 50 % (P = 0,016). El cisplatino neoadyuvante como sustancia única no se relacionó con ningún beneficio de supervivencia en el metanálisis.[2]
- En un metanálisis posterior, se evaluó un conjunto casi idéntico de datos (11 ensayos controlados aleatorizados con 2605 pacientes) y se llegó a conclusiones similares. Cuando el análisis se limitó a los 8 ensayos en los que se usó quimioterapia multifarmacológica a base de cisplatino, la quimioterapia neoadyuvante en comparación con la cistectomía sola se relacionó con un beneficio absoluto del 6,5 % de la tasa de SG a 5 años (56,5 vs. 50 %; P = 0,006).[4]
La mayoría de los pacientes incluidos en estos estudios recibió cisplatino, metotrexato y vinblastina con doxorrubicina o sin esta. No se sabe si el régimen doble de cisplatino y gemcitabina ofrece algún beneficio cuando se administran en el entorno preoperatorio, ni hay evidencia de beneficio para los regímenes de quimioterapia a base de carboplatino.
Sobre la base de estos hallazgos, la quimioterapia combinada preoperatoria a base de cisplatino seguida de cistectomía radical representa una opción terapéutica estándar para los pacientes de cáncer de vejiga con invasión muscular que son aptos para recibir quimioterapia y para quienes la prioridad es aumentar al máximo la supervivencia.
Cistectomía radical seguida de quimioterapia adyuvante o inmunoterapia
Quimioterapia adyuvante
En numerosos ensayos, se ha investigado si la administración de quimioterapia después de una cistectomía radical mejora la supervivencia sin progresión (SSP) y la SG. Aunque en algunos ensayos se ha observado beneficio para la SSP de la quimioterapia postoperatoria a base de cisplatino, los ensayos suelen ser pequeños y de poca potencia, y ninguno demostró algún beneficio convincente para la SG.
Evidencia (quimioterapia adyuvante):
- En una revisión sistemática y en un metanálisis se evaluaron 9 ensayos controlados aleatorizados en los que participaron 945 pacientes. Se usaron diversos regímenes de quimioterapia a base de cisplatino.[22][Nivel de evidencia A2]
- En este análisis se informó de un beneficio significativo para la SG en los pacientes que recibieron quimioterapia adyuvante (CRI, 0,77; IC 95 %, 0,49–0,99).
- El beneficio en la supervivencia sin enfermedad (SSE) fue similar (CRI, 0,66; IC 95 %, 0,45–0,91).
Inmunoterapia adyuvante
Evidencia (inmunoterapia adyuvante):
- En un ensayo controlado aleatorizado, se comparó el nivolumab con placebo en 709 pacientes con carcinoma urotelial de grados patológicos T3, T4 o con compromiso ganglionar e invasión muscular que se habían sometido a cistectomía radical. Es importante mencionar que los pacientes en este ensayo recibieron quimioterapia preoperatoria a base de cisplatino, rechazaron la quimioterapia postoperatoria a base de cisplatino o no se les consideró aptos para recibir quimioterapia a base de cisplatino.[23][Nivel de evidencia B1]
- Cuando se analizaron en el momento de una mediana de seguimiento de 20 meses, no hubo ninguna diferencia en la SG.
- Se informó de una diferencia importante en la SSE (criterio principal de valoración) para los pacientes con una expresión alta del ligando 1 de muerte celular programada (PD-L1). La mediana de SSE fue de 20,8 meses (IC 95 %, 16,5–27,6) en el grupo de nivolumab y de 10,8 meses (IC 95 %, 8,3–13,9) en el grupo de placebo. La tasa de SSE a 6 meses fue del 74,9 % para los pacientes que recibieron nivolumab y del 60,3 % para los que recibieron placebo (CRI, 0,70; IC 98 %, 0,55–0,90). Sin embargo, no hubo ningún beneficio significativo para los pacientes con una expresión baja (<1 %) de PD-L1.
- Se observaron eventos adversos de grado 3 o superior en el 42,7 % de los pacientes en el grupo de nivolumab y en el 36,8 % de los del grupo de placebo. Se observaron eventos adversos de grado alto relacionados con el tratamiento en el 17,9 % de los pacientes en el grupo de nivolumab y en el 7,2 % de los del grupo de placebo. Los eventos adversos más comunes fueron prurito, fatiga y diarrea, mientras que la mayoría de los eventos adversos de grado alto fueron concentraciones altas de lipasa o amilasa, diarrea, colitis y neumonitis. En el grupo de nivolumab, 2 pacientes murieron por neumonitis, y 1 paciente murió debido a una perforación intestinal.
- Los datos de la SG (criterio secundario de valoración) son preliminares.
Radioterapia de haz externo con quimioterapia simultánea o sin esta
La radioterapia definitiva es una opción estándar que produce tasas de supervivencia a 5 años de alrededor del 30 % al 40 %.[24] Los resultados mejoran cuando la radioterapia y la quimioterapia se administran de forma simultánea. Sin embargo, mientras que se observó que la adición de quimioterapia a la radioterapia reduce las tasas de recaídas locales, no se observó que aumente la supervivencia, reduzca la mortalidad o mejore de la calidad de vida.
La mayoría de los protocolos para preservar la vejiga que utilizan una combinación de quimioterapia y radioterapia han seguido un algoritmo relativamente complejo. Después de la etapa inicial de resección transuretral (RTU) del tumor de vejiga, los pacientes se someten a una repetición de la RTU para resecar al máximo el tumor. A continuación, se trata al paciente con quimiorradioterapia sincrónica en una dosis de casi 40 Gy, seguida de una repetición de la cistoscopia con biopsias para evaluar si hay cáncer residual. Si se detecta cáncer residual en el estudio histopatológico, se considera que la quimiorradioterapia fracasó y se aconseja que el paciente se someta a una cistectomía radical. Si las biopsias después de dosis de 40 Gy son benignas, a continuación se completa la quimiorradioterapia con una dosis de cerca de 65 Gy.
Con la radioterapia definitiva, los mejores resultados se observan en pacientes con lesiones solitarias y sin carcinoma in situ ni hidronefrosis.
Después de la radioterapia, casi el 50 % de los pacientes experimentan disuria y frecuencia urinaria durante el tratamiento, que se soluciona varias semanas después de este, y el 15 % informa sufrir de efectos tóxicos intestinales.
No se han llevado a cabo ensayos aleatorizados con el fin de comparar directamente el abordaje de quimiorradioterapia para preservar la vejiga con la cistectomía radical; en consecuencia, no se conoce la eficacia relativa de estos dos tratamientos.
Evidencia (radioterapia de haz externo con quimioterapia simultánea o sin esta):
Resección transuretral seguida de quimiorradioterapia
- En un ensayo multicéntrico de fase III, se asignó al azar a 360 pacientes de cáncer de vejiga con invasión muscular a radioterapia y quimioterapia simultánea con fluorouracilo y mitomicina, o sin esta.[24]
- La tasa de SSE locorregional a 2 años fue más alta en el grupo que recibió quimiorradioterapia (67 vs. 54 %; CRI, 0,68; IC 95 %, 0,48–0,96; P = 0,03). La tasa de SG a 5 años fue del 48 % en el grupo que recibió quimiorradioterapia y del 35 % en el grupo de radioterapia, pero la diferencia no fue estadísticamente significativa (P = 0,16).
- Del mismo modo, se notificaron tasas de SG a 5 años del 50 % al 60 % y de supervivencia con la vejiga intacta en el 40 % al 45 % de los pacientes que recibieron quimiorradioterapia sincrónica con otros regímenes de quimioterapia, como cisplatino solo o combinado con fluorouracilo; las cifras son más altas que las que se notifican en general en estudios de radioterapia sola.[25]
Resección transuretral seguida de quimiorradioterapia
- En algunos estudios no aleatorizados, el 50 % o más de los pacientes sometidos a tratamiento para preservar la vejiga (es decir, RTU inicial de la mayor parte posible del tumor seguida de quimiorradioterapia simultánea), permanecían vivos a los 5 años y el 75 % de los sobrevivientes tenían la vejiga intacta.[26-28]
Radioterapia y quimioterapia
- En un ensayo controlado aleatorizado se asignó al azar a 99 pacientes de carcinoma urotelial de vejiga T2 a T4b a radioterapia con 3 ciclos de 14 días de cisplatino (100 mg/m2 el día 1) o sin estos. Los pacientes y sus médicos decidieron si la radioterapia era definitiva o se administraba como tratamiento antes de la cistectomía. La tasa de recaída pélvica se redujo (CRI con modelo de regresión multivariante, 0,50; IC 90 %, 0,29–0,86; P = 0,036), pero no hubo diferencia en la presentación de metástasis a distancia ni en la SG. La reducción de la recaída pélvica fue similar en los pacientes que recibieron radioterapia definitiva y radioterapia antes de la cistectomía.[29]
Quimioterapia neoadyuvante seguida de quimiorradioterapia
- En un estudio de fase III (RTOG-8903), el Radiation Therapy Oncology Group evaluó el beneficio potencial de añadir 2 ciclos de metotrexato, cisplatino y vinblastina neoadyuvantes antes de la administración simultánea de cisplatino y radioterapia. La quimioterapia neoadyuvante se relacionó con un aumento de los efectos tóxicos hematológicos y no produjo ninguna mejora en la tasa de respuesta, ausencia de metástasis a distancia o SG, en comparación con el tratamiento con quimiorradioterapia sola.[30]
Cistectomía segmentaria (para pacientes seleccionados)
La cistectomía segmentaria solo es apropiada para pacientes muy seleccionados.[1] No hay ensayos controlados aleatorizados en los que se compare la cistectomía segmentaria con la cistectomía radical. Solo se trata de rutina con cistectomía segmentaria a los pacientes con adenocarcinomas del uraco. Estos tumores suelen ser adenocarcinomas mucinosos que se presentan en la cúpula de la vejiga y se tratan con una resección en bloque de la cúpula de la vejiga y el uraco remanente, incluso el ombligo.[31-34]
Resección transuretral con fulguración (para pacientes seleccionados)
El cáncer de vejiga en estadio II se puede controlar en algunos pacientes mediante una resección transuretral (RTU) pero, a menudo, son necesarias formas más intensivas para tratar un tumor recidivante o de tamaño grande, focos múltiples o grado indiferenciado de la neoplasia.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Richie JP: Surgery for invasive bladder cancer. Hematol Oncol Clin North Am 6 (1): 129-45, 1992. [PUBMED Abstract]
- Advanced Bladder Cancer Meta-analysis Collaboration: Neoadjuvant chemotherapy in invasive bladder cancer: a systematic review and meta-analysis. Lancet 361 (9373): 1927-34, 2003. [PUBMED Abstract]
- Sherif A, Holmberg L, Rintala E, et al.: Neoadjuvant cisplatinum based combination chemotherapy in patients with invasive bladder cancer: a combined analysis of two Nordic studies. Eur Urol 45 (3): 297-303, 2004. [PUBMED Abstract]
- Winquist E, Kirchner TS, Segal R, et al.: Neoadjuvant chemotherapy for transitional cell carcinoma of the bladder: a systematic review and meta-analysis. J Urol 171 (2 Pt 1): 561-9, 2004. [PUBMED Abstract]
- Olsson CA: Management of invasive carcinoma of the bladder. In: deKernion JB, Paulson DF, eds.: Genitourinary Cancer Management. Lea and Febiger, 1987, pp 59-94.
- Stein JP, Lieskovsky G, Cote R, et al.: Radical cystectomy in the treatment of invasive bladder cancer: long-term results in 1,054 patients. J Clin Oncol 19 (3): 666-75, 2001. [PUBMED Abstract]
- Madersbacher S, Hochreiter W, Burkhard F, et al.: Radical cystectomy for bladder cancer today--a homogeneous series without neoadjuvant therapy. J Clin Oncol 21 (4): 690-6, 2003. [PUBMED Abstract]
- Manoharan M, Ayyathurai R, Soloway MS: Radical cystectomy for urothelial carcinoma of the bladder: an analysis of perioperative and survival outcome. BJU Int 104 (9): 1227-32, 2009. [PUBMED Abstract]
- Ather MH, Fatima S, Sinanoglu O: Extent of lymphadenectomy in radical cystectomy for bladder cancer. World J Surg Oncol 3: 43, 2005. [PUBMED Abstract]
- Hart S, Skinner EC, Meyerowitz BE, et al.: Quality of life after radical cystectomy for bladder cancer in patients with an ileal conduit, cutaneous or urethral kock pouch. J Urol 162 (1): 77-81, 1999. [PUBMED Abstract]
- Miyao N, Adachi H, Sato Y, et al.: Recovery of sexual function after nerve-sparing radical prostatectomy or cystectomy. Int J Urol 8 (4): 158-64, 2001. [PUBMED Abstract]
- Zippe CD, Raina R, Shah AD, et al.: Female sexual dysfunction after radical cystectomy: a new outcome measure. Urology 63 (6): 1153-7, 2004. [PUBMED Abstract]
- Brendler CB, Steinberg GD, Marshall FF, et al.: Local recurrence and survival following nerve-sparing radical cystoprostatectomy. J Urol 144 (5): 1137-40; discussion 1140-1, 1990. [PUBMED Abstract]
- Skinner DG, Boyd SD, Lieskovsky G: Clinical experience with the Kock continent ileal reservoir for urinary diversion. J Urol 132 (6): 1101-7, 1984. [PUBMED Abstract]
- Fowler JE: Continent urinary reservoirs and bladder substitutes in the adult: part I. Monographs in Urology 8 (2): 1987.
- Fowler JE: Continent urinary reservoirs and bladder substitutes in the adult: part II. Monographs in Urology 8 (3): 1987.
- Figueroa AJ, Stein JP, Dickinson M, et al.: Radical cystectomy for elderly patients with bladder carcinoma: an updated experience with 404 patients. Cancer 83 (1): 141-7, 1998. [PUBMED Abstract]
- Smith JA, Crawford ED, Paradelo JC, et al.: Treatment of advanced bladder cancer with combined preoperative irradiation and radical cystectomy versus radical cystectomy alone: a phase III intergroup study. J Urol 157 (3): 805-7; discussion 807-8, 1997. [PUBMED Abstract]
- Neoadjuvant cisplatin, methotrexate, and vinblastine chemotherapy for muscle-invasive bladder cancer: a randomised controlled trial. International collaboration of trialists. Lancet 354 (9178): 533-40, 1999. [PUBMED Abstract]
- Griffiths G, Hall R, Sylvester R, et al.: International phase III trial assessing neoadjuvant cisplatin, methotrexate, and vinblastine chemotherapy for muscle-invasive bladder cancer: long-term results of the BA06 30894 trial. J Clin Oncol 29 (16): 2171-7, 2011. [PUBMED Abstract]
- Grossman HB, Natale RB, Tangen CM, et al.: Neoadjuvant chemotherapy plus cystectomy compared with cystectomy alone for locally advanced bladder cancer. N Engl J Med 349 (9): 859-66, 2003. [PUBMED Abstract]
- Leow JJ, Martin-Doyle W, Rajagopal PS, et al.: Adjuvant chemotherapy for invasive bladder cancer: a 2013 updated systematic review and meta-analysis of randomized trials. Eur Urol 66 (1): 42-54, 2014. [PUBMED Abstract]
- Bajorin DF, Witjes JA, Gschwend JE, et al.: Adjuvant Nivolumab versus Placebo in Muscle-Invasive Urothelial Carcinoma. N Engl J Med 384 (22): 2102-2114, 2021. [PUBMED Abstract]
- James ND, Hussain SA, Hall E, et al.: Radiotherapy with or without chemotherapy in muscle-invasive bladder cancer. N Engl J Med 366 (16): 1477-88, 2012. [PUBMED Abstract]
- Efstathiou JA, Zietman AL, Kaufman DS, et al.: Bladder-sparing approaches to invasive disease. World J Urol 24 (5): 517-29, 2006. [PUBMED Abstract]
- Kachnic LA, Kaufman DS, Heney NM, et al.: Bladder preservation by combined modality therapy for invasive bladder cancer. J Clin Oncol 15 (3): 1022-9, 1997. [PUBMED Abstract]
- Housset M, Maulard C, Chretien Y, et al.: Combined radiation and chemotherapy for invasive transitional-cell carcinoma of the bladder: a prospective study. J Clin Oncol 11 (11): 2150-7, 1993. [PUBMED Abstract]
- Rödel C, Grabenbauer GG, Kühn R, et al.: Combined-modality treatment and selective organ preservation in invasive bladder cancer: long-term results. J Clin Oncol 20 (14): 3061-71, 2002. [PUBMED Abstract]
- Coppin CM, Gospodarowicz MK, James K, et al.: Improved local control of invasive bladder cancer by concurrent cisplatin and preoperative or definitive radiation. The National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol 14 (11): 2901-7, 1996. [PUBMED Abstract]
- Shipley WU, Winter KA, Kaufman DS, et al.: Phase III trial of neoadjuvant chemotherapy in patients with invasive bladder cancer treated with selective bladder preservation by combined radiation therapy and chemotherapy: initial results of Radiation Therapy Oncology Group 89-03. J Clin Oncol 16 (11): 3576-83, 1998. [PUBMED Abstract]
- Ashley RA, Inman BA, Sebo TJ, et al.: Urachal carcinoma: clinicopathologic features and long-term outcomes of an aggressive malignancy. Cancer 107 (4): 712-20, 2006. [PUBMED Abstract]
- Siefker-Radtke A: Urachal carcinoma: surgical and chemotherapeutic options. Expert Rev Anticancer Ther 6 (12): 1715-21, 2006. [PUBMED Abstract]
- Herr HW, Bochner BH, Sharp D, et al.: Urachal carcinoma: contemporary surgical outcomes. J Urol 178 (1): 74-8; discussion 78, 2007. [PUBMED Abstract]
- Bruins HM, Visser O, Ploeg M, et al.: The clinical epidemiology of urachal carcinoma: results of a large, population based study. J Urol 188 (4): 1102-7, 2012. [PUBMED Abstract]
Tratamiento del cáncer de vejiga en estadio IV
Pocos pacientes de cáncer de vejiga en estadio IV se pueden curar y, para muchos pacientes, el énfasis está en la paliación de los síntomas. El potencial curativo se restringe a pacientes con enfermedad en estadio IV con compromiso de los órganos pélvicos por diseminación directa o metástasis en ganglios linfáticos regionales.[1]
Opciones de tratamiento para el cáncer de vejiga en estadio IV
Opciones de tratamiento para pacientes con enfermedad T4b, N0, M0
Las opciones de tratamiento para pacientes con enfermedad T4b, N0, M0 son las siguientes:
- Enfortumab vedotina con pembrolizumab.
- Quimioterapia con inmunoterapia.
- Quimioterapia sola.
- Terapia sistémica seguida de cistectomía radical.
- Radioterapia de haz externo con quimioterapia simultánea o sin esta.
- Derivación urinaria o cistectomía para la paliación.
Enfortumab vedotina con pembrolizumab
El enfortumab vedotina es un conjugado anticuerpo-fármaco, en el que se combina un anticuerpo que se une a la nectina-4 con un inhibidor de microtúbulos. La Administración de Alimentos y Medicamentos (FDA) de los Estados Unidos aprobó el uso de enfortumab vedotina en monoterapia para los pacientes con carcinoma urotelial metastásico que ya ha sido tratado. El pembrolizumab es un anticuerpo contra la proteína de muerte celular programada-1 (PD-1) que la FDA aprobó en monoterapia para el tratamiento de pacientes con cáncer de vejiga metastásico. La combinación de los dos fármacos demostró una tasa de respuesta y una duración de la respuesta alentadoras, lo que derivó en un ensayo de fase II de un solo grupo y luego en una comparación con quimioterapia en un ensayo de fase III aleatorizado, controlado.[2-4] Si bien, entre los ensayos, los resultados no se pueden extrapolar, la combinación de enfortumab vedotina con pembrolizumab es una opción de terapia de primera línea para pacientes que no presentan una contraindicación.
Evidencia (enfortumab vedotina con pembrolizumab):
- En un ensayo de fase III (NCT04223856), que se publicó en forma de resumen, 886 pacientes se asignaron al azar de manera aleatoria para recibir enfortumab vedotina con pembrolizumab (n = 442) o gemcitabina con cisplatino o carboplatino (n = 444). La mediana de seguimiento fue de 17 meses.[4][Nivel de evidencia A1]
- La supervivencia general (SG) y la supervivencia sin progresión (SSP) fueron superiores en los pacientes del grupo de enfortumab vedotina con pembrolizumab que en el grupo de quimioterapia.
- La mediana de SG fue de 31,5 meses en los pacientes que recibieron enfortumab vedotina con pembrolizumab y de 16,1 meses en los pacientes que recibieron quimioterapia (cociente de riesgos instantáneos [CRI], 0,47; intervalo de confianza [IC] 95 %, 0,38–0,58; P < 0,00001).
- La SSP fue de 12,5 meses en los pacientes que recibieron enfortumab vedotina con pembrolizumab y 6,3 meses en los pacientes que recibieron quimioterapia (CRI, 0,45; IC 95 %, 0,38–0,54).
- Se presentaron efectos adversos de grado 3 o superior en el 55,9 % de los pacientes que recibieron enfortumab vedotina con pembrolizumab y en el 69,5 % de los pacientes que recibieron quimioterapia.
- En el grupo experimental, los efectos adversos de grado alto más frecuentes fueron reacciones en la piel, neuropatía periférica, hiperglicemia y neutropenia.
Quimioterapia con inmunoterapia
Durante muchos años, la quimioterapia a base de cisplatino fue el tratamiento sistémico de primera línea estándar para los pacientes con carcinoma urotelial en estadio IV que eran aptos para recibir cisplatino. En un ensayo de fase III aleatorizado controlado se notificó una SG más prolongada cuando se administró quimioterapia a base de cisplatino con nivolumab, en comparación con la quimioterapia sola.[5]
Evidencia (quimioterapia con inmunoterapia):
- En un ensayo de fase III controlado (CheckMate901 [NCT03036098]) se asignaron al azar 608 pacientes (304 a cada grupo) a recibir nivolumab con gemcitabina y cisplatino o gemcitabina y cisplatino solos. Los pacientes recibieron hasta 6 ciclos de quimioterapia y hasta 2 años de nivolumab. La mediana de seguimiento fue de 33,6 meses.[5]
- La mediana de SG fue de 21,7 meses en los pacientes que recibieron nivolumab y de 18,9 meses en los pacientes que recibieron quimioterapia sola (CRIde muerte, 0,78; IC 95 %, 0,63–0,96; P = 0,02).[5][Nivel de evidencia A1]
- La mediana de SSP fue de 7,9 meses en los pacientes que recibieron nivolumab y de 7,6 meses en los pacientes que recibieron quimioterapia sola (CRIde progresión o muerte, 0,72; IC 95 %, 0,59–0,88; P = 0,001).
- Al cabo de 1 año, la tasa de SSP fue del 34,2 % en el grupo de nivolumab y del 21,8 % en el grupo de quimioterapia sola.
- La tasa de respuesta general fu del 57,6 % en el grupo de nivolumab y del 21,7 % en el grupo de quimioterapia sola. La tasa de respuesta completa fue del 21,7 % en el grupo de nivolumab y del 11,8 % en el grupo de quimioterapia sola.
- La duración de la respuesta completa fue de 37,1 meses en el grupo de nivolumab y de 13,2 meses en el grupo de quimioterapia sola.
- Se presentaron efectos adversos de grado 3 o superior en el 61,8 % de los pacientes en el grupo de nivolumab y en el 51,7 % de los pacientes en el grupo de quimioterapia sola.
Quimioterapia sola
Los regímenes de quimioterapia combinada a base de cisplatino son la opción de tratamiento estándar para los pacientes con cáncer de vejiga en estadio IV.[6-10] Los únicos regímenes de quimioterapia que demostraron proporcionar una supervivencia más larga en los ensayos controlados aleatorizados son el metotrexato, la vinblastina, la doxorrubicina y el cisplatino (MVAC); dosis altas del régimen MVAC, y el cisplatino, el metotrexato y la vinblastina (CMV). En un ensayo controlado aleatorizado, se comparó la combinación de gemcitabina y cisplatino (GC) con el régimen MVAC y no se notificaron diferencias en la tasa de respuesta o la supervivencia. Es de destacar que los pacientes con buen estado funcional y enfermedad solo en los ganglios linfáticos tienen una tasa baja, pero significativa, de lograr una remisión completa duradera con el régimen MVAC o la combinación GC. Por ejemplo, en el ensayo grande controlado aleatorizado en el que se comparó el régimen MVAC con la combinación GC, la tasa de supervivencia general (SG) a 5 años en pacientes con enfermedad solo en los ganglios linfáticos fue del 20,9 %.[11]
El cisplatino como sustancia única y los regímenes multifarmacológicos que no incluyen cisplatino no han demostrado mejorar la supervivencia en ningún ensayo controlado aleatorizado. No hay un régimen que haya demostrado prolongar la supervivencia en pacientes que no son aptos para los regímenes de quimioterapia multifarmacológica a base de cisplatino; sin embargo, muchos regímenes han demostrado respuestas radiológicas mensurables.
Estos incluyen carboplatino y paclitaxel,[12] carboplatino y gemcitabina,[13-15] paclitaxel y gemcitabina,[16-18] gemcitabina como sustancia única [19,20] y paclitaxel como sustancia única.[21-23] Si bien se estudiaron los regímenes de carboplatino, metotrexato y vinblastina; carboplatino, epirrubicina, metotrexato y vinblastina, y paclitaxel, gemcitabina y carboplatino, estos no se utilizan ampliamente.[24-27]
Evidencia (quimioterapia sola):
- En un ensayo controlado aleatorizado en el que se comparó el régimen MVAC con docetaxel y cisplatino en 220 pacientes, se notificó que el régimen MVAC se relacionó con una SG más larga (mediana de supervivencia, 14,2 vs. 9,3 meses; P = 0,026).[28]
- En un ensayo aleatorizado en el que se comparó el régimen MVAC con cisplatino, ciclofosfamida y doxorrubicina, se demostró una mejora de la respuesta y las medianas de tasas de supervivencia (48 vs. 36 semanas; P = 0,003) con el régimen MVAC.[29]
- Los resultados de un ensayo aleatorizado en el que se comparó el régimen MVAC con cisplatino como sustancia única para el cáncer de vejiga en estadio avanzado también mostraron una ventaja significativa con el régimen MVAC, tanto en la tasa de respuesta como en la mediana de supervivencia (12,5 vs. 8,2 meses; P = 0,002).[30]
- En un ensayo controlado aleatorizado multicéntrico se comparó el régimen CMV con la combinación de metotrexato y vinblastina sin cisplatino en 214 pacientes. El riesgo relativo de muerte fue de 0,68 (intervalo de confianza [IC] 95 %: 0,51–0,90; P = 0,0065) en favor del régimen CMV. La mediana de supervivencia fue de 7 meses con el régimen CMV y de 4,5 meses con metotrexato y vinblastina.[31]
- La European Organisation for Research and Treatment of Cancer (EORTC) llevó a cabo otro ensayo aleatorizado, que estudió a 263 pacientes con cáncer de vejiga avanzado, en el que se evaluó la eficacia del régimen MVAC de dosis de intensidad alta administrado cada 2 semanas con el factor estimulante de colonias de granulocitos (G-CSF) en comparación con un régimen MVAC clásico administrado cada 4 semanas.[32]
- Aunque no hubo una diferencia significativa en la SG en el momento de una mediana de seguimiento de 3,2 años (cociente de riesgos instantáneos [CRI], 0,80; IC 95 %, 0,60–1,06; P = 0,122), una actualización en el momento de una mediana de seguimiento de 7,3 años notificó que las dosis de intensidad alta del régimen MVAC se relacionaron con una mejora de la SG (CRI, 0,76; IC 95 %, 0,58–0,99; P = 0,042), y una tasa de supervivencia a 5 años del 22 % en comparación con el 14 % en los pacientes tratados con el régimen MVAC clásico.
- Las dosis de intensidad alta del régimen MVAC también se relacionaron con tasas de respuesta más altas (72 vs. 58 %; P = 0,016), mejora de la mediana de supervivencia sin progresión (SSP) (9,5 vs. 8,1 meses; P = 0,017) y disminución de la neutropenia febril (10 vs. 26 %; P < 0,001), aunque solo el 19 % de los pacientes tratados con un régimen MVAC clásico recibieron alguna vez G-CSF.[32][Nivel de evidencia A1] Se encontró un desequilibrio en los factores pronósticos iniciales (es decir, se encontraron metástasis viscerales en 37 pacientes asignados al azar al régimen MVAC de dosis altas y en 47 pacientes asignados al régimen MVAC clásico), que puede explicar, en parte, estos resultados.
- Gemcitabina y cisplatino.
- En un ensayo multicéntrico aleatorizado de fase III en el que se comparó la combinación GC con el régimen MVAC en 405 pacientes de cáncer de vejiga avanzado o metastásico, la combinación GC rindió tasas de respuesta, tiempo transcurrido hasta la progresión y SG (CRI, 1,04; IC 95 %, 0,82–1,32; P = 0,75), similares al régimen MVAC, pero la combinación GC tuvo un mejor perfil de inocuidad y se toleró mejor que el régimen MVAC.
- Aunque este estudio no se diseñó para demostrar la equivalencia de los dos regímenes, la eficacia similar y los menores efectos tóxicos de la combinación GC, la convierten en una alternativa razonable para pacientes que no pueden tolerar el régimen MVAC.[33][Nivel de evidencia A1]
Radioterapia de haz externo, con quimioterapia simultánea o sin esta
La radioterapia definitiva con quimioterapia simultánea o sin esta, que se evaluó sobre todo para pacientes con enfermedad localmente avanzada (T2–T4), parece tener un potencial curativo mínimo en pacientes con metástasis en ganglios linfáticos regionales.[34,35] En consecuencia, los pacientes con indicios de metástasis ganglionares en general se excluyeron de los ensayos de fase III de radioterapia.[36,37]
Derivación urinaria o cistectomía para la paliación
La derivación urinaria se puede indicar no solo para la paliación de los síntomas urinarios sino, también, para preservar el funcionamiento renal de quienes son aptos para recibir quimioterapia.
Opciones de tratamiento para pacientes con enfermedad con cualquier T, cualquier N, M1
Las opciones de tratamiento para pacientes con enfermedad con cualquier T, cualquier N, M1 son las siguientes:
- Enfortumab vedotina con pembrolizumab.
- Quimioterapia con inmunoterapia.
- Quimioterapia sola o adjunta al tratamiento local.
- Inmunoterapia.
- Radioterapia de haz externo para la paliación.
- Derivación urinaria o cistectomía para la paliación.
- Otros fármacos quimioterapéuticos eficaces para el tratamiento del cáncer de vejiga metastásico, como paclitaxel, docetaxel e ifosfamida (en evaluación clínica).[38,39][Nivel de evidencia C3]
- Participación en ensayos clínicos.
Enfortumab vedotina con pembrolizumab
El enfortumab vedotina es un conjugado anticuerpo-fármaco, en el que se combina un anticuerpo que se une a la nectina-4 con un inhibidor de microtúbulos. La FDA de los Estados Unidos aprobó el uso de enfortumab vedotina en monoterapia para los pacientes con carcinoma urotelial metastásico que ya ha sido tratado. El pembrolizumab es un anticuerpo contra PD-1 que aprobó la FDA en monoterapia para el tratamiento de pacientes con cáncer de vejiga metastásico. La combinación de los dos fármacos demostró una tasa de respuesta y una duración de la respuesta alentadoras, lo que derivó en un ensayo de fase II de un solo grupo y luego en una comparación con quimioterapia en un ensayo de fase III aleatorizado, controlado.[2-4] Si bien, entre los ensayos, los resultados no se pueden extrapolar, la combinación de enfortumab vedotina con pembrolizumab es una opción de terapia de primera línea para pacientes que no presentan una contraindicación.
Evidencia (enfortumab vedotina con pembrolizumab):
- En un ensayo de fase III (NCT04223856), que se publicó en forma de resumen, 886 pacientes se asignaron al azar de manera aleatoria para recibir enfortumab vedotina con pembrolizumab (n = 442) o gemcitabina con cisplatino o carboplatino (n = 444). La mediana de seguimiento fue de 17 meses.[4][Nivel de evidencia A1]
- La SG y la SSP fueron superiores en los pacientes del grupo de enfortumab vedotina con pembrolizumab que en el grupo de quimioterapia.
- La mediana de SG fue de 31,5 meses en los pacientes que recibieron enfortumab vedotina con pembrolizumab y de 16,1 meses en los pacientes que recibieron quimioterapia (CRI, 0,47; IC 95 %, 0,38–0,58; P < 0,00001).
- La SSP fue de 12,5 meses en los pacientes que recibieron enfortumab vedotina con pembrolizumab y 6,3 meses en los pacientes que recibieron quimioterapia (CRI, 0,45; IC 95 %, 0,38–0,54).
- Se presentaron efectos adversos de grado 3 o superior en el 55,9 % de los pacientes que recibieron enfortumab vedotina con pembrolizumab y en el 69,5 % de los pacientes que recibieron quimioterapia.
- En el grupo experimental, los efectos adversos de grado alto más frecuentes fueron reacciones en la piel, neuropatía periférica, hiperglicemia y neutropenia.
Quimioterapia con inmunoterapia
Durante muchos años, la quimioterapia a base de cisplatino fue el tratamiento sistémico de primera línea estándar para los pacientes con carcinoma urotelial en estadio IV que eran aptos para recibir cisplatino. En un ensayo de fase III aleatorizado controlado se notificó una SG más prolongada cuando se administró quimioterapia a base de cisplatino con nivolumab, en comparación con la quimioterapia sola.[5]
Evidencia (quimioterapia con inmunoterapia):
- En un ensayo de fase III controlado (CheckMate901 [NCT03036098]) se asignaron al azar 608 pacientes (304 a cada grupo) a recibir nivolumab con gemcitabina y cisplatino o gemcitabina y cisplatino solos. Los pacientes recibieron hasta 6 ciclos de quimioterapia y hasta 2 años de nivolumab. La mediana de seguimiento fue de 33,6 meses.[5]
- La mediana de SG fue de 21,7 meses en los pacientes que recibieron nivolumab y de 18,9 meses en los pacientes que recibieron quimioterapia sola (CRIde muerte, 0,78; IC 95 %, 0,63–0,96, P = 0,02).[5][Nivel de evidencia A1]
- La mediana de SSP fue de 7,9 meses en los pacientes que recibieron nivolumab y de 7,6 meses en los pacientes que recibieron quimioterapia sola (CRIde progresión o muerte, 0,72; IC 95 %, 0,59–0,88; P = 0,001).
- Al cabo de 1 año, la tasa de SSP fue del 34,2 % en el grupo de nivolumab y del 21,8 % en el grupo de quimioterapia sola.
- La tasa de respuesta general fu del 57,6 % en el grupo de nivolumab y del 21,7 % en el grupo de quimioterapia sola. La tasa de respuesta completa fue del 21,7 % en el grupo de nivolumab y del 11,8 % en el grupo de quimioterapia sola.
- La duración de la respuesta completa fue de 37,1 meses en el grupo de nivolumab y de 13,2 meses en el grupo de quimioterapia sola.
- Se presentaron efectos adversos de grado 3 o superior en el 61,8 % de los pacientes en el grupo de nivolumab y en el 51,7 % de los pacientes en el grupo de quimioterapia sola.
Quimioterapia sola o adjunta al tratamiento local
Los regímenes de quimioterapia combinada a base de cisplatino son el estándar de atención de la terapia de primera línea para pacientes con cáncer de vejiga en estadio IV que la pueden tolerar.[6-10] Los únicos regímenes de quimioterapia que demostraron proporcionar una supervivencia más larga en los ensayos controlados aleatorizados son el régimen MVAC; el régimen MVAC de dosis densas y el régimen CMV. En un ensayo controlado aleatorizado, se comparó la combinación GC con el régimen MVAC y ninguno de los dos regímenes se relacionó con diferencias estadísticamente significativas en la tasa de respuesta o la supervivencia. Por lo general, los dos regímenes se consideran equivalentes, pero nunca se compararon en un ensayo de ausencia de inferioridad. Es de destacar que los pacientes con buen estado funcional y enfermedad solo en los ganglios linfáticos tienen una tasa baja, pero significativa, de lograr una remisión completa duradera con el régimen MVAC o la combinación GC. Por ejemplo, en el ensayo grande controlado aleatorizado en el que se comparó el régimen MVAC con la combinación GC, la tasa de SG a 5 años en pacientes con enfermedad solo en los ganglios linfáticos fue del 20,9 %.[11] El régimen MVAC de dosis densas y el régimen MVAC de dosis estándar se compararon en un ensayo controlado aleatorizado: el MVAC de dosis densas se relacionó con una supervivencia más prolongada.
El cisplatino como sustancia única y los regímenes multifarmacológicos que no incluyen cisplatino no han demostrado mejorar la supervivencia en ningún ensayo controlado aleatorizado. No hay un régimen que haya demostrado prolongar la supervivencia en pacientes que no son aptos para los regímenes de quimioterapia multifarmacológica a base de cisplatino; sin embargo, muchos regímenes han demostrado respuestas radiológicas mensurables.
Estos incluyen carboplatino y paclitaxel,[12] carboplatino y gemcitabina,[13-15] paclitaxel y gemcitabina,[16-18] gemcitabina como sustancia única [19,20] y paclitaxel como sustancia única.[21-23] Si bien se estudiaron los regímenes de carboplatino, metotrexato y vinblastina; carboplatino, epirrubicina, metotrexato y vinblastina, y paclitaxel, gemcitabina y carboplatino, estos no se utilizan ampliamente.[24-27]
En los estudios en curso se evalúan nuevas combinaciones de quimioterapia.
Evidencia (quimioterapia):
- En un ensayo aleatorizado prospectivo en el que se comparó el régimen MVAC con cisplatino, ciclofosfamida y doxorrubicina, se demostró una mejor tasa de respuesta y una mediana de supervivencia más alta (48 vs. 36 semanas; P = 0,003) con el régimen MVAC.[29]
- Los resultados de un ensayo aleatorizado en el que se comparó el régimen MVAC con cisplatino como sustancia única para el cáncer de vejiga en estadio avanzado también mostraron una ventaja significativa con el régimen MVAC, tanto en la tasa de respuesta como en la mediana de supervivencia (12,5 vs. 8,2 meses; P = 0,002).[30]
- En un ensayo controlado aleatorizado multicéntrico se comparó el régimen CMV con la combinación de metotrexato y vinblastina sin cisplatino en 214 pacientes. El riesgo relativo de muerte fue de 0,68 (IC 95 %: 0,51–0,90; P = 0,0065) a favor del régimen CMV. La mediana de supervivencia fue de 7 meses con el régimen CMV y de 4,5 meses con metotrexato y vinblastina.[31]
- La EORTC llevó a cabo otro ensayo aleatorizado en el que se estudió a 263 pacientes de cáncer de vejiga avanzado para evaluar la eficacia de un régimen MVAC de dosis de intensidad alta administradas cada 2 semanas con el G-CSF en comparación con un régimen MVAC clásico administrado cada 4 semanas.[32]
- Aunque no hubo una diferencia significativa en la SG en el momento de una mediana de seguimiento de 3,2 años (CRI, 0,80; IC 95 %, 0,60–1,06; P = 0,122), en una actualización realizada en el momento de una mediana de seguimiento de 7,3 años se notificó que las dosis de intensidad alta del régimen MVAC se relacionaron con una mejora de la SG (CRI, 0,76; IC 95 %, 0,58–0,99; P = 0,042), con una tasa de supervivencia a 5 años del 22 % en comparación con el 14 % en los pacientes tratados con el régimen MVAC clásico.
- Las dosis de intensidad alta del régimen MVAC también se relacionaron con tasas de respuesta más altas (72 vs. 58 %; P = 0,016), mejor mediana de SSP (9,5 vs. 8,1 meses; P = 0,017) y disminución de la neutropenia febril (10 vs. 26 %; P < 0,001), aunque solo el 19 % de los pacientes tratados con un régimen MVAC clásico recibieron alguna vez G-CSF.[32][Nivel de evidencia A1] Se encontró un desequilibrio en los factores pronósticos iniciales (es decir, se encontraron metástasis viscerales en 37 pacientes asignados al azar al régimen MVAC de dosis altas y en 47 pacientes asignados al régimen MVAC clásico), lo que puede explicar, en parte, estos resultados.
- Gemcitabina y cisplatino.
- En un ensayo multicéntrico aleatorizado de fase III en el que se comparó la combinación GC con el régimen MVAC en 405 pacientes de cáncer de vejiga avanzado o metastásico, la combinación GC rindió tasas de respuesta, tiempo transcurrido hasta la progresión y SG (CRI, 1,04; IC 95 %, 0,82–1,32; P = 0,75) similares al régimen MVAC, pero la combinación GC tuvo un mejor perfil de inocuidad y se toleró mejor que el régimen MVAC.
- Aunque este estudio no se diseñó para demostrar la equivalencia de los dos regímenes, la eficacia similar y los menores efectos tóxicos de la combinación GC la convierten en una alternativa razonable para pacientes que no pueden tolerar el régimen MVAC.[33][Nivel de evidencia A1]
- Otros regímenes de quimioterapia que demostraron producir un efecto sobre el cáncer de vejiga metastásico incluyen el paclitaxel, la gemcitabina y el pemetrexed como sustancias únicas, el carboplatino combinado con gemcitabina o paclitaxel, y la gemcitabina combinada con paclitaxel. No hay ensayos de fase III que demuestren un beneficio para la supervivencia o la calidad de vida producido por la quimioterapia de segunda línea.[13,16,18,19,27,40-52]
En los estudios en curso se evalúan nuevas combinaciones de quimioterapia.
Inmunoterapia
La inmunoterapia se propone como una alternativa de tratamiento para los pacientes de cáncer de vejiga en estadio IV. En los ensayos clínicos, los inhibidores de puntos de control inmunitario que exhiben actividad contra PD-1 o contra el ligando 1 de muerte celular programada (PD-L1) tuvieron efecto contra el carcinoma urotelial de pacientes tratados antes con quimioterapia con derivados del cisplatino o que no eran aptos para recibirla.[53-57] Actualmente hay varios fármacos aprobados; sin embargo, el pembrolizumab es el fármaco que tiene el mayor nivel de evidencia científica y los mejores datos de supervivencia.
Pembrolizumab
El pembrolizumab es un anticuerpo monoclonal humanizado que se une al PD-1. En pacientes tratados antes con quimioterapia con derivados del platino, se observó que el pembrolizumab prolongó más la SG que la quimioterapia de segunda línea. Como resultado, la FDA aprobó el pembrolizumab para pacientes de carcinoma urotelial localmente avanzado o metastásico que pertenecen a una de las tres categorías siguientes:
- No son aptos para recibir cisplatino y tienen tumores que expresan PD-L1 (puntaje positivo combinado [CPS] de por lo menos el 10 %).
- No son aptos para recibir cisplatino y carboplatino.
- Exhiben progresión de la enfermedad después de recibir quimioterapia con derivados del platino.
Es importante señalar que, en 2018, la FDA emitió una alerta sobre los datos preliminares de 2 ensayos de tratamiento de primera línea en curso que compararon el tratamiento con pembrolizumab o atezolizumab con el tratamiento a base de cisplatino o carboplatino. Los datos mostraron que la inmunoterapia se relacionó con una supervivencia más breve en los pacientes con una expresión de PD-L1 baja. Como resultado, se enmendaron las fichas técnicas para restringir el uso de ambos fármacos para las tres categorías de pacientes descritas más arriba.
Evidencia (pembrolizumab):
- En un ensayo internacional de fase III, sin anonimato, aleatorizado y controlado (NCT02256436) de pembrolizumab (200 mg intravenosos [IV] cada 21 días) versus quimioterapia de segunda línea (paclitaxel, docetaxel o vinflunina, a elección del investigador) para pacientes cuya enfermedad progresó después del tratamiento con quimioterapia a base de derivados del platino, la mediana de SG fue más larga con pembrolizumab (10,3 meses vs. 7,4 meses; CRI, 0,73; IC 95 %, 0,59–0,91).[58]
- En pacientes con un CPS de PD-L1 de por lo menos el 10 %, la mediana de SG fue de 8,0 meses con pembrolizumab comparada con 5,2 meses de quimioterapia (CRI, 0,57; IC 95 %, 0,37–0,88).
- La tasa de SSP a los 12 meses fue del 16,8 % (IC 95 %, 12,3–22,0 %) en el grupo de pembrolizumab y del 6,2 % (IC 95 %, 3,3–10,2 %) en el grupo de quimioterapia.
- La tasa de respuesta objetiva fue del 21,1 % en el grupo de pembrolizumab y del 11,4 % en el grupo de quimioterapia. Entre quienes respondieron, la mediana de duración de la respuesta superó los 18 meses con pembrolizumab comparada con una respuesta de 4,3 meses con quimioterapia.
- El pembrolizumab se relacionó con una tasa más baja de efectos adversos relacionados con el tratamiento que la quimioterapia (60,9 vs. 90,2 %) y una tasa más baja de efectos adversos de grado alto (15,0 vs. 49,4 %). Los efectos adversos más comunes con pembrolizumab fueron prurito, fatiga, náuseas, diarrea y disminución del apetito.[58][Nivel de evidencia A1]
- En un ensayo de fase II (NCT02335424) de pembrolizumab con un solo grupo de 370 pacientes de carcinoma urotelial localmente avanzado o metastásico que nunca se trataron y no eran aptos para recibir cisplatino, la tasa de respuesta general fue del 29 %. En pacientes con un puntaje combinado de PD-L1 con un CPS de por lo menos el 10 %, la tasa de respuesta general fue del 51 %.[59]
- La mediana de duración de la respuesta no se había alcanzado. De las respuestas, el 82 % duraron por lo menos 6 meses.
- Diez por ciento de los pacientes sufrieron un efecto adverso grave y 1 paciente murió como consecuencia de efectos adversos relacionados con el tratamiento. Los efectos adversos de grado alto más comunes fueron fatiga (2 %), elevación de la fosfatasa alcalina (1 %), colitis (1 %) y debilidad muscular (1 %).[59][Nivel de evidencia C3]
Atezolizumab
El atezolizumab es un anticuerpo monoclonal humanizado que se une a la PD-L1 e impide que esta se fije a sus receptores PD-1 o B7-1. Se ha notificado en ensayos clínicos que el atezolizumab es eficaz contra el carcinoma urotelial, pero no se observó prolongación de la SG o mejoría de la calidad de vida. En el único ensayo controlado aleatorizado en el que se probó el atezolizumab, no se notificó una diferencia significativa de SG en comparación con la quimioterapia de segunda línea.
La FDA aprobó el atezolizumab para pacientes de carcinoma urotelial avanzado localmente o metastásico que pertenecen a una de las tres categorías siguientes:
- No son aptos para recibir cisplatino y tienen tumores que expresan PD-L1 (por lo menos el 5 % del área del tumor cubierta por células inmunitarias que infiltran el tumor con tinción para PD-L1).
- No son aptos para recibir cisplatino y carboplatino.
- Exhiben progresión de la enfermedad después de recibir quimioterapia con derivados del platino.
Es importante señalar que, en 2018, la FDA emitió una alerta para informar sobre los datos preliminares de 2 ensayos de tratamiento de primera línea en curso que compararon el tratamiento con pembrolizumab o atezolizumab con el tratamiento a base de cisplatino o carboplatino. Los datos mostraron que la inmunoterapia se relacionó con una supervivencia más breve en los pacientes con una expresión de PD-L1 baja. Como resultado, se enmendaron las fichas técnicas para restringir el uso de ambos fármacos para las tres categorías de pacientes descritas más arriba.
Evidencia (atezolizumab):
- El ensayo IMvigor211 (NCT02302807) es un ensayo aleatorizado y controlado en el que se comparó el atezolizumab con la quimioterapia de segunda línea (docetaxel, paclitaxel o vinflunina) en 931 pacientes de carcinoma urotelial localmente avanzado o metastásico que se trataron antes con quimioterapia con derivados del platino.[60] En el diseño del ensayo se especificó que la SG se evaluaría principalmente en pacientes cuyos tumores exhibieran por lo menos el 5 % de células con expresión de PD-L1.
- La mediana de SG fue de 11,1 meses con atezolizumab versus 10,6 meses con quimioterapia en pacientes con un mínimo del 5 % de células tumorales que expresaban PD-L1 (P = 0,41).[60][Nivel de evidencia A1]
- Las tasas de respuesta también fueron similares: el 23 % con atezolizumab y el 22 % con quimioterapia.
- Los pacientes que recibieron atezolizumab presentaron una tasa más baja de toxicidad de grado alto (20 vs. 43 %) y una tasa más baja de abandono del tratamiento por efectos adversos (7 vs. 18 %).
- En un ensayo multicéntrico de un solo grupo (NCT0108652) se incluyeron 315 pacientes con carcinoma urotelial localmente avanzado inoperable o metastásico que no eran aptos para recibir cisplatino o que se habían tratado antes con quimioterapia con derivados del platino. Los pacientes recibieron atezolizumab (1200 mg IV cada 21 días). Se notificaron los siguientes resultados:[56][Nivel de evidencia C2]
- La tasa de respuesta general fue del 15 %.
- Tras una mediana de seguimiento de 11,7 meses, 38 de 45 participantes (84 %) tuvieron una respuesta continua.
- Se obtuvo una tasa de respuesta del 27 % en aquellos con expresión de PD-L1 de por lo menos el 5 %, del 10 % en aquellos con expresión de PD-L1 del 1 al 5 %, y del 8 % en aquellos con expresión de PD-L1 menor del 1 %.
- Se notificaron efectos adversos de grados 3 y 4 en el 16 % de los pacientes, y efectos adversos de grado alto relacionados con el sistema inmunitario en el 5 % de los pacientes.
- De modo similar, en un estudio (NCT02108652) de 123 pacientes de carcinoma urotelial localmente avanzado metastásico sin tratamiento previo que no eran aptos para recibir cisplatino, y que se trataron con atezolizumab, se notificó una tasa de respuesta objetiva del 23 % y respuesta completa en el 9 % de los pacientes en el momento de una mediana de seguimiento de 17,2 meses.[57][Nivel de evidencia C2]
- De las 27 respuestas, 19 estaban en curso cuando se analizaron los datos. La mediana de SG fue de 15,9 meses.
- Se notificaron efectos adversos de grado alto en el 16 % de los pacientes; se interrumpió el tratamiento en el 8 % de los pacientes por efectos adversos y hubo una muerte relacionada con el tratamiento.
Nivolumab
El nivolumab es un anticuerpo completamente humano tipo inmunoglobulina G4 que actúa como inhibidor del punto de control inmunitario PD-1 y bloquea la interacción entre PD-L1 y PD-L2 con PD-1. Debido a la carencia de publicaciones de ensayos controlados, no se dispone de datos que demuestren que el consumo de nivolumab prolongue la supervivencia o mejore la calidad de vida.
Evidencia (nivolumab):
- En un ensayo multicéntrico (NCT01928394) se incluyeron 86 pacientes de carcinoma urotelial metastásico cuya enfermedad progresó después de recibir quimioterapia con derivados del platino. Los pacientes recibieron nivolumab (3 mg/kg IV cada 2 semanas).[55][Nivel de evidencia B4]
- Tras un seguimiento mínimo de 9 meses y una mediana de seguimiento de 15 meses, el 24 % de los pacientes tuvo una respuesta objetiva y el 22 % presentó efectos adversos de grado 3 o 4.
- Entre los efectos adversos más frecuentes se observaron concentraciones altas de lipasa o amilasa, fatiga, exantema, disnea, linfopenia y neutropenia.
- En otro estudio multicéntrico (NCT02387996) de 270 pacientes de carcinoma urotelial metastásico o localmente avanzado con progresión después del tratamiento con quimioterapia con derivados del platino, se notificó una tasa de respuesta objetiva de 20 %.[54][Nivel de evidencia B4]
- Al evaluar la expresión de PD-L1, la tasa de respuesta objetiva fue del 28 % en aquellos con una expresión de PD-L1 del 5 % o más; el 24 % en aquellos con una expresión de PD-L1 del 1 % o más; y el 16 % en aquellos con una expresión de PD-L1 de menos del 1 %.
- Se notificaron efectos adversos de grado 3 y 4 en el 18 % de los pacientes.
- Hubo 3 muertes relacionadas con el tratamiento.
Avelumab
El avelumab es un anticuerpo monoclonal anti–PD-L1 que exhibió actividad contra el carcinoma urotelial. En un ensayo controlado aleatorizado, se informó un beneficio de la SG con el avelumab de mantenimiento cuando se administró después de la quimioterapia con derivados del platino en pacientes cuyo cáncer no progresó durante la quimioterapia.
Evidencia (avelumab):
- En un estudio de fase III (NCT02603432), se evaluó el avelumab de mantenimiento (10 mg/kg IV cada 14 días) en pacientes con carcinoma urotelial metastásico que no progresó durante el tratamiento con quimioterapia de primera línea con gemcitabina combinada con cisplatino o carboplatino. Después de 4 a 6 ciclos de quimioterapia, 700 pacientes se asignaron al azar a recibir los mejores cuidados médicos de apoyo (grupo de control) o los mejores cuidados médicos de apoyo y avelumab de mantenimiento(grupo de avelumab).[61][Nivel de evidencia A1]
- La tasa de SG a 1 año fue del 71,3 % en el grupo de avelumab en comparación con el 58,4 % en el grupo de control (CRI, 0,69; IC 95 %, 0,56–0,86).
- El beneficio en la SG se limitó a los pacientes cuyos tumores eran positivos para PD-L1. La SG de los pacientes con tumores negativos para PD-L1 no fue significativamente diferente entre los dos grupos.
- Los pacientes con tumores positivos para PD-L1, tuvieron una tasa de SG a 1 año del 79,1 % en el grupo de avelumab y del 60,4 % en el grupo de control (CRI, 0,56; IC 95 %, 0,40–0,79).
- En la población general del estudio, la mediana de la SSP fue de 3,7 meses en los pacientes del grupo de avelumab y de 2,0 meses en los pacientes del grupo de control (CRI, 0,62; IC 95 %, 0,52–0,75). En los pacientes con tumores positivos para PD-L1, la mediana de la SSP fue de 5,7 meses en el grupo con avelumab y de 2,1 meses en el grupo que recibió solo los mejores cuidados médicos de apoyo (CRI, 0,56; IC 95 %, 0,43–0,73).
- Se notificaron eventos adversos de grado 3 o superior en el 47,4 % de los pacientes en el grupo de avelumab y en el 25,2 % de los pacientes en el grupo de control. La mayoría de los eventos adversos con avelumab fueron inmunitarios, el 9 % de los pacientes que recibieron avelumab se trataron con dosis altas de glucocorticoides por estos eventos.
- En un estudio (NCT01772004) de avelumab (10 mg/kg IV cada 14 días) administrado a 249 pacientes de carcinoma urotelial metastásico que presentaron progresión de la enfermedad después del tratamiento con quimioterapia con derivados del platino, se notificaron los siguientes resultados:[62,63][Nivel de evidencia C3]
- Entre los 161 pacientes a quienes se les dio seguimiento durante por lo menos 6 meses, la tasa de respuesta general fue del 17 % y la respuesta fue continua en 23 de 28 pacientes que respondieron luego de una mediana de seguimiento de 7,3 meses. La respuesta completa se presentó en el 6 % de los pacientes.
- La tasa de respuesta general fue del 25,0 % en pacientes que tenían como mínimo el 5 % de las células tumorales con expresión de PD-L1 y el 14,7 % de ellos con menos del 5 % con expresión de PD-L1.
- La mediana de SSP fue de 6,3 semanas; el 23 % de los pacientes estaban libres de progresión a las 24 semanas.
- Se notificaron efectos adversos relacionados con el tratamiento en el 66,7 % de los pacientes y el 8,4 % de los pacientes presentaron efectos adversos de grado alto. Hubo 1 muerte por neumonía relacionada con el tratamiento. Se notificaron efectos adversos inmunitarios de grado alto en el 2,4 % de los pacientes.
Durvalumab
El durvalumab es un anticuerpo monoclonal anti–PD-L1 que exhibió actividad contra el carcinoma urotelial. No se han publicado ensayos clínicos controlados ni datos que demuestren que este fármaco prolongue la supervivencia o mejore la calidad de vida.
Evidencia (durvalumab):
- En un estudio (NCT01693562) se evaluó la eficacia del durvalumab (10 mg/kg IV cada 14 días) en 191 pacientes de carcinoma urotelial metastásico localmente avanzado, cuya enfermedad había progresado mientras se sometían a quimioterapia, no eran aptos o no deseaban ser tratados con quimioterapia.[64][Nivel de evidencia C3]
- Luego de una mediana de seguimiento de 5,78 meses, la tasa de respuesta general fue del 17,8 %.
- La tasa de respuesta fue del 27,6% en pacientes con expresión alta de PD-L1 comparada con el 5,1 % en pacientes que presentaban una expresión baja de PD-L1 o no la presentaban.
- Se notificaron efectos adversos de grado alto en el 6,8 % de los pacientes, incluso el 2,1 % con efectos adversos inmunitarios de grado alto.
Radioterapia de haz externo para la paliación
La radioterapia definitiva con quimioterapia o sin esta, que se evaluó sobre todo para pacientes con enfermedad localmente avanzada (T2–T4), parece tener un potencial curativo mínimo en pacientes con metástasis en los ganglios linfáticos regionales.
Derivación urinaria o cistectomía para la paliación
La derivación urinaria se puede indicar no solo para la paliación de los síntomas urinarios sino, también, para preservar el funcionamiento renal de quienes son aptos para recibir quimioterapia.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Vieweg J, Gschwend JE, Herr HW, et al.: The impact of primary stage on survival in patients with lymph node positive bladder cancer. J Urol 161 (1): 72-6, 1999. [PUBMED Abstract]
- Hoimes CJ, Flaig TW, Milowsky MI, et al.: Enfortumab Vedotin Plus Pembrolizumab in Previously Untreated Advanced Urothelial Cancer. J Clin Oncol 41 (1): 22-31, 2023. [PUBMED Abstract]
- O'Donnell PH, Milowsky MI, Petrylak DP, et al.: Enfortumab Vedotin With or Without Pembrolizumab in Cisplatin-Ineligible Patients With Previously Untreated Locally Advanced or Metastatic Urothelial Cancer. J Clin Oncol 41 (25): 4107-4117, 2023. [PUBMED Abstract]
- Powles TB, Perez Valderrama B, Gupta S, et al.: LBA6 EV-302/KEYNOTE-A39: Open-label, randomized phase III study of enfortumab vedotin in combination with pembrolizumab (EV+P) vs chemotherapy (Chemo) in previously untreated locally advanced metastatic urothelial carcinoma (la/mUC). [Abstract] Ann Oncol 34 (Suppl 2): A-6, S1340, 2023.
- van der Heijden MS, Sonpavde G, Powles T, et al.: Nivolumab plus Gemcitabine-Cisplatin in Advanced Urothelial Carcinoma. N Engl J Med 389 (19): 1778-1789, 2023. [PUBMED Abstract]
- Kachnic LA, Kaufman DS, Heney NM, et al.: Bladder preservation by combined modality therapy for invasive bladder cancer. J Clin Oncol 15 (3): 1022-9, 1997. [PUBMED Abstract]
- Tester W, Porter A, Asbell S, et al.: Combined modality program with possible organ preservation for invasive bladder carcinoma: results of RTOG protocol 85-12. Int J Radiat Oncol Biol Phys 25 (5): 783-90, 1993. [PUBMED Abstract]
- Logothetis CJ, Johnson DE, Chong C, et al.: Adjuvant chemotherapy of bladder cancer: a preliminary report. J Urol 139 (6): 1207-11, 1988. [PUBMED Abstract]
- Skinner DG, Daniels JR, Russell CA, et al.: The role of adjuvant chemotherapy following cystectomy for invasive bladder cancer: a prospective comparative trial. J Urol 145 (3): 459-64; discussion 464-7, 1991. [PUBMED Abstract]
- Scher HI: Chemotherapy for invasive bladder cancer: neoadjuvant versus adjuvant. Semin Oncol 17 (5): 555-65, 1990. [PUBMED Abstract]
- von der Maase H, Sengelov L, Roberts JT, et al.: Long-term survival results of a randomized trial comparing gemcitabine plus cisplatin, with methotrexate, vinblastine, doxorubicin, plus cisplatin in patients with bladder cancer. J Clin Oncol 23 (21): 4602-8, 2005. [PUBMED Abstract]
- Vaishampayan UN, Faulkner JR, Small EJ, et al.: Phase II trial of carboplatin and paclitaxel in cisplatin-pretreated advanced transitional cell carcinoma: a Southwest Oncology Group study. Cancer 104 (8): 1627-32, 2005. [PUBMED Abstract]
- Carles J, Nogué M: Gemcitabine/carboplatin in advanced urothelial cancer. Semin Oncol 28 (3 Suppl 10): 19-24, 2001. [PUBMED Abstract]
- Linardou H, Aravantinos G, Efstathiou E, et al.: Gemcitabine and carboplatin combination as first-line treatment in elderly patients and those unfit for cisplatin-based chemotherapy with advanced bladder carcinoma: Phase II study of the Hellenic Co-operative Oncology Group. Urology 64 (3): 479-84, 2004. [PUBMED Abstract]
- De Santis M, Bellmunt J, Mead G, et al.: Randomized phase II/III trial assessing gemcitabine/ carboplatin and methotrexate/carboplatin/vinblastine in patients with advanced urothelial cancer "unfit" for cisplatin-based chemotherapy: phase II--results of EORTC study 30986. J Clin Oncol 27 (33): 5634-9, 2009. [PUBMED Abstract]
- Sternberg CN, Calabrò F, Pizzocaro G, et al.: Chemotherapy with an every-2-week regimen of gemcitabine and paclitaxel in patients with transitional cell carcinoma who have received prior cisplatin-based therapy. Cancer 92 (12): 2993-8, 2001. [PUBMED Abstract]
- Kaufman DS, Carducci MA, Kuzel TM, et al.: A multi-institutional phase II trial of gemcitabine plus paclitaxel in patients with locally advanced or metastatic urothelial cancer. Urol Oncol 22 (5): 393-7, 2004 Sep-Oct. [PUBMED Abstract]
- Calabrò F, Lorusso V, Rosati G, et al.: Gemcitabine and paclitaxel every 2 weeks in patients with previously untreated urothelial carcinoma. Cancer 115 (12): 2652-9, 2009. [PUBMED Abstract]
- Stadler WM, Kuzel T, Roth B, et al.: Phase II study of single-agent gemcitabine in previously untreated patients with metastatic urothelial cancer. J Clin Oncol 15 (11): 3394-8, 1997. [PUBMED Abstract]
- Lorusso V, Pollera CF, Antimi M, et al.: A phase II study of gemcitabine in patients with transitional cell carcinoma of the urinary tract previously treated with platinum. Italian Co-operative Group on Bladder Cancer. Eur J Cancer 34 (8): 1208-12, 1998. [PUBMED Abstract]
- Roth BJ, Dreicer R, Einhorn LH, et al.: Significant activity of paclitaxel in advanced transitional-cell carcinoma of the urothelium: a phase II trial of the Eastern Cooperative Oncology Group. J Clin Oncol 12 (11): 2264-70, 1994. [PUBMED Abstract]
- Dreicer R, Gustin DM, See WA, et al.: Paclitaxel in advanced urothelial carcinoma: its role in patients with renal insufficiency and as salvage therapy. J Urol 156 (5): 1606-8, 1996. [PUBMED Abstract]
- Vaughn DJ, Broome CM, Hussain M, et al.: Phase II trial of weekly paclitaxel in patients with previously treated advanced urothelial cancer. J Clin Oncol 20 (4): 937-40, 2002. [PUBMED Abstract]
- Bellmunt J, Albanell J, Gallego OS, et al.: Carboplatin, methotrexate, and vinblastine in patients with bladder cancer who were ineligible for cisplatin-based chemotherapy. Cancer 70 (7): 1974-9, 1992. [PUBMED Abstract]
- Bellmunt J, Ribas A, Albanell J, et al.: M-CAVI, a neoadjuvant carboplatin-based regimen for the treatment of T2-4N0M0 carcinoma of the bladder. Am J Clin Oncol 19 (4): 344-8, 1996. [PUBMED Abstract]
- Skarlos DV, Aravantinos G, Linardou E, et al.: Chemotherapy with methotrexate, vinblastine, epirubicin and carboplatin (Carbo-MVE) in transitional cell urothelial cancer. A Hellenic Co-Operative Oncology Group study. Eur Urol 31 (4): 420-7, 1997. [PUBMED Abstract]
- Hainsworth JD, Meluch AA, Litchy S, et al.: Paclitaxel, carboplatin, and gemcitabine in the treatment of patients with advanced transitional cell carcinoma of the urothelium. Cancer 103 (11): 2298-303, 2005. [PUBMED Abstract]
- Bamias A, Aravantinos G, Deliveliotis C, et al.: Docetaxel and cisplatin with granulocyte colony-stimulating factor (G-CSF) versus MVAC with G-CSF in advanced urothelial carcinoma: a multicenter, randomized, phase III study from the Hellenic Cooperative Oncology Group. J Clin Oncol 22 (2): 220-8, 2004. [PUBMED Abstract]
- Logothetis CJ, Dexeus FH, Finn L, et al.: A prospective randomized trial comparing MVAC and CISCA chemotherapy for patients with metastatic urothelial tumors. J Clin Oncol 8 (6): 1050-5, 1990. [PUBMED Abstract]
- Loehrer PJ, Einhorn LH, Elson PJ, et al.: A randomized comparison of cisplatin alone or in combination with methotrexate, vinblastine, and doxorubicin in patients with metastatic urothelial carcinoma: a cooperative group study. J Clin Oncol 10 (7): 1066-73, 1992. [PUBMED Abstract]
- Mead GM, Russell M, Clark P, et al.: A randomized trial comparing methotrexate and vinblastine (MV) with cisplatin, methotrexate and vinblastine (CMV) in advanced transitional cell carcinoma: results and a report on prognostic factors in a Medical Research Council study. MRC Advanced Bladder Cancer Working Party. Br J Cancer 78 (8): 1067-75, 1998. [PUBMED Abstract]
- Sternberg CN, de Mulder P, Schornagel JH, et al.: Seven year update of an EORTC phase III trial of high-dose intensity M-VAC chemotherapy and G-CSF versus classic M-VAC in advanced urothelial tract tumours. Eur J Cancer 42 (1): 50-4, 2006. [PUBMED Abstract]
- von der Maase H, Hansen SW, Roberts JT, et al.: Gemcitabine and cisplatin versus methotrexate, vinblastine, doxorubicin, and cisplatin in advanced or metastatic bladder cancer: results of a large, randomized, multinational, multicenter, phase III study. J Clin Oncol 18 (17): 3068-77, 2000. [PUBMED Abstract]
- Jahnson S, Pedersen J, Westman G: Bladder carcinoma--a 20-year review of radical irradiation therapy. Radiother Oncol 22 (2): 111-7, 1991. [PUBMED Abstract]
- Coppin CM, Gospodarowicz MK, James K, et al.: Improved local control of invasive bladder cancer by concurrent cisplatin and preoperative or definitive radiation. The National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol 14 (11): 2901-7, 1996. [PUBMED Abstract]
- Shipley WU, Winter KA, Kaufman DS, et al.: Phase III trial of neoadjuvant chemotherapy in patients with invasive bladder cancer treated with selective bladder preservation by combined radiation therapy and chemotherapy: initial results of Radiation Therapy Oncology Group 89-03. J Clin Oncol 16 (11): 3576-83, 1998. [PUBMED Abstract]
- James ND, Hussain SA, Hall E, et al.: Radiotherapy with or without chemotherapy in muscle-invasive bladder cancer. N Engl J Med 366 (16): 1477-88, 2012. [PUBMED Abstract]
- Raghavan D, Huben R: Management of bladder cancer. Curr Probl Cancer 19 (1): 1-64, 1995 Jan-Feb. [PUBMED Abstract]
- Sweeney CJ, Roth BJ, Kabbinavar FF, et al.: Phase II study of pemetrexed for second-line treatment of transitional cell cancer of the urothelium. J Clin Oncol 24 (21): 3451-7, 2006. [PUBMED Abstract]
- Vaughn DJ, Malkowicz SB, Zoltick B, et al.: Paclitaxel plus carboplatin in advanced carcinoma of the urothelium: an active and tolerable outpatient regimen. J Clin Oncol 16 (1): 255-60, 1998. [PUBMED Abstract]
- Zielinski CC, Schnack B, Grbovic M, et al.: Paclitaxel and carboplatin in patients with metastatic urothelial cancer: results of a phase II trial. Br J Cancer 78 (3): 370-4, 1998. [PUBMED Abstract]
- Bajorin DF, McCaffrey JA, Dodd PM, et al.: Ifosfamide, paclitaxel, and cisplatin for patients with advanced transitional cell carcinoma of the urothelial tract: final report of a phase II trial evaluating two dosing schedules. Cancer 88 (7): 1671-8, 2000. [PUBMED Abstract]
- Carles J, Nogué M, Domènech M, et al.: Carboplatin-gemcitabine treatment of patients with transitional cell carcinoma of the bladder and impaired renal function. Oncology 59 (1): 24-7, 2000. [PUBMED Abstract]
- Dreicer R, Manola J, Roth BJ, et al.: Phase II study of cisplatin and paclitaxel in advanced carcinoma of the urothelium: an Eastern Cooperative Oncology Group Study. J Clin Oncol 18 (5): 1058-61, 2000. [PUBMED Abstract]
- Hussain M, Vaishampayan U, Du W, et al.: Combination paclitaxel, carboplatin, and gemcitabine is an active treatment for advanced urothelial cancer. J Clin Oncol 19 (9): 2527-33, 2001. [PUBMED Abstract]
- Meluch AA, Greco FA, Burris HA, et al.: Paclitaxel and gemcitabine chemotherapy for advanced transitional-cell carcinoma of the urothelial tract: a phase II trial of the Minnie Pearl cancer research network. J Clin Oncol 19 (12): 3018-24, 2001. [PUBMED Abstract]
- Albers P, Siener R, Härtlein M, et al.: Gemcitabine monotherapy as second-line treatment in cisplatin-refractory transitional cell carcinoma - prognostic factors for response and improvement of quality of life. Onkologie 25 (1): 47-52, 2002. [PUBMED Abstract]
- Li J, Juliar B, Yiannoutsos C, et al.: Weekly paclitaxel and gemcitabine in advanced transitional-cell carcinoma of the urothelium: a phase II Hoosier Oncology Group study. J Clin Oncol 23 (6): 1185-91, 2005. [PUBMED Abstract]
- Lorusso V, Crucitta E, Silvestris N, et al.: Randomised, open-label, phase II trial of paclitaxel, gemcitabine and cisplatin versus gemcitabine and cisplatin as first-line chemotherapy in advanced transitional cell carcinoma of the urothelium. Oncol Rep 13 (2): 283-7, 2005. [PUBMED Abstract]
- Fechner G, Siener R, Reimann M, et al.: Randomised phase II trial of gemcitabine and paclitaxel second-line chemotherapy in patients with transitional cell carcinoma (AUO Trial AB 20/99). Int J Clin Pract 60 (1): 27-31, 2006. [PUBMED Abstract]
- Galsky MD, Mironov S, Iasonos A, et al.: Phase II trial of pemetrexed as second-line therapy in patients with metastatic urothelial carcinoma. Invest New Drugs 25 (3): 265-70, 2007. [PUBMED Abstract]
- Chee CE, Jett JR, Bernath AM, et al.: Phase 2 trial of pemetrexed disodium and carboplatin in previously untreated extensive-stage small cell lung cancer, N0423. Cancer 116 (10): 2382-9, 2010. [PUBMED Abstract]
- Plimack ER, Bellmunt J, Gupta S, et al.: Safety and activity of pembrolizumab in patients with locally advanced or metastatic urothelial cancer (KEYNOTE-012): a non-randomised, open-label, phase 1b study. Lancet Oncol 18 (2): 212-220, 2017. [PUBMED Abstract]
- Sharma P, Retz M, Siefker-Radtke A, et al.: Nivolumab in metastatic urothelial carcinoma after platinum therapy (CheckMate 275): a multicentre, single-arm, phase 2 trial. Lancet Oncol 18 (3): 312-322, 2017. [PUBMED Abstract]
- Sharma P, Callahan MK, Bono P, et al.: Nivolumab monotherapy in recurrent metastatic urothelial carcinoma (CheckMate 032): a multicentre, open-label, two-stage, multi-arm, phase 1/2 trial. Lancet Oncol 17 (11): 1590-1598, 2016. [PUBMED Abstract]
- Rosenberg JE, Hoffman-Censits J, Powles T, et al.: Atezolizumab in patients with locally advanced and metastatic urothelial carcinoma who have progressed following treatment with platinum-based chemotherapy: a single-arm, multicentre, phase 2 trial. Lancet 387 (10031): 1909-20, 2016. [PUBMED Abstract]
- Balar AV, Galsky MD, Rosenberg JE, et al.: Atezolizumab as first-line treatment in cisplatin-ineligible patients with locally advanced and metastatic urothelial carcinoma: a single-arm, multicentre, phase 2 trial. Lancet 389 (10064): 67-76, 2017. [PUBMED Abstract]
- Bellmunt J, de Wit R, Vaughn DJ, et al.: Pembrolizumab as Second-Line Therapy for Advanced Urothelial Carcinoma. N Engl J Med 376 (11): 1015-1026, 2017. [PUBMED Abstract]
- Balar AV, Castellano D, O'Donnell PH, et al.: First-line pembrolizumab in cisplatin-ineligible patients with locally advanced and unresectable or metastatic urothelial cancer (KEYNOTE-052): a multicentre, single-arm, phase 2 study. Lancet Oncol 18 (11): 1483-1492, 2017. [PUBMED Abstract]
- Powles T, Durán I, van der Heijden MS, et al.: Atezolizumab versus chemotherapy in patients with platinum-treated locally advanced or metastatic urothelial carcinoma (IMvigor211): a multicentre, open-label, phase 3 randomised controlled trial. Lancet 391 (10122): 748-757, 2018. [PUBMED Abstract]
- Powles T, Park SH, Voog E, et al.: Avelumab Maintenance Therapy for Advanced or Metastatic Urothelial Carcinoma. N Engl J Med 383 (13): 1218-1230, 2020. [PUBMED Abstract]
- Apolo AB, Ellerton JA, Infante JR, et al.: Updated efficacy and safety of avelumab in metastatic urothelial carcinoma (mUC): pooled analysis from 2 cohorts of the phase 1b Javelin solid tumor study. [Abstract] J Clin Oncol 35 (Suppl 15): A-4529, 2017.
- Patel MR, Ellerton J, Infante JR, et al.: Avelumab in metastatic urothelial carcinoma after platinum failure (JAVELIN Solid Tumor): pooled results from two expansion cohorts of an open-label, phase 1 trial. Lancet Oncol 19 (1): 51-64, 2018. [PUBMED Abstract]
- Powles T, O'Donnell PH, Massard C, et al.: Efficacy and Safety of Durvalumab in Locally Advanced or Metastatic Urothelial Carcinoma: Updated Results From a Phase 1/2 Open-label Study. JAMA Oncol 3 (9): e172411, 2017. [PUBMED Abstract]
Tratamiento del cáncer de vejiga recidivante
Por lo general, el pronóstico para cualquier paciente con cáncer de vejiga invasivo progresivo o recidivante es precario. El tratamiento de la recidiva depende del tratamiento previo, los sitios de recidiva y las consideraciones individuales del paciente.
Opciones de tratamiento del cáncer de vejiga recidivante
Las opciones de tratamiento del cáncer de vejiga recidivante son las siguientes:
- Quimioterapia combinada.
- Inmunoterapia.
- Terapia dirigida.
- Cirugía para tumores superficiales nuevos o localizados.
- Terapia paliativa.
- Participación en ensayos clínicos.
Quimioterapia combinada
Los pacientes que no recibieron quimioterapia previa por un carcinoma urotelial, se deberían considerar para recibir quimioterapia como se describió más arriba para la enfermedad en estadio IV.
Para los pacientes de carcinoma de células de transición recidivante, la quimioterapia combinada produjo tasas altas de respuesta, con respuestas ocasionales completas.[1,2]
Los regímenes de quimioterapia combinada con base en cisplatino son el estándar de atención para el tratamiento inicial de pacientes con cáncer de vejiga en estadio IV que pueden tolerarlos.[3-7] En el marco de ensayos controlados aleatorizados, los únicos regímenes de quimioterapia que mostraron como resultado una supervivencia más prolongada son MVAC (metotrexato, vinblastina, doxorrubicina y cisplatino), MVAC de dosis densa y CMV (cisplatino, metotrexato y vinblastina).
En un ensayo controlado aleatorizado se comparó GC (gemcitabina y cisplatino) con MVAC; ninguno régimen se relacionó con una diferencia estadísticamente significativa en la tasa de respuesta o la supervivencia. En general, aunque ambos regímenes se consideran equivalentes, no se han comparado en un ensayo de ausencia de inferioridad. Es de destacar que los pacientes con buen estado funcional y enfermedad solo en los ganglios linfáticos tienen una tasa baja pero significativa de lograr una remisión completa duradera con MVAC o GC. En el ensayo grande, aleatorizado y controlado en el que se comparó MVAC con GC, por ejemplo, la tasa de supervivencia general (SG) a 5 años en pacientes con enfermedad solo en los ganglios linfáticos fue de 20,9 %.[8] En un ensayo controlado aleatorizado, se comparó MVAC de dosis densa con MVAC de dosis estándar; MVAC se dosis densa se relacionó con una supervivencia más prolongada.
Los regímenes con cisplatino como sustancia única y aquellos con sustancias múltiples que no incluyen cisplatino nunca lograron mostrar una mejora de la supervivencia en un ensayo controlado aleatorizado. Para los pacientes que no son aptos para someterse a regímenes de quimioterapia de sustancias múltiples que incluyen cisplatino, ningún régimen logró exhibir una prolongación de la supervivencia; sin embargo, se han demostrado respuestas radiológicas mensurables con muchos regímenes.
Estos regímenes incluyen carboplatino más paclitaxel,[9] carboplatino más gemcitabina,[10-12] paclitaxel más gemcitabina,[13-15] gemcitabina como sustancia única y [16,17] paclitaxel como sustancia única.[18-20] Se han estudiado, pero no ampliamente usado, los regímenes con carboplatino, metotrexato y vinblastina; carboplatino, epirrubicina, metotrexato y vinblastina; y paclitaxel, gemcitabina y carboplatino.[21-24]
Evidencia (quimioterapia combinada):
- En un ensayo prospectivo aleatorizado en el que se comparó MVAC con cisplatino, ciclofosfamida y doxorrubicina, el régimen MVAC demostró mejorar la tasa de respuesta y prolongar la mediana de supervivencia (48 vs. 36 semanas; P = 0,003).[25]
- Los resultados de un ensayo aleatorizado en el que se comparó MVAC con cisplatino como sustancia única para el cáncer de vejiga en estadio avanzado también mostraron una ventaja significativa de MVAC, tanto en términos de tasa de respuesta como de mediana de supervivencia (12,5 vs. 8,2 meses; P = 0,002).[26]
- En un ensayo controlado aleatorizado de varios centros, se comparó CMV con metotrexato más vinblastina sin cisplatino en 214 pacientes. El riesgo relativo de muerte fue de 0,68 (intervalo de confianza [IC] 95 %, 0,51–0,90; P = 0,0065) en favor de CMV. La mediana de supervivencia fue de 7 meses con CMV comparada con 4,5 meses con metotrexato más vinblastina.[27]
- La European Organisation for Research and Treatment of Cancer (EORTC) condujo otro ensayo aleatorizado para estudiar a 263 pacientes de cáncer de vejiga en estadio avanzado y evaluar la eficacia del régimen MVAC con dosis de intensidad alta administrado cada 2 semanas con el factor estimulante de colonias de granulocitos (G-CSF) versus el régimen MVAC clásico administrado cada 4 semanas.[28]
- Aunque no hubo una diferencia significativa en la SG en el momento de una mediana de seguimiento de 3,2 años (cociente de riesgos instantáneos [CRI], 0,80; IC 95 %, 0,60–1,06; P = 0,122), en una actualización de la mediana de seguimiento a los 7,3 años, se notificó que el régimen MVAC con dosis de intensidad alta se relacionó con una mejora de la SG (CRI, 0,76; IC 95 %, 0,58–0,99; P = 0,042), con una tasa de supervivencia a 5 años del 22 % comparada con el 14 %en los pacientes tratados con el régimen MVAC clásico.
- El régimen MVAC con dosis de intensidad alta también se relacionó con tasas de respuesta más altas (72 vs. 58 %; P =0,016), mejora de la mediana de supervivencia sin progresión (SSP) (9,5 vs. 8,1 meses; P = 0,017) y disminución de la fiebre neutropénica (10 vs. 26 %; P < 0,001), aunque solo el 19 % de los pacientes tratados con un régimen MVAC clásico alguna vez recibieron G-CSF.[28][Nivel de evidencia A1] Un desequilibrio en los factores pronósticos iniciales (es decir, se encontraron metástasis viscerales en 37 pacientes asignados aleatoriamente al régimen MVAC de dosis alta y 47 pacientes asignados al régimen MVAC clásico) puede explicar, en parte, estos resultados.
- Gemcitabina más cisplatino.
- En un ensayo aleatorizado de fase III realizado en múltiples centros en el que se comparó el régimen GC con MVAC en 405 pacientes de cáncer de vejiga en estadio avanzado o metastásico, GC produjo tasas de respuesta, tiempo transcurrido hasta la progresión y SG (CRI, 1,04; IC 95 %, 0,82–1,32; P = 0,75) similares a MVAC; sin embargo, GC exhibió un mejor perfil de toxicidad y se toleró mejor que MVAC.
Aunque este estudio no se diseñó para mostrar la equivalencia de los dos regímenes, la eficacia similar y la reducción de los efectos tóxicos con GC, este régimen es una alternativa razonable para pacientes que no pueden tolerar el régimen MVAC.[29][Nivel de evidencia A1]
- Otros regímenes quimioterapéuticos que han mostrado actividad para el cáncer de vejiga metastásico son paclitaxel como sustancia única, gemcitabina como sustancia única, pemetrexed como sustancia única, carboplatino combinado con gemcitabina o paclitaxel, y gemcitabina combinada con paclitaxel. No hay ensayos de fase III que demuestren un beneficio de la quimioterapia de segunda línea para la supervivencia o la calidad de vida.[30-37]
Inmunoterapia
La inmunoterapia se propone como una alternativa de tratamiento para los pacientes de cáncer de vejiga recidivante. En los ensayos clínicos, los inhibidores de puntos de control inmunitario que exhiben actividad contra la proteína de muerte celular programada 1 (PD-1) o el ligando 1 de muerte celular programada (PD-L1) tuvieron efecto contra el carcinoma urotelial de pacientes tratados antes con quimioterapia con derivados del cisplatino o que no eran aptos para recibirla.[38-42] Actualmente hay cuatro fármacos aprobados; sin embargo, el pembrolizumab es el fármaco que tiene el mayor nivel de evidencia científica y los mejores datos de supervivencia.
Pembrolizumab
El pembrolizumab es un anticuerpo monoclonal humanizado que se une al PD-1. En pacientes tratados antes con quimioterapia con derivados del platino, se observó que el pembrolizumab prolongó más la SG que la quimioterapia de segunda línea. Como resultado, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó el pembrolizumab para pacientes de carcinoma urotelial localmente avanzado o metastásico que pertenecen a una de las tres categorías siguientes:
- No son aptos para recibir cisplatino y tienen tumores que expresan PD-L1 (puntaje positivo combinado [CPS] de por lo menos el 10 %).
- No son aptos para recibir cisplatino y carboplatino.
- Exhiben progresión de la enfermedad después de recibir quimioterapia con derivados del platino.
Es importante señalar que, en 2018, la FDA emitió una alerta para informar que los datos preliminares de dos ensayos en curso exhibieron una supervivencia más breve en los ensayos de primera línea que compararon el tratamiento con pembrolizumab o atezolizumab con el tratamiento con base en cisplatino o carboplatino. Como resultado, se enmendaron las fichas técnicas para restringir el uso de ambos fármacos para las tres categorías de pacientes descritas más arriba.
Evidencia (pembrolizumab):
- En un ensayo internacional de fase III, sin anonimato, aleatorizado y controlado (NCT02256436) de pembrolizumab (200 mg intravenosos [IV] cada 21 días) versus quimioterapia de segunda línea (paclitaxel, docetaxel o vinflunina, a elección del investigador) para pacientes cuya enfermedad progresó después del tratamiento con quimioterapia a base de derivados del platino, la mediana de SG fue más larga con pembrolizumab (10,3 meses vs. 7,4 meses; CRI, 0,73; IC 95 %, 0,59–0,91).[43]
- En pacientes con un CPS de PD-L1 de por lo menos el 10 %, la mediana de SG fue de 8,0 meses con pembrolizumab comparada con 5,2 meses de quimioterapia (CRI, 0,57; IC 95 %, 0,37–0,88).
- La tasa de SSP a los 12 meses fue del 16,8 % (IC 95 %, 12,3–22,0 %) en el grupo de pembrolizumab y del 6,2 % (IC 95 %, 3,3–10,2 %) en el grupo de quimioterapia.
- La tasa de respuesta objetiva fue del 21,1 % en el grupo de pembrolizumab y del 11,4 % en el grupo de quimioterapia. Entre quienes respondieron, la mediana de duración de la respuesta superó los 18 meses con pembrolizumab comparada con una respuesta de 4,3 meses con quimioterapia.
- El pembrolizumab se relacionó con una tasa más baja de efectos adversos relacionados con el tratamiento que la quimioterapia (60,9 vs. 90,2 %) y una tasa más baja de efectos adversos de grado alto (15,0 vs. 49,4 %). Los efectos adversos más comunes con pembrolizumab fueron prurito, fatiga, náuseas, diarrea y disminución del apetito.[43][Nivel de evidencia A1]
- En un ensayo de fase II (NCT02335424) de pembrolizumab con un solo grupo de 370 pacientes de carcinoma urotelial localmente avanzado o metastásico que nunca se trataron y no eran aptos para recibir cisplatino, la tasa de respuesta general fue del 29 %. En pacientes con un CPS de PD-L1 de por lo menos el 10 %, la tasa de respuesta general fue del 51 %.[44]
- La mediana de duración de la respuesta no se había alcanzado. De las respuestas, el 82 % duraron por lo menos 6 meses.
- Diez por ciento de los pacientes sufrieron un efecto adverso grave y 1 paciente murió como consecuencia de efectos adversos relacionados con el tratamiento. Los efectos adversos de grado alto más comunes fueron fatiga (2 %), aumento de la fosfatasa alcalina (1 %), colitis (1 %) y debilidad muscular (1 %).[44][Nivel de evidencia C3]
Atezolizumab
El atezolizumab es un anticuerpo monoclonal humanizado que se une a la PD-L1 e impide que esta se fije a sus receptores PD-1 o B7-1. Se ha notificado en ensayos clínicos que el atezolizumab es eficaz contra el carcinoma urotelial, pero no se observó prolongación de la SG o mejoría de la calidad de vida. En el único ensayo controlado aleatorizado en el que se probó el atezolizumab, no se notificó una diferencia significativa de SG en comparación con la quimioterapia de segunda línea.
La FDA aprobó el atezolizumab para pacientes de carcinoma urotelial localmente avanzado o metastásico que pertenecen a una de las tres categorías siguientes:
- No son aptos para recibir cisplatino y tienen tumores que expresan PD-L1 (por lo menos el 5 % del área tumoral cubierto por células inmunitarias que se infiltran en el tumor y se tiñen con PD-L1).
- No son aptos para recibir cisplatino y carboplatino.
- Exhiben progresión de la enfermedad después de recibir quimioterapia con derivados del platino.
Es importante señalar que, en 2018, la FDA emitió una alerta para informar que los datos preliminares de dos ensayos en curso exhibieron una supervivencia más breve en los ensayos de primera línea que compararon el tratamiento con pembrolizumab o atezolizumab con el tratamiento con base en cisplatino o carboplatino. Como resultado, se enmendaron las fichas técnicas para restringir el uso de ambos fármacos para las tres categorías de pacientes descritas más arriba.
Evidencia (atezolizumab):
- El ensayo IMvigor211 (NCT02302807) es un ensayo aleatorizado y controlado en el que se comparó el atezolizumab con la quimioterapia de segunda línea (docetaxel, paclitaxel o vinflunina) en 931 pacientes de carcinoma urotelial localmente avanzado o metastásico que se trataron antes con quimioterapia con derivados del platino.[45] En el diseño del ensayo se especificó que la SG se evaluaría principalmente en pacientes cuyos tumores exhibieran por lo menos el 5 % de células con expresión de PD-L1.
- La mediana de SG fue de 11,1 meses con atezolizumab versus 10,6 meses con quimioterapia en pacientes con un mínimo del 5 % de células tumorales que expresaban PD-L1 (P = 0,41).[45][Nivel de evidencia A1]
- Las tasas de respuesta también fueron similares: el 23 % con atezolizumab y el 22 % con quimioterapia.
- Los pacientes que recibieron atezolizumab presentaron una tasa más baja de toxicidad de grado alto (20 vs. 43 %) y una tasa más baja de abandono del tratamiento por efectos adversos (7 vs. 18 %).
- En un ensayo multicéntrico de un solo grupo (NCT0108652) se incluyeron 315 pacientes con carcinoma urotelial localmente avanzado inoperable o metastásico que no eran aptos para recibir cisplatino o que se habían tratado antes con quimioterapia con derivados del platino. Los pacientes recibieron atezolizumab (1200 mg IV cada 21 días). Se notificaron los siguientes resultados:[41][Nivel de evidencia C2]
- La tasa de respuesta general fue del 15 %.
- Tras una mediana de seguimiento de 11,7 meses, 38 de 45 participantes (84 %) tuvieron una respuesta continua.
- Se obtuvo una tasa de respuesta del 27 % en aquellos con expresión de PD-L1 de por lo menos el 5 %, del 10 % en aquellos con expresión de PD-L1 del 1 % al 5 %, y del 8 % en aquellos con expresión de PD-L1 menor del 1 %.
- Se notificaron efectos adversos de grados 3 y 4 en el 16 % de los pacientes, y efectos adversos de grado alto relacionados con el sistema inmunitario en el 5 % de los pacientes.
- De forma similar, en un estudio (NCT02108652) de 123 pacientes de carcinoma urotelial localmente avanzado metastásico sin tratamiento previo que no eran aptos para recibir cisplatino, y que se trataron con atezolizumab, se notificó una tasa de respuesta objetiva del 23 % y respuesta completa en el 9 % de los pacientes en el momento de la mediana de seguimiento de 17,2 meses.[42][Nivel de evidencia C2]
- De las 27 respuestas, 19 estaban en curso cuando se analizaron los datos. La mediana de SG fue de 15,9 meses.
- Se notificaron efectos adversos de grado alto en el 16 % de los pacientes; se interrumpió el tratamiento en el 8 % de los pacientes por efectos adversos y hubo una muerte relacionada con el tratamiento.
Nivolumab
El nivolumab es un anticuerpo completamente humano de tipo inmunoglobulina G4 que se une al inhibidor de punto de control inmunitario PD-1 y bloquea la interacción entre PD-L1 y PD-L2 con PD-1. Debido a la carencia de publicaciones de ensayos controlados, no se dispone de datos que demuestren que el consumo de nivolumab prolongue la supervivencia o mejore la calidad de vida.
Evidencia (nivolumab):
- En un ensayo multicéntrico (NCT01928394) se incluyeron 86 pacientes de carcinoma urotelial metastásico cuya enfermedad progresó después de recibir quimioterapia con derivados del platino. Los pacientes recibieron nivolumab (3 mg/kg IV cada 2 semanas).[40][Nivel de evidencia B4]
- Tras un seguimiento mínimo de 9 meses y una mediana de seguimiento de 15 meses, el 24 % de los pacientes tuvo una respuesta objetiva y el 22 % presentó efectos adversos de grado 3 o 4.
- Entre los efectos adversos más frecuentes se observaron concentraciones altas de lipasa o amilasa, fatiga, exantema, disnea, linfopenia y neutropenia.
- En otro estudio multicéntrico (NCT02387996) de 270 pacientes de carcinoma urotelial metastásico o localmente avanzado con progresión después del tratamiento con quimioterapia con derivados del platino, se notificó una tasa de respuesta objetiva de 20 %.[39][Nivel de evidencia B4]
- Al evaluar la expresión de PD-L1, la tasa de respuesta objetiva fue del 28 % en aquellos con una expresión de PD-L1 del 5 % o más; el 24 % en aquellos con una expresión de PD-L1 del 1 % o más; y el 16 % en aquellos con una expresión de PD-L1 de menos del 1 %.
- Se notificaron efectos adversos de grado 3 y 4 en el 18 % de los pacientes.
- Hubo 3 muertes relacionadas con el tratamiento.
Avelumab
El avelumab es un anticuerpo monoclonal anti–PD-L1 que exhibió actividad contra el carcinoma urotelial. En un ensayo controlado aleatorizado, se informó un beneficio de la SG con el avelumab de mantenimiento cuando se administró después de la quimioterapia con derivados del platino en pacientes cuyo cáncer no progresó durante la quimioterapia.
Evidencia (avelumab):
- En un estudio de fase III (NCT02603432) se evaluó el avelumab de mantenimiento (10 mg/kg IV cada 14 días) en pacientes con carcinoma urotelial metastásico que no progresó durante el tratamiento con quimioterapia de primera línea con gemcitabina combinada con cisplatino o carboplatino. Después de 4 a 6 ciclos de quimioterapia, 700 pacientes se asignaron al azar a recibir los mejores cuidados médicos de apoyo (grupo de control) o los mejores cuidados médicos de apoyo y avelumab de mantenimiento (grupo de avelumab).[46][Nivel de evidencia A1]
- La tasa de SG a 1 año fue del 71,3 % en el grupo de avelumab en comparación con el 58,4 % en el grupo de control (CRI, 0,69; IC 95 %, 0,56–0,86).
- El beneficio en la SG se limitó a los pacientes cuyos tumores eran positivos para PD-L1. La SG de los pacientes con tumores negativos para PD-L1 no fue significativamente diferente entre los dos grupos.
- Los pacientes con tumores positivos para PD-L1, tuvieron una tasa de SG a 1 año del 79,1 % en el grupo de avelumab y del 60,4 % en el grupo de control (CRI, 0,56; IC 95 %, 0,40–0,79).
- En la población general del estudio, la mediana de la SSP fue de 3,7 meses en los pacientes del grupo de avelumab y de 2,0 meses en los pacientes del grupo de control (CRI, 0,62; IC 95 %, 0,52–0,75). En los pacientes con tumores positivos para PD-L1, la mediana de la SSP fue de 5,7 meses en el grupo con avelumab y de 2,1 meses en el grupo que recibió solo los mejores cuidados médicos de apoyo (CRI, 0,56; IC 95 %, 0,43–0,73).
- Se notificaron eventos adversos de grado 3 o superior en el 47,4 % de los pacientes en el grupo de avelumab y en el 25,2 % de los pacientes en el grupo de control. La mayoría de los eventos adversos con avelumab fueron inmunitarios, el 9 % de los pacientes que recibieron avelumab se trataron con dosis altas de glucocorticoides por estos eventos.
- En un estudio (NCT01772004) de avelumab (10 mg/kg IV cada 14 días) administrado a 249 pacientes de carcinoma urotelial metastásico que presentaron progresión de la enfermedad después del tratamiento con quimioterapia con derivados del platino), se notificaron los siguientes resultados:.[47,48][Nivel de evidencia C3]
- Entre los 161 pacientes a quienes se les dio seguimiento durante por lo menos 6 meses, la tasa de respuesta general fue del 17 % y la respuesta fue continua en 23 de 28 pacientes que respondieron luego de una mediana de seguimiento de 7,3 meses. La respuesta completa se presentó en el 6 % de los pacientes.
- La tasa de respuesta general fue del 25,0 % en pacientes que tenían como mínimo el 5 % de las células tumorales con expresión de PD-L1 y el 14,7 % de ellos con menos del 5 % con expresión de PD-L1.
- La mediana de SSP fue de 6,3 semanas; el 23 % de los pacientes estaban libres de progresión a las 24 semanas.
- Se notificaron efectos adversos relacionados con el tratamiento en el 66,7 % de los pacientes y el 8,4 % de los pacientes presentaron efectos adversos de grado alto. Hubo 1 muerte por neumonía relacionada con el tratamiento. Se notificaron efectos adversos inmunitarios de grado alto en el 2,4 % de los pacientes.
Durvalumab
El durvalumab es un anticuerpo monoclonal anti–PD-L1 que exhibió actividad contra el carcinoma urotelial. No se han publicado ensayos clínicos controlados ni datos que demuestren que este fármaco prolongue la supervivencia o mejore la calidad de vida.
Evidencia (durvalumab):
- En un estudio (NCT01693562) se evaluó la eficacia del durvalumab (10 mg/kg IV cada 14 días) en 191 pacientes de carcinoma urotelial metastásico localmente avanzado, cuya enfermedad había progresado mientras se sometían a quimioterapia, no eran aptos o no deseaban ser tratados con quimioterapia.[49][Nivel de evidencia C3]
- Luego de una mediana de seguimiento de 5,78 meses, la tasa de respuesta general fue del 17,8 %.
- La tasa de respuesta fue del 27,6 % en pacientes con expresión alta de PD-L1 comparada con el 5,1 % en pacientes que presentaba una expresión baja de PD-L1 o no la presentaban.
- Se notificaron efectos adversos de grado alto en el 6,8 % de los pacientes, incluso el 2,1 % con efectos adversos inmunitarios de grado alto.
Terapia dirigida
Ramucirumab
El ramucirumab es un anticuerpo monoclonal de tipo inmunoglobulina G1 que bloquea el receptor 2 del factor de crecimiento endotelial vascular (VEGFR-2). La FDA aprobó su uso en pacientes con carcinoma gástrico y adenocarcinoma de unión gastroesofágica, pero no en pacientes con cáncer de vejiga.
Evidencia (ramucirumab):
- En un ensayo multicéntrico con enmascaramiento doble, aleatorizado y controlado de fase III, se comparó la quimioterapia de docetaxel y ramucirumab con docetaxel y placebo, en 530 pacientes con carcinoma urotelial metastásico que progresó después del tratamiento de quimioterapia con derivados del platino. De estos pacientes, 45 (8,5 %) habían recibido tratamiento previo con inmunoterapia.[50][Nivel de evidencia B1]
- No hubo diferencia significativa en la SG de ambos grupos.
- La mediana de la SSP fue de 1,3 meses (39 días) más larga en el grupo de ramucirumab en comparación con el grupo de placebo (4,1 meses vs. 2,8 meses; CRI, 0,696; IC 95 %, 0,573–0,845, P = 0,0002).
- La tasa de respuesta general fue del 26 % en el grupo de ramucirumab y del 14 % en el grupo de placebo.
- Se interrumpió el tratamiento debido a los eventos adversos en el 19 % de los pacientes que recibieron docetaxel con ramucirumab y en el 8 % de los pacientes que recibieron docetaxel con placebo.
- Se notificaron eventos adversos de grado 3 o superior en el 48 % de los pacientes en el grupo de ramucirumab y en el 41 % de los pacientes en el grupo de placebo. Los eventos adversos incluyeron neutropenia febril, epistaxis, hipertensión, hematuria y proteinuria. Ocurrió sepsis en el 2 % de los pacientes que recibieron ramucirumab y en ninguno de los pacientes que recibió placebo.
Enfortumab vedotina
Enfortumab vedotina es un tipo de medicamento para la terapia dirigida que se llama conjugado anticuerpo-fármaco. Los conjugados anticuerpo-fármaco contienen un anticuerpo monoclonal ligado químicamente a un medicamento. La parte de anticuerpo monoclonal en la enfortumab vedotina se enlaza a una proteína llamada nectina-4, que se encuentra sobre la superficie de la mayoría de las células cancerosas de la vejiga. El anticuerpo se liga químicamente a la monometilauristatina E, o MMAE, un tipo de fármaco de quimioterapia llamado inhibidor de microtúbulos. Una vez que las células absorben el conjugado, el medicamento les impide multiplicarse y provoca su muerte.
La FDA aprobó enfortumab vedotina para administrar a pacientes de carcinoma urotelial metastásico que progresó después de tratarse con quimioterapia con derivados del platino de primera línea y con terapia de segunda línea con un inhibidor de punto de control inmunitario. La aprobación se fundamentó en un ensayo de un solo grupo de 125 pacientes de carcinoma urotelial metastásico.[51]
Evidencia (enfortumab vedotina):
- En un ensayo de un solo grupo, se trató con enfortumab vedotina a 125 pacientes de carcinoma urotelial metastásico.[51]
- Se logró una tasa de respuesta general del 44 % y una tasa de respuesta completa del 12 %.
- La mediana de duración de la respuesta fue de 7,6 meses.
- Los episodios adversos incluyeron fatiga (50 %), neuropatía periférica (50 %), alopecia (49 %), exantema (48 %), disminución del apetito (44 %) y disgeusia (40 %).
Debido a que no hubo un grupo de control, en este estudio no se pudieron demostrar mejoras de la SG o la calidad de vida. Está en marcha un ensayo de seguimiento de fase III para evaluar los beneficios de esta medicación.
Erdafitinib
Erdafitinib (JNJ-42756493) es un potente inhibidor de tirosina–cinasas de los FGFR 1–4. La FDA aprobó el erdafitinib para pacientes con carcinoma urotelial que presentan una variante en 1 de los 4 genes FGFR y enfermedad que progresó después de recibir quimioterapia.
Alrededor del 20 % de los carcinomas uroteliales metastásicos de vejiga tienen variantes de FGFR, así como el 35 % de los carcinomas uroteliales de los uréteres y la pelvis renal.
Evidencia (erdafitinib):
- En un estudio de fase II se incluyó a pacientes de carcinoma urotelial metastásico cuya enfermedad había progresado durante la quimioterapia sistémica o después de esta.[52] Para ser aptos para el estudio, era necesario que los pacientes tuvieran tumores con una variante de FGFR3 o una fusión génica FGFR2::FGFR3. El ensayo se diseñó en un principio como un ensayo aleatorizado de fase II para comparar el tratamiento continuo con el intermitente; sin embargo, luego de un análisis de toxicidad, el ensayo se convirtió en un estudio de un solo grupo sometido a tratamiento continuo con aumento de la dosis. El análisis publicado se enfoca en esta última fase del estudio, llamado "grupo de régimen seleccionado". El grupo de régimen seleccionado incluyó a 99 pacientes: 74 con una variante de FGFR3 y 25 con una fusión génica FGFR2::FGFR3.
- La tasa de respuesta evaluada mediante una revisión radiológica independiente fue del 34 %.
- La tasa de respuesta fue más alta en los pacientes con variantes de FGFR3 que en aquellos con fusiones génicas FGFR2::FGFR3.
- Los episodios adversos de grado 3 que afectaron por lo menos al 10 % de los pacientes incluyeron estomatitis e hiponatremia. Los episodios adversos más comunes de cualquier grado fueron hiponatremia (77 %), estomatitis (58 %), diarrea (51 %), xerostomía (46 %), disminución del apetito (38 %) y disgeusia (37 %).
Cirugía para tumores superficiales nuevos o localizados
El tratamiento de tumores superficiales nuevos o localmente invasivos que se presentan en el entorno de una terapia conservadora previa para una neoplasia de vejiga superficial se trató en el estadio I de este resumen.
Terapia paliativa
Se deberá considerar la terapia paliativa para pacientes con tumores sintomáticos.
Participación en ensayos clínicos
La enfermedad recidivante o progresiva en sitios distantes o que se presenta después de la terapia local definitiva tiene un pronóstico muy adverso y los pacientes deben considerar la participación en ensayos clínicos toda vez que sea posible.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Sternberg CN, Yagoda A, Scher HI, et al.: Methotrexate, vinblastine, doxorubicin, and cisplatin for advanced transitional cell carcinoma of the urothelium. Efficacy and patterns of response and relapse. Cancer 64 (12): 2448-58, 1989. [PUBMED Abstract]
- Harker WG, Meyers FJ, Freiha FS, et al.: Cisplatin, methotrexate, and vinblastine (CMV): an effective chemotherapy regimen for metastatic transitional cell carcinoma of the urinary tract. A Northern California Oncology Group study. J Clin Oncol 3 (11): 1463-70, 1985. [PUBMED Abstract]
- Kachnic LA, Kaufman DS, Heney NM, et al.: Bladder preservation by combined modality therapy for invasive bladder cancer. J Clin Oncol 15 (3): 1022-9, 1997. [PUBMED Abstract]
- Tester W, Porter A, Asbell S, et al.: Combined modality program with possible organ preservation for invasive bladder carcinoma: results of RTOG protocol 85-12. Int J Radiat Oncol Biol Phys 25 (5): 783-90, 1993. [PUBMED Abstract]
- Logothetis CJ, Johnson DE, Chong C, et al.: Adjuvant chemotherapy of bladder cancer: a preliminary report. J Urol 139 (6): 1207-11, 1988. [PUBMED Abstract]
- Skinner DG, Daniels JR, Russell CA, et al.: The role of adjuvant chemotherapy following cystectomy for invasive bladder cancer: a prospective comparative trial. J Urol 145 (3): 459-64; discussion 464-7, 1991. [PUBMED Abstract]
- Scher HI: Chemotherapy for invasive bladder cancer: neoadjuvant versus adjuvant. Semin Oncol 17 (5): 555-65, 1990. [PUBMED Abstract]
- von der Maase H, Sengelov L, Roberts JT, et al.: Long-term survival results of a randomized trial comparing gemcitabine plus cisplatin, with methotrexate, vinblastine, doxorubicin, plus cisplatin in patients with bladder cancer. J Clin Oncol 23 (21): 4602-8, 2005. [PUBMED Abstract]
- Vaishampayan UN, Faulkner JR, Small EJ, et al.: Phase II trial of carboplatin and paclitaxel in cisplatin-pretreated advanced transitional cell carcinoma: a Southwest Oncology Group study. Cancer 104 (8): 1627-32, 2005. [PUBMED Abstract]
- Carles J, Nogué M: Gemcitabine/carboplatin in advanced urothelial cancer. Semin Oncol 28 (3 Suppl 10): 19-24, 2001. [PUBMED Abstract]
- Linardou H, Aravantinos G, Efstathiou E, et al.: Gemcitabine and carboplatin combination as first-line treatment in elderly patients and those unfit for cisplatin-based chemotherapy with advanced bladder carcinoma: Phase II study of the Hellenic Co-operative Oncology Group. Urology 64 (3): 479-84, 2004. [PUBMED Abstract]
- De Santis M, Bellmunt J, Mead G, et al.: Randomized phase II/III trial assessing gemcitabine/ carboplatin and methotrexate/carboplatin/vinblastine in patients with advanced urothelial cancer "unfit" for cisplatin-based chemotherapy: phase II--results of EORTC study 30986. J Clin Oncol 27 (33): 5634-9, 2009. [PUBMED Abstract]
- Sternberg CN, Calabrò F, Pizzocaro G, et al.: Chemotherapy with an every-2-week regimen of gemcitabine and paclitaxel in patients with transitional cell carcinoma who have received prior cisplatin-based therapy. Cancer 92 (12): 2993-8, 2001. [PUBMED Abstract]
- Kaufman DS, Carducci MA, Kuzel TM, et al.: A multi-institutional phase II trial of gemcitabine plus paclitaxel in patients with locally advanced or metastatic urothelial cancer. Urol Oncol 22 (5): 393-7, 2004 Sep-Oct. [PUBMED Abstract]
- Calabrò F, Lorusso V, Rosati G, et al.: Gemcitabine and paclitaxel every 2 weeks in patients with previously untreated urothelial carcinoma. Cancer 115 (12): 2652-9, 2009. [PUBMED Abstract]
- Stadler WM, Kuzel T, Roth B, et al.: Phase II study of single-agent gemcitabine in previously untreated patients with metastatic urothelial cancer. J Clin Oncol 15 (11): 3394-8, 1997. [PUBMED Abstract]
- Lorusso V, Pollera CF, Antimi M, et al.: A phase II study of gemcitabine in patients with transitional cell carcinoma of the urinary tract previously treated with platinum. Italian Co-operative Group on Bladder Cancer. Eur J Cancer 34 (8): 1208-12, 1998. [PUBMED Abstract]
- Roth BJ, Dreicer R, Einhorn LH, et al.: Significant activity of paclitaxel in advanced transitional-cell carcinoma of the urothelium: a phase II trial of the Eastern Cooperative Oncology Group. J Clin Oncol 12 (11): 2264-70, 1994. [PUBMED Abstract]
- Dreicer R, Gustin DM, See WA, et al.: Paclitaxel in advanced urothelial carcinoma: its role in patients with renal insufficiency and as salvage therapy. J Urol 156 (5): 1606-8, 1996. [PUBMED Abstract]
- Vaughn DJ, Broome CM, Hussain M, et al.: Phase II trial of weekly paclitaxel in patients with previously treated advanced urothelial cancer. J Clin Oncol 20 (4): 937-40, 2002. [PUBMED Abstract]
- Bellmunt J, Albanell J, Gallego OS, et al.: Carboplatin, methotrexate, and vinblastine in patients with bladder cancer who were ineligible for cisplatin-based chemotherapy. Cancer 70 (7): 1974-9, 1992. [PUBMED Abstract]
- Bellmunt J, Ribas A, Albanell J, et al.: M-CAVI, a neoadjuvant carboplatin-based regimen for the treatment of T2-4N0M0 carcinoma of the bladder. Am J Clin Oncol 19 (4): 344-8, 1996. [PUBMED Abstract]
- Skarlos DV, Aravantinos G, Linardou E, et al.: Chemotherapy with methotrexate, vinblastine, epirubicin and carboplatin (Carbo-MVE) in transitional cell urothelial cancer. A Hellenic Co-Operative Oncology Group study. Eur Urol 31 (4): 420-7, 1997. [PUBMED Abstract]
- Hainsworth JD, Meluch AA, Litchy S, et al.: Paclitaxel, carboplatin, and gemcitabine in the treatment of patients with advanced transitional cell carcinoma of the urothelium. Cancer 103 (11): 2298-303, 2005. [PUBMED Abstract]
- Logothetis CJ, Dexeus FH, Finn L, et al.: A prospective randomized trial comparing MVAC and CISCA chemotherapy for patients with metastatic urothelial tumors. J Clin Oncol 8 (6): 1050-5, 1990. [PUBMED Abstract]
- Loehrer PJ, Einhorn LH, Elson PJ, et al.: A randomized comparison of cisplatin alone or in combination with methotrexate, vinblastine, and doxorubicin in patients with metastatic urothelial carcinoma: a cooperative group study. J Clin Oncol 10 (7): 1066-73, 1992. [PUBMED Abstract]
- Mead GM, Russell M, Clark P, et al.: A randomized trial comparing methotrexate and vinblastine (MV) with cisplatin, methotrexate and vinblastine (CMV) in advanced transitional cell carcinoma: results and a report on prognostic factors in a Medical Research Council study. MRC Advanced Bladder Cancer Working Party. Br J Cancer 78 (8): 1067-75, 1998. [PUBMED Abstract]
- Sternberg CN, de Mulder P, Schornagel JH, et al.: Seven year update of an EORTC phase III trial of high-dose intensity M-VAC chemotherapy and G-CSF versus classic M-VAC in advanced urothelial tract tumours. Eur J Cancer 42 (1): 50-4, 2006. [PUBMED Abstract]
- von der Maase H, Hansen SW, Roberts JT, et al.: Gemcitabine and cisplatin versus methotrexate, vinblastine, doxorubicin, and cisplatin in advanced or metastatic bladder cancer: results of a large, randomized, multinational, multicenter, phase III study. J Clin Oncol 18 (17): 3068-77, 2000. [PUBMED Abstract]
- Roth BJ: Preliminary experience with paclitaxel in advanced bladder cancer. Semin Oncol 22 (3 Suppl 6): 1-5, 1995. [PUBMED Abstract]
- Witte RS, Elson P, Bono B, et al.: Eastern Cooperative Oncology Group phase II trial of ifosfamide in the treatment of previously treated advanced urothelial carcinoma. J Clin Oncol 15 (2): 589-93, 1997. [PUBMED Abstract]
- Einhorn LH, Roth BJ, Ansari R, et al.: Phase II trial of vinblastine, ifosfamide, and gallium combination chemotherapy in metastatic urothelial carcinoma. J Clin Oncol 12 (11): 2271-6, 1994. [PUBMED Abstract]
- Pollera CF, Ceribelli A, Crecco M, et al.: Weekly gemcitabine in advanced bladder cancer: a preliminary report from a phase I study. Ann Oncol 5 (2): 182-4, 1994. [PUBMED Abstract]
- Seidman AD, Scher HI, Heinemann MH, et al.: Continuous infusion gallium nitrate for patients with advanced refractory urothelial tract tumors. Cancer 68 (12): 2561-5, 1991. [PUBMED Abstract]
- Roth BJ: Ifosfamide in the treatment of bladder cancer. Semin Oncol 23 (3 Suppl 6): 50-5, 1996. [PUBMED Abstract]
- Bajorin DF: Paclitaxel in the treatment of advanced urothelial cancer. Oncology (Huntingt) 14 (1): 43-52, 57; discussion 58, 61-2, 2000. [PUBMED Abstract]
- Sweeney CJ, Roth BJ, Kabbinavar FF, et al.: Phase II study of pemetrexed for second-line treatment of transitional cell cancer of the urothelium. J Clin Oncol 24 (21): 3451-7, 2006. [PUBMED Abstract]
- Plimack ER, Bellmunt J, Gupta S, et al.: Safety and activity of pembrolizumab in patients with locally advanced or metastatic urothelial cancer (KEYNOTE-012): a non-randomised, open-label, phase 1b study. Lancet Oncol 18 (2): 212-220, 2017. [PUBMED Abstract]
- Sharma P, Retz M, Siefker-Radtke A, et al.: Nivolumab in metastatic urothelial carcinoma after platinum therapy (CheckMate 275): a multicentre, single-arm, phase 2 trial. Lancet Oncol 18 (3): 312-322, 2017. [PUBMED Abstract]
- Sharma P, Callahan MK, Bono P, et al.: Nivolumab monotherapy in recurrent metastatic urothelial carcinoma (CheckMate 032): a multicentre, open-label, two-stage, multi-arm, phase 1/2 trial. Lancet Oncol 17 (11): 1590-1598, 2016. [PUBMED Abstract]
- Rosenberg JE, Hoffman-Censits J, Powles T, et al.: Atezolizumab in patients with locally advanced and metastatic urothelial carcinoma who have progressed following treatment with platinum-based chemotherapy: a single-arm, multicentre, phase 2 trial. Lancet 387 (10031): 1909-20, 2016. [PUBMED Abstract]
- Balar AV, Galsky MD, Rosenberg JE, et al.: Atezolizumab as first-line treatment in cisplatin-ineligible patients with locally advanced and metastatic urothelial carcinoma: a single-arm, multicentre, phase 2 trial. Lancet 389 (10064): 67-76, 2017. [PUBMED Abstract]
- Bellmunt J, de Wit R, Vaughn DJ, et al.: Pembrolizumab as Second-Line Therapy for Advanced Urothelial Carcinoma. N Engl J Med 376 (11): 1015-1026, 2017. [PUBMED Abstract]
- Balar AV, Castellano D, O'Donnell PH, et al.: First-line pembrolizumab in cisplatin-ineligible patients with locally advanced and unresectable or metastatic urothelial cancer (KEYNOTE-052): a multicentre, single-arm, phase 2 study. Lancet Oncol 18 (11): 1483-1492, 2017. [PUBMED Abstract]
- Powles T, Durán I, van der Heijden MS, et al.: Atezolizumab versus chemotherapy in patients with platinum-treated locally advanced or metastatic urothelial carcinoma (IMvigor211): a multicentre, open-label, phase 3 randomised controlled trial. Lancet 391 (10122): 748-757, 2018. [PUBMED Abstract]
- Powles T, Park SH, Voog E, et al.: Avelumab Maintenance Therapy for Advanced or Metastatic Urothelial Carcinoma. N Engl J Med 383 (13): 1218-1230, 2020. [PUBMED Abstract]
- Apolo AB, Ellerton JA, Infante JR, et al.: Updated efficacy and safety of avelumab in metastatic urothelial carcinoma (mUC): pooled analysis from 2 cohorts of the phase 1b Javelin solid tumor study. [Abstract] J Clin Oncol 35 (Suppl 15): A-4529, 2017.
- Patel MR, Ellerton J, Infante JR, et al.: Avelumab in metastatic urothelial carcinoma after platinum failure (JAVELIN Solid Tumor): pooled results from two expansion cohorts of an open-label, phase 1 trial. Lancet Oncol 19 (1): 51-64, 2018. [PUBMED Abstract]
- Powles T, O'Donnell PH, Massard C, et al.: Efficacy and Safety of Durvalumab in Locally Advanced or Metastatic Urothelial Carcinoma: Updated Results From a Phase 1/2 Open-label Study. JAMA Oncol 3 (9): e172411, 2017. [PUBMED Abstract]
- Petrylak DP, de Wit R, Chi KN, et al.: Ramucirumab plus docetaxel versus placebo plus docetaxel in patients with locally advanced or metastatic urothelial carcinoma after platinum-based therapy (RANGE): overall survival and updated results of a randomised, double-blind, phase 3 trial. Lancet Oncol 21 (1): 105-120, 2020. [PUBMED Abstract]
- Rosenberg JE, O'Donnell PH, Balar AV, et al.: Pivotal Trial of Enfortumab Vedotin in Urothelial Carcinoma After Platinum and Anti-Programmed Death 1/Programmed Death Ligand 1 Therapy. J Clin Oncol 37 (29): 2592-2600, 2019. [PUBMED Abstract]
- Loriot Y, Necchi A, Park SH, et al.: Erdafitinib in Locally Advanced or Metastatic Urothelial Carcinoma. N Engl J Med 381 (4): 338-348, 2019. [PUBMED Abstract]
Actualizaciones más recientes a este resumen (03/28/2025)
Los resúmenes del PDQ con información sobre el cáncer se revisan con regularidad y se actualizan a medida que se obtiene nueva información. Esta sección describe los cambios más recientes introducidos en este resumen a partir de la fecha arriba indicada.
Información general sobre el cáncer de vejiga
Se actualizaron las estadísticas con el número estimado de casos nuevos y defunciones para 2025 (se citó a la American Cancer Society como referencia 2).
El Consejo editorial del PDQ sobre el tratamiento para adultos es responsable de la redacción y actualización de este resumen y mantiene independencia editorial respecto del NCI. El resumen refleja una revisión independiente de la bibliografía médica y no representa las políticas del NCI ni de los NIH. Para obtener más información sobre las políticas relativas a los resúmenes y la función de los consejos editoriales del PDQ responsables de su actualización, consultar Información sobre este resumen del PDQ e Información del PDQ® sobre el cáncer dirigida a profesionales de la salud.
Información sobre este resumen del PDQ
Propósito de este resumen
Este resumen de información del PDQ sobre el cáncer dirigido a profesionales de la salud proporciona información integral revisada por expertos y basada en la evidencia sobre el tratamiento del cáncer de vejiga. El objetivo es servir como fuente de información y ayuda para los profesionales clínicos durante la atención de pacientes. No ofrece pautas ni recomendaciones formales para tomar decisiones relacionadas con la atención sanitaria.
Revisores y actualizaciones
El consejo editorial del PDQ sobre el tratamiento para adultos, que mantiene independencia editorial respecto del Instituto Nacional del Cáncer (NCI), revisa este resumen de manera periódica y, en caso necesario, lo actualiza. Este resumen es el resultado de una revisión bibliográfica independiente y no constituye una declaración de política del NCI ni de los Institutos Nacionales de la Salud (NIH).
Cada mes, los integrantes de este consejo revisan los artículos publicados recientemente para determinar lo siguiente:
- Si el artículo se debe analizar en una reunión del consejo.
- Si conviene añadir texto acerca del artículo.
- Si se debe reemplazar o actualizar un artículo que ya se citó.
Los cambios en los resúmenes se deciden mediante consenso de los integrantes del consejo después de evaluar la solidez de la evidencia de los artículos publicados y determinar la forma de incorporar el artículo en el resumen.
Los revisores principales del sumario sobre Tratamiento del cáncer de vejiga son:
- Juskaran S. Chadha, DO (Moffitt Cancer Center)
- Jad Chahoud, MD, MPH (Moffitt Cancer Center)
- Timothy Gilligan, MD (Cleveland Clinic Taussig Cancer Institute)
- Joseph J. Park, MD (Duke University Medical Center)
Cualquier comentario o pregunta sobre el contenido de este resumen se debe enviar al Servicio de Información de Cáncer del Instituto Nacional del Cáncer. Por favor, no enviar preguntas o comentarios directamente a los integrantes del consejo, ya que no responderán consultas de manera individual.
Niveles de evidencia
Algunas de las referencias bibliográficas de este resumen se acompañan del nivel de evidencia. El propósito de esto es ayudar al lector a evaluar la solidez de la evidencia que respalda el uso de ciertas intervenciones o abordajes. El consejo editorial del PDQ sobre el tratamiento para adultos emplea un sistema de jerarquización formal para asignar los niveles de evidencia científica.
Permisos para el uso de este resumen
PDQ (Physician Data Query) es una marca registrada. Se autoriza el uso del texto de los documentos del PDQ; sin embargo, no se podrá identificar como un resumen de información sobre cáncer del PDQ del NCI, salvo que el resumen se reproduzca en su totalidad y se actualice de manera periódica. Por otra parte, se permitirá que un autor escriba una oración como “En el resumen del PDQ del NCI de información sobre la prevención del cáncer de mama se describen, de manera concisa, los siguientes riesgos: [incluir fragmento del resumen]”.
Se sugiere citar la referencia bibliográfica de este resumen del PDQ de la siguiente forma:
PDQ® sobre el tratamiento para adultos. PDQ Tratamiento del cáncer de vejiga. Bethesda, MD: National Cancer Institute. Actualización: <MM/DD/YYYY>. Disponible en: https://www.cancer.gov/espanol/tipos/vejiga/pro/tratamiento-vejiga-pdq. Fecha de acceso: <MM/DD/YYYY>.
Las imágenes en este resumen se reproducen con autorización del autor, el artista o la editorial para uso exclusivo en los resúmenes del PDQ. La utilización de las imágenes fuera del PDQ requiere la autorización del propietario, que el Instituto Nacional del Cáncer no puede otorgar. Para obtener más información sobre el uso de las ilustraciones de este resumen o de otras imágenes relacionadas con el cáncer, consultar Visuals Online, una colección de más de 2000 imágenes científicas.
Cláusula sobre el descargo de responsabilidad
Según la solidez de la evidencia, las opciones de tratamiento se clasifican como “estándar” o “en evaluación clínica”. Estas clasificaciones no se deben utilizar para justificar decisiones sobre reembolsos de seguros. Para obtener más información sobre la cobertura de seguros, consultar la página Manejo de la atención del cáncer en Cancer.gov/espanol.
Comuníquese con el Instituto Nacional del Cáncer
Para obtener más información sobre las opciones para comunicarse con el NCI, incluso la dirección de correo electrónico, el número telefónico o el chat, consultar la página del Servicio de Información de Cáncer del Instituto Nacional del Cáncer.