Tratamiento del meduloblastoma y otros tumores embrionarios del sistema nervioso central infantil (PDQ®)–Versión para profesionales de salud
Información general sobre el meduloblastoma y otros tumores embrionarios del sistema nervioso central
Clasificación de la Organización Mundial de la Salud de los tumores embrionarios del sistema nervioso central y del pineoblastoma
Los tumores embrionarios son un grupo de lesiones biológicamente heterogéneas que comparten la tendencia a diseminarse por el recorrido del líquido cefalorraquídeo (LCR) en el sistema nervioso central (SNC). Aunque hay una variabilidad importante, estos tumores se agrupan juntos desde el punto de vista histológico porque se componen, al menos en parte, de células hipercromáticas (tumores de células azules en tinción estándar), con citoplasma escaso, concentración densa y grado alto de actividad mitótica. Para diferenciar estos tumores es posible utilizar, en cierta medida, otras características histológicas e inmunohistoquímicas, como el grado de transformación celular visible y los linajes celulares identificables (ependimarios, gliales, etc.). Sin embargo, una convención, aceptada por la Organización Mundial de la Salud (OMS), también separa estos tumores según la presunta ubicación de origen dentro del SNC. Los estudios moleculares han corroborado las diferencias entre los tumores que surgen en distintas áreas del encéfalo y dan credibilidad parcial a este abordaje de clasificación.[1]
En 2016, la OMS propuso un sistema de clasificación de integración fenotípica y genotípica para los tumores del SNC en el que se usa un diagnóstico escalonado que tiene en cuenta el grado de la OMS, la clasificación histológica y la clasificación molecular.[2] El término tumor neuroectodérmico primitivo (TNEP) se ha eliminado del léxico diagnóstico de la OMS, aunque se conservan algunas entidades poco frecuentes (por ejemplo, el meduloepitelioma). Además, se agregó una entidad diferente desde el punto de vista molecular, el tumor embrionario con rosetas de capas múltiples (ETMR) y alteración de C19MC, que abarca el tumor embrionario con neurópilo abundante y rosetas verdaderas (ETANTR), el ependimoblastoma y el meduloepitelioma. La clasificación de la OMS se actualizará a medida que se definan otras entidades diferentes desde el punto de vista molecular.
El diagnóstico patológico de los tumores embrionarios se basa sobre todo en las características microscópicas histológicas e inmunohistológicas. No obstante, los estudios genético-moleculares se emplean cada vez más para subclasificar estos tumores. Estos hallazgos genético-moleculares también se utilizan para la estratificación del riesgo y la planificación del tratamiento.[3-6]
La clasificación de los tumores embrionarios de la OMS de 2021 es la siguiente:[7,8]
- Meduloblastoma.
- Meduloblastoma definido por características moleculares.
- Meduloblastoma con activación de WNT.
- Meduloblastoma con activación de SHH y TP53 natural.
- Meduloblastoma con activación de SHH y alteración de TP53.
- Meduloblastoma sin activación de WNT o SHH.
- Meduloblastoma definido por características histológicas.
- Meduloblastoma nodular desmoplásico.
- Meduloblastoma con nodularidad extensa.
- Meduloblastoma de células grandes.
- Meduloblastoma anaplásico.
- Meduloblastoma definido por características moleculares.
- Otros tumores embrionarios del sistema nervioso central.
- Tumor teratoide rabdoide atípico.
- Tumor neuroepitelial cribiforme.
- Tumor embrionario con rosetas de capas múltiples.
- Neuroblastoma del sistema nervioso central con activación de FOXR2.
- Tumor del sistema nervioso central con duplicación interna en tándem de BCOR.
- Tumor embrionario del sistema nervioso central sin clasificar o sin otra indicación.
Antes, el pineoblastoma se agrupaba de manera convencional con los tumores embrionarios. Sin embargo, ahora la OMS lo clasifica como un tumor de parénquima pineal. La clasificación de la OMS de 2021 para estos tumores es la siguiente:[7,8]
- Pineocitoma.
- Tumor de parénquima pineal de diferenciación intermedia.
- Pineoblastoma.
- Tumor papilar de la región pineal.
- Tumor mixoide desmoplásico de la región pineal con alteración de SMARCB1.
Debido a que el tratamiento de los pineoblastomas es muy similar al de los tumores embrionarios, en este resumen se incluyen los pineoblastomas. También se ha identificado un tumor algo alineado, el tumor de parénquima pineal de diferenciación intermedia, pero este no se considera un tumor embrionario y surge principalmente en adultos.[2]
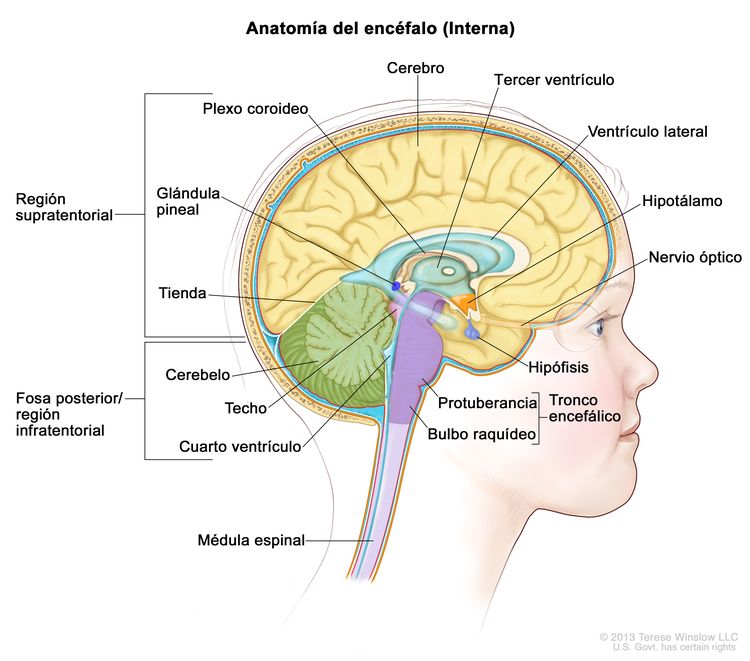
Características anatómicas
Incidencia
Los tumores embrionarios representan cerca del 20 % de los tumores primarios del SNC (neoplasias malignas del SNC y astrocitomas pilocíticos) que surgen en la niñez. Estos tumores aparecen a cualquier edad en la niñez, pero suelen agruparse en edades tempranas. La incidencia de tumores embrionarios en niños de 1 a 9 años es de 5 a 10 veces más alta que en adultos (consultar el Cuadro 1).[9,10]
| Grupo etario (años) | Tasa de incidencia anual (casos por millón) |
|---|---|
| aFuente: National Childhood Cancer Registry.[9] | |
| <5 | 10 |
| 5–9 | 7 |
| 10–19 | 2–3 |
Los meduloblastomas comprenden la gran mayoría de los tumores embrionarios en pediatría. Por definición, estos tumores surgen en la fosa posterior (consultar la Figura 1), donde constituyen cerca del 40 % de todos los tumores de fosa posterior. Cada una de las otras formas de tumores embrionarios constituyen el 2 % o menos de todos los tumores encefálicos infantiles.
Evaluación para el diagnóstico y la estadificación
Los estudios con imágenes y el análisis del LCR se incluyen en la evaluación para el diagnóstico y la estadificación.
Estudios con imágenes
Por lo general, el diagnóstico se establece mediante imágenes por resonancia magnética (IRM) o tomografía computarizada (TC). La IRM es preferible porque la relación anatómica entre el tumor y el encéfalo circundante y la diseminación tumoral se visualizan mejor con este método.[11,12]
Después del diagnóstico, la evaluación de todos los tumores embrionarios es bastante similar; en esencia, es independiente del subtipo histológico y de la ubicación del tumor. Dada la tendencia de estos tumores a diseminarse por todo el SNC de manera temprana en el curso de la enfermedad, se indica la evaluación con IRM de todo el eje encefalomedular. Es preferible captar las imágenes antes de la cirugía para evitar artefactos posoperatorios, en especial, sangre. A veces, estas imágenes son difíciles de interpretar y se deben obtener por lo menos en dos planos, con y sin contraste (gadolinio).[13] En un estudio sobre la importancia de los hallazgos equívocos en las IRM espinales de niños con meduloblastoma, se identificaron hallazgos equívocos en 48 de 100 pacientes (48 %). En el estudio se notificaron los siguientes resultados:[14]
- En el análisis por subgrupos se identificó una proporción más alta de hallazgos equívocos en el subgrupo SHH (P = 0,007).
- La supervivencia general (SG) a 5 años en niños con hallazgos equívocos en la IRM (80 %) no fue diferente a la SG a 5 años en pacientes con hallazgos normales (84,8 %) en la IRM, mientras que la SG en los pacientes con metástasis M3 fue inferior (54,7 %) (P = 0,02).
No obstante, en un estudio prospectivo del Children's Oncology Group (COG) se trató a 400 niños sin enfermedad metastásica con una dosis reducida (23,4 Gy) de radioterapia craneoespinal. Se encontraron indicios de posible enfermedad residual excesiva o enfermedad metastásica, o se consideró que las imágenes eran inadecuadas para la evaluación completa del sistema nervioso central, en casi el 20 % de los pacientes sometidos a revisión neurorradiográfica central. Entre los pacientes con revisión central de las imágenes, se encontró una supervivencia más precaria en los niños con enfermedad metastásica, en comparación con aquellos con enfermedad no diseminada. El subgrupo con imágenes inadecuadas, según la revisión central, tuvo una tasa de supervivencia intermedia entre la de los niños con imágenes adecuadas y la de quienes tenían enfermedad metastásica.[13] En un estudio prospectivo posterior del COG en el que se trató a más de 500 niños con dosis reducidas de radioterapia craneoespinal (23,4 Gy o 18 Gy), los pacientes con imágenes inadecuadas tuvieron una supervivencia más precaria.[15] Se han formulado directrices consensuadas que abarcan las técnicas de neuroimágenes, el momento oportuno para obtenerlas, además de los detalles que definen los estándares para la evaluación preoperatoria de todo el neuroeje y la evaluación posoperatoria de la cantidad de enfermedad residual.[16]
Después de la cirugía, se indican imágenes del sitio del tumor primario para determinar la extensión de la enfermedad residual.
Análisis del líquido cefalorraquídeo
Después de la cirugía, se hace un análisis del líquido cefalorraquídeo (LCR) lumbar, si se considera inocuo. Las neuroimágenes y la evaluación del LCR se consideran complementarias porque hasta el 10 % de los pacientes tienen indicios de células tumorales flotantes libres en el LCR en ausencia de indicios claros de enfermedad leptomeníngea en la IRM.[17]
El análisis del LCR se hace de manera convencional de 14 a 21 días después de la cirugía. Si el LCR se obtiene en el transcurso de los 14 días que siguen a la operación, es posible que la detección de células tumorales en el LCR se relacione con la intervención quirúrgica. En la mayoría de los sistemas de estadificación, si se obtiene líquido en los primeros días después de la cirugía y hay positividad, este resultado se debe confirmar con una punción lumbar posterior para que se considere de importancia diagnóstica. Por el contrario, si no se detectan células tumorales en el LCR no se necesita ninguna confirmación. Cuando la punción lumbar para obtener LCR se considera nociva entonces se puede obtener líquido ventricular. Sin embargo, es posible que este método no sea tan sensible como la evaluación del líquido lumbar.[17]
Debido a que los tumores embrionarios casi nunca presentan metástasis óseas, medulares o en otras partes del cuerpo en el momento del diagnóstico, no se indican otros estudios como aspiraciones de la médula ósea, radiografías del tórax o gammagrafías óseas, a menos que haya síntomas o signos que indiquen compromiso orgánico.
Factores pronósticos
Hay varios parámetros clínicos y biológicos que se relacionan con la probabilidad de controlar los tumores embrionarios después del tratamiento.[4] Se ha demostrado que muchos de estos factores son predictivos para los meduloblastomas, aunque algunos se usan para asignar el riesgo, en cierta medida, de otros tumores embrionarios. Los parámetros que se usan con mayor frecuencia para predecir el desenlace son los siguientes:[18,19]
Cada vez es más evidente, en especial, para los meduloblastomas, que el desenlace también se vincula con las características moleculares del tumor, pero esto no se ha demostrado de manera definitiva para otros tumores embrionarios.[1,5,6,20-23] Las tasas de SG oscilan entre el 30 % y el 90 %, según el subtipo molecular del meduloblastoma, la extensión de la diseminación en el momento del diagnóstico y, posiblemente, otros factores, como el grado de resección. Los niños con meduloblastoma que sobreviven durante 5 años se consideran curados de su tumor. Las tasas de supervivencia para otros tumores embrionarios son, por lo general, más precarias y oscilan entre el 5 % y el 50 %. En este resumen se describen las tasas de supervivencia específicas para cada subgrupo.[24-27]
En los estudios más antiguos, se observó que la presencia de compromiso del tronco encefálico en niños con meduloblastoma era un factor pronóstico. En estudios posteriores de pacientes tratados con radiación y quimioterapia, no se encontró un valor predictivo para este compromiso.[13,18]
Es fundamental obtener un diagnóstico exacto en los pacientes con tumores embrionarios. Por ejemplo, en el ensayo ACNS0332 (NCT00392327) en el que se inscribieron 80 pacientes con meduloblastoma de riesgo alto, tumores neuroectodérmico primitivos supratentoriales del sistema nervioso central (TNEP-SNC) y pineoblastoma, 60 pacientes tenían tejido suficiente para la evaluación. De estos tumores, 31 estaban fuera de la glándula pineal y 22 (71 %) eran tumores que no se pretendían incluir en el ensayo: 18 gliomas de grado alto, 2 tumores teratoides rabdoides atípicos y 2 ependimomas. Los desenlaces entre los diferentes tipos de tumores fueron muy diversos. Los pacientes con tumores embrionarios supratentoriales o pineoblastomas exhibieron una tasa de SSC a 5 años del 62,8 % (intervalo de confianza [IC] 95 %, 43,4–82,2 %) y una tasa de SG del 78,5 % (IC 95 %, 62,2–94,8 %), mientras que los pacientes con una clasificación molecular de gliomas de grado alto exhibieron una tasa de SSC del 5,6 % (IC 95 %, 0–13 %) y una tasa de SG del 12 % (IC 95 %, 0–24,7 %). Las tasas de supervivencia de los pacientes con gliomas de grado alto fueron similares a las tasas de los pacientes que participaron en estudios históricos en los que se evitó el uso de irradiación craneoespinal y quimioterapia intensiva. Por lo tanto, el pronóstico de los pacientes con TNEP-SNC o pineoblastoma es mucho más favorable que el que se suponía en pacientes sometidos a extirpación de gliomas de grado alto confirmados por análisis molecular.[28]
El pronóstico es precario para los pacientes con meduloepitelioma y ETMR, con tasas de supervivencia a 5 años que oscilan entre el 0 % y el 30 %.[29-31] En un análisis multivariante retrospectivo de 38 pacientes, la resección total o casi total, el uso de radioterapia y la administración de dosis altas de quimioterapia se relacionaron con un mejor pronóstico.[32][Nivel de evidencia C1] Otro análisis retrospectivo del Rare Brain Tumor Registry se hizo con datos de 159 pacientes con diagnóstico molecular confirmado de ETMR primario (mediana de edad en el momento del diagnóstico, 26 meses; IIC, 18–36 meses). En este estudio se observó una tasa de SSC del 57 % (IC 95 %, 47–68 %) a los 6 meses y del 31 % (IC 95 %, 21–42 %) a los 2 años. La tasa de SG fue del 29 % (IC 95 %, 20–38 %) a los 2 años y del 27 % (IC 95 %, 18–37 %) a los 4 años. La SG se relacionó con la presencia de enfermedad no metastásica (cociente de riesgos instantáneos [CRI], 0,48; IC 95 %, 0,28–0,80; P = 0,0057) y localización fuera del tronco encefálico (CRI, 0,42; IC 95 %, 0,22–0,81; P = 0,013) en el análisis univariante, así como con resección macroscópica total (CRI, 0,30; IC 95 %, 0,16–0,58; P = 0,0014), administración de dosis altas de quimioterapia (CRI, 0,35; IC 95 %, 0,19–0,67; P = 0,0020), y uso de radioterapia (CRI, 0,21; IC 95 %, 0,10–0,41; P < 0,0001) en el análisis multivariante.[33][Nivel de evidencia C1]
Alcance de la enfermedad en el sistema nervioso central en el momento del diagnóstico
Los pacientes con enfermedad diseminada en el sistema nervioso central (SNC) tienen el mayor riesgo de recaída de la enfermedad.[17-19] Del 10 % al 40 % de los pacientes con meduloblastoma tienen diseminación por el SNC en el momento del diagnóstico. Los lactantes presentan la incidencia más alta y los adolescentes y adultos presentan la incidencia más baja de diseminación por el SNC.
Los tumores embrionarios distintos del meduloblastoma y los pineoblastomas también pueden estar diseminados en el momento del diagnóstico, aunque la incidencia es algo inferior a la de los meduloblastomas, de cerca del 10 % al 20 %.[24,25] Los pacientes con tumores embrionarios distintos del meduloblastoma y pineoblastomas que tienen enfermedad diseminada en el momento del diagnóstico presentan una SG precaria, con tasas de supervivencia notificadas a 5 años que oscilan entre el 10 % y el 30 %.[24-27,34]
Edad en el momento del diagnóstico
Una edad menor a 3 años en el momento del diagnóstico presagia un pronóstico desfavorable para aquellos pacientes con meduloblastoma y, tal vez, otros tumores embrionarios.[35-40] La excepción es para aquellos pacientes con diagnóstico de meduloblastoma desmoplásico o meduloblastoma con nodularidad extensa (MBEN).
Cantidad de enfermedad residual después de la cirugía definitiva
La medición posoperatoria por IRM de la cantidad de enfermedad residual después de la cirugía definitiva ha reemplazado a la extensión de la resección como factor de predicción del desenlace.[13]
En los estudios más antiguos, el alcance de la resección del meduloblastoma se relacionó con la supervivencia.[18,19,41,42] En uno estudio Hirntumor (HIT) llevado a cabo con la International Society of Paediatric Oncology en 340 niños, se notificó que la enfermedad residual (>1,5 cm2) connotó una tasa de SSC a 5 años más precaria.[43] La extensión de la resección después de la cirugía todavía se usa para separar a los pacientes en grupos de riesgo; los pacientes que tienen más de 1,5 cm2 de enfermedad residual se clasifican en grupos de riesgo alto y se someten a intensificación de la irradiación craneoespinal con dosis de 36 Gy.
En un estudio internacional retrospectivo de colaboración, se incluyeron 787 pacientes de todas las edades con meduloblastoma tratados de diversas maneras. En el análisis del estudio se tuvieron en cuenta los subgrupos moleculares y los factores clínicos. En el análisis multivariante se encontró que la resección subtotal (>1,5 cm2 de enfermedad residual), pero no la resección casi total (<1,5 cm2 de enfermedad residual), se relacionó con una supervivencia sin progresión inferior, en comparación con la resección macroscópica total. En el estudio se indicó que no se justifican los intentos por extirpar el tumor completo, en especial, cuando la probabilidad de complicaciones neurológicas es alta, porque la resección macroscópica total tiene muy pocos beneficios, o no los tiene, cuando se compara con la resección casi total. Esto otorga cierta credibilidad al abordaje actual, en el que los pacientes con más de 1,5 cm2 de enfermedad residual se consideran pacientes de riesgo más alto.[44] En un análisis retrospectivo de 1100 pacientes con meduloblastoma caracterizado molecularmente, la resección subtotal se relacionó con una supervivencia más precaria en el análisis univariante (P < 0,0001). Sin embargo, la resección subtotal no fue un factor de pronóstico independiente en los análisis multivariantes ni fue un factor de pronóstico en los pacientes que no tenían enfermedad metastásica y que recibieron irradiación craneoespinal inicial.[45] Se necesitan estudios prospectivos para definir mejor el efecto de la extensión de la resección en el desenlace dentro de los subgrupos definidos molecularmente.
En los pacientes con otras formas de tumores embrionarios, no se ha mostrado de forma definitiva que la extensión de la resección afecte la supervivencia.[26] Sin embargo, en un estudio del COG de 66 niños con tumores embrionarios supratentoriales, se encontró que la extensión de la resección era pronóstica para aquellos pacientes con enfermedad localizada en el momento del diagnóstico.[46]
Características histopatológicas del tumor
Meduloblastoma. En análisis retrospectivos de este tipo de tumor se observó que las características histopatológicas, como la variante de células grandes, la anaplasia y la desmoplasia, se correlacionan con el desenlace.[36,47,48] En estudios prospectivos, los hallazgos inmunohistoquímicos e histopatológicos no predijeron el desenlace en niños mayores de 3 años en el momento del diagnóstico, a excepción de la variante anaplásica o de células grandes, que se relacionó con un pronóstico más precario.[13,22,49] En varios estudios se observó que el hallazgo histológico de desmoplasia, observado en pacientes de 3 años o menos con meduloblastoma desmoplásico, en especial MBEN, connota un pronóstico significativamente mejor, en comparación con los desenlaces de lactantes y niños pequeños con meduloblastoma clásico anaplásico o de células grandes.[22,35-37,50]; [38][Nivel de evidencia B4] En el grupo de tumores SHH con variantes de TP53 se observan variante somáticas y constitucionales de TP53. Ambos tipos de variantes connotan un pronóstico precario, en comparación con otros tumores con activación de la vía de SHH.[23]
Otros tumores embrionarios. En otros tipos de tumores embrionarios, las variaciones histológicas no se relacionan con desenlaces diferentes.
Características biológicas y moleculares de las células tumorales
Medida de la enfermedad residual mínima
En un estudio, las variaciones en el número de copias en el LCR, similares a las medidas en los tumores primarios, pronosticaron la recaída cuando estaban presentes después de la radioterapia, durante la quimioterapia o después de esta. Si este hallazgo se reproduce en ensayos clínicos prospectivos y la técnica se hace disponible en el ámbito clínico, será una medida importante de la enfermedad residual mínima y es probable que forme parte de la evaluación inicial, así como de las pruebas de vigilancia.[51]
Análisis genómico
Meduloblastoma. Los análisis genómicos (como los perfiles de expresión génica de ARN y metilación del DNA, así como la secuenciación del DNA para identificar variantes) permitieron identificar subtipos moleculares en secciones congeladas en fresco, incluidas en parafina y fijadas con formol.[3-6,20,21,52-59] Estos subtipos incluyen aquellos caracterizados por activación de la vía WNT y activación de la vía SHH, así como otros subgrupos caracterizados por alteraciones en los genes MYC o MYCN y otras alteraciones genómicas.[3-6,20,21,52-58] Los niños con meduloblastomas cuyos tumores exhiben activación de la vía WNT, por lo general, tienen un pronóstico excelente. Dentro del grupo de meduloblastomas sin activación de WNT ni SHH, existen subconjuntos de pacientes con pronósticos diferentes. Por ejemplo, los pacientes con pérdida del cromosoma 11 tienen un pronóstico excelente, similar al de aquellos con tumores WNT.[15,60,61] Los pacientes con tumores con activación de la vía SHH tienen un pronóstico que depende de la presencia o ausencia de variantes de TP53 (pronóstico favorable vs. desfavorable, respectivamente).[61] El desenlace para el resto de los pacientes es menos favorable que para los pacientes con activación de la vía WNT. En el meduloblastoma, las variantes se observan en un modo específico por subtipos. Las variantes de CTNNB1 se encuentran en la mayoría de los tumores del subtipo WNT. Las variantes de PTCH1, SMO y SUFU se encuentran en los tumores del subtipo SHH. La importancia pronóstica de las variantes recurrentes se alinea de cerca con la importancia del subtipo molecular con el que se relacionan.[4,62] En el momento de la recidiva, el subtipo permanece sin cambios respecto al subtipo molecular original en el momento del diagnóstico.[63]
Tumores embrionarios distintos del meduloblastoma. El análisis genómico integrado también ha permitido identificar subtipos moleculares de estos tumores con desenlaces diferentes. Para obtener información más detallada, consultar la sección Subtipos de tumores embrionarios distintos del meduloblastoma.
Seguimiento después del tratamiento
En los niños con tumores embrionarios lo más probable es que la recaída se presente dentro de los primeros 18 meses del diagnóstico.[43,64] La vigilancia mediante imágenes del encéfalo y la médula espinal suele hacerse a intervalos regulares durante el tratamiento y después de este (consultar el Cuadro 2). La frecuencia de estas imágenes, diseñadas para detectar la enfermedad recidivante en un estado asintomático temprano, se ha determinado de manera arbitraria y no se ha demostrado que influya de manera clara en la supervivencia.[65-68] La terapia de reemplazo de la hormona del crecimiento tampoco ha demostrado aumentar la probabilidad de recaída de la enfermedad y no debe afectar la frecuencia de las pruebas de vigilancia.[37]
| Período de vigilancia | Frecuencia de las consultas durante el período de vigilancia | Pruebas |
|---|---|---|
| IRM = Imagen por resonancia magnética. | ||
| aPara el pineoblastoma, continuar con evaluaciones de la médula espinal cada 6 meses durante 5 años desde el momento del diagnóstico. Aunque estas sugerencias se basan en una muestra pequeña, hay evidencia para continuar las pruebas de vigilancia en la médula espinal hasta 5 años después del diagnóstico.[69] | ||
| Primeros 3 años después del diagnóstico | Cada 3 meses | Examen físico |
| Imágenes del encéfalo cada 3 meses durante los 3 primeros años; luego, cada 6 meses durante los 2 años siguientes y después por elección del médico de cabecera o según el protocolo; IRM de la médula espinal cada 3 meses durante los primeros 2 años; luego, cada 6 meses durante 1 año, y luego por elección del médico tratante o según el protocolo.a | ||
| Evaluación endocrinológica anual | ||
| Pruebas neuropsicológicas cada 1–2 años | ||
| 3–5 años después del diagnóstico | Cada 6 meses | Examen físico |
| Imágenes del encéfalo y la médula espinal anuales | ||
| Evaluación endocrinológica anual | ||
| Pruebas neuropsicológicas cada 1–2 años | ||
| Más de 5 años después del diagnóstico | Una vez por año | Examen físico |
| Imágenes del encéfalo anuales | ||
| Evaluación endocrinológica anual | ||
| Pruebas neuropsicológicas cada 1–2 años (opcionales) | ||
La formulación de otras estrategias de vigilancia diferentes a las pruebas con imágenes para pacientes con meduloblastoma es objeto de investigación en curso. En un estudio de 134 niños con meduloblastoma recién diagnosticado, se detectaron variantes del número de copias al inicio en 123 pacientes (92 %) mediante pruebas de tumor primario y en 65 pacientes (49 %) mediante pruebas de LCR. Las variantes en el número de copias se detectaron con mayor frecuencia en el LCR de pacientes con enfermedad diseminada y en aquellos con progresión posterior. Se necesitarán estudios prospectivos para evaluar la posibilidad de que el análisis del número de copias en el LCR se convierta en un componente de las pruebas de vigilancia como medida de la enfermedad residual mínima y la recaída temprana en el meduloblastoma.[51]
Los niños y adolescentes sobrevivientes de cáncer necesitan un seguimiento minucioso, ya que es posible que los efectos secundarios del tratamiento del cáncer persistan o se presenten meses o años después de este. Para obtener información específica sobre la incidencia, el tipo y la vigilancia de los efectos tardíos en los niños y adolescentes sobrevivientes de cáncer, consultar Efectos tardíos del tratamiento anticanceroso en la niñez.
Bibliografía
- Pomeroy SL, Tamayo P, Gaasenbeek M, et al.: Prediction of central nervous system embryonal tumour outcome based on gene expression. Nature 415 (6870): 436-42, 2002. [PUBMED Abstract]
- Louis DN, Perry A, Reifenberger G, et al.: The 2016 World Health Organization Classification of Tumors of the Central Nervous System: a summary. Acta Neuropathol 131 (6): 803-20, 2016. [PUBMED Abstract]
- Pfister S, Remke M, Benner A, et al.: Outcome prediction in pediatric medulloblastoma based on DNA copy-number aberrations of chromosomes 6q and 17q and the MYC and MYCN loci. J Clin Oncol 27 (10): 1627-36, 2009. [PUBMED Abstract]
- Taylor MD, Northcott PA, Korshunov A, et al.: Molecular subgroups of medulloblastoma: the current consensus. Acta Neuropathol 123 (4): 465-72, 2012. [PUBMED Abstract]
- Kool M, Koster J, Bunt J, et al.: Integrated genomics identifies five medulloblastoma subtypes with distinct genetic profiles, pathway signatures and clinicopathological features. PLoS One 3 (8): e3088, 2008. [PUBMED Abstract]
- Ellison DW, Onilude OE, Lindsey JC, et al.: beta-Catenin status predicts a favorable outcome in childhood medulloblastoma: the United Kingdom Children's Cancer Study Group Brain Tumour Committee. J Clin Oncol 23 (31): 7951-7, 2005. [PUBMED Abstract]
- WHO Classification of Tumours Editorial Board, ed.: WHO Classification of Tumours: Central Nervous System Tumours. Vol. 6. 5th ed. IARC Press; 2021.
- Louis DN, Perry A, Wesseling P, et al.: The 2021 WHO Classification of Tumors of the Central Nervous System: a summary. Neuro Oncol 23 (8): 1231-1251, 2021. [PUBMED Abstract]
- National Cancer Institute: NCCR*Explorer: An interactive website for NCCR cancer statistics. Bethesda, MD: National Cancer Institute. Available online. Last accessed February 25, 2025.
- Surveillance Research Program, National Cancer Institute: SEER*Explorer: An interactive website for SEER cancer statistics. Bethesda, MD: National Cancer Institute. Available online. Last accessed December 30, 2024.
- Chintagumpala MM, Paulino A, Panigrahy A, et al.: Embryonal and pineal region tumors. In: Pizzo PA, Poplack DG, eds.: Principles and Practice of Pediatric Oncology. 7th ed. Lippincott Williams and Wilkins, 2015, pp 671-99.
- Jaju A, Li Y, Dahmoush H, et al.: Imaging of pediatric brain tumors: A COG Diagnostic Imaging Committee/SPR Oncology Committee/ASPNR White Paper. Pediatr Blood Cancer 70 Suppl 4 (Suppl 4): e30147, 2023. [PUBMED Abstract]
- Packer RJ, Gajjar A, Vezina G, et al.: Phase III study of craniospinal radiation therapy followed by adjuvant chemotherapy for newly diagnosed average-risk medulloblastoma. J Clin Oncol 24 (25): 4202-8, 2006. [PUBMED Abstract]
- Bennett J, Ashmawy R, Ramaswamy V, et al.: The clinical significance of equivocal findings on spinal MRI in children with medulloblastoma. Pediatr Blood Cancer 64 (8): , 2017. [PUBMED Abstract]
- Michalski JM, Janss AJ, Vezina LG, et al.: Children's Oncology Group Phase III Trial of Reduced-Dose and Reduced-Volume Radiotherapy With Chemotherapy for Newly Diagnosed Average-Risk Medulloblastoma. J Clin Oncol 39 (24): 2685-2697, 2021. [PUBMED Abstract]
- Warren KE, Vezina G, Poussaint TY, et al.: Response assessment in medulloblastoma and leptomeningeal seeding tumors: recommendations from the Response Assessment in Pediatric Neuro-Oncology committee. Neuro Oncol 20 (1): 13-23, 2018. [PUBMED Abstract]
- Fouladi M, Gajjar A, Boyett JM, et al.: Comparison of CSF cytology and spinal magnetic resonance imaging in the detection of leptomeningeal disease in pediatric medulloblastoma or primitive neuroectodermal tumor. J Clin Oncol 17 (10): 3234-7, 1999. [PUBMED Abstract]
- Zeltzer PM, Boyett JM, Finlay JL, et al.: Metastasis stage, adjuvant treatment, and residual tumor are prognostic factors for medulloblastoma in children: conclusions from the Children's Cancer Group 921 randomized phase III study. J Clin Oncol 17 (3): 832-45, 1999. [PUBMED Abstract]
- Yao MS, Mehta MP, Boyett JM, et al.: The effect of M-stage on patterns of failure in posterior fossa primitive neuroectodermal tumors treated on CCG-921: a phase III study in a high-risk patient population. Int J Radiat Oncol Biol Phys 38 (3): 469-76, 1997. [PUBMED Abstract]
- Thompson MC, Fuller C, Hogg TL, et al.: Genomics identifies medulloblastoma subgroups that are enriched for specific genetic alterations. J Clin Oncol 24 (12): 1924-31, 2006. [PUBMED Abstract]
- Northcott PA, Korshunov A, Witt H, et al.: Medulloblastoma comprises four distinct molecular variants. J Clin Oncol 29 (11): 1408-14, 2011. [PUBMED Abstract]
- Rutkowski S, von Hoff K, Emser A, et al.: Survival and prognostic factors of early childhood medulloblastoma: an international meta-analysis. J Clin Oncol 28 (33): 4961-8, 2010. [PUBMED Abstract]
- Kolodziejczak AS, Guerrini-Rousseau L, Planchon JM, et al.: Clinical outcome of pediatric medulloblastoma patients with Li-Fraumeni syndrome. Neuro Oncol 25 (12): 2273-2286, 2023. [PUBMED Abstract]
- Cohen BH, Zeltzer PM, Boyett JM, et al.: Prognostic factors and treatment results for supratentorial primitive neuroectodermal tumors in children using radiation and chemotherapy: a Childrens Cancer Group randomized trial. J Clin Oncol 13 (7): 1687-96, 1995. [PUBMED Abstract]
- Reddy AT, Janss AJ, Phillips PC, et al.: Outcome for children with supratentorial primitive neuroectodermal tumors treated with surgery, radiation, and chemotherapy. Cancer 88 (9): 2189-93, 2000. [PUBMED Abstract]
- Timmermann B, Kortmann RD, Kühl J, et al.: Role of radiotherapy in the treatment of supratentorial primitive neuroectodermal tumors in childhood: results of the prospective German brain tumor trials HIT 88/89 and 91. J Clin Oncol 20 (3): 842-9, 2002. [PUBMED Abstract]
- Jakacki RI, Zeltzer PM, Boyett JM, et al.: Survival and prognostic factors following radiation and/or chemotherapy for primitive neuroectodermal tumors of the pineal region in infants and children: a report of the Childrens Cancer Group. J Clin Oncol 13 (6): 1377-83, 1995. [PUBMED Abstract]
- Hwang EI, Kool M, Burger PC, et al.: Extensive Molecular and Clinical Heterogeneity in Patients With Histologically Diagnosed CNS-PNET Treated as a Single Entity: A Report From the Children's Oncology Group Randomized ACNS0332 Trial. J Clin Oncol : JCO2017764720, 2018. [PUBMED Abstract]
- Louis DN, Ohgaki H, Wiestler OD, et al.: The 2007 WHO classification of tumours of the central nervous system. Acta Neuropathol 114 (2): 97-109, 2007. [PUBMED Abstract]
- Sharma MC, Mahapatra AK, Gaikwad S, et al.: Pigmented medulloepithelioma: report of a case and review of the literature. Childs Nerv Syst 14 (1-2): 74-8, 1998 Jan-Feb. [PUBMED Abstract]
- Müller K, Zwiener I, Welker H, et al.: Curative treatment for central nervous system medulloepithelioma despite residual disease after resection. Report of two cases treated according to the GPHO Protocol HIT 2000 and review of the literature. Strahlenther Onkol 187 (11): 757-62, 2011. [PUBMED Abstract]
- Horwitz M, Dufour C, Leblond P, et al.: Embryonal tumors with multilayered rosettes in children: the SFCE experience. Childs Nerv Syst 32 (2): 299-305, 2016. [PUBMED Abstract]
- Khan S, Solano-Paez P, Suwal T, et al.: Clinical phenotypes and prognostic features of embryonal tumours with multi-layered rosettes: a Rare Brain Tumor Registry study. Lancet Child Adolesc Health 5 (11): 800-813, 2021. [PUBMED Abstract]
- Hansford JR, Huang J, Endersby R, et al.: Pediatric pineoblastoma: A pooled outcome study of North American and Australian therapeutic data. Neurooncol Adv 4 (1): vdac056, 2022. [PUBMED Abstract]
- Leary SE, Zhou T, Holmes E, et al.: Histology predicts a favorable outcome in young children with desmoplastic medulloblastoma: a report from the children's oncology group. Cancer 117 (14): 3262-7, 2011. [PUBMED Abstract]
- Giangaspero F, Perilongo G, Fondelli MP, et al.: Medulloblastoma with extensive nodularity: a variant with favorable prognosis. J Neurosurg 91 (6): 971-7, 1999. [PUBMED Abstract]
- von Bueren AO, von Hoff K, Pietsch T, et al.: Treatment of young children with localized medulloblastoma by chemotherapy alone: results of the prospective, multicenter trial HIT 2000 confirming the prognostic impact of histology. Neuro Oncol 13 (6): 669-79, 2011. [PUBMED Abstract]
- Rutkowski S, Gerber NU, von Hoff K, et al.: Treatment of early childhood medulloblastoma by postoperative chemotherapy and deferred radiotherapy. Neuro Oncol 11 (2): 201-10, 2009. [PUBMED Abstract]
- Rutkowski S, Bode U, Deinlein F, et al.: Treatment of early childhood medulloblastoma by postoperative chemotherapy alone. N Engl J Med 352 (10): 978-86, 2005. [PUBMED Abstract]
- Mynarek M, Pizer B, Dufour C, et al.: Evaluation of age-dependent treatment strategies for children and young adults with pineoblastoma: analysis of pooled European Society for Paediatric Oncology (SIOP-E) and US Head Start data. Neuro Oncol 19 (4): 576-585, 2017. [PUBMED Abstract]
- Albright AL, Wisoff JH, Zeltzer PM, et al.: Effects of medulloblastoma resections on outcome in children: a report from the Children's Cancer Group. Neurosurgery 38 (2): 265-71, 1996. [PUBMED Abstract]
- Taylor RE, Bailey CC, Robinson K, et al.: Results of a randomized study of preradiation chemotherapy versus radiotherapy alone for nonmetastatic medulloblastoma: The International Society of Paediatric Oncology/United Kingdom Children's Cancer Study Group PNET-3 Study. J Clin Oncol 21 (8): 1581-91, 2003. [PUBMED Abstract]
- Lannering B, Rutkowski S, Doz F, et al.: Hyperfractionated versus conventional radiotherapy followed by chemotherapy in standard-risk medulloblastoma: results from the randomized multicenter HIT-SIOP PNET 4 trial. J Clin Oncol 30 (26): 3187-93, 2012. [PUBMED Abstract]
- Thompson EM, Hielscher T, Bouffet E, et al.: Prognostic value of medulloblastoma extent of resection after accounting for molecular subgroup: a retrospective integrated clinical and molecular analysis. Lancet Oncol 17 (4): 484-95, 2016. [PUBMED Abstract]
- Keeling C, Davies S, Goddard J, et al.: The clinical significance of sub-total surgical resection in childhood medulloblastoma: a multi-cohort analysis of 1100 patients. EClinicalMedicine 69: 102469, 2024. [PUBMED Abstract]
- Jakacki RI, Burger PC, Kocak M, et al.: Outcome and prognostic factors for children with supratentorial primitive neuroectodermal tumors treated with carboplatin during radiotherapy: a report from the Children's Oncology Group. Pediatr Blood Cancer 62 (5): 776-83, 2015. [PUBMED Abstract]
- McManamy CS, Lamont JM, Taylor RE, et al.: Morphophenotypic variation predicts clinical behavior in childhood non-desmoplastic medulloblastomas. J Neuropathol Exp Neurol 62 (6): 627-32, 2003. [PUBMED Abstract]
- Massimino M, Antonelli M, Gandola L, et al.: Histological variants of medulloblastoma are the most powerful clinical prognostic indicators. Pediatr Blood Cancer 60 (2): 210-6, 2013. [PUBMED Abstract]
- Eberhart CG, Kratz J, Wang Y, et al.: Histopathological and molecular prognostic markers in medulloblastoma: c-myc, N-myc, TrkC, and anaplasia. J Neuropathol Exp Neurol 63 (5): 441-9, 2004. [PUBMED Abstract]
- Garrè ML, Cama A, Bagnasco F, et al.: Medulloblastoma variants: age-dependent occurrence and relation to Gorlin syndrome--a new clinical perspective. Clin Cancer Res 15 (7): 2463-71, 2009. [PUBMED Abstract]
- Liu APY, Smith KS, Kumar R, et al.: Serial assessment of measurable residual disease in medulloblastoma liquid biopsies. Cancer Cell 39 (11): 1519-1530.e4, 2021. [PUBMED Abstract]
- Tabori U, Baskin B, Shago M, et al.: Universal poor survival in children with medulloblastoma harboring somatic TP53 mutations. J Clin Oncol 28 (8): 1345-50, 2010. [PUBMED Abstract]
- Onvani S, Etame AB, Smith CA, et al.: Genetics of medulloblastoma: clues for novel therapies. Expert Rev Neurother 10 (5): 811-23, 2010. [PUBMED Abstract]
- Dubuc AM, Northcott PA, Mack S, et al.: The genetics of pediatric brain tumors. Curr Neurol Neurosci Rep 10 (3): 215-23, 2010. [PUBMED Abstract]
- Giangaspero F, Wellek S, Masuoka J, et al.: Stratification of medulloblastoma on the basis of histopathological grading. Acta Neuropathol 112 (1): 5-12, 2006. [PUBMED Abstract]
- Jones DT, Jäger N, Kool M, et al.: Dissecting the genomic complexity underlying medulloblastoma. Nature 488 (7409): 100-5, 2012. [PUBMED Abstract]
- Peyrl A, Chocholous M, Kieran MW, et al.: Antiangiogenic metronomic therapy for children with recurrent embryonal brain tumors. Pediatr Blood Cancer 59 (3): 511-7, 2012. [PUBMED Abstract]
- Kool M, Korshunov A, Remke M, et al.: Molecular subgroups of medulloblastoma: an international meta-analysis of transcriptome, genetic aberrations, and clinical data of WNT, SHH, Group 3, and Group 4 medulloblastomas. Acta Neuropathol 123 (4): 473-84, 2012. [PUBMED Abstract]
- Schwalbe EC, Williamson D, Lindsey JC, et al.: DNA methylation profiling of medulloblastoma allows robust subclassification and improved outcome prediction using formalin-fixed biopsies. Acta Neuropathol 125 (3): 359-71, 2013. [PUBMED Abstract]
- Shih DJ, Northcott PA, Remke M, et al.: Cytogenetic prognostication within medulloblastoma subgroups. J Clin Oncol 32 (9): 886-96, 2014. [PUBMED Abstract]
- Goschzik T, Schwalbe EC, Hicks D, et al.: Prognostic effect of whole chromosomal aberration signatures in standard-risk, non-WNT/non-SHH medulloblastoma: a retrospective, molecular analysis of the HIT-SIOP PNET 4 trial. Lancet Oncol 19 (12): 1602-1616, 2018. [PUBMED Abstract]
- Polkinghorn WR, Tarbell NJ: Medulloblastoma: tumorigenesis, current clinical paradigm, and efforts to improve risk stratification. Nat Clin Pract Oncol 4 (5): 295-304, 2007. [PUBMED Abstract]
- Ramaswamy V, Remke M, Bouffet E, et al.: Recurrence patterns across medulloblastoma subgroups: an integrated clinical and molecular analysis. Lancet Oncol 14 (12): 1200-7, 2013. [PUBMED Abstract]
- Packer RJ, Zhou T, Holmes E, et al.: Survival and secondary tumors in children with medulloblastoma receiving radiotherapy and adjuvant chemotherapy: results of Children's Oncology Group trial A9961. Neuro Oncol 15 (1): 97-103, 2013. [PUBMED Abstract]
- Shaw DW, Geyer JR, Berger MS, et al.: Asymptomatic recurrence detection with surveillance scanning in children with medulloblastoma. J Clin Oncol 15 (5): 1811-3, 1997. [PUBMED Abstract]
- Torres CF, Rebsamen S, Silber JH, et al.: Surveillance scanning of children with medulloblastoma. N Engl J Med 330 (13): 892-5, 1994. [PUBMED Abstract]
- Kramer ED, Vezina LG, Packer RJ, et al.: Staging and surveillance of children with central nervous system neoplasms: recommendations of the Neurology and Tumor Imaging Committees of the Children's Cancer Group. Pediatr Neurosurg 20 (4): 254-62; discussion 262-3, 1994. [PUBMED Abstract]
- Sabel M, Fleischhack G, Tippelt S, et al.: Relapse patterns and outcome after relapse in standard risk medulloblastoma: a report from the HIT-SIOP-PNET4 study. J Neurooncol 129 (3): 515-524, 2016. [PUBMED Abstract]
- Perreault S, Lober RM, Carret AS, et al.: Surveillance imaging in children with malignant CNS tumors: low yield of spine MRI. J Neurooncol 116 (3): 617-23, 2014. [PUBMED Abstract]
Meduloblastoma infantil
Síndromes hereditarios de predisposición al cáncer relacionados con el meduloblastoma
Cada vez más se han encontrado subgrupos de niños con tumores de encéfalo, incluso meduloblastoma, que tienen variantes germinales patogénicas o probablemente patogénicas, lo que los predispone al meduloblastoma y otros cánceres.[1,2] Estas variantes tienen connotaciones obvias para el niño afectado, los hermanos de ambos sexos, los progenitores, y tal vez para otros familiares, en cuanto a la vigilancia, la prevención, el diagnóstico y el tratamiento del cáncer. Es posible que las variantes también afecten aspectos específicos del tratamiento de los tumores.
El meduloblastoma surge en el entorno de síndromes hereditarios de predisposición al cáncer en cerca del 5 % de los pacientes.[1,2] En un estudio grande con más de 1000 pacientes se demostró que hay variantes patogénicas germinales en alrededor del 5 % de todos los pacientes con diagnóstico de meduloblastoma. Se han identificado variantes patogénicas germinales de los genes APC, BRCA2, PALB2, PTCH1, SUFU y TP53.[2]
Entre los síndromes que se sabe que están relacionados con el meduloblastoma están los siguientes:
- Síndrome de Turcot (vinculado con variantes patogénicas germinales de APC),[3] exclusivo del subtipo con activación de WNT.[2]
- Síndrome de Rubinstein-Taybi (vinculado con variantes patogénicas germinales de CREBBP).[4-6]
- Síndrome de Gorlin (también conocido como síndrome de nevo de células basales o síndrome de carcinoma de células basales nevoides, vinculado con variantes patogénicas germinales de PTCH1 y SUFU).[7-11] El riesgo de presentar meduloblastoma en pacientes con síndrome de Gorlin es más alto en los pacientes que tienen variantes germinales de SUFU que en los que tienen variantes patogénicas de PTCH1. En un estudio, 2 de 115 personas (1,7 %) con síndrome de Gorlin y una variante de PTCH1 presentaron meduloblastoma comprobado por análisis patológico, en comparación con 3 de 9 personas (33 %) de 3 familias con síndrome de Gorlin vinculado con alteraciones en SUFU. Todos los pacientes con alteraciones en SUFU presentaron meduloblastoma antes de los 3 años de edad.[11]
- El síndrome de Li-Fraumeni se vincula con variantes patogénicas germinales de TP53.[12,13] Las variantes patogénicas germinales de TP53 se restringen al subtipo con activación de la vía de erizo sónico (Sonic Hedgehog, SHH).[2,14]
- Anemia de Fanconi (vinculada con variantes de BRCA2).[15-18]
Se identificaron variantes patogénicas germinales deletéreas heterocigotas en GPR161 en cerca del 3 % de los casos de meduloblastoma SHH.[19] El gen GPR161 es un inhibidor de la señalización de SHH. La mediana de edad en el momento del diagnóstico para los pacientes con variantes de GPR161 fue de 1,5 años. La pérdida de heterocigosidad (LOH) en el locus de GPR161 se registró en todos los tumores, y los tumores de 5 de 6 pacientes exhibieron LOH sin cambio en el número de copias del cromosoma 1q (donde está GPR161). No se ha definido el riesgo de cánceres distintos del meduloblastoma en pacientes con variantes deletéreas de GPR161.
En el 14 % de los pacientes pediátricos con meduloblastoma SHH se identificaron nuevas variantes patogénicas germinales de pérdida de función en la subunidad mayor del complejo elongador en el gen ELP1, conservado evolutivamente. El gen de predisposición al meduloblastoma más común fue ELP1, que aumentó la prevalencia de predisposición genética hasta el 40 % en los pacientes pediátricos con meduloblastoma SHH.[20]
A veces, el meduloblastoma es la manifestación inicial de las variantes patogénicas germinales de estos genes de predisposición. Las pruebas de la línea germinal se deben considerar en las siguientes circunstancias:
- Se hace una prueba de variantes de APC en pacientes que tienen meduloblastoma con activación de WNT en ausencia de una variante somática de CTNNB1.
- Se hacen pruebas de variantes de los genes SUFU, PTCH1, TP53, PALB2 y BRCA2 en pacientes que tienen meduloblastoma con activación de SHH. Los pacientes que tienen tumores desmoplásicos con nodularidad extensa se deberán evaluar atentamente para identificar estigmas del síndrome de Gorlin.[7] En un informe se observó que el meduloblastoma con nodularidad extensa (MBEN) se relacionó con el síndrome de Gorlin en 5 de 12 casos.[7] El síndrome de Gorlin es un trastorno autosómico dominante en el que las personas afectadas tienen predisposición a presentar carcinomas de células basales, en especial en la piel del sitio de administración de la radiación. El síndrome se diagnostica en una etapa temprana de la vida por la detección de características dermatológicas y esqueléticas, como queratoquistes mandibulares, costillas bífidas o fusionadas, macrocefalia y calcificaciones en la hoz del cerebelo.[7]
- Pruebas de variantes de PALB2 y BRCA2 en pacientes con antecedentes familiares de cánceres relacionados con BRCA o deficiencia de reparación por recombinación homóloga.
Dada la alta frecuencia de variantes patogénicas germinales subyacentes o probablemente patogénicas relacionadas con el meduloblastoma SHH, todos los pacientes con esta enfermedad se deben derivar para recibir asesoramiento genético.
Cuadro clínico inicial
Los meduloblastomas, por definición, surgen en la fosa posterior.[21,22] Alrededor del 80 % de los casos en la niñez surgen en la región del cuarto ventrículo. La mayor parte de la sintomatología temprana se relaciona con obstrucción de la circulación del líquido cefalorraquídeo (LCR) que produce hidrocefalia por acumulación de líquido en el encéfalo. El diagnóstico de meduloblastoma en la niñez a menudo se establece en el transcurso de 2 o 3 meses después del inicio de los síntomas. El meduloblastoma presenta con frecuencia los siguientes signos y síntomas:[23]
- Inicio relativamente súbito de cefaleas, en especial, al levantarse por la mañana.
- Náuseas o vómitos.
- Letargo.
- Ataxia, incluso inestabilidad del tronco.
- Cierto grado de nistagmo.
- Papiledema.
El 20 % de los pacientes con meduloblastoma no tiene hidrocefalia en el momento del diagnóstico y es más probable que exhiban al inicio deficiencias cerebelosas. Por ejemplo, es posible que los meduloblastomas ubicados en porciones más laterales del cerebelo no causen hidrocefalia y, que debido a su ubicación, produzcan disfunción cerebelosa lateralizante (ataxia apendicular), que se manifiesta por dismetría unilateral, inestabilidad y debilidad de los pares craneales VI y VII en el mismo lado del tumor. Luego, cuando el tumor crece hacia la línea media y bloquea el LCR, se hacen evidentes los síntomas más clásicos relacionados con la hidrocefalia.
Las manifestaciones en los pares craneales son menos frecuentes, salvo por parálisis unilateral o bilateral del par craneal VI que, por lo general, se relaciona con la hidrocefalia.[23] A veces, los meduloblastomas se presentan de manera explosiva, con inicio agudo de letargo y pérdida de conciencia como resultado de una hemorragia dentro del tumor.
En los lactantes, el cuadro clínico inicial del meduloblastoma es más variable y a veces incluye los siguientes signos y síntomas:
- Letargo inespecífico.
- Retrasos psicomotores.
- Pérdida de los hitos del desarrollo.
- Dificultades de alimentación.
- Aumento de la circunferencia de la cabeza.
En el examen clínico, a veces se observa un abultamiento de la fontanela anterior por aumento de la presión intracraneal y movimientos oculares anormales, como desviación de la mirada hacia abajo (el llamado signo del sol poniente) debido a la pérdida de la mirada hacia arriba secundaria a la compresión del techo del mesencéfalo.
Clasificación celular y molecular
En la clasificación de la Organización Mundial de la Salud (OMS) de 2021, el meduloblastoma se clasifica según las características histológicas y moleculares. El tumor se clasifica como meduloblastoma definido por características histológicas si no se han realizado pruebas moleculares.[22,24]
- Meduloblastoma.
- Meduloblastoma definido por características moleculares.
- Meduloblastoma con activación de WNT.
- Meduloblastoma con activación de SHH y TP53 natural.
- Meduloblastoma con activación de SHH y alteración de TP53.
- Meduloblastoma sin activación de WNT o SHH.
- Meduloblastoma definido por características histológicas.
- Meduloblastoma nodular desmoplásico.
- Meduloblastoma con nodularidad extensa.
- Meduloblastoma de células grandes.
- Meduloblastoma anaplásico.
- Meduloblastoma definido por características moleculares.
Se ha prestado gran atención a los meduloblastomas que exhiben características anaplásicas, como aumento del tamaño nuclear, pleomorfismo citológico marcado, numerosas mitosis y cuerpos apoptóticos.[25,26] El uso de los criterios de anaplasia es subjetivo porque la mayoría de los meduloblastomas presentan algún grado de anaplasia. Es posible que los focos de anaplasia aparezcan en tumores con características histológicas tanto de meduloblastomas de células grandes como clásicos, y hay una superposición significativa entre las variantes anaplásicas y de células grandes, está variante a menudo se denomina meduloblastoma anaplásico de células grandes o anaplásico.[25,26] Se ha acordado declarar a los meduloblastomas como anaplásicos cuando la anaplasia es difusa (definida de manera variable como anaplasia que se presenta en entre el 50 % al 80 % del tumor).
La incidencia de meduloblastoma con la variante histológica desmoplásica o nodular, que por lo común surge en un hemisferio cerebeloso, es más alta durante la lactancia, menos común durante la niñez y vuelve a aumentar en la adolescencia y adultez. La variante histológica desmoplásica o nodular es diferente al MBEN. La variante nodular tiene una arquitectura lobulillar expandida. El subtipo MBEN se presenta casi exclusivamente en lactantes y, por lo general, acarrea excelente pronóstico.[7,27,28] Sin embargo, en un informe reciente se usó la secuenciación del transcriptoma para identificar un subconjunto de pacientes con MBNE que presentaban una frecuencia alta de alteraciones de la línea germinal en PTCH1 o SUFU. Estos pacientes tuvieron desenlaces menos favorables.[29]
Subtipos moleculares del meduloblastoma
Se han identificado múltiples subtipos de meduloblastoma mediante análisis molecular integrador.[30-53] Desde 2012, el consenso general es que el meduloblastoma se puede separar desde el punto de vista molecular en por lo menos 4 subtipos principales: meduloblastoma con activación de WNT, meduloblastoma con activación del erizo sónico (sonic hedgehog [SHH]), meduloblastoma del grupo 3 y meduloblastoma del grupo 4. En la clasificación de 2021 de la Organización Mundial de la Salud (OMS), el subgrupo SHH se dividió en 2 grupos en función del estado de TP53. El grupo 3 y el grupo 4, que requieren un análisis de metilación para una separación fiable, se combinaron en meduloblastoma sin activación de WNT ni SHH. Debido a que en los estudios realizados la terminología de los grupos 3 y 4 se utilizó de manera amplia y se sigue usando en los estudios en curso y planificados, esta nomenclatura se mantendrá a lo largo del análisis clínico en este resumen.[22,24]
Es probable que diferentes áreas del mismo tumor presenten variantes genéticas dispares, lo que aumenta la complejidad al elaborar un tratamiento eficaz dirigido al nivel molecular.[48] Sin embargo, los principales subtipos señalados antes se mantienen estables en los componentes primarios y metastásicos.[49,52]
Es posible establecer nuevas divisiones dentro de estos subgrupos, lo que proporcionará aún más información pronóstica útil.[50-52]
Meduloblastoma con activación de WNT
Los tumores WNT son meduloblastomas con alteraciones en la vía de señalización WNT que representan alrededor del 10 % de todos los meduloblastomas.[50] Los meduloblastomas WNT exhiben una firma de expresión génica de señalización de WNT y tinción nuclear de catenina β en el análisis inmunohistoquímico.[54] Por lo general, su clasificación histológica es como tumores de meduloblastoma clásico y, con escasa frecuencia, su aspecto es de células grandes o anaplásico. Los meduloblastomas WNT por lo general se presentan en pacientes de más edad (mediana de edad, 10 años) y es infrecuente que tengan metástasis en el momento del diagnóstico. En estudios recientes se demostró el valor del perfil de metilación para la identificación de los meduloblastomas con activación de WNT. Estos estudios incluyeron casos que no se hubiesen detectado mediante otros métodos vigentes (por ejemplo, prueba inmunohistoquímica de betacatenina β, análisis de variantes de CTNNB1 y evaluación de monosomía 6).[55]
Se observan variantes de CTNNB1 en el 85 % al 90 % de los casos de meduloblastoma WNT, y se detectan variantes de APC en muchos de los casos que no tienen variantes de CTNNB1. Los pacientes de meduloblastoma WNT con tumores que tienen variantes de APC a menudo presentan el síndrome de Turcot (es decir, variantes patogénicas de la línea germinal en APC).[51] Además de las variantes de CTNNB1, los tumores de meduloblastoma WNT exhiben pérdida de 6q (monosomía 6) en el 80 % al 90 % de los casos. Si bien la monosomía 6 se observa en la mayoría de los pacientes con meduloblastoma menores de 18 años en el momento del diagnóstico, es mucho menos común (alrededor del 25 % de los casos) en pacientes mayores de 18 años.[50,54]
El subconjunto WNT se observa de manera primaria en niños grandes, adolescentes y adultos, y no muestra un predominio por el sexo masculino. Se cree que el subconjunto tiene origen en el tronco encefálico, en la región del labio rómbico embrionario.[56] Los meduloblastomas WNT se relacionan con un desenlace muy bueno en niños, en especial, en personas cuyos tumores exhiben tinción nuclear de catenina β y pérdida comprobada de 6q o variantes de CTNNB1.[45,57-59] En estudios retrospectivos se indicó que es posible que otras variantes de TP53 y ganancias en el número de copias de OTX2 se vinculen con un pronóstico más precario en los pacientes con meduloblastoma WNT.[60] Estas últimas asociaciones deben verificarse en estudios prospectivos.[61]
Meduloblastoma con activación de SHH y alteración de TP53, y meduloblastoma con activación de SHH y TP53 natural
Los tumores SHH son meduloblastomas con alteraciones en la vía de señalización SHH y representan alrededor del 25 % de todos los casos de meduloblastomas.[50] Los meduloblastomas SHH se caracterizan por deleciones en el cromosoma 9q, características histológicas desmoplásicas o nodulares, y variantes de genes de la vía SHH, como PTCH1, PTCH2, SMO, SUFU y GLI2.[54]
Las variantes patogénicas germinales heterocigotas deletéreas en el gen GPR161 se identificaron en cerca del 3 % de los casos de meduloblastoma SHH.[19] El gen GPR161 es un inhibidor de la señalización de SHH. La mediana de edad en el momento del diagnóstico para los casos con alteraciones de GPR161 fue de 1,5 años. La pérdida de heterocigosis (LOH) en el locus de GPR161 se registró en todos los tumores, y los tumores de 5 entre 6 pacientes exhibieron LOH sin cambio en el número de copias del cromosoma 1q (donde está GPR161).
Las variantes del tercer nucleótido (r.3A>G) de los RNA nucleares pequeños (snRNA) U1 de los empalmosomas son muy específicas del meduloblastoma SHH.[62,63] Las variantes r.3A>G en los snRNA U1 se observan prácticamente en todos los casos de meduloblastoma SHH en adultos, en cerca de un tercio de los casos en niños y adolescentes, pero no se observan en casos de lactantes.[63] Las variantes de los snRNA U1 alteran el empalme del RNA, lo que produce inactivación de genes supresores de tumores (por ejemplo, PTCH1) y activación de oncogenes (por ejemplo, GLI2). A continuación, se describe la importancia de las variantes r.3A>G en los snRNA U1 de subtipos específicos de meduloblastoma SHH.
Los meduloblastomas SHH exhiben una distribución etaria bimodal y se observan más a menudo en niños menores de 3 años, al final de la adolescencia y en la edad adulta. Se cree que los tumores surgen en la capa granular externa del cerebelo. La heterogeneidad en la edad de presentación esquematiza diferentes subgrupos identificados mediante caracterización molecular adicional, como se describe a continuación:
- El subgrupo de meduloblastoma más común en niños de 3 a 16 años, que se llama SHH-α (subgrupo provisional en la clasificación de meduloblastoma de 2021), tiene alteración de TP53 y exhibe enriquecimiento de amplificaciones de MYCN y GLI2.[50,52] Las amplificaciones de PTCH1 y SUFU en ocasiones se presentan en este subtipo y son mutuamente excluyentes de las variantes de TP53 (a menudo de la línea germinal), mientras que la variante de SMO es infrecuente.[14,52,64] Las variantes de los snRNA U1 se presentan en cerca del 25 % de los casos de meduloblastoma SSH-α e indican un pronóstico muy precario.[63]
- Se han descrito dos subtipos de meduloblastomas SHH que se presentan de manera primaria en niños menores de 3 años.[50] Uno de estos subtipos, que se llama SHH-1 (SHH-β), a menudo es metastásico, y a menudo tiene amplificaciones focales.[65] El segundo de estos subtipos, que se llama SSH-2 (SHH-γ), exhibe enriquecimiento del tipo histológico del meduloblastoma con nodularidad extensa (MBNE). Las variantes de la vía SHH en niños menores de 3 años con meduloblastoma incluyen las variantes de PTCH1 y SUFU.[52] Las variantes de SUFU casi no se observan en niños más grandes ni en adultos; en ellos, son comunes las alteraciones de la línea germinal.[64]
En informes en los que se usaron matrices de metilación del DNA también se identificaron 2 subtipos de meduloblastoma SHH en niños jóvenes.[28,65] Uno de estos subtipos abarcó todos los casos con variantes de SMO y se relacionó con un pronóstico favorable. El otro subtipo exhibió la mayoría de las variantes de SUFU y se relacionó con una tasa de supervivencia sin progresión (SSP) mucho más baja. Ambos subtipos exhibieron variantes de PTCH1.
- Un cuarto subtipo de SHH, que se llama SHH-δ, incluye la mayoría de los casos de meduloblastomas SHH en adultos.[50] Prácticamente todos los casos de meduloblastoma SHH-δ tienen la variante r.A>3 en los snRNA U1 [63] y cerca del 90 % de los casos exhiben una variante del promotor de TERT.[50] También se observan variantes de PTCH1 y SMO en adultos con meduloblastoma SHH.
El desenlace de los pacientes con meduloblastoma SHH no metastásico es relativamente favorable para niños menores de 3 años y adultos.[50] Los niños pequeños con un tipo histológico MBNE tienen un pronóstico particularmente favorable.[7,27,66-68] Los pacientes con meduloblastoma SHH tienen un riesgo más alto de fracaso terapéutico que los niños mayores de 3 años cuyos tumores tienen variantes de TP53, que a menudo presentan de manera simultánea amplificaciones en GLI2 o MYCN y un tipo histológico de células grandes o anaplásico.[50,64,69]
Los pacientes con hallazgos moleculares desfavorables tienen un pronóstico desfavorable, menos del 50 % de los pacientes sobreviven después del tratamiento convencional.[46,64,69-72]
En la clasificación de 2021 de la OMS, el meduloblastoma SHH con variante de TP53 se considera una entidad diferenciada (meduloblastoma con activación de SHH y alteración de TP53).[22,24] Alrededor de un 25 % de los casos de meduloblastoma con activación de SHH exhiben variantes de TP53 y un gran porcentaje de estos casos también exhiben una variante patogénica germinal en TP53 (9 de 20 en un estudio). Por lo general, estos pacientes tienen entre 5 y 18 años y su pronóstico es más precario (tasa de supervivencia general a 5 años, <30 %).[71] Los tumores a menudo exhiben un tipo histológico de células grandes anaplásicas.[71] En un estudio retrospectivo más grande se confirmó el pronóstico precario de estos pacientes.[14]
Meduloblastoma sin activación de WNT ni SHH
En la clasificación de la OMS se combinan los casos de meduloblastomas de los grupos 3 y 4 en una sola entidad, en parte por la ausencia de efecto clínico inmediato de esta diferenciación. El grupo 3 representa cerca de un 25 % de los casos de meduloblastoma, mientras que el grupo 4 representa cerca de un 40 % de los casos de meduloblastoma.[50,54] La mayoría de los pacientes de los meduloblastomas de los grupos 3 y 4 son varones.[39,52] Los meduloblastomas de los grupos 3 y 4 se pueden subdividir a partir de características como los perfiles de expresión génica y de metilación del DNA, pero no se ha establecido el abordaje óptimo para esta subdivisión.[50,51]
Se observan varias alteraciones genómicas en los meduloblastomas del grupo 3 y 4. No obstante, ninguna alteración única se presenta en más de un 10 % a un 20 % de los casos. Las alteraciones genómicas son las siguientes:
- La amplificación de MYC fue la alteración diferenciada más común notificada para los meduloblastomas del grupo 3, que se presenta en alrededor del 15 % de los casos.[44,51]
- La alteración genómica diferenciada más común descrita para el meduloblastoma del grupo 4 (alrededor de un 15 % de los casos) fue la activación de PRDM6 por secuestro del activador de transcripción como consecuencia de duplicación en tándem del gen adyacente SNCAIP.[51]
- Otras alteraciones genómicas que se observaron en casos de los grupos 3 y 4 fueron amplificación de MYCN y variantes estructurales que llevan a la sobreexpresión de GFI1 o GFI1B mediante secuestro del activador de transcripción.
- El isocromosoma 17q (i17q) es la anormalidad citogenética más común y se observa en un porcentaje alto de los casos del grupo 4, así como en los casos del grupo 3, pero pocas veces se observa en los meduloblastomas WNT y SHH.[44,51] La presencia de i17q no parece afectar el pronóstico de los pacientes de los grupos 3 y 4.[73]
Los pacientes del grupo 3 con amplificación de MYC o sobreexpresión de MYC tienen un pronóstico precario.[52] Menos de un 50 % de estos pacientes sobreviven 5 años después del diagnóstico.[50] Este pronóstico adverso es particularmente cierto en niños menores de 4 años en el momento del diagnóstico.[46] No obstante, los pacientes con meduloblastomas del grupo 3 sin amplificación de MYC mayores de 3 años tienen un pronóstico similar al de la mayoría de pacientes con meduloblastoma sin activación de WWT, con una tasa de supervivencia sin progresión a 5 años superior al 70 %.[70,73]
Los meduloblastomas del grupo 4 se presentan durante toda la infancia y la niñez, así como en la edad adulta. El pronóstico de los pacientes con meduloblastoma del grupo 4 es similar al de los pacientes con meduloblastoma sin activación de WNT. Es posible que el pronóstico se vea afectado por otros factores como la presencia de enfermedad metastásica, pérdida del cromosoma 11q y pérdida del cromosoma 17p.[43,44,50,69] En un estudio, se observó que los pacientes del grupo 4 con pérdida del cromosoma 11 o ganancia del cromosoma 17 exhibieron un riesgo bajo, con independencia de las metástasis. En casos que no tienen ninguna de estas características citogenéticas, las metástasis en el cuadro clínico inicial permiten diferenciar entre el riesgo intermedio y el riesgo alto.[69]
Para los pacientes de riesgo estándar del grupo 3 y 4 (es decir, sin amplificación de MYC ni enfermedad metastásica), la ganancia o pérdida de cromosomas enteros acarrea un pronóstico favorable. Estos hallazgos se obtuvieron de datos de 91 pacientes con meduloblastoma sin activación de WNT ni SHH que participaron en el ensayo clínico SIOP-PNET-4 (NCT01351870) y se confirmaron en un grupo independiente de 70 niños con meduloblastoma sin activación de WNT ni SHH tratados entre 1990 y 2014.[73] Las anormalidades cromosómicas son las siguientes:
- La ganancia o pérdida de uno o más cromosomas enteros se relacionó con una tasa de supervivencia sin complicaciones (SSC) a 5 años del 93 % en comparación con el 64 % para la ausencia de ganancia o pérdida de cromosomas enteros.
- Las ganancias o pérdidas de cromosomas enteros más comunes son la ganancia del cromosoma 7 y la pérdida de los cromosomas 8 y 11.
- El discriminador pronóstico con desempeño óptimo es la presentación simultánea de dos o más de las siguientes alteraciones: ganancia del cromosoma 7, pérdida del cromosoma 8 y pérdida del cromosoma 11. Alrededor del 40 % de los pacientes de riesgo estándar de los grupos 3 y 4 tuvieron 2 o más de estas alteraciones cromosómicas; la tasa de SSC a 5 años fue del 100 % en comparación con el 68 % para los pacientes con menos de 2 de estas alteraciones.
- En una cohorte independiente, se confirmó la importancia pronóstica de 2 o más ganancias o pérdidas versus 0 o 1 ganancias o pérdidas de los cromosomas 7, 8 y 11 (tasa de SSC a 5 años, el 95 % de los pacientes con 2 o más vs. el 59 % de los pacientes con 1 o menos).
Es probable que la clasificación del meduloblastoma en cuatro subtipos principales se modifique en el futuro.[50,51,72,74,75] Es posible que se establezcan nuevas subdivisiones en subgrupos a partir de las características moleculares porque se hacen más análisis moleculares por subgrupo; los estudios se acercan a un consenso a medida que surge información de múltiples estudios independientes. Por ejemplo, mediante abordajes bioinformáticos complementarios, se analizó la concordancia de varias cohortes grandes publicadas y se describió una subdivisión más unificada. En los niños con meduloblastomas de grupo 3 y 4, se determinaron 8 subgrupos diferentes mediante agrupamiento de perfiles de metilación del DNA. Los subgrupos específicos tienen pronósticos diferentes.[43,54,64,76]
No se sabe si la clasificación para los adultos con meduloblastoma tiene la misma capacidad pronóstica que para los niños.[44,46] En un estudio de meduloblastoma en pacientes adultos, se observaron con poca frecuencia amplificaciones del oncogén MYC; los tumores con deleción de 6q y activación de WNT (identificados mediante tinción nuclear de catenina β) no compartieron el excelente pronóstico que se observó en los meduloblastomas infantiles. Sin embargo, en otro estudio se confirmó un excelente pronóstico para los tumores con activación de WNT en adultos.[44,46]
Evaluación para la estadificación
Tradicionalmente, la estadificación se basó en una evaluación intraoperatoria del tamaño y la extensión del tumor, junto con neuroimágenes posoperatorias del encéfalo y la médula espinal, así como evaluación citológica del líquido cefalorraquídeo (LCR) (sistema Chang). La evaluación intraoperatoria de la extensión del tumor se reemplazó; ahora se usan imágenes del eje encefalomedular antes del diagnóstico e imágenes posoperatorias para determinar la cantidad de enfermedad residual en el sitio primario. Se utilizan las siguientes pruebas y procedimientos para la estadificación:
La extensión del tumor se define como sigue:
- M0: Sin diseminación.
- M1: Solo prueba citológica positiva en el LCR.
- M2: Diseminación nodular macroscópica en el espacio subaracnoideo cerebeloso o cerebral, en un ventrículo lateral o en el tercer ventrículo.
- M3: Diseminación nodular macroscópica en el espacio subaracnoideo de la médula espinal.
- M4: Metástasis extraneural.
El grado de enfermedad residual posoperatorio se designa como sigue:
- Resección macroscópica total o resección casi total: Ausencia de enfermedad residual o cantidad mínima (≤1,5 cm 2) de enfermedad residual después de la resección.
- Resección subtotal: Enfermedad residual después del diagnóstico (>1,5 cm2 de enfermedad residual cuantificable).
- Biopsia: Ausencia de resección tumoral; solo se extrae una muestra de tejido tumoral.
Desde la década de 1990, se han realizado estudios prospectivos con este sistema de estadificación para separar a los pacientes en subgrupos de meduloblastoma de riesgo promedio y riesgo alto.[78-80]
La presencia de anaplasia histológica difusa (>50 % de la muestra patológica) se ha añadido a los sistemas de estadificación. Si se encuentra anaplasia difusa, se aumenta el estadio para los pacientes que tienen enfermedad de riesgo promedio con el fin de reflejar una enfermedad de riesgo alto.
Estratificación del riesgo
La estratificación del riesgo se basa en la evaluación neurorradiográfica de la enfermedad diseminada, el examen citológico del LCR, la evaluación posoperatoria mediante neuroimágenes para determinar la cantidad de enfermedad residual y la edad del paciente. Para obtener más información, consultar la sección Evaluación para la estadificación. Los pacientes mayores de 3 años con meduloblastoma se estratificaron en los siguientes dos grupos de riesgo:
- Riesgo promedio: Niños mayores de 3 años con resección completa o casi completa del tumor (≤1,5 cm2 de enfermedad residual) sin enfermedad metastásica.[78]
- Riesgo alto: Niños mayores de 3 años con enfermedad metastásica o sometidos a resección subtotal (>1,5 cm2 de enfermedad residual).[78] La enfermedad metastásica incluye evidencia neurorradiográfica de enfermedad diseminada, positividad en el examen citológico del LCR lumbar o ventricular obtenido más de 14 días después de la cirugía o enfermedad extraneural.[78] Los niños con tumores que muestran anaplasia difusa y que de otro modo se considerarían de riesgo promedio se asignan al grupo de riesgo alto.[26,38]
En los niños más pequeños (menores de 3 años en algunos estudios y menores de 4 o 5 años en otros), se ha utilizado una separación similar en grupos de riesgo promedio (sin diseminación y ≤1,5 cm2 de enfermedad residual) o de riesgo alto (enfermedad diseminada o >1,5 cm2 de enfermedad residual). Los hallazgos histológicos de desmoplasia también se han utilizado para connotar una subagrupación de riesgo más favorable, en especial para el subgrupo con MBEN.[81,82]
Es posible que la asignación a un grupo de riesgo en función de la extensión de la resección de la enfermedad en el momento del diagnóstico no pronostique el resultado del tratamiento. Los factores genéticos, histológico y moleculares tal vez sean más informativos, aunque se deben evaluar en el contexto de la edad del paciente, la extensión de la enfermedad en el momento del diagnóstico y el tratamiento recibido.[43,72,83] Las caracterizaciones de riesgo de las subdivisiones moleculares está cambiando y se están integrando en el esquema de estratificación del riesgo para asignación del tratamiento en los estudios prospectivos de América del Norte (por ejemplo, NCT01878617 y NCT02724579).[74]
Aspectos generales de las opciones de tratamiento del meduloblastoma infantil
En el Cuadro 3 se describen las opciones de tratamiento del meduloblastoma infantil recién diagnosticado y recidivante.
| Grupo de tratamiento | Opciones de tratamiento estándar | |
|---|---|---|
| Meduloblastoma infantil recién diagnosticado | Niños más pequeños con meduloblastoma | Cirugía |
| Quimioterapia adyuvante | ||
| Niños mayores de 3 años con meduloblastoma de riesgo promedio | Cirugía | |
| Radioterapia adyuvante | ||
| Quimioterapia adyuvante | ||
| Niños mayores de 3 años con meduloblastoma de riesgo alto | Cirugía | |
| Radioterapia adyuvante | ||
| Quimioterapia adyuvante | ||
| Meduloblastoma infantil recidivante | No hay opciones de tratamiento estándar. Para obtener más información, consultar la sección Tratamiento del meduloblastoma y otros tumores embrionarios del sistema nervioso central infantil recidivantes. | |
Cirugía
La cirugía se considera una parte del tratamiento estándar para la confirmación histológica del tipo de tumor y como mecanismo para mejorar el desenlace. Las resecciones totales o casi totales se consideran óptimas si se pueden realizar de manera inocua.[84,85]
En el período posoperatorio, es posible que los niños tengan deficiencias neurológicas significativas causadas por lesión encefálica preoperatoria relacionada con el tumor, hidrocefalia o lesión encefálica causada por la cirugía.[86][Nivel de evidencia C1] Un número significativo de pacientes con meduloblastoma presentan síndrome de mutismo cerebeloso (también conocido como síndrome de la fosa posterior). Los síntomas del síndrome de mutismo cerebeloso, que por lo general aparecen 1 o 2 días después de la cirugía, son los siguientes:
- Pérdida del habla.
- Parálisis suprabulbares.
- Ataxia.
- Hipotonía.
- Labilidad emocional.
La causa del síndrome de mutismo cerebeloso sigue sin estar clara, aunque se ha postulado que el daño al vermis cerebeloso o la alteración de las vías cortico-cerebelosas son la posible causa del mutismo.[87,88]; [89][Nivel de evidencia C1] En dos estudios del Children’s Cancer Group en los que se evaluó a niños con meduloblastoma de riesgo promedio y de riesgo alto, se identificó el síndrome en casi el 25 % de los pacientes.[88-90]; [91][Nivel de evidencia C1] En Un análisis retrospectivo de 370 pacientes con meduloblastoma, se identificó una edad más temprana, un tamaño tumoral más grande y la localización del tumor en la línea media como factores de riesgo de presentar mutismo. Estos hallazgos fueron congruentes con observaciones anteriores. Los investigadores también observaron una correlación entre el subtipo de meduloblastoma y el riesgo de mutismo. El mutismo fue más común en los pacientes con meduloblastomas de los grupos 3 y 4 (30–35 % de los pacientes) y menos frecuente en los niños que tenían tumores con activación de SHH (7 % de los pacientes).[92] En un estudio prospectivo de exploración neurológica longitudinal en 178 pacientes con meduloblastoma, se identificaron similares factores de riesgo de mutismo (riesgo más alto con una edad más temprana; riesgo más bajo con el subtipo de SHH), probablemente porque los tumores con activación de SHH tienden a presentarse en los hemisferios y no en la línea media. En el estudio también se notificó un mayor riesgo de desarrollar mutismo en pacientes sometidos a resecciones tumorales en centros quirúrgicos con bajo volumen de pacientes.[93] Cerca del 50 % de los pacientes con este síndrome manifiestan secuelas neurológicas y neurocognitivas permanentes a largo plazo.[89,91]
Radioterapia
La dosis de radioterapia dirigida al sitio del tumor primario, por lo general, oscila entre 54 Gy y 55,8 Gy.[94] En la mayoría de los casos, esta terapia se administra con un margen de 1 cm a 2 cm alrededor del sitio del tumor primario, preferiblemente mediante técnicas conformadas.[94] La reducción de los volúmenes de refuerzo para toda la fosa posterior y para el lecho tumoral y los márgenes no afectó el desenlace de los pacientes de riesgo promedio del estudio ACNS0331 (NCT00085735) del Children's Oncology Group (COG).[59][Nivel de evidencia A1] Para todos los meduloblastomas en niños mayores de 3 o 4 años en el momento del diagnóstico, se administra radioterapia craneoespinal en dosis que oscilan entre 23,4 Gy y 36 Gy, según los factores de riesgo, como la extensión de la enfermedad en el momento del diagnóstico. En un estudio prospectivo de fase II sobre la toxicidad de la radioterapia de protones[95] y en un informe retrospectivo de eficacia de la radioterapia de protones versus la radioterapia de fotones para el meduloblastoma [96] se demostraron desenlaces equivalentes en cuanto a la SSP, la supervivencia general (SG), los patrones de recaída y los efectos tóxicos diferidos. En un estudio retrospectivo de 84 niños que recibieron radioterapia de protones (n = 38) o de fotones (n = 46) se observaron tasas similares de ototoxicidad de grado 3 y 4, a pesar de las dosis cocleares medias bajas en los niños que recibieron radioterapia de protones, lo que indica que otros factores (por ejemplo, el cisplatino, la ubicación inicial del tumor en relación con el nervio vestibulococlear [VII par craneal]) contribuyen a la ototoxicidad.[97] Se están investigando los desenlaces comparativos de estos métodos de tratamiento.
La quimioterapia, por lo general, se administra durante la radioterapia y después de esta.
En los niños menores de 3 años, se intenta evitar o posponer la radioterapia por el gran efecto que tiene en esta edad. Los niños de todas las edades son susceptibles a los efectos adversos de la radiación en el desarrollo encefálico. Con frecuencia se observan efectos debilitantes en el desarrollo neurocognitivo, el crecimiento y el funcionamiento endocrino, en especial, en los niños más pequeños.[98-102]
Quimioterapia
La quimioterapia, que suele administrase durante la radioterapia y después de esta, es un componente estándar del tratamiento para los niños mayores con meduloblastoma y otros tumores embrionarios. La quimioterapia se puede usar para retrasar y, a veces, evitar la necesidad de radioterapia en el 20 % al 40 % de los niños menores de 3 a 4 años con meduloblastoma no diseminado.[103,104]; [102][Nivel de evidencia C1]
Tratamiento del meduloblastoma infantil
Tratamiento de los niños más pequeños con meduloblastoma
Las tasas de supervivencia sin complicaciones (SSC) a 5 años para niños pequeños con meduloblastoma, descritos de manera arbitraria en el pasado como niños de 3 años o menos en el momento del diagnóstico, han oscilado entre el 30 % y el 70 %. No hay consenso sobre qué edad constituye la población de niños más pequeños con meduloblastoma cuyo tratamiento óptimo es quimioterapia postoperatoria inmediata y radioterapia diferida o sin radioterapia. La mayoría de los estudios coinciden en que, en los pacientes de 3 años o menos, se debe considerar seriamente la quimioterapia inicial. Algunos investigadores han recomendado retrasar la radioterapia o evitarla por completo en pacientes de 3 a 4 años, y tal vez de hasta 5 años. Estas decisiones se basan en múltiples factores, como el subtipo histológico, el subtipo molecular, la extensión de la enfermedad en el momento del diagnóstico, el estado neurológico y del neurodesarrollo preexistente y las preferencias de la familia. La mayoría de los sobrevivientes a largo plazo tratados de manera exitosa con quimioterapia sola tenían tumores no diseminados completamente resecados.[81,103,105]; [106][Nivel de evidencia B4] En varios estudios en los que se usó quimioterapia sola para los pacientes más jóvenes se observó que el hallazgo de desmoplasia (en pacientes con meduloblastoma desmoplásico o MBEN) o indicios moleculares de señalización SHH indica un pronóstico significativamente mejor que el hallazgo de meduloblastoma clásico o meduloblastoma anaplásico o células grandes.[7,27,66-68]; [82][Nivel de evidencia B4]
El tratamiento de los niños más pequeños con meduloblastoma recién diagnosticado continúa evolucionando. Los resultados son contradictorios y la comparación entre estudios es difícil por las diferencias en los regímenes farmacológicos, el uso de radioterapia craneoespinal y de refuerzo local de radioterapia al final de la quimioterapia, o cuando los niños alcanzan la edad de 3 años.
Las opciones de tratamiento estándar para los niños más pequeños con meduloblastoma recién diagnosticado son las siguientes:
Cirugía
Si es viable, la resección quirúrgica completa del tumor es el tratamiento óptimo. La resecabilidad quirúrgica se relaciona con el tipo histológico, ya que los pacientes con meduloblastoma desmoplásico o nodular o MBEN tienen una tasa más alta de resección completa que los pacientes con meduloblastoma clásico.[67,68]
Quimioterapia adyuvante
El tratamiento para los niños más pequeños con meduloblastoma ha incluido opciones como abordajes quimioterapéuticos multifarmacológicos, con fármacos como ciclofosfamida, etopósido, cisplatino y vincristina, acompañados de dosis altas de metotrexato intravenoso o intraventricular o sin estas.[68,81,103,105,107,108]; [109,110][Nivel de evidencia B4] La eficacia de la quimioterapia varió según el tipo histológico o el subtipo molecular del tumor.
Meduloblastoma desmoplásico, meduloblastoma con nodularidad extensa o tumores con señalización de SHH
En una serie de estudios se ha demostró que la quimioterapia intensiva, que incluye dosis altas de metotrexato sistémico y metotrexato intraventricular o dosis altas de quimioterapia con rescate de células madre, sin radioterapia, es un tratamiento eficaz para la mayoría de los lactantes y niños muy pequeños con meduloblastoma.
Evidencia (quimioterapia):
- En el ensayo multicéntrico alemán Hirntumor (HIT) 2000, se usó un régimen de quimioterapia multifarmacológica que incluía dosis altas de metotrexato intravenoso e intraventricular. Este régimen farmacológico no incluyó dosis altas de quimioterapia con apoyo de rescate con médula ósea o células madre periféricas.[81]
- En el estudio, 19 pacientes con meduloblastoma desmoplásico o con nodularidad extensa (MBNE) tuvieron una tasa de SSC a 5 años del 90 % (± 7 %) y una tasa de SG del 100 % (± 0 %).
- Todos los pacientes recibieron quimioterapia posoperatoria sola, y no recibieron radiación antes de la progresión.
- En una cohorte ampliada del ensayo alemán HIT 2000 participaron otros 23 niños con desmoplasia nodular o MBNE tratados con el mismo régimen. Se observaron los siguientes resultados:[111]
- Los resultados combinados confirmaron una supervivencia excelente, con una tasa de SSC a 5 años superior al 90 %.
- En esta cohorte ampliada, se realizó una caracterización molecular y se identificó un subconjunto de tumores con señalización de SHH. Estos pacientes con tumores que exhibían señalización de SHH tenían un pronóstico excelente similar.
- La caracterización adicional del subtipo molecular con señalización de SHH mediante anomalías cromosómicas no identificó ninguna diferencia en la SSC ni en la SG.
- En otros estudios se ha indicado que la subdivisión adicional por anomalías cromosómicas en niños pequeños con meduloblastoma con activación de SHH era predictiva del desenlace.
- En un ensayo clínico del COG (CCG-9921) también se observó un resultado favorable para los niños con meduloblastoma desmoplásico (incluso MBNE). En este estudio, los pacientes con tumores desmoplásicos no recibieron radioterapia antes de la progresión.[103]
- Los pacientes del grupo de tumores desmoplásicos lograron una tasa de SSC del 77 % (±9 %) y una tasa de SG del 85 % (±8 %), en comparación con una tasa de SSC del 17 % (±5 %) y una tasa de SG del 29 % (±6 %) para los pacientes del grupo de tumores no desmoplásicos (P < 0,0001 para las comparaciones de SSC y SG).
- En el estudio COG-ACNS1221 (NCT02017964) se probó un régimen de quimioterapia sistémica idéntico al utilizado en el ensayo alemán HIT 2000, excepto por la omisión del metotrexato intraventricular.[28]
- El estudio se suspendió antes de lo previsto debido a una tasa de recaídas superior a la esperada, con una tasa de SSP a 2 años del 52 % en los 25 pacientes estudiados.
- Otra opción de tratamiento para los niños menores de 3 años en el momento del diagnóstico es la quimioterapia de dosis alta. En los resultados de ensayos en los que se usaron regímenes quimioterapéuticos de dosis más altas con apoyo de rescate de células madre, también se demostró que un subgrupo de pacientes con meduloblastoma menores de 3 años y, en algunos estudios, menores de 5 años en el momento del diagnóstico, se puede tratar con éxito usando quimioterapia sola.[104,106,112][Nivel de evidencia B4]; [113]
- Las mejores tasas de supervivencia con este abordaje de quimioterapia de dosis más altas se observaron en pacientes con meduloblastoma desmoplásico y MBEN.[113]
- Tras el tratamiento con quimioterapia sin radioterapia simultánea, los pacientes con enfermedad no diseminada lograron tasas de supervivencia de casi el 90 %, y los pacientes con enfermedad diseminada lograron tasas de supervivencia del 80 %.
- Las mejores tasas de supervivencia con este abordaje de quimioterapia de dosis más altas se observaron en pacientes con meduloblastoma desmoplásico y MBEN.[113]
- En un estudio se notificaron los desenlaces de lactantes y niños pequeños con meduloblastoma en recaída que recibieron tratamiento inicial sin irradiación craneoespinal (ICE).[114]
- Una parte importante de estos niños recibió tratamiento de rescate con regímenes a base de ICE se consideró exitoso.
- La tasa de supervivencia después de la recaída a 3 años fue del 52,4 % en los pacientes tratados con intención curativa.
- En el informe se indicó que la edad más avanzada en el momento del diagnóstico, la recaída local y el meduloblastoma infantil de subtipo SHH se relacionaron con mejor supervivencia después de la recaída.
- La adición de quimioterapia a la ICE no mejoró los desenlaces.
Meduloblastoma no desmoplásico, meduloblastoma sin nodularidad extensa y sin señalización de SHH
En comparación con los niños que tienen meduloblastoma desmoplásico o MBNE tratados con los regímenes de quimioterapia intensiva vigentes en la actualidad, los niños con otros subtipos histológicos o moleculares no evolucionan tan bien. En un estudio se indicó que los pacientes con tumores clasificados en el grupo 4 según sus características moleculares presentaron buenos resultados con quimioterapia sola.[111]
Evidencia (quimioterapia):
- En los niños con tumores no desmoplásicos, sin nodularidad extensa o sin señalización de SHH, las tasas de SSC son inferiores al 40 %, a pesar del uso de quimioterapia intensiva suplementada con metotrexato (intravenoso e intraventricular) o el uso de regímenes de quimioterapia de dosis altas con apoyo de rescate con células madre.[68,103,111,113,115]
- El desenlace es particularmente precario cuando estos pacientes tienen enfermedad diseminada.
- En algunos estudios, se agregó radioterapia dirigida al sitio del tumor primario o al eje craneoespinal después de la quimioterapia, lo que dificulta la evaluación de la eficacia de la quimioterapia.[111,113,115]
No hay acuerdo sobre cuánta radioterapia (dosis y alcance) se debe administrar, y a qué edad se debe comenzar la radioterapia para los pacientes jóvenes con enfermedad localizada o diseminada.
- En el estudio HIT 2000 ampliado, la adición de radioterapia focal al sitio del tumor primario en pacientes con enfermedad localizada después de la quimioterapia no mejoró la SSC ni la SG.[111]
- En el estudio del St. Jude Children's Research Hospital (SJCRH) SJYC07 (NCT00602667), la radioterapia focal tampoco mejoró la SSC en lactantes con meduloblastoma clasificado como de riesgo intermedio (tasa de SSC a 5 años, 25 % ± 12 %).[65]
- En el estudio del COG P9934 (NCT00006461), en el que también se empleó radioterapia focal, se observó una SSC similar (tasa de SSC a 4 años, 23 % ± 12 %) en los pacientes con meduloblastoma no desmoplásico.[116]
- En el estudio SJCRH SJYC07, 29 de los 54 lactantes con meduloblastoma cuya enfermedad progresó recibieron ICE (mediana de dosis, 36 Gy). De los 29 pacientes, 18 (62 %) sobrevivieron, en comparación con 6 de 25 pacientes (24 %) que no recibieron ICE.[65]
Tratamiento de los niños mayores de 3 años con meduloblastoma de riesgo promedio
Las opciones de tratamiento estándar para los niños mayores de 3 años con meduloblastoma recién diagnosticado de riesgo promedio son las siguientes:
Cirugía
Si es posible, la extirpación total o casi total del tumor se considera óptima.[84]
Radioterapia adyuvante
La radioterapia, por lo general, se inicia después de la cirugía con quimioterapia simultánea o sin esta.[117-119] Los mejores resultados de supervivencia para los niños con meduloblastoma se obtuvieron cuando la radioterapia se inició dentro de las 4 a 6 semanas posteriores a la cirugía.[118-120]; [94,121][Nivel de evidencia A1] En un estudio piloto en niños con meduloblastoma con activación de WNT se intentó omitir la radioterapia craneoespinal (y tratar a los pacientes con quimioterapia posquirúrgica sola). El estudio se suspendió después de que los primeros dos pacientes presentaran recidivas tumorales tempranas.[122]
La dosis de radiación para los pacientes con meduloblastoma de riesgo promedio es de 54 Gy dirigidos a la fosa posterior o al lecho tumoral local y de 23,4 Gy dirigidos a todo el eje encefalomedular (es decir, todo el encéfalo y la médula espinal), denominado ICE.[117-119,123]
Evidencia (radioterapia adyuvante):
- La radioterapia sola, con una dosis de radiación craneoespinal de 35 Gy y un refuerzo a la fosa posterior de 55 Gy, produce unas tasas de SSC a 5 años que oscilan entre el 50 % y el 65 % en pacientes con enfermedad no diseminada.[80,118]
- No se conoce la dosis mínima de radiación craneoespinal necesaria para el control de la enfermedad. Los intentos de disminuir la dosis de radioterapia craneoespinal hasta 23,4 Gy sin quimioterapia han dado lugar a un aumento de la incidencia de recaídas leptomeníngeas aisladas.[123] En una serie se intentó tratar a niños con tumores con activación de WNT con radioterapia focal sola, sin ICE. En el estudio se observó una incidencia inaceptable de fracaso del tratamiento en el eje craneoespinal con la omisión de la ICE inicial.[124]
Se evaluaron dosis y volúmenes de refuerzo de radiación craneoespinal más bajas en un estudio del COG (NCT00085735). Los niños de 3 a 7 años se asignaron al azar para recibir una dosis de radiación craneoespinal de 18 Gy o 23,4 Gy, así como radiación dirigida a toda fosa posterior versus un refuerzo de volumen objetivo limitado al lecho tumoral.[59][Nivel de evidencia A1]
- En los resultados se reveló que la dosis de 18 Gy de ICE fue menos eficaz que la dosis de 23,4 Gy de ICE (tasa de SSC a 5 años del 82,6 % ± 4,2 % y tasa de SG del 85,8 % en los pacientes que recibieron 23,4 Gy vs. tasa de SSC del 71,9 % ± 4,9 % y tasa de SG del 77,9 % ± 4,9 % en los pacientes que recibieron 18 Gy).
- La tasa de SSC a 5 años fue del 82,5 % en los pacientes que recibieron radioterapia dirigida al lecho tumoral, en comparación con el 80,5 % en los pacientes que recibieron radioterapia en la fosa posterior. Por lo tanto, la radioterapia dirigida al lecho tumoral no fue menos eficaz que la radioterapia dirigida a la fosa posterior (cociente de riesgos instantáneos, 0,97; intervalo de confianza superior 94 %, 1,32).
El análisis por subgrupos moleculares demostró que los niños con meduloblastoma del grupo 4 que recibieron 18 Gy de radioterapia craneoespinal tuvieron una SSC más precaria que los que recibieron 23,4 Gy. Esto no se observó en los otros subgrupos moleculares, aunque el estudio no tenía el tamaño necesario para el análisis por subgrupos moleculares.[59] Actualmente se está investigando la reducción de la dosis de radiación craneoespinal hasta 18 Gy en pacientes con meduloblastoma WNT (NCT02724579), el subgrupo molecular con mejor pronóstico.
- En el estudio SIOP-PNET-4 (NCT01351870) se comparó la radioterapia diaria (fracciones de 1,8 Gy con 23,4 Gy dirigidas al eje encefalomedular y un refuerzo de 30 Gy dirigido a la fosa posterior) con radiación 2 veces al día (fracciones de 1 Gy con 36 Gy y refuerzo de 24 Gy dirigido a la fosa posterior).[125]
- Al cabo de una mediana de seguimiento de 7,8 años, la SG a 10 años no fue significativamente diferente entre los dos grupos de radiación.
- No se notificaron efectos secundarios a largo plazo en este estudio.
- Si se agrega quimioterapia después de la radioterapia, se ha demostrado que la dosis efectiva de radioterapia craneoespinal es de 23,4 Gy.[94,125-127] Se están evaluando dosis más bajas.
- Aunque el refuerzo estándar en el meduloblastoma se dirige a toda la fosa posterior, los patrones de los datos de fracaso revelan que la radioterapia dirigida al lecho tumoral, en lugar de toda la fosa posterior, es igualmente eficaz y a veces se relaciona con reducción de la toxicidad.[128,129]; [59][Nivel de evidencia A1]
Quimioterapia adyuvante
En la actualidad, la quimioterapia es un componente estándar del tratamiento de los niños con meduloblastoma de riesgo promedio.
Evidencia (quimioterapia adyuvante):
- En ensayos prospectivos aleatorizados y en ensayos de un solo grupo se indica que la quimioterapia adyuvante, administrada al mismo tiempo que la radioterapia y después, mejoró la SG de niños con meduloblastoma de riesgo promedio.[91,117-121]
- Con la administración pre y posoperatoria de radioterapia y quimioterapia se han observado tasas de SSC a 5 años del 70 % al 85 %.[117-119]; [130][Nivel de evidencia B4]
- Se ha demostrado que una dosis más baja de radiación de 23,4 Gy dirigida al eje encefalomedular cuando se combina con quimioterapia produce control de la enfermedad en hasta el 85 % de los pacientes y puede disminuir la gravedad de las secuelas neurocognitivas a largo plazo.[94,126,127,131]
- Se han utilizado con éxito una variedad de regímenes quimioterapéuticos, como la combinación de cisplatino, lomustina y vincristina o la combinación de cisplatino, ciclofosfamida y vincristina.[117,118,131,132]
- Estas terapias aumentaron las tasas de SSC y SG a los 5 y 10 años, y es posible que redujeran la incidencia de la recaída tardía.
- Sin embargo, los sobrevivientes a largo plazo tratados con terapia multimodal tienen un riesgo alto de efectos tardíos, como hipoacusia, complicaciones cardíacas y segundas neoplasias.[133]
Además, la administración de dosis altas de ciclofosfamida después de la radiación con apoyo de rescate de células madre periféricas, pero con dosis acumuladas reducidas de vincristina y cisplatino, ha producido tasas de supervivencia similares.[58]
- Aunque el meduloblastoma a menudo es sensible a la quimioterapia, la quimioterapia prerradiación no ha mostrado mejorar la supervivencia en pacientes con meduloblastoma de riesgo promedio, en comparación con el tratamiento de radioterapia y quimioterapia posterior. En algunos estudios prospectivos, la administración de quimioterapia prerradiación se relacionó con una supervivencia más precaria.[118-121]
Tratamiento de los niños mayores de 3 años con meduloblastoma de riesgo alto
Las opciones de tratamiento estándar para los niños mayores de 3 años con diagnóstico reciente de meduloblastoma y que tienen enfermedad metastásica o que se sometieron a una resección subtotal incluyen los siguientes procedimientos:
En varios estudios con pacientes de riesgo alto, se demostró que la terapia multimodal mejora la duración del control de la enfermedad y la supervivencia sin enfermedad general.[58,134] En los estudios se observó que entre el 50 % y el 70 % de los pacientes con enfermedad de riesgo alto, incluso aquellos con enfermedad metastásica, presentarán control de la enfermedad a largo plazo.[58,117,134-138]; [139,140][Nivel de evidencia A1]; [141][Nivel de evidencia B4] En un estudio del COG completado se demostró que los niños con tumores amplificados con MYC del grupo 3 que se asignaron al azar para recibir carboplatino durante la radioterapia mejoraron las tasas de SSC y SG a 5 años, en comparación con aquellos que no recibieron carboplatino simultáneamente con la radioterapia.[135] No se ha determinado el tratamiento óptimo para los niños con meduloblastoma con activación de SHH o meduloblastoma con alteración de TP53, ya que se espera que menos del 30 % de los pacientes sobrevivan 5 años después del diagnóstico cuando reciben el tratamiento vigente en la actualidad.[14]
Cirugía
El tratamiento de los pacientes de riesgo alto es el mismo que para los pacientes de riesgo promedio. Si es posible, se considera óptimo intentar una resección macroscópica total.[80,84]
Radioterapia adyuvante
A diferencia del tratamiento de los pacientes de riesgo estándar, la dosis de radiación craneoespinal, por lo general, es de 36 Gy.
Quimioterapia adyuvante
Evidencia (quimioterapia adyuvante):
- Los fármacos que son útiles en niños con enfermedad de riesgo promedio son los mismos que se han usado de manera extensa en niños con enfermedad de riesgo alto, como el cisplatino, la lomustina, la ciclofosfamida, el etopósido o la vincristina.[139]
- Estas terapias aumentaron las tasas de SSC y SG a los 5 y 10 años, y es posible que redujeran la incidencia de la recaída tardía.
- Sin embargo, los sobrevivientes a largo plazo tratados con terapia multimodal tienen un riesgo alto de efectos tardíos, como hipoacusia, complicaciones cardíacas y segundas neoplasias.[133]
- También se ha utilizado quimioterapia no mielosupresora de dosis altas después de la radiación con apoyo de rescate de células madre periféricas, pero usando dosis acumuladas reducidas de vincristina y cisplatino, lo que produjo tasas de SSP a 5 años de alrededor del 60 %.[58]
- En el estudio del COG ACNS0332 (NCT00392327) se asignó al azar a los pacientes para recibir carboplatino diario, en comparación con vincristina semanal, durante la radioterapia (36 Gy craneoespinales y refuerzo en la fosa posterior) seguido de 6 ciclos de tratamiento adyuvante con cisplatino, ciclofosfamida y vincristina.[135]
- En los 261 pacientes evaluables, la tasa de SSC a 5 años fue del 62,9 % y la tasa de SG fue del 73,4 %.
- En toda la cohorte, no hubo diferencia en la tasa de SSC entre los pacientes tratados con carboplatino (66,4 %) y los pacientes que no recibieron carboplatino (59,2 %).
- En un análisis de subconjuntos basado en la subagrupación molecular, los pacientes con meduloblastoma del grupo 3 se beneficiaron del uso de carboplatino diario durante la radioterapia, con una tasa de SSC a 5 años del 73,2 % para los pacientes que recibieron carboplatino, en comparación con el 53,7 % para los que no lo recibieron.
- En una segunda aleatorización se probó la utilidad del tratamiento de mantenimiento con isotretinoína, pero esta asignación se cerró por futilidad en el momento de un análisis interino planificado.
- En un ensayo de 51 pacientes con enfermedad de riesgo alto recién diagnosticada, los pacientes recibieron quimioterapia de inducción posoperatoria (etopósido y carboplatino), seguida de 2 cursos de dosis altas de tiotepa con rescate de células madre periféricas y radioterapia craneoespinal adaptada al riesgo.[136]
- Las tasas de SSC y SG a 5 años fueron del 76 %.
Opciones de tratamiento en evaluación clínica para el meduloblastoma infantil
Tal vez haya ensayos clínicos terapéuticos de fase inicial disponibles para pacientes seleccionados. Es posible que estos ensayos estén disponibles a través del COG, el Pediatric Brain Tumor Consortium u otras entidades. La información en inglés sobre los ensayos clínicos patrocinados por el Instituto Nacional del Cáncer (NCI) se encuentra en el portal de Internet del NCI. Para obtener información en inglés sobre ensayos clínicos patrocinados por otras organizaciones, consultar el portal de Internet ClinicalTrials.gov.
Bibliografía
- Zhang J, Walsh MF, Wu G, et al.: Germline Mutations in Predisposition Genes in Pediatric Cancer. N Engl J Med 373 (24): 2336-46, 2015. [PUBMED Abstract]
- Waszak SM, Northcott PA, Buchhalter I, et al.: Spectrum and prevalence of genetic predisposition in medulloblastoma: a retrospective genetic study and prospective validation in a clinical trial cohort. Lancet Oncol 19 (6): 785-798, 2018. [PUBMED Abstract]
- Hamilton SR, Liu B, Parsons RE, et al.: The molecular basis of Turcot's syndrome. N Engl J Med 332 (13): 839-47, 1995. [PUBMED Abstract]
- Taylor MD, Mainprize TG, Rutka JT, et al.: Medulloblastoma in a child with Rubenstein-Taybi Syndrome: case report and review of the literature. Pediatr Neurosurg 35 (5): 235-8, 2001. [PUBMED Abstract]
- Miller RW, Rubinstein JH: Tumors in Rubinstein-Taybi syndrome. Am J Med Genet 56 (1): 112-5, 1995. [PUBMED Abstract]
- Bourdeaut F, Miquel C, Richer W, et al.: Rubinstein-Taybi syndrome predisposing to non-WNT, non-SHH, group 3 medulloblastoma. Pediatr Blood Cancer 61 (2): 383-6, 2014. [PUBMED Abstract]
- Garrè ML, Cama A, Bagnasco F, et al.: Medulloblastoma variants: age-dependent occurrence and relation to Gorlin syndrome--a new clinical perspective. Clin Cancer Res 15 (7): 2463-71, 2009. [PUBMED Abstract]
- Pastorino L, Ghiorzo P, Nasti S, et al.: Identification of a SUFU germline mutation in a family with Gorlin syndrome. Am J Med Genet A 149A (7): 1539-43, 2009. [PUBMED Abstract]
- Brugières L, Remenieras A, Pierron G, et al.: High frequency of germline SUFU mutations in children with desmoplastic/nodular medulloblastoma younger than 3 years of age. J Clin Oncol 30 (17): 2087-93, 2012. [PUBMED Abstract]
- Evans DG, Farndon PA, Burnell LD, et al.: The incidence of Gorlin syndrome in 173 consecutive cases of medulloblastoma. Br J Cancer 64 (5): 959-61, 1991. [PUBMED Abstract]
- Smith MJ, Beetz C, Williams SG, et al.: Germline mutations in SUFU cause Gorlin syndrome-associated childhood medulloblastoma and redefine the risk associated with PTCH1 mutations. J Clin Oncol 32 (36): 4155-61, 2014. [PUBMED Abstract]
- Li FP, Fraumeni JF: Rhabdomyosarcoma in children: epidemiologic study and identification of a familial cancer syndrome. J Natl Cancer Inst 43 (6): 1365-73, 1969. [PUBMED Abstract]
- Pearson AD, Craft AW, Ratcliffe JM, et al.: Two families with the Li-Fraumeni cancer family syndrome. J Med Genet 19 (5): 362-5, 1982. [PUBMED Abstract]
- Kolodziejczak AS, Guerrini-Rousseau L, Planchon JM, et al.: Clinical outcome of pediatric medulloblastoma patients with Li-Fraumeni syndrome. Neuro Oncol 25 (12): 2273-2286, 2023. [PUBMED Abstract]
- Offit K, Levran O, Mullaney B, et al.: Shared genetic susceptibility to breast cancer, brain tumors, and Fanconi anemia. J Natl Cancer Inst 95 (20): 1548-51, 2003. [PUBMED Abstract]
- Dewire MD, Ellison DW, Patay Z, et al.: Fanconi anemia and biallelic BRCA2 mutation diagnosed in a young child with an embryonal CNS tumor. Pediatr Blood Cancer 53 (6): 1140-2, 2009. [PUBMED Abstract]
- Reid S, Renwick A, Seal S, et al.: Biallelic BRCA2 mutations are associated with multiple malignancies in childhood including familial Wilms tumour. J Med Genet 42 (2): 147-51, 2005. [PUBMED Abstract]
- Sönksen M, Obrecht-Sturm D, Hernáiz Driever P, et al.: Medulloblastoma in children with Fanconi anemia: Association with FA-D1/FA-N, SHH type and poor survival independent of treatment strategies. Neuro Oncol 26 (11): 2125-2139, 2024. [PUBMED Abstract]
- Begemann M, Waszak SM, Robinson GW, et al.: Germline GPR161 Mutations Predispose to Pediatric Medulloblastoma. J Clin Oncol 38 (1): 43-50, 2020. [PUBMED Abstract]
- Waszak SM, Robinson GW, Gudenas BL, et al.: Germline Elongator mutations in Sonic Hedgehog medulloblastoma. Nature 580 (7803): 396-401, 2020. [PUBMED Abstract]
- Rorke LB: The cerebellar medulloblastoma and its relationship to primitive neuroectodermal tumors. J Neuropathol Exp Neurol 42 (1): 1-15, 1983. [PUBMED Abstract]
- Louis DN, Perry A, Wesseling P, et al.: The 2021 WHO Classification of Tumors of the Central Nervous System: a summary. Neuro Oncol 23 (8): 1231-1251, 2021. [PUBMED Abstract]
- Ramaswamy V, Remke M, Shih D, et al.: Duration of the pre-diagnostic interval in medulloblastoma is subgroup dependent. Pediatr Blood Cancer 61 (7): 1190-4, 2014. [PUBMED Abstract]
- WHO Classification of Tumours Editorial Board, ed.: WHO Classification of Tumours: Central Nervous System Tumours. Vol. 6. 5th ed. IARC Press; 2021.
- McManamy CS, Lamont JM, Taylor RE, et al.: Morphophenotypic variation predicts clinical behavior in childhood non-desmoplastic medulloblastomas. J Neuropathol Exp Neurol 62 (6): 627-32, 2003. [PUBMED Abstract]
- Eberhart CG, Kratz J, Wang Y, et al.: Histopathological and molecular prognostic markers in medulloblastoma: c-myc, N-myc, TrkC, and anaplasia. J Neuropathol Exp Neurol 63 (5): 441-9, 2004. [PUBMED Abstract]
- Giangaspero F, Perilongo G, Fondelli MP, et al.: Medulloblastoma with extensive nodularity: a variant with favorable prognosis. J Neurosurg 91 (6): 971-7, 1999. [PUBMED Abstract]
- Lafay-Cousin L, Bouffet E, Strother D, et al.: Phase II Study of Nonmetastatic Desmoplastic Medulloblastoma in Children Younger Than 4 Years of Age: A Report of the Children's Oncology Group (ACNS1221). J Clin Oncol 38 (3): 223-231, 2020. [PUBMED Abstract]
- Korshunov A, Okonechnikov K, Sahm F, et al.: Transcriptional profiling of medulloblastoma with extensive nodularity (MBEN) reveals two clinically relevant tumor subsets with VSNL1 as potent prognostic marker. Acta Neuropathol 139 (3): 583-596, 2020. [PUBMED Abstract]
- Onvani S, Etame AB, Smith CA, et al.: Genetics of medulloblastoma: clues for novel therapies. Expert Rev Neurother 10 (5): 811-23, 2010. [PUBMED Abstract]
- Dubuc AM, Northcott PA, Mack S, et al.: The genetics of pediatric brain tumors. Curr Neurol Neurosci Rep 10 (3): 215-23, 2010. [PUBMED Abstract]
- Thompson MC, Fuller C, Hogg TL, et al.: Genomics identifies medulloblastoma subgroups that are enriched for specific genetic alterations. J Clin Oncol 24 (12): 1924-31, 2006. [PUBMED Abstract]
- Kool M, Koster J, Bunt J, et al.: Integrated genomics identifies five medulloblastoma subtypes with distinct genetic profiles, pathway signatures and clinicopathological features. PLoS One 3 (8): e3088, 2008. [PUBMED Abstract]
- Tabori U, Baskin B, Shago M, et al.: Universal poor survival in children with medulloblastoma harboring somatic TP53 mutations. J Clin Oncol 28 (8): 1345-50, 2010. [PUBMED Abstract]
- Pfister S, Remke M, Benner A, et al.: Outcome prediction in pediatric medulloblastoma based on DNA copy-number aberrations of chromosomes 6q and 17q and the MYC and MYCN loci. J Clin Oncol 27 (10): 1627-36, 2009. [PUBMED Abstract]
- Ellison DW, Onilude OE, Lindsey JC, et al.: beta-Catenin status predicts a favorable outcome in childhood medulloblastoma: the United Kingdom Children's Cancer Study Group Brain Tumour Committee. J Clin Oncol 23 (31): 7951-7, 2005. [PUBMED Abstract]
- Polkinghorn WR, Tarbell NJ: Medulloblastoma: tumorigenesis, current clinical paradigm, and efforts to improve risk stratification. Nat Clin Pract Oncol 4 (5): 295-304, 2007. [PUBMED Abstract]
- Giangaspero F, Wellek S, Masuoka J, et al.: Stratification of medulloblastoma on the basis of histopathological grading. Acta Neuropathol 112 (1): 5-12, 2006. [PUBMED Abstract]
- Northcott PA, Korshunov A, Witt H, et al.: Medulloblastoma comprises four distinct molecular variants. J Clin Oncol 29 (11): 1408-14, 2011. [PUBMED Abstract]
- Pomeroy SL, Tamayo P, Gaasenbeek M, et al.: Prediction of central nervous system embryonal tumour outcome based on gene expression. Nature 415 (6870): 436-42, 2002. [PUBMED Abstract]
- Jones DT, Jäger N, Kool M, et al.: Dissecting the genomic complexity underlying medulloblastoma. Nature 488 (7409): 100-5, 2012. [PUBMED Abstract]
- Peyrl A, Chocholous M, Kieran MW, et al.: Antiangiogenic metronomic therapy for children with recurrent embryonal brain tumors. Pediatr Blood Cancer 59 (3): 511-7, 2012. [PUBMED Abstract]
- Taylor MD, Northcott PA, Korshunov A, et al.: Molecular subgroups of medulloblastoma: the current consensus. Acta Neuropathol 123 (4): 465-72, 2012. [PUBMED Abstract]
- Kool M, Korshunov A, Remke M, et al.: Molecular subgroups of medulloblastoma: an international meta-analysis of transcriptome, genetic aberrations, and clinical data of WNT, SHH, Group 3, and Group 4 medulloblastomas. Acta Neuropathol 123 (4): 473-84, 2012. [PUBMED Abstract]
- Pietsch T, Schmidt R, Remke M, et al.: Prognostic significance of clinical, histopathological, and molecular characteristics of medulloblastomas in the prospective HIT2000 multicenter clinical trial cohort. Acta Neuropathol 128 (1): 137-49, 2014. [PUBMED Abstract]
- Cho YJ, Tsherniak A, Tamayo P, et al.: Integrative genomic analysis of medulloblastoma identifies a molecular subgroup that drives poor clinical outcome. J Clin Oncol 29 (11): 1424-30, 2011. [PUBMED Abstract]
- Gajjar A, Bowers DC, Karajannis MA, et al.: Pediatric Brain Tumors: Innovative Genomic Information Is Transforming the Diagnostic and Clinical Landscape. J Clin Oncol 33 (27): 2986-98, 2015. [PUBMED Abstract]
- Morrissy AS, Cavalli FMG, Remke M, et al.: Spatial heterogeneity in medulloblastoma. Nat Genet 49 (5): 780-788, 2017. [PUBMED Abstract]
- Wang X, Dubuc AM, Ramaswamy V, et al.: Medulloblastoma subgroups remain stable across primary and metastatic compartments. Acta Neuropathol 129 (3): 449-57, 2015. [PUBMED Abstract]
- Cavalli FMG, Remke M, Rampasek L, et al.: Intertumoral Heterogeneity within Medulloblastoma Subgroups. Cancer Cell 31 (6): 737-754.e6, 2017. [PUBMED Abstract]
- Northcott PA, Buchhalter I, Morrissy AS, et al.: The whole-genome landscape of medulloblastoma subtypes. Nature 547 (7663): 311-317, 2017. [PUBMED Abstract]
- Schwalbe EC, Lindsey JC, Nakjang S, et al.: Novel molecular subgroups for clinical classification and outcome prediction in childhood medulloblastoma: a cohort study. Lancet Oncol 18 (7): 958-971, 2017. [PUBMED Abstract]
- Hicks D, Rafiee G, Schwalbe EC, et al.: The molecular landscape and associated clinical experience in infant medulloblastoma: prognostic significance of second-generation subtypes. Neuropathol Appl Neurobiol 47 (2): 236-250, 2021. [PUBMED Abstract]
- Northcott PA, Jones DT, Kool M, et al.: Medulloblastomics: the end of the beginning. Nat Rev Cancer 12 (12): 818-34, 2012. [PUBMED Abstract]
- Korshunov A, Sahm F, Zheludkova O, et al.: DNA methylation profiling is a method of choice for molecular verification of pediatric WNT-activated medulloblastomas. Neuro Oncol 21 (2): 214-221, 2019. [PUBMED Abstract]
- Gibson P, Tong Y, Robinson G, et al.: Subtypes of medulloblastoma have distinct developmental origins. Nature 468 (7327): 1095-9, 2010. [PUBMED Abstract]
- Ellison DW, Dalton J, Kocak M, et al.: Medulloblastoma: clinicopathological correlates of SHH, WNT, and non-SHH/WNT molecular subgroups. Acta Neuropathol 121 (3): 381-96, 2011. [PUBMED Abstract]
- Gajjar A, Chintagumpala M, Ashley D, et al.: Risk-adapted craniospinal radiotherapy followed by high-dose chemotherapy and stem-cell rescue in children with newly diagnosed medulloblastoma (St Jude Medulloblastoma-96): long-term results from a prospective, multicentre trial. Lancet Oncol 7 (10): 813-20, 2006. [PUBMED Abstract]
- Michalski JM, Janss AJ, Vezina LG, et al.: Children's Oncology Group Phase III Trial of Reduced-Dose and Reduced-Volume Radiotherapy With Chemotherapy for Newly Diagnosed Average-Risk Medulloblastoma. J Clin Oncol 39 (24): 2685-2697, 2021. [PUBMED Abstract]
- Goschzik T, Mynarek M, Doerner E, et al.: Genetic alterations of TP53 and OTX2 indicate increased risk of relapse in WNT medulloblastomas. Acta Neuropathol 144 (6): 1143-1156, 2022. [PUBMED Abstract]
- Gottardo NG: Genetic alterations of TP53 and OTX2 indicate increased risk of relapse in WNT medulloblastomas: "it's a numbers game"-implications for WNT medulloblastoma dose-reduction clinical trials. Acta Neuropathol 145 (1): 145-147, 2023. [PUBMED Abstract]
- Shuai S, Suzuki H, Diaz-Navarro A, et al.: The U1 spliceosomal RNA is recurrently mutated in multiple cancers. Nature 574 (7780): 712-716, 2019. [PUBMED Abstract]
- Suzuki H, Kumar SA, Shuai S, et al.: Recurrent noncoding U1 snRNA mutations drive cryptic splicing in SHH medulloblastoma. Nature 574 (7780): 707-711, 2019. [PUBMED Abstract]
- Kool M, Jones DT, Jäger N, et al.: Genome sequencing of SHH medulloblastoma predicts genotype-related response to smoothened inhibition. Cancer Cell 25 (3): 393-405, 2014. [PUBMED Abstract]
- Robinson GW, Rudneva VA, Buchhalter I, et al.: Risk-adapted therapy for young children with medulloblastoma (SJYC07): therapeutic and molecular outcomes from a multicentre, phase 2 trial. Lancet Oncol 19 (6): 768-784, 2018. [PUBMED Abstract]
- Leary SE, Zhou T, Holmes E, et al.: Histology predicts a favorable outcome in young children with desmoplastic medulloblastoma: a report from the children's oncology group. Cancer 117 (14): 3262-7, 2011. [PUBMED Abstract]
- Rutkowski S, von Hoff K, Emser A, et al.: Survival and prognostic factors of early childhood medulloblastoma: an international meta-analysis. J Clin Oncol 28 (33): 4961-8, 2010. [PUBMED Abstract]
- von Bueren AO, von Hoff K, Pietsch T, et al.: Treatment of young children with localized medulloblastoma by chemotherapy alone: results of the prospective, multicenter trial HIT 2000 confirming the prognostic impact of histology. Neuro Oncol 13 (6): 669-79, 2011. [PUBMED Abstract]
- Shih DJ, Northcott PA, Remke M, et al.: Cytogenetic prognostication within medulloblastoma subgroups. J Clin Oncol 32 (9): 886-96, 2014. [PUBMED Abstract]
- Schwalbe EC, Williamson D, Lindsey JC, et al.: DNA methylation profiling of medulloblastoma allows robust subclassification and improved outcome prediction using formalin-fixed biopsies. Acta Neuropathol 125 (3): 359-71, 2013. [PUBMED Abstract]
- Zhukova N, Ramaswamy V, Remke M, et al.: Subgroup-specific prognostic implications of TP53 mutation in medulloblastoma. J Clin Oncol 31 (23): 2927-35, 2013. [PUBMED Abstract]
- Gajjar A, Robinson GW, Smith KS, et al.: Outcomes by Clinical and Molecular Features in Children With Medulloblastoma Treated With Risk-Adapted Therapy: Results of an International Phase III Trial (SJMB03). J Clin Oncol 39 (7): 822-835, 2021. [PUBMED Abstract]
- Goschzik T, Schwalbe EC, Hicks D, et al.: Prognostic effect of whole chromosomal aberration signatures in standard-risk, non-WNT/non-SHH medulloblastoma: a retrospective, molecular analysis of the HIT-SIOP PNET 4 trial. Lancet Oncol 19 (12): 1602-1616, 2018. [PUBMED Abstract]
- Gottardo NG, Hansford JR, McGlade JP, et al.: Medulloblastoma Down Under 2013: a report from the third annual meeting of the International Medulloblastoma Working Group. Acta Neuropathol 127 (2): 189-201, 2014. [PUBMED Abstract]
- Louis DN, Perry A, Burger P, et al.: International Society Of Neuropathology--Haarlem consensus guidelines for nervous system tumor classification and grading. Brain Pathol 24 (5): 429-35, 2014. [PUBMED Abstract]
- Sharma T, Schwalbe EC, Williamson D, et al.: Second-generation molecular subgrouping of medulloblastoma: an international meta-analysis of Group 3 and Group 4 subtypes. Acta Neuropathol 138 (2): 309-326, 2019. [PUBMED Abstract]
- Fouladi M, Gajjar A, Boyett JM, et al.: Comparison of CSF cytology and spinal magnetic resonance imaging in the detection of leptomeningeal disease in pediatric medulloblastoma or primitive neuroectodermal tumor. J Clin Oncol 17 (10): 3234-7, 1999. [PUBMED Abstract]
- Zeltzer PM, Boyett JM, Finlay JL, et al.: Metastasis stage, adjuvant treatment, and residual tumor are prognostic factors for medulloblastoma in children: conclusions from the Children's Cancer Group 921 randomized phase III study. J Clin Oncol 17 (3): 832-45, 1999. [PUBMED Abstract]
- Yao MS, Mehta MP, Boyett JM, et al.: The effect of M-stage on patterns of failure in posterior fossa primitive neuroectodermal tumors treated on CCG-921: a phase III study in a high-risk patient population. Int J Radiat Oncol Biol Phys 38 (3): 469-76, 1997. [PUBMED Abstract]
- Taylor RE, Bailey CC, Robinson K, et al.: Results of a randomized study of preradiation chemotherapy versus radiotherapy alone for nonmetastatic medulloblastoma: The International Society of Paediatric Oncology/United Kingdom Children's Cancer Study Group PNET-3 Study. J Clin Oncol 21 (8): 1581-91, 2003. [PUBMED Abstract]
- Rutkowski S, Bode U, Deinlein F, et al.: Treatment of early childhood medulloblastoma by postoperative chemotherapy alone. N Engl J Med 352 (10): 978-86, 2005. [PUBMED Abstract]
- Rutkowski S, Gerber NU, von Hoff K, et al.: Treatment of early childhood medulloblastoma by postoperative chemotherapy and deferred radiotherapy. Neuro Oncol 11 (2): 201-10, 2009. [PUBMED Abstract]
- Ramaswamy V, Remke M, Adamski J, et al.: Medulloblastoma subgroup-specific outcomes in irradiated children: who are the true high-risk patients? Neuro Oncol 18 (2): 291-7, 2016. [PUBMED Abstract]
- Albright AL, Wisoff JH, Zeltzer PM, et al.: Effects of medulloblastoma resections on outcome in children: a report from the Children's Cancer Group. Neurosurgery 38 (2): 265-71, 1996. [PUBMED Abstract]
- Thompson EM, Hielscher T, Bouffet E, et al.: Prognostic value of medulloblastoma extent of resection after accounting for molecular subgroup: a retrospective integrated clinical and molecular analysis. Lancet Oncol 17 (4): 484-95, 2016. [PUBMED Abstract]
- Stargatt R, Rosenfeld JV, Maixner W, et al.: Multiple factors contribute to neuropsychological outcome in children with posterior fossa tumors. Dev Neuropsychol 32 (2): 729-48, 2007. [PUBMED Abstract]
- Pollack IF, Polinko P, Albright AL, et al.: Mutism and pseudobulbar symptoms after resection of posterior fossa tumors in children: incidence and pathophysiology. Neurosurgery 37 (5): 885-93, 1995. [PUBMED Abstract]
- Robertson PL, Muraszko KM, Holmes EJ, et al.: Incidence and severity of postoperative cerebellar mutism syndrome in children with medulloblastoma: a prospective study by the Children's Oncology Group. J Neurosurg 105 (6): 444-51, 2006. [PUBMED Abstract]
- Wells EM, Khademian ZP, Walsh KS, et al.: Postoperative cerebellar mutism syndrome following treatment of medulloblastoma: neuroradiographic features and origin. J Neurosurg Pediatr 5 (4): 329-34, 2010. [PUBMED Abstract]
- Gudrunardottir T, Sehested A, Juhler M, et al.: Cerebellar mutism: review of the literature. Childs Nerv Syst 27 (3): 355-63, 2011. [PUBMED Abstract]
- Wolfe-Christensen C, Mullins LL, Scott JG, et al.: Persistent psychosocial problems in children who develop posterior fossa syndrome after medulloblastoma resection. Pediatr Blood Cancer 49 (5): 723-6, 2007. [PUBMED Abstract]
- Jabarkheel R, Amayiri N, Yecies D, et al.: Molecular correlates of cerebellar mutism syndrome in medulloblastoma. Neuro Oncol 22 (2): 290-297, 2020. [PUBMED Abstract]
- Khan RB, Patay Z, Klimo P, et al.: Clinical features, neurologic recovery, and risk factors of postoperative posterior fossa syndrome and delayed recovery: a prospective study. Neuro Oncol 23 (9): 1586-1596, 2021. [PUBMED Abstract]
- Packer RJ, Gajjar A, Vezina G, et al.: Phase III study of craniospinal radiation therapy followed by adjuvant chemotherapy for newly diagnosed average-risk medulloblastoma. J Clin Oncol 24 (25): 4202-8, 2006. [PUBMED Abstract]
- Yock TI, Yeap BY, Ebb DH, et al.: Long-term toxic effects of proton radiotherapy for paediatric medulloblastoma: a phase 2 single-arm study. Lancet Oncol 17 (3): 287-98, 2016. [PUBMED Abstract]
- Eaton BR, Esiashvili N, Kim S, et al.: Clinical Outcomes Among Children With Standard-Risk Medulloblastoma Treated With Proton and Photon Radiation Therapy: A Comparison of Disease Control and Overall Survival. Int J Radiat Oncol Biol Phys 94 (1): 133-8, 2016. [PUBMED Abstract]
- Paulino AC, Mahajan A, Ye R, et al.: Ototoxicity and cochlear sparing in children with medulloblastoma: Proton vs. photon radiotherapy. Radiother Oncol 128 (1): 128-132, 2018. [PUBMED Abstract]
- Ris MD, Packer R, Goldwein J, et al.: Intellectual outcome after reduced-dose radiation therapy plus adjuvant chemotherapy for medulloblastoma: a Children's Cancer Group study. J Clin Oncol 19 (15): 3470-6, 2001. [PUBMED Abstract]
- Packer RJ, Sutton LN, Atkins TE, et al.: A prospective study of cognitive function in children receiving whole-brain radiotherapy and chemotherapy: 2-year results. J Neurosurg 70 (5): 707-13, 1989. [PUBMED Abstract]
- Johnson DL, McCabe MA, Nicholson HS, et al.: Quality of long-term survival in young children with medulloblastoma. J Neurosurg 80 (6): 1004-10, 1994. [PUBMED Abstract]
- Walter AW, Mulhern RK, Gajjar A, et al.: Survival and neurodevelopmental outcome of young children with medulloblastoma at St Jude Children's Research Hospital. J Clin Oncol 17 (12): 3720-8, 1999. [PUBMED Abstract]
- Laughton SJ, Merchant TE, Sklar CA, et al.: Endocrine outcomes for children with embryonal brain tumors after risk-adapted craniospinal and conformal primary-site irradiation and high-dose chemotherapy with stem-cell rescue on the SJMB-96 trial. J Clin Oncol 26 (7): 1112-8, 2008. [PUBMED Abstract]
- Geyer JR, Sposto R, Jennings M, et al.: Multiagent chemotherapy and deferred radiotherapy in infants with malignant brain tumors: a report from the Children's Cancer Group. J Clin Oncol 23 (30): 7621-31, 2005. [PUBMED Abstract]
- Chi SN, Gardner SL, Levy AS, et al.: Feasibility and response to induction chemotherapy intensified with high-dose methotrexate for young children with newly diagnosed high-risk disseminated medulloblastoma. J Clin Oncol 22 (24): 4881-7, 2004. [PUBMED Abstract]
- Grill J, Sainte-Rose C, Jouvet A, et al.: Treatment of medulloblastoma with postoperative chemotherapy alone: an SFOP prospective trial in young children. Lancet Oncol 6 (8): 573-80, 2005. [PUBMED Abstract]
- Cohen BH, Geyer JR, Miller DC, et al.: Pilot Study of Intensive Chemotherapy With Peripheral Hematopoietic Cell Support for Children Less Than 3 Years of Age With Malignant Brain Tumors, the CCG-99703 Phase I/II Study. A Report From the Children's Oncology Group. Pediatr Neurol 53 (1): 31-46, 2015. [PUBMED Abstract]
- Duffner PK, Horowitz ME, Krischer JP, et al.: Postoperative chemotherapy and delayed radiation in children less than three years of age with malignant brain tumors. N Engl J Med 328 (24): 1725-31, 1993. [PUBMED Abstract]
- Ater JL, van Eys J, Woo SY, et al.: MOPP chemotherapy without irradiation as primary postsurgical therapy for brain tumors in infants and young children. J Neurooncol 32 (3): 243-52, 1997. [PUBMED Abstract]
- Grundy RG, Wilne SH, Robinson KJ, et al.: Primary postoperative chemotherapy without radiotherapy for treatment of brain tumours other than ependymoma in children under 3 years: results of the first UKCCSG/SIOP CNS 9204 trial. Eur J Cancer 46 (1): 120-33, 2010. [PUBMED Abstract]
- Blaney SM, Kocak M, Gajjar A, et al.: Pilot study of systemic and intrathecal mafosfamide followed by conformal radiation for infants with intracranial central nervous system tumors: a pediatric brain tumor consortium study (PBTC-001). J Neurooncol 109 (3): 565-71, 2012. [PUBMED Abstract]
- Mynarek M, von Hoff K, Pietsch T, et al.: Nonmetastatic Medulloblastoma of Early Childhood: Results From the Prospective Clinical Trial HIT-2000 and An Extended Validation Cohort. J Clin Oncol 38 (18): 2028-2040, 2020. [PUBMED Abstract]
- Dhall G, Grodman H, Ji L, et al.: Outcome of children less than three years old at diagnosis with non-metastatic medulloblastoma treated with chemotherapy on the "Head Start" I and II protocols. Pediatr Blood Cancer 50 (6): 1169-75, 2008. [PUBMED Abstract]
- Dhall G, O'Neil SH, Ji L, et al.: Excellent outcome of young children with nodular desmoplastic medulloblastoma treated on "Head Start" III: a multi-institutional, prospective clinical trial. Neuro Oncol 22 (12): 1862-1872, 2020. [PUBMED Abstract]
- Erker C, Mynarek M, Bailey S, et al.: Outcomes of Infants and Young Children With Relapsed Medulloblastoma After Initial Craniospinal Irradiation-Sparing Approaches: An International Cohort Study. J Clin Oncol 41 (10): 1921-1932, 2023. [PUBMED Abstract]
- Lafay-Cousin L, Smith A, Chi SN, et al.: Clinical, Pathological, and Molecular Characterization of Infant Medulloblastomas Treated with Sequential High-Dose Chemotherapy. Pediatr Blood Cancer 63 (9): 1527-34, 2016. [PUBMED Abstract]
- Ashley DM, Merchant TE, Strother D, et al.: Induction chemotherapy and conformal radiation therapy for very young children with nonmetastatic medulloblastoma: Children's Oncology Group study P9934. J Clin Oncol 30 (26): 3181-6, 2012. [PUBMED Abstract]
- Packer RJ, Sutton LN, Elterman R, et al.: Outcome for children with medulloblastoma treated with radiation and cisplatin, CCNU, and vincristine chemotherapy. J Neurosurg 81 (5): 690-8, 1994. [PUBMED Abstract]
- Bailey CC, Gnekow A, Wellek S, et al.: Prospective randomised trial of chemotherapy given before radiotherapy in childhood medulloblastoma. International Society of Paediatric Oncology (SIOP) and the (German) Society of Paediatric Oncology (GPO): SIOP II. Med Pediatr Oncol 25 (3): 166-78, 1995. [PUBMED Abstract]
- Kortmann RD, Kühl J, Timmermann B, et al.: Postoperative neoadjuvant chemotherapy before radiotherapy as compared to immediate radiotherapy followed by maintenance chemotherapy in the treatment of medulloblastoma in childhood: results of the German prospective randomized trial HIT '91. Int J Radiat Oncol Biol Phys 46 (2): 269-79, 2000. [PUBMED Abstract]
- Taylor RE, Bailey CC, Robinson KJ, et al.: Impact of radiotherapy parameters on outcome in the International Society of Paediatric Oncology/United Kingdom Children's Cancer Study Group PNET-3 study of preradiotherapy chemotherapy for M0-M1 medulloblastoma. Int J Radiat Oncol Biol Phys 58 (4): 1184-93, 2004. [PUBMED Abstract]
- von Hoff K, Hinkes B, Gerber NU, et al.: Long-term outcome and clinical prognostic factors in children with medulloblastoma treated in the prospective randomised multicentre trial HIT'91. Eur J Cancer 45 (7): 1209-17, 2009. [PUBMED Abstract]
- Cohen KJ, Munjapara V, Aguilera D, et al.: A Pilot Study Omitting Radiation in the Treatment of Children with Newly Diagnosed Wnt-Activated Medulloblastoma. Clin Cancer Res 29 (24): 5031-5037, 2023. [PUBMED Abstract]
- Thomas PR, Deutsch M, Kepner JL, et al.: Low-stage medulloblastoma: final analysis of trial comparing standard-dose with reduced-dose neuraxis irradiation. J Clin Oncol 18 (16): 3004-11, 2000. [PUBMED Abstract]
- Gupta T, Pervez S, Dasgupta A, et al.: Omission of Upfront Craniospinal Irradiation in Patients with Low-Risk WNT-Pathway Medulloblastoma Is Associated with Unacceptably High Risk of Neuraxial Failure. Clin Cancer Res 28 (19): 4180-4185, 2022. [PUBMED Abstract]
- Sabel M, Fleischhack G, Tippelt S, et al.: Relapse patterns and outcome after relapse in standard risk medulloblastoma: a report from the HIT-SIOP-PNET4 study. J Neurooncol 129 (3): 515-524, 2016. [PUBMED Abstract]
- Oyharcabal-Bourden V, Kalifa C, Gentet JC, et al.: Standard-risk medulloblastoma treated by adjuvant chemotherapy followed by reduced-dose craniospinal radiation therapy: a French Society of Pediatric Oncology Study. J Clin Oncol 23 (21): 4726-34, 2005. [PUBMED Abstract]
- Merchant TE, Kun LE, Krasin MJ, et al.: Multi-institution prospective trial of reduced-dose craniospinal irradiation (23.4 Gy) followed by conformal posterior fossa (36 Gy) and primary site irradiation (55.8 Gy) and dose-intensive chemotherapy for average-risk medulloblastoma. Int J Radiat Oncol Biol Phys 70 (3): 782-7, 2008. [PUBMED Abstract]
- Fukunaga-Johnson N, Sandler HM, Marsh R, et al.: The use of 3D conformal radiotherapy (3D CRT) to spare the cochlea in patients with medulloblastoma. Int J Radiat Oncol Biol Phys 41 (1): 77-82, 1998. [PUBMED Abstract]
- Huang E, Teh BS, Strother DR, et al.: Intensity-modulated radiation therapy for pediatric medulloblastoma: early report on the reduction of ototoxicity. Int J Radiat Oncol Biol Phys 52 (3): 599-605, 2002. [PUBMED Abstract]
- Carrie C, Grill J, Figarella-Branger D, et al.: Online quality control, hyperfractionated radiotherapy alone and reduced boost volume for standard risk medulloblastoma: long-term results of MSFOP 98. J Clin Oncol 27 (11): 1879-83, 2009. [PUBMED Abstract]
- Packer RJ, Goldwein J, Nicholson HS, et al.: Treatment of children with medulloblastomas with reduced-dose craniospinal radiation therapy and adjuvant chemotherapy: A Children's Cancer Group Study. J Clin Oncol 17 (7): 2127-36, 1999. [PUBMED Abstract]
- Nageswara Rao AA, Wallace DJ, Billups C, et al.: Cumulative cisplatin dose is not associated with event-free or overall survival in children with newly diagnosed average-risk medulloblastoma treated with cisplatin based adjuvant chemotherapy: report from the Children's Oncology Group. Pediatr Blood Cancer 61 (1): 102-6, 2014. [PUBMED Abstract]
- Salloum R, Chen Y, Yasui Y, et al.: Late Morbidity and Mortality Among Medulloblastoma Survivors Diagnosed Across Three Decades: A Report From the Childhood Cancer Survivor Study. J Clin Oncol 37 (9): 731-740, 2019. [PUBMED Abstract]
- Verlooy J, Mosseri V, Bracard S, et al.: Treatment of high risk medulloblastomas in children above the age of 3 years: a SFOP study. Eur J Cancer 42 (17): 3004-14, 2006. [PUBMED Abstract]
- Leary SES, Packer RJ, Li Y, et al.: Efficacy of Carboplatin and Isotretinoin in Children With High-risk Medulloblastoma: A Randomized Clinical Trial From the Children's Oncology Group. JAMA Oncol 7 (9): 1313-1321, 2021. [PUBMED Abstract]
- Dufour C, Foulon S, Geoffray A, et al.: Prognostic relevance of clinical and molecular risk factors in children with high-risk medulloblastoma treated in the phase II trial PNET HR+5. Neuro Oncol 23 (7): 1163-1172, 2021. [PUBMED Abstract]
- Gandola L, Massimino M, Cefalo G, et al.: Hyperfractionated accelerated radiotherapy in the Milan strategy for metastatic medulloblastoma. J Clin Oncol 27 (4): 566-71, 2009. [PUBMED Abstract]
- Evans AE, Jenkin RD, Sposto R, et al.: The treatment of medulloblastoma. Results of a prospective randomized trial of radiation therapy with and without CCNU, vincristine, and prednisone. J Neurosurg 72 (4): 572-82, 1990. [PUBMED Abstract]
- Jakacki RI, Burger PC, Zhou T, et al.: Outcome of children with metastatic medulloblastoma treated with carboplatin during craniospinal radiotherapy: a Children's Oncology Group Phase I/II study. J Clin Oncol 30 (21): 2648-53, 2012. [PUBMED Abstract]
- Tarbell NJ, Friedman H, Polkinghorn WR, et al.: High-risk medulloblastoma: a pediatric oncology group randomized trial of chemotherapy before or after radiation therapy (POG 9031). J Clin Oncol 31 (23): 2936-41, 2013. [PUBMED Abstract]
- von Bueren AO, Kortmann RD, von Hoff K, et al.: Treatment of Children and Adolescents With Metastatic Medulloblastoma and Prognostic Relevance of Clinical and Biologic Parameters. J Clin Oncol 34 (34): 4151-4160, 2016. [PUBMED Abstract]
Tumores embrionarios distintos del meduloblastoma infantil
La clasificación de la Organización Mundial de la Salud (OMS) de 2021 de los tumores del sistema nervioso central (SNC) se, enumera en la sección Clasificación celular y molecular. Todos los tumores de origen neuroectodérmico distintos del meduloblastoma y que carecen de las características histopatológicas específicas o alteraciones moleculares que definen a otros tumores del SNC se clasifican como tumores embrionarios del SNC.[1,2] Estos tumores se analizarán en esta sección, excepto los tumores teratoides rabdoides atípicos (TTRA). Para obtener más información, consultar Tratamiento del tumor teratoide rabdoide atípico del sistema nervioso central infantil. El pineoblastoma también se aborda en este resumen porque comparte características histológicas con los tumores embrionarios y, por lo general, se trata de la misma forma. Para obtener más información, consultar la sección Pineoblastoma infantil.
Cuadro clínico inicial
Los tumores embrionarios distintos del meduloblastoma presentan un cuadro clínico inicial que también es relativamente rápido y depende de la ubicación del tumor en el sistema nervioso. Los tumores embrionarios suelen crecer rápido y, por lo común, se diagnostican durante los primeros 3 meses a partir de la aparición de los síntomas.
Los tumores embrionarios distintos del meduloblastoma surgen en cualquier lugar del SNC y su presentación clínica es variable. Por lo general, producen disfunción neurológica importante acompañada de letargo y vómitos. Los tumores embrionarios supratentoriales (consultar la Figura 1) producen deficiencias neurológicas focales, como hemiparesia y pérdida del campo visual, según la porción de la corteza cerebral comprometida. A veces también causan convulsiones y obnubilación.
Clasificación celular y molecular
En la clasificación de tumores del SNC de la OMS de 2021 se incluyen los tumores embrionarios distintos del meduloblastoma, a partir de sus características histológicas e inmunohistológicas y, en algunos casos, por hallazgos moleculares. La clasificación incluye los siguientes tumores:[1,2]
- Tumor teratoide rabdoide atípico (TTRA).
- Tumor neuroepitelial cribiforme.
- Tumor embrionario con rosetas de capas múltiples (ETMR).
- Neuroblastoma del sistema nervioso central con activación de FOXR2.
- Tumor del sistema nervioso central con duplicación interna en tándem de BCOR.
- Tumor embrionario del sistema nervioso central, sin clasificar o sin otra indicación.
El tumor sin clasificar se define como un tumor no clasificado en otro lugar. La nomenclatura sin otra indicación se usa para los tumores que no pueden clasificarse más. En muchas lesiones, hay características histológicas superpuestas y la agrupación a base del estado de metilación es fundamental para el diagnóstico específico.[1,2] La contribución del perfil de metilación del DNA para diagnosticar de manera correcta los tumores embrionarios supratentoriales se demostró en un ensayo clínico de pacientes con tumores neuroectodérmicos primitivos supratentoriales del sistema nervioso central (TNEP-SNC) y pineoblastoma.[3] En los casos de pineoblastoma, hubo una concordancia alta entre el diagnóstico por perfil de metilación y el diagnóstico por revisión patológica central (26 de 29). Sin embargo, en los 31 pacientes restantes del estudio que no presentaban pineoblastoma, el diagnóstico mediante perfiles de metilación fue glioma de grado alto en 18 pacientes, TTRA en 2 pacientes y ependimoma positivo para una fusión de RELA en 2 pacientes. La adjudicación de las discrepancias entre el diagnóstico por revisión patológica central o perfil de metilación fue favorable para el perfil de metilación en los 10 casos que se volvieron a examinar.
Subtipos de tumores embrionarios distintos del meduloblastoma
Subtipos moleculares de tumores embrionarios distintos del meduloblastoma
En los estudios en el que se aplicaron métodos de agrupamiento sin supervisión de los patrones de metilación del DNA a tumores embrionarios distintos del meduloblastoma, se observó que cerca de la mitad de los tumores diagnosticados como tumores embrionarios distintos del meduloblastoma exhibían perfiles moleculares característicos de otros tumores de encéfalo (cerebrales) infantiles conocidos (por ejemplo, gliomas de grado alto).[4,5] Esta observación destaca la utilidad de la caracterización molecular para asignar el diagnóstico molecular apropiado para esta clase de tumores de acuerdo con las características biológicas.
Entre los tumores diagnosticados como tumores embrionarios distintos del meduloblastoma, la caracterización molecular permitió identificar subtipos distintivos por sus características genómicas y biológicas. Estos subtipos son los siguientes:
- Tumor neuroepitelial cribiforme. Este subtipo, que representa menos del 50 % de los tumores embrionarios distintos del meduloblastoma, es un tumor no rabdoide que se presenta en las proximidades de cualquiera de los ventrículos (tercer, cuarto o laterales). Se caracteriza por presentar cordones y cintas cribiformes y exhibe la pérdida de expresión nuclear de SMARCB1. La mediana de edad en el momento del diagnóstico es de 20 meses. Este tumor se presenta con más frecuencia en los hombres, con una proporción hombre-mujer de 1,5 a 1.[6]
En la caracterización genómica de 10 casos de tumores neuroepiteliales cribiformes se observaron deleciones grandes heterocigóticas de 22q en 9 de 10 casos con variantes de SMARCB1 en el otro alelo.[6] Se observaron perfiles de metilación de DNA en el tumor neuroepitelial cribiforme que son compatibles con el subtipo tirosinasa (TYR) de tumor teratoide rabdoide atípico (TRTA), un tumor que también surge en niños pequeños y exhibe pérdida de la expresión de SMARCB1. Los pacientes con tumores neuroepiteliales cribiformes tienen pronóstico relativamente favorable, en contraste con los pacientes que tienen TRTA de subtipo TYR.[6]
- Tumor embrionario con rosetas de capas múltiples (ETMR). Este subtipo, que representa hasta el 20 % de los tumores embrionarios distintos del meduloblastoma, abarca los tumores neuroepiteliales embrionarios de encéfalo que forman rosetas, que antes se clasificaban como tumores embrionarios con neurópilo abundante y rosetas verdaderas (ETANTR), ependimoblastomas o meduloepiteliomas.[4,7] Los ETMR se presentan con mayor frecuencia en niños pequeños (mediana de edad en el momento del diagnóstico, 2-3 años), pero es posible que se presenten también en niños más grandes.[5,7-11]
A nivel molecular, los ETMR se definen por el alto grado de amplificación del complejo de microRNA C19MC y por una fusión génica entre TTYH1 y C19MC.[7,12,13] Esta fusión génica pone la expresión de C19MC bajo el control del promotor de TTYH1, lo que produce un grado alto de expresión anormal de los microRNA dentro del conglomerado. La Organización Mundial de la Salud (OMS) admite que se clasifiquen como ETMR, sin otra indicación (SAI), los tumores con características histológicas semejantes, pero sin alteraciones de C19MC. Es posible que esta subclase de tumores sin alteraciones de C19MC albergue variantes bialélicas de DICER1.
- Neuroblastoma del sistema nervioso central (SNC) con activación de FOXR2 (NB-FOXR2 del SNC). Este tumor, que representa entre el 10 % y el 15 % de los tumores embrionarios distintos del meduloblastoma, tal vez se presente en niños menores de 3 años, pero es más frecuente en niños más grandes. Este subtipo se caracteriza por alteraciones genómicas que conducen a un aumento de la expresión del factor de transcripción FOXR2.[4] El NB-FOXR2 del SNC se observa sobre todo en niños menores de 10 años; las características histológicas de estos tumores suelen ser las del neuroblastoma del SNC o el ganglioneuroblastoma del SNC.[4,14] No hay una alteración genómica única en los tumores NB-FOXR2 del SNC que conduzca a la sobreexpresión de FOXR2; se han identificado fusiones génicas en las que participan múltiples genes recíprocos de FOXR2.[4] La expresión proteica de SOX10 y ANKRD55 detectada mediante inmunohistoquímica se ha propuesto como un potencial biomarcador para diferenciar los tumores NB-FOXR2 del SNC de otros tipos de tumores relacionados.[14]
- Tumor neuroepitelial de grado alto con alteración en BCOR (HGNET-BCOR del SNC). Este subtipo representa hasta el 3 % de los tumores embrionarios distintos del meduloblastoma y se caracteriza por duplicaciones internas en tándem en BCOR,[4] una alteración genómica que también se encuentra en el sarcoma de células claras de riñón.[15,16] A pesar de que la mediana de edad en el momento del diagnóstico es de menos de 10 años, se presentan casos en la segunda década de la vida y más tarde.[4]
Aunque no figuran como entidades separadas en la clasificación de tumores del SNC de la OMS de 2021, también se han descrito otros tumores embrionarios distintos del meduloblastoma como entidades separadas, entre ellos los siguientes:
- Tumor de la familia de sarcomas de Ewing del SNC con alteración de CIC (EFT-CIC del SNC). Este subtipo de tumor representa entre el 2 % y el 4 % de los tumores embrionarios distintos del meduloblastoma; se caracteriza por alteraciones genómicas que afectan CIC (localizado en el cromosoma 19q13.2); y se ha identificado una fusión con NUTM1 en varios casos evaluados.[4,5] Las fusiones del gen CIC también se identificaron en sarcomas similares al de Ewing fuera del SNC; además, la firma de expresión génica de los tumores EFT-CIC del SNC es similar al de estos sarcomas.[4] Los tumores EFT-CIC del SNC por lo general se presentan en niños menores de 10 años y se caracterizan por un fenotipo de células pequeñas, pero con características histológicas variables.[4]
- Tumor neuroepitelial de grado alto del SNC con alteración en MN1 (HGNET-MN1 del SNC). Este subtipo representa entre el 1 % y el 3 % de los tumores embrionarios distintos del meduloblastoma y se caracteriza por fusiones génicas en las que participa MN1 (localizado en el cromosoma 22q12.3) con genes recíprocos de fusión como BEND2 y CXXC5.[4,5] El subtipo HGNET-MN1 del SNC muestra un llamativo predominio en el sexo femenino y tiende a presentarse en la segunda década de vida.[4] Este subtipo representaba la mayoría de los casos diagnosticados como astroblastoma según el esquema de clasificación de la OMS de 2007.[4] Este subtipo no se ha agregado al vocabulario diagnóstico de la OMS. En otros 2 informes en los que se examinaron 35 casos de astroblastomas definidos mediante análisis histológico se observó que 14 exhibían perfiles de metilación compatibles con HGNET-MN1 del SNC o alteraciones de MN1 identificadas por hibridación fluorescente in situ.[17,18]
- Meduloepitelioma. El meduloepitelioma con la clásica amplificación de C19MC se considera un ETMR con alteración de C19MC (consultar la información anterior sobre ETMR). No obstante, cuando un tumor tiene características histológicas de meduloblastoma, pero carece de la amplificación de C19MC, se identifica como un ETMR.[19,20] Los tumores de meduloepiteliomas son poco frecuentes y tienden a presentarse con más frecuencia en lactantes y niños pequeños. Los meduloepiteliomas, que en el análisis histológico se asemejan al tubo neural embrionario, tienden a presentarse a nivel supratentorial, sobre todo dentro de los ventrículos, pero también aparecen a nivel infratentorial, en la cola de caballo e incluso en una ubicación extraneural, junto a las raíces de los nervios.[19,20] El meduloepitelioma intraocular es biológicamente diferente del meduloepitelioma intraaxial.[21,22]
- Tumor embrionario del SNC con amplificación de PLAGL. En un análisis retrospectivo de más de 90 000 tumores encefálicos en niños y adultos se identificó un pequeño subconjunto de tumores embrionarios (n = 31) con perfiles de metilación característicos, con amplificación de grado alto y sobreexpresión de PLAGL1 o PLAGL2.[23] En estos casos no se observaron las alteraciones genéticas recurrentes adicionales que se advirtieron en otros tipos de tumores pediátricos del SNC. Estos tumores se presentaron en todo el encéfalo y estaban compuestos, en la mayoría de los casos, por células primitivas de tipo embrionario sin marcadores de diferenciación glial o neuronal. En esta pequeña cohorte, se observaron diferencias en la edad en el momento del diagnóstico y en las tasas de supervivencia general (SG) a los 10 años entre los pacientes con amplificación de PLAGL1 (mediana de edad, 10,5 años; tasa de SG, 66 %), en comparación con los pacientes con amplificación de PLAGL2 (mediana de edad, 2 años; tasa de SG, 25 %).
Evaluación para la estadificación
Los pacientes con tumores embrionarios distintos del meduloblastoma se estadifican de forma similar a la utilizada para los niños con meduloblastoma. Sin embargo, los pacientes no se asignan a subgrupos de riesgo promedio y de riesgo alto para fines de tratamiento porque todos los pacientes se consideran de riesgo alto. Para obtener más información, consultar la sección Evaluación para la estadificación del meduloblastoma.
Tratamiento de los tumores embrionarios distintos del meduloblastoma infantiles
Para obtener más información sobre el tratamiento de los tumores teratoides rabdoides atípicos del sistema nervioso central, consultar Tratamiento del tumor teratoide rabdoide atípico del sistema nervioso central infantil.
Para obtener más información sobre el tratamiento del meduloepitelioma, consultar la sección Tratamiento de los tumores embrionarios con rosetas de capas múltiples o meduloepitelioma infantiles.
Tratamiento de los niños de 3 años o menos
El tratamiento óptimo de los tumores embrionarios distintos del meduloblastoma infantil sigue sin estar claro y está en estudio. En estudios retrospectivos de un número bastante grande de pacientes se han indicado abordajes de tratamiento para los subgrupos más comunes, como los TTRA, los ETMR y los tumores con activación de FOXR2. Para obtener más información sobre el tratamiento del TTRA, consultar Tratamiento del tumor teratoide rabdoide atípico del sistema nervioso central infantil.
Las opciones de tratamiento estándar para los niños de 3 años o menos con tumores embrionarios distintos del meduloblastoma recién diagnosticados (excepto TTRA, ETMR y tumores con activación de FOXR2 ) son las siguientes:
- Cirugía.
- Quimioterapia adyuvante.
El tratamiento de los niños de 3 años o menos con tumores embrionarios es similar al indicado para niños de 3 años o menos con meduloblastoma. La resección quirúrgica radical es razonable, dada la mejor tasa de supervivencia de los pacientes con meduloblastomas y otros ETMR tras la resección total o casi total.[11] Para obtener más información, consultar la sección Tratamiento de los niños más pequeños con meduloblastoma.
El desenlace ha sido variable cuando se administra quimioterapia sola; las tasas de supervivencia a 5 años oscilaron entre el 0 % y el 50 %.[24-26]; [27][Nivel de evidencia B4] La adición de irradiación craneoespinal a los regímenes basados en quimioterapia es exitosa para algunos niños, pero se anticipa deterioro del desarrollo neurológico.[28][Nivel de evidencia B4] Aunque no hay datos que respalden su eficacia, también se ha administrado radioterapia localizada dirigida al sitio del tumor, antes o después de la quimioterapia.
Tratamiento de los niños mayores de 3 años
Las opciones de tratamiento estándar para los niños mayores de 3 años con tumores embrionarios distintos del meduloblastoma (excepto TTRA, ETMR y tumores con activación de FOXR2), recién diagnosticados son las siguientes:
Cirugía
Evidencia (cirugía):
- A menudo es posible extirpar los tumores embrionarios distintos del meduloblastoma; En las series de casos notificadas, entre el 50 % y el 75 % de los tumores de los pacientes se sometieron a resección total o casi total.[29,30]; [3][Nivel de evidencia A1]
- El primer paso del tratamiento de los tumores embrionarios distintos del meduloblastoma recién diagnosticados es intentar una resección quirúrgica radical. Aunque en estudios previos no se demostró que la extensión de la resección fuera predictiva del desenlace,[29-31] en un estudio se observó mejora de la supervivencia cuando el tumor se resecó por completo.[32][Nivel de evidencia B4] En un estudio publicado (COG-ACNS0332 [NCT00392327]) de tumores embrionarios distintos del meduloblastoma clasificados según sus características moleculares, se observó mejora de la supervivencia general (SG) en los pacientes que tenían menos de 1,5 cm2 de enfermedad residual, en comparación con los pacientes que tenían más de 1,5 cm2 de enfermedad residual.[3][Nivel de evidencia A1]
Radioterapia adyuvante
Después de la cirugía, los niños con tumores embrionarios distintos del meduloblastoma suelen recibir un tratamiento similar al de los niños con meduloblastoma de riesgo alto.
Convencionalmente, los pacientes se tratan con radiación dirigida a todo el eje encefalomedular, con refuerzo de radioterapia local, como se administra para el meduloblastoma.[31] El refuerzo de radioterapia local puede ser problemático debido al tamaño del tumor y su ubicación en la corteza cerebral. Además, no hay evidencia definitiva de que la radioterapia craneoespinal sea superior a la radiación dirigida al sitio del tumor primario sola en niños con lesiones no diseminadas.[29-31]
Quimioterapia adyuvante
Los abordajes quimioterapéuticos durante la radioterapia y después de esta son similares a los utilizados para los niños con meduloblastoma de riesgo alto. Las tasas de SG a 3 y 5 años oscilan entre el 25 % y el 50 %.[29-31]; [32,33][Nivel de evidencia B4]; [34][Nivel de evidencia C1]
En un estudio publicado de pacientes con tumores fuera de la glándula pineal diagnosticados como tumores neuroectodérmicos primitivos (TNEP) del SNC mediante estudio patológico tradicional, se descubrió que el 71 % de los casos eran glioblastomas u otro tipo de diagnóstico mediante estudios de metilación del DNA. Los pacientes con tumores embrionarios distintos del meduloblastoma (n = 36) (incluso pineoblastomas, n = 26) tuvieron una SG a 5 años del 78,5 % (intervalo de confianza [IC] 95 %, 62,2–94,8 %). Por el contrario, los pacientes con glioblastoma tuvieron una tasa de SG a 5 años del 12 % (IC 95 %, 0–24,7 %). En el estudio no se observó ningún beneficio para los niños que recibieron carboplatino o isotretinoína.[3][Nivel de evidencia A1] En este estudio se destaca la importancia de la clasificación molecular de los tumores tradicionalmente denominados como TNEP-SNC.[4]
Tratamiento de los tumores embrionarios con rosetas de capas múltiples o meduloepitelioma infantiles
En una revisión basada en un registro, se notificaron los resultados de supervivencia de 159 pacientes con diagnóstico molecular confirmado de ETMR que recibieron diferentes tratamientos.[11]
- Las tasas de supervivencia sin complicaciones (SSC) y de SG a 2 años fueron ambas del 0 % para los pacientes tratados con quimioterapia convencional sin radioterapia, con independencia del grado de resección quirúrgica.
- La tasa de SSC a 2 años fue del 21 % y la tasa de SG fue del 30 % para los pacientes que se sometieron a una resección macroscópica total y fueron tratados con quimioterapia de dosis alta sin radioterapia.
- La tasa de SSC a 2 años fue del 44 % para los niños tratados con quimioterapia de dosis alta y radioterapia tras una resección subtotal y del 66 % para los pacientes que recibieron tratamiento con quimioterapia de dosis alta y radioterapia tras una resección macroscópica total.
- Las funciones relativas de la radioterapia focal versus la radioterapia craneoespinal no pudieron evaluarse en esta revisión.
En una revisión retrospectiva internacional separada, pero posiblemente solapada, 49 pacientes con ETMR confirmados mediante análisis histológico (por la institución tratante) fueron tratados entre 1988 y 2017 de diversas maneras.[35] La tasa de supervivencia sin progresión a 5 años fue del 18 % (± 6 %) y la tasa de SG fue del 24 % (± 6 %). La mayoría de los sobrevivientes recibieron radioterapia, incluso tratamiento local y craneoespinal, y no hubo ninguna diferencia clara en los desenlaces entre los tipos y el alcance de la radioterapia. No se pudieron evaluar los beneficios relativos de la quimioterapia convencional en comparación con la quimioterapia de dosis altas.[5]
En una publicación posterior, en la que probablemente se incluyeron algunos de los pacientes del estudio retrospectivo, el tratamiento se limitó solo a los pacientes que recibieron quimioterapia y radioterapia en un estudio prospectivo P-HIT o según el protocolo del estudio. En el estudio P-HIT el tratamiento incluyó quimioterapia postoperatoria, quimioterapia con dosis altas y radioterapia para algunos pacientes. Entre 35 pacientes con ETMR, se identificaron 8 supervivientes a largo plazo, 6 de los cuales habían recibido radioterapia craneoespinal o local, además de quimioterapia de inducción y de dosis altas. Ninguno de los pacientes que tenía enfermedad en el tronco encefálico sobrevivió. La supervivencia a 5 años fue mejor para los pacientes con enfermedad localizada, posiblemente para aquellos tratados tanto con quimioterapia de inducción como con quimioterapia de dosis altas. No se pudo determinar la función de la radioterapia o el volumen óptimo de la radioterapia (local versus craneoespinal).[10]
En estos estudios se indica que el pronóstico de los niños con ETMR tal vez no sea tan nefasto como se observó en los estudios iniciales, en los que la tasa de supervivencia a 5 años fue del 25 % o inferior. El desenlace es más favorable en los niños con enfermedad localizada en el momento del diagnóstico y en los que recibieron tratamiento con quimioterapia posquirúrgica intensiva, incluso de inducción y de consolidación con dosis altas. La función de la radioterapia todavía no se ha demostrado, y no hay evidencia de que la radiación craneoespinal en pacientes con enfermedad localizada sea superior a la radioterapia focal.[5,10,11]
Tratamiento del neuroblastoma del sistema nervioso central con activación de FOXR2
El tratamiento óptimo de los pacientes con neuroblastoma del SNC con activación de FOXR2 no ha sido confirmado en estudios prospectivos. En una revisión retrospectiva de pacientes diagnosticados entre 1988 y 2007, las tasas más altas de supervivencia se observaron tras resecciones completas o casi completas en pacientes con tumores no metastásicos que también recibieron radioterapia craneoespinal y, tal vez, quimioterapia. Con este tipo de abordaje, hasta el 75 % de los niños (35 de 42) estaban vivos 5 años después del diagnóstico y el tratamiento. Este tumor tiende a presentarse en pacientes de mayor edad que algunos de los otros tumores embrionarios distintos del meduloblastoma.[5]
Bibliografía
- Louis DN, Perry A, Wesseling P, et al.: The 2021 WHO Classification of Tumors of the Central Nervous System: a summary. Neuro Oncol 23 (8): 1231-1251, 2021. [PUBMED Abstract]
- WHO Classification of Tumours Editorial Board, ed.: WHO Classification of Tumours: Central Nervous System Tumours. Vol. 6. 5th ed. IARC Press; 2021.
- Hwang EI, Kool M, Burger PC, et al.: Extensive Molecular and Clinical Heterogeneity in Patients With Histologically Diagnosed CNS-PNET Treated as a Single Entity: A Report From the Children's Oncology Group Randomized ACNS0332 Trial. J Clin Oncol : JCO2017764720, 2018. [PUBMED Abstract]
- Sturm D, Orr BA, Toprak UH, et al.: New Brain Tumor Entities Emerge from Molecular Classification of CNS-PNETs. Cell 164 (5): 1060-72, 2016. [PUBMED Abstract]
- von Hoff K, Haberler C, Schmitt-Hoffner F, et al.: Therapeutic implications of improved molecular diagnostics for rare CNS embryonal tumor entities: results of an international, retrospective study. Neuro Oncol 23 (9): 1597-1611, 2021. [PUBMED Abstract]
- Johann PD, Hovestadt V, Thomas C, et al.: Cribriform neuroepithelial tumor: molecular characterization of a SMARCB1-deficient non-rhabdoid tumor with favorable long-term outcome. Brain Pathol 27 (4): 411-418, 2017. [PUBMED Abstract]
- Korshunov A, Sturm D, Ryzhova M, et al.: Embryonal tumor with abundant neuropil and true rosettes (ETANTR), ependymoblastoma, and medulloepithelioma share molecular similarity and comprise a single clinicopathological entity. Acta Neuropathol 128 (2): 279-89, 2014. [PUBMED Abstract]
- Picard D, Miller S, Hawkins CE, et al.: Markers of survival and metastatic potential in childhood CNS primitive neuro-ectodermal brain tumours: an integrative genomic analysis. Lancet Oncol 13 (8): 838-48, 2012. [PUBMED Abstract]
- Spence T, Sin-Chan P, Picard D, et al.: CNS-PNETs with C19MC amplification and/or LIN28 expression comprise a distinct histogenetic diagnostic and therapeutic entity. Acta Neuropathol 128 (2): 291-303, 2014. [PUBMED Abstract]
- Juhnke BO, Gessi M, Gerber NU, et al.: Treatment of embryonal tumors with multilayered rosettes with carboplatin/etoposide induction and high-dose chemotherapy within the prospective P-HIT trial. Neuro Oncol 24 (1): 127-137, 2022. [PUBMED Abstract]
- Khan S, Solano-Paez P, Suwal T, et al.: Clinical phenotypes and prognostic features of embryonal tumours with multi-layered rosettes: a Rare Brain Tumor Registry study. Lancet Child Adolesc Health 5 (11): 800-813, 2021. [PUBMED Abstract]
- Kleinman CL, Gerges N, Papillon-Cavanagh S, et al.: Fusion of TTYH1 with the C19MC microRNA cluster drives expression of a brain-specific DNMT3B isoform in the embryonal brain tumor ETMR. Nat Genet 46 (1): 39-44, 2014. [PUBMED Abstract]
- Li M, Lee KF, Lu Y, et al.: Frequent amplification of a chr19q13.41 microRNA polycistron in aggressive primitive neuroectodermal brain tumors. Cancer Cell 16 (6): 533-46, 2009. [PUBMED Abstract]
- Korshunov A, Okonechnikov K, Schmitt-Hoffner F, et al.: Molecular analysis of pediatric CNS-PNET revealed nosologic heterogeneity and potent diagnostic markers for CNS neuroblastoma with FOXR2-activation. Acta Neuropathol Commun 9 (1): 20, 2021. [PUBMED Abstract]
- Ueno-Yokohata H, Okita H, Nakasato K, et al.: Consistent in-frame internal tandem duplications of BCOR characterize clear cell sarcoma of the kidney. Nat Genet 47 (8): 861-3, 2015. [PUBMED Abstract]
- Roy A, Kumar V, Zorman B, et al.: Recurrent internal tandem duplications of BCOR in clear cell sarcoma of the kidney. Nat Commun 6: 8891, 2015. [PUBMED Abstract]
- Wood MD, Tihan T, Perry A, et al.: Multimodal molecular analysis of astroblastoma enables reclassification of most cases into more specific molecular entities. Brain Pathol 28 (2): 192-202, 2018. [PUBMED Abstract]
- Lehman NL, Usubalieva A, Lin T, et al.: Genomic analysis demonstrates that histologically-defined astroblastomas are molecularly heterogeneous and that tumors with MN1 rearrangement exhibit the most favorable prognosis. Acta Neuropathol Commun 7 (1): 42, 2019. [PUBMED Abstract]
- Louis DN, Ohgaki H, Wiestler OD, et al.: The 2007 WHO classification of tumours of the central nervous system. Acta Neuropathol 114 (2): 97-109, 2007. [PUBMED Abstract]
- Sharma MC, Mahapatra AK, Gaikwad S, et al.: Pigmented medulloepithelioma: report of a case and review of the literature. Childs Nerv Syst 14 (1-2): 74-8, 1998 Jan-Feb. [PUBMED Abstract]
- Jakobiec FA, Kool M, Stagner AM, et al.: Intraocular Medulloepitheliomas and Embryonal Tumors With Multilayered Rosettes of the Brain: Comparative Roles of LIN28A and C19MC. Am J Ophthalmol 159 (6): 1065-1074.e1, 2015. [PUBMED Abstract]
- Korshunov A, Jakobiec FA, Eberhart CG, et al.: Comparative integrated molecular analysis of intraocular medulloepitheliomas and central nervous system embryonal tumors with multilayered rosettes confirms that they are distinct nosologic entities. Neuropathology 35 (6): 538-44, 2015. [PUBMED Abstract]
- Keck MK, Sill M, Wittmann A, et al.: Amplification of the PLAG-family genes-PLAGL1 and PLAGL2-is a key feature of the novel tumor type CNS embryonal tumor with PLAGL amplification. Acta Neuropathol 145 (1): 49-69, 2023. [PUBMED Abstract]
- Geyer JR, Sposto R, Jennings M, et al.: Multiagent chemotherapy and deferred radiotherapy in infants with malignant brain tumors: a report from the Children's Cancer Group. J Clin Oncol 23 (30): 7621-31, 2005. [PUBMED Abstract]
- Marec-Berard P, Jouvet A, Thiesse P, et al.: Supratentorial embryonal tumors in children under 5 years of age: an SFOP study of treatment with postoperative chemotherapy alone. Med Pediatr Oncol 38 (2): 83-90, 2002. [PUBMED Abstract]
- Grill J, Sainte-Rose C, Jouvet A, et al.: Treatment of medulloblastoma with postoperative chemotherapy alone: an SFOP prospective trial in young children. Lancet Oncol 6 (8): 573-80, 2005. [PUBMED Abstract]
- Fangusaro J, Finlay J, Sposto R, et al.: Intensive chemotherapy followed by consolidative myeloablative chemotherapy with autologous hematopoietic cell rescue (AuHCR) in young children with newly diagnosed supratentorial primitive neuroectodermal tumors (sPNETs): report of the Head Start I and II experience. Pediatr Blood Cancer 50 (2): 312-8, 2008. [PUBMED Abstract]
- Friedrich C, von Bueren AO, von Hoff K, et al.: Treatment of young children with CNS-primitive neuroectodermal tumors/pineoblastomas in the prospective multicenter trial HIT 2000 using different chemotherapy regimens and radiotherapy. Neuro Oncol 15 (2): 224-34, 2013. [PUBMED Abstract]
- Cohen BH, Zeltzer PM, Boyett JM, et al.: Prognostic factors and treatment results for supratentorial primitive neuroectodermal tumors in children using radiation and chemotherapy: a Childrens Cancer Group randomized trial. J Clin Oncol 13 (7): 1687-96, 1995. [PUBMED Abstract]
- Reddy AT, Janss AJ, Phillips PC, et al.: Outcome for children with supratentorial primitive neuroectodermal tumors treated with surgery, radiation, and chemotherapy. Cancer 88 (9): 2189-93, 2000. [PUBMED Abstract]
- Timmermann B, Kortmann RD, Kühl J, et al.: Role of radiotherapy in the treatment of supratentorial primitive neuroectodermal tumors in childhood: results of the prospective German brain tumor trials HIT 88/89 and 91. J Clin Oncol 20 (3): 842-9, 2002. [PUBMED Abstract]
- Jakacki RI, Burger PC, Kocak M, et al.: Outcome and prognostic factors for children with supratentorial primitive neuroectodermal tumors treated with carboplatin during radiotherapy: a report from the Children's Oncology Group. Pediatr Blood Cancer 62 (5): 776-83, 2015. [PUBMED Abstract]
- Chintagumpala M, Hassall T, Palmer S, et al.: A pilot study of risk-adapted radiotherapy and chemotherapy in patients with supratentorial PNET. Neuro Oncol 11 (1): 33-40, 2009. [PUBMED Abstract]
- Johnston DL, Keene DL, Lafay-Cousin L, et al.: Supratentorial primitive neuroectodermal tumors: a Canadian pediatric brain tumor consortium report. J Neurooncol 86 (1): 101-8, 2008. [PUBMED Abstract]
- Liu APY, Dhanda SK, Lin T, et al.: Molecular classification and outcome of children with rare CNS embryonal tumors: results from St. Jude Children's Research Hospital including the multi-center SJYC07 and SJMB03 clinical trials. Acta Neuropathol 144 (4): 733-746, 2022. [PUBMED Abstract]
Pineoblastoma infantil
La Organización Mundial de la Salud clasifica los pineoblastomas dentro del grupo de tumores de la región pineal. Sin embargo, se analizan en este resumen porque comparten características histológicas con otros tumores embrionarios y, de manera convencional, se tratan igual que otros tumores embrionarios.[1-3]
Cuadro clínico inicial
Los pineoblastomas a menudo producen hidrocefalia debido a la obstrucción de la circulación del líquido cefalorraquídeo a la altura del tercer ventrículo, y también causan otros síntomas relacionados con la presión en la parte posterior del tronco encefálico en la región tectal. Es posible que los síntomas incluyan muchas alteraciones de los movimientos oculares (síndrome de Parinaud) que se manifiestan con pupilas que reaccionan mal a la luz, pero reaccionan mejor a la acomodación; pérdida de la mirada hacia arriba; nistagmo de retracción o convergencia; y retracción palpebral. A medida que crecen, estos tumores también pueden llegar a causar hemiparesia y ataxia.[4]
Clasificación celular y molecular
El pineoblastoma tiene características histológicas similares al meduloblastoma y comparte características histológicas con los tumores embrionarios. El pineoblastoma se clasifica como un subgrupo dentro de los tumores de parénquima pineal.[5,6]
El pineoblastoma se subdivide en 4 subtipos diferentes con características clínicas y moleculares únicas:[7]
- Los subtipos con alteración del procesamiento de microRNA (miRNA) 1 (PB-miRNA1) y 2 (PB-miRNA2) se caracterizan por presentar variantes somáticas o germinales que afectan los genes que participan en la biogénesis del microRNA (DICER1, DROSHA, y DGCR8). Los subtipos se distinguen entre sí por sus perfiles de metilación del DNA.
- El subtipo PB-MYC/FOXR2 muestra activación de MYC y sobreexpresión de FOXR2.
- El subtipo PB-RB1 presenta alteraciones en RB1 y una minoría de los casos tienen un diagnóstico clínico de retinoblastoma trilateral.
A continuación, se proporciona más información sobre cada uno de los subtipos.
Características genómicas del pineoblastoma
El pineoblastoma, que convencionalmente se agrupaba con los tumores embrionarios, ahora se clasifica como un tumor de parénquima pineal según la Organización Mundial de la Salud (OMS). Debido a que las opciones de tratamiento para el pineoblastoma son muy similares al tratamiento de otros tumores embrionarios, en este documento se usa la convención anterior de incluir el pineoblastoma con los tumores embrionarios del sistema nervioso central. El pineoblastoma se ha vinculado con variantes patogénicas germinales, tanto en el gen RB1 como en el gen DICER1, como se describe a continuación:
- Se estableció una relación del pineoblastoma con variantes patogénicas germinales de RB1. El término retinoblastoma trilateral se usa para referirse al retinoblastoma ocular que se presenta de manera simultánea con un tumor encefálico histológicamente similar, que suele aparecer en la glándula pineal o en otras estructuras de la línea media. Históricamente, se han notificado tumores intracraneales en el 5 % al 15 % de los niños con retinoblastoma hereditario.[8] Es posible que las tasas de pineoblastoma en niños con retinoblastoma hereditario que se someten a los programas de tratamiento vigentes en la actualidad sean más bajas que estas estimaciones históricas.[9-11] En un estudio de pacientes con tumores de parénquima pineal clasificados a partir de sus características moleculares, se observó que 6 de 221 casos (3 %) tenían un diagnóstico clínico de retinoblastoma trilateral.[7]
- Se observan variantes patogénicas germinales de DICER1 en algunos pacientes con pineoblastoma.[12] En un estudio de 18 pacientes con pineoblastoma se identificaron 3 pacientes con variantes patogénicas germinales de DICER1 y otros 3 pacientes, que se sabía que eran portadores de variantes patogénicas germinales de DICER1, presentaron pineoblastoma.[12] Las variantes de DICER1 en pacientes con pineoblastoma son variantes de pérdida de función que se diferencian de las variantes observadas en los tumores relacionados con el síndrome DICER1, como el blastoma pleuropulmonar.[12]
Se han aplicado métodos genómicos para estudiar el pineoblastoma con el fin de obtener más información sobre las características biológicas del tumor y guiar la clasificación molecular en el futuro. En un metanálisis internacional retrospectivo, se incluyeron 221 niños y adultos con pineoblastoma (n = 178) y tumores de parénquima pineal de diferenciación intermedia (n = 43).[7] En la evaluación se identificaron 4 grupos moleculares de pineoblastoma según la metilación del DNA, el perfil del transcriptoma y la secuenciación génica, como se describe a continuación.
- Los subtipos con alteración del procesamiento de microRNA (miRNA) 1 (PB-miRNA1) y 2 (PB-miRNA2) se caracterizan por variantes somáticas o germinales que afectan genes que participan en la biogénesis del miRNA (DICER1, DROSHA y DGCR8).
- El subtipo PB-miRNA1 representó cerca del 50 % de los casos de pineoblastoma clasificados por sus características moleculares, mientras que el subtipo PB-miRNA2 representó cerca del 15 % de los casos.
- La mediana de edad en el momento de la presentación del subtipo PB-miRNA1 fue de alrededor de 8 años y la mediana de edad en el momento de la presentación del subtipo PB-miRNA2 fue de alrededor de 12 años.
- La tasa de supervivencia a 5 años de los pacientes con el subtipo PB-miRNA2 (100 %) superó la de los pacientes con el subtipo PB-miRNA1 (70 %).
- El subtipo PB-MYC/FOXR2 muestra activación del gen MYC (a veces con ganancia del número de copias de MYC y, en ocasiones, con amplificación de MYC) y sobreexpresión de FOXR2.
- El subtipo PB-MYC/FOXR2 representa cerca del 20 % de los casos de pineoblastoma clasificados por sus características moleculares.
- Los casos de PB-MYC/FOXR2 ocurrieron a una edad temprana (mediana, 1,4 años).
- Alrededor del 40 % de los pacientes con PB-MYC/FOXR2 tenían enfermedad metastásica.
- La tasa de supervivencia a 5 años en los pacientes con PB-MYC/FOXR2 fue de alrededor del 20 %.
- El subtipo PB-RB1 tiene alteraciones en el gen RB1. En un estudio, 6 de 25 pacientes con el subtipo PB-RB1 tenían un diagnóstico clínico de retinoblastoma trilateral.
- El subtipo PB-RB1 representó cerca del 10 % de los casos de pineoblastoma clasificados por sus características moleculares.
- Cerca del 70 % de los casos de PB-RB1 tenían enfermedad metastásica.
- La tasa de supervivencia a 5 años en los pacientes con el subtipo PB-RB1 fue de alrededor del 30 %.
- En ocasiones, los casos con perfiles de metilación del DNA que indicaban un tumor de parénquima pineal de diferenciación intermedia tenían un diagnóstico histológico de pineoblastoma, pero las características clínicas y biológicas de estos casos eran distintas de las de los subtipos de pineoblastoma descritos antes.
- Cerca del 75 % de los casos con una clasificación molecular de tumor de parénquima pineal de diferenciación intermedia presentaron tumores con variantes de KBTBD4, un gen que también se altera en los meduloblastomas de los grupos 3 y 4.
- La mayoría de los casos de tumores de parénquima pineal de diferenciación intermedia se presentaron en adultos, con una mediana de edad superior a 30 años.
- La tasa de supervivencia a 5 años en los pacientes con tumores de parénquima pineal de diferenciación intermedia fue del 85 %.
Evaluación para la estadificación
El 10 % al 30 % de los pacientes con pineoblastoma tiene diseminación en el momento del diagnóstico.[13] Debido a la ubicación del tumor, las resecciones totales son infrecuentes y la mayoría de los pacientes solo se someten a una biopsia o una resección subtotal antes del tratamiento posquirúrgico.[13,14] La estadificación para los niños con pineoblastomas es la misma que para los niños con meduloblastoma. Sin embargo, los pacientes no se asignan a los subgrupos de riesgo promedio y riesgo alto para fines de tratamiento[13] Para obtener más información, consultar la sección Evaluación para la estadificación.
Aspectos generales de las opciones de tratamiento del pineoblastoma infantil
En el Cuadro 4 se describen las opciones de tratamiento para el pineoblastoma infantil recién diagnosticado o recidivante
| Grupo de tratamiento | Opciones de tratamiento | |
|---|---|---|
| Pineoblastoma infantil recién diagnosticado | Niños de 3 años o menos | Biopsia (para el diagnóstico) o resección total, si es posible |
| Quimioterapia adyuvante | ||
| Dosis altas de quimioterapia mielosupresora con rescate autógeno de médula ósea o rescate de células madre periféricas | ||
| Niños mayores de 3 años | Cirugía | |
| Radioterapia adyuvante | ||
| Quimioterapia adyuvante | ||
| Pineoblastoma infantil recidivante | No hay opciones de tratamiento estándar. Para obtener más información, consultar la sección Tratamiento del meduloblastoma y otros tumores embrionarios del sistema nervioso central infantil recidivantes. | |
Tratamiento del pineoblastoma infantil
Tratamiento de los niños de 3 años o menos
En la actualidad, no hay opciones de tratamiento estándar para los niños de 3 años o menos con pineoblastoma.[15] Se dispone de los siguientes abordajes de tratamiento:
Biopsia
Por lo general, se realiza una biopsia y, si es posible, una resección total para diagnosticar el pineoblastoma.
Quimioterapia adyuvante
Los niños de 3 años o menos con pineoblastoma se suelen tratar al inicio con quimioterapia con el objetivo de retrasar, o evitar, la necesidad de radioterapia.[16] El pronóstico para este grupo continúa siendo muy precario.[17-19] En 2 ensayos clínicos prospectivos multicéntricos secuenciales murieron los 5 niños menores de 3 años tratados con quimioterapia.[20][Nivel de evidencia B4] En los niños que responden a la quimioterapia, no está claro el momento ni la cantidad de radioterapia necesaria después de la quimioterapia. Es posible que la adición de irradiación craneoespinal a los regímenes basados en quimioterapia sea exitosa para algunos niños, pero con deterioro del desarrollo neurológico.[21][Nivel de evidencia B4] En 2 grandes análisis agrupados se observó una supervivencia precaria en niños menores de 3 o 4 años con pineoblastoma.[18,19]
Dosis altas de quimioterapia mielosupresora con rescate autógeno de médula ósea o rescate de células madre periféricas
La quimioterapia ablativa de la médula ósea de dosis altas con rescate autógeno de médula ósea o rescate de células madre periféricas se ha utilizado con cierto éxito en niños pequeños.[22][Nivel de evidencia B4] En dos análisis agrupados también se reveló que esta modalidad quizás tenga cierta eficacia.[18,19]
Tratamiento de los niños mayores de 3 años
Las opciones de tratamiento estándar para los niños mayores de 3 años con pineoblastoma recién diagnosticado son las siguientes:
Cirugía
Por lo general, la cirugía es el tratamiento inicial de los pacientes con pineoblastoma y sirve para diagnosticar el tipo de tumor.[23] Las resecciones totales se relacionaron con mejores desenlaces.
Radioterapia adyuvante
El tratamiento posquirúrgico habitual para los pacientes con pineoblastomas empieza con radioterapia, aunque en algunos ensayos se ha utilizado quimioterapia antes de la radiación. La dosis total de radioterapia dirigida al sitio del tumor es de 54 Gy a 55,8 Gy con fraccionamiento convencional.[13,14]
También se recomienda la irradiación craneoespinal con dosis de 23,4 Gy a 36 Gy debido a la propensión de este tumor a diseminarse por todo el espacio subaracnoideo.[13,14,17]
Quimioterapia adyuvante
La quimioterapia, por lo general, se utiliza de la misma manera que se describió para los meduloblastomas de riesgo alto en niños con enfermedad no diseminada en el momento del diagnóstico.[15] Para obtener más información, consultar la sección Tratamiento de los niños mayores de 3 años con meduloblastoma de riesgo alto.
La tasa de supervivencia sin enfermedad a 5 años supera el 50 % en los niños con enfermedad localizada en el momento del diagnóstico que se someten a resección radical.[13,14,24,25][Nivel de evidencia A1] En el estudio del Children's Oncology Group (COG) COG-ACNS0332 (NCT00392327) de 36 pacientes con tumores embrionarios distintos del meduloblastoma (que incluyeron 26 pineoblastomas), se notificó una tasa de supervivencia general (SG) a 5 años del 78,5 % (intervalo de confianza 95 %, 62,2–94,8 %).[25][Nivel de evidencia A1]
En los pacientes con enfermedad diseminada en el momento del diagnóstico, la supervivencia es considerablemente más precaria.[13,14] En el estudio COG-ACNS0332 (NCT00392327) no hubo diferencia significativa en la supervivencia sin complicaciones ni en la SG según el estado metastásico.
Opciones de tratamiento en evaluación clínica para el pineoblastoma infantil
Está en evaluación una variedad de métodos de tratamiento para los pacientes de pineoblastoma, como el uso de dosis más altas de quimioterapia después de la radioterapia con apoyo de rescate de células madre periféricas, así como la administración de quimioterapia durante la radioterapia.
Tal vez haya ensayos clínicos terapéuticos de fase inicial disponibles para pacientes seleccionados. Es posible que estos ensayos estén disponibles a través del COG, el Pediatric Brain Tumor Consortium u otras entidades. La información en inglés sobre los ensayos clínicos patrocinados por el Instituto Nacional del Cáncer (NCI) se encuentra en el portal de Internet del NCI. Para obtener información en inglés sobre ensayos clínicos patrocinados por otras organizaciones, consultar el portal de Internet ClinicalTrials.gov.
Bibliografía
- Louis DN, Perry A, Reifenberger G, et al.: The 2016 World Health Organization Classification of Tumors of the Central Nervous System: a summary. Acta Neuropathol 131 (6): 803-20, 2016. [PUBMED Abstract]
- Louis DN, Perry A, Wesseling P, et al.: The 2021 WHO Classification of Tumors of the Central Nervous System: a summary. Neuro Oncol 23 (8): 1231-1251, 2021. [PUBMED Abstract]
- WHO Classification of Tumours Editorial Board, ed.: WHO Classification of Tumours: Central Nervous System Tumours. Vol. 6. 5th ed. IARC Press; 2021.
- Chintagumpala MM, Paulino A, Panigrahy A, et al.: Embryonal and pineal region tumors. In: Pizzo PA, Poplack DG, eds.: Principles and Practice of Pediatric Oncology. 7th ed. Lippincott Williams and Wilkins, 2015, pp 671-99.
- Li BK, Vasiljevic A, Dufour C, et al.: Pineoblastoma segregates into molecular sub-groups with distinct clinico-pathologic features: a Rare Brain Tumor Consortium registry study. Acta Neuropathol 139 (2): 223-241, 2020. [PUBMED Abstract]
- Pfaff E, Aichmüller C, Sill M, et al.: Molecular subgrouping of primary pineal parenchymal tumors reveals distinct subtypes correlated with clinical parameters and genetic alterations. Acta Neuropathol 139 (2): 243-257, 2020. [PUBMED Abstract]
- Liu APY, Li BK, Pfaff E, et al.: Clinical and molecular heterogeneity of pineal parenchymal tumors: a consensus study. Acta Neuropathol 141 (5): 771-785, 2021. [PUBMED Abstract]
- de Jong MC, Kors WA, de Graaf P, et al.: Trilateral retinoblastoma: a systematic review and meta-analysis. Lancet Oncol 15 (10): 1157-67, 2014. [PUBMED Abstract]
- Ramasubramanian A, Kytasty C, Meadows AT, et al.: Incidence of pineal gland cyst and pineoblastoma in children with retinoblastoma during the chemoreduction era. Am J Ophthalmol 156 (4): 825-9, 2013. [PUBMED Abstract]
- Abramson DH, Dunkel IJ, Marr BP, et al.: Incidence of pineal gland cyst and pineoblastoma in children with retinoblastoma during the chemoreduction era. Am J Ophthalmol 156 (6): 1319-20, 2013. [PUBMED Abstract]
- Turaka K, Shields CL, Meadows AT, et al.: Second malignant neoplasms following chemoreduction with carboplatin, etoposide, and vincristine in 245 patients with intraocular retinoblastoma. Pediatr Blood Cancer 59 (1): 121-5, 2012. [PUBMED Abstract]
- de Kock L, Sabbaghian N, Druker H, et al.: Germ-line and somatic DICER1 mutations in pineoblastoma. Acta Neuropathol 128 (4): 583-95, 2014. [PUBMED Abstract]
- Jakacki RI, Zeltzer PM, Boyett JM, et al.: Survival and prognostic factors following radiation and/or chemotherapy for primitive neuroectodermal tumors of the pineal region in infants and children: a report of the Childrens Cancer Group. J Clin Oncol 13 (6): 1377-83, 1995. [PUBMED Abstract]
- Timmermann B, Kortmann RD, Kühl J, et al.: Role of radiotherapy in the treatment of supratentorial primitive neuroectodermal tumors in childhood: results of the prospective German brain tumor trials HIT 88/89 and 91. J Clin Oncol 20 (3): 842-9, 2002. [PUBMED Abstract]
- Liu APY, Li BK, Vasiljevic A, et al.: SNO-EANO-EURACAN consensus on management of pineal parenchymal tumors. Neuro Oncol 26 (12): 2159-2173, 2024. [PUBMED Abstract]
- Mason WP, Grovas A, Halpern S, et al.: Intensive chemotherapy and bone marrow rescue for young children with newly diagnosed malignant brain tumors. J Clin Oncol 16 (1): 210-21, 1998. [PUBMED Abstract]
- Liu APY, Gudenas B, Lin T, et al.: Risk-adapted therapy and biological heterogeneity in pineoblastoma: integrated clinico-pathological analysis from the prospective, multi-center SJMB03 and SJYC07 trials. Acta Neuropathol 139 (2): 259-271, 2020. [PUBMED Abstract]
- Hansford JR, Huang J, Endersby R, et al.: Pediatric pineoblastoma: A pooled outcome study of North American and Australian therapeutic data. Neurooncol Adv 4 (1): vdac056, 2022. [PUBMED Abstract]
- Mynarek M, Pizer B, Dufour C, et al.: Evaluation of age-dependent treatment strategies for children and young adults with pineoblastoma: analysis of pooled European Society for Paediatric Oncology (SIOP-E) and US Head Start data. Neuro Oncol 19 (4): 576-585, 2017. [PUBMED Abstract]
- Hinkes BG, von Hoff K, Deinlein F, et al.: Childhood pineoblastoma: experiences from the prospective multicenter trials HIT-SKK87, HIT-SKK92 and HIT91. J Neurooncol 81 (2): 217-23, 2007. [PUBMED Abstract]
- Friedrich C, von Bueren AO, von Hoff K, et al.: Treatment of young children with CNS-primitive neuroectodermal tumors/pineoblastomas in the prospective multicenter trial HIT 2000 using different chemotherapy regimens and radiotherapy. Neuro Oncol 15 (2): 224-34, 2013. [PUBMED Abstract]
- Fangusaro J, Finlay J, Sposto R, et al.: Intensive chemotherapy followed by consolidative myeloablative chemotherapy with autologous hematopoietic cell rescue (AuHCR) in young children with newly diagnosed supratentorial primitive neuroectodermal tumors (sPNETs): report of the Head Start I and II experience. Pediatr Blood Cancer 50 (2): 312-8, 2008. [PUBMED Abstract]
- Jakacki RI, Burger PC, Kocak M, et al.: Outcome and prognostic factors for children with supratentorial primitive neuroectodermal tumors treated with carboplatin during radiotherapy: a report from the Children's Oncology Group. Pediatr Blood Cancer 62 (5): 776-83, 2015. [PUBMED Abstract]
- Gururangan S, McLaughlin C, Quinn J, et al.: High-dose chemotherapy with autologous stem-cell rescue in children and adults with newly diagnosed pineoblastomas. J Clin Oncol 21 (11): 2187-91, 2003. [PUBMED Abstract]
- Hwang EI, Kool M, Burger PC, et al.: Extensive Molecular and Clinical Heterogeneity in Patients With Histologically Diagnosed CNS-PNET Treated as a Single Entity: A Report From the Children's Oncology Group Randomized ACNS0332 Trial. J Clin Oncol : JCO2017764720, 2018. [PUBMED Abstract]
Tratamiento del meduloblastoma y otros tumores embrionarios del sistema nervioso central infantil recidivantes
No es raro observar la recidiva de todas las formas de tumores embrionarios del sistema nervioso central (SNC) que se suele presentar en el transcurso de los primeros 36 meses posteriores al tratamiento. No obstante, también se pueden presentar tumores recidivantes muchos años después del tratamiento inicial.[1-3] En estas recaídas tardías, en especial las que se presentan 5 o más años después del diagnóstico, puede ser difícil la diferenciación de los tumores secundarios, como los gliomas de grado alto. Se recomienda, y por lo general se requiere, la confirmación histológica. En un informe de 2021, se estudio una cohorte molecular emparejada compuesta por 127 pacientes con muestras de tejidos disponibles de un meduloblastoma primario y de tumores subsiguientes relacionados con una recaída. Se usaron las muestras de tumor emparejadas de cada paciente para los análisis moleculares comparativos. Se identificaron 9 casos de recaídas (7 %), con características histológicas diferentes a las del meduloblastoma, mediante la clasificación a partir de la metilación del DNA.[4] La enfermedad puede recidivar en el sitio primario o estar diseminada en el momento de la recaída. Los sitios de recaída no adyacente a veces incluyen las leptomenínges medulares, sitios intracraneales y líquido cefalorraquídeo, ya sea como presentación aislada o en cualquier combinación, y es posible que estas lesiones se presenten al mismo tiempo que una recaída del tumor primario.[1,2,5] La recaída extraneural de la enfermedad es infrecuente y se observa principalmente en pacientes tratados con radioterapia sola.[6][Nivel de evidencia C1]
En los estudios se ha observado que incluso en pacientes con enfermedad no diseminada en el momento del diagnóstico, y con independencia de la dosis de radioterapia o del tipo de quimioterapia, cerca de un tercio de los pacientes presentarán una recaída en el sitio del tumor primario solo, un tercio la presentará en el sitio del tumor primario y en sitios distantes y otro tercio la presentará en sitios distantes sin recaída en el sitio primario.[1,2,5]
Opciones de tratamiento
No hay opciones de tratamiento estándar para los tumores embrionarios del SNC infantil recidivantes. Para obtener más información, consultar la sección Tratamiento del tumor teratoide rabdoide atípico del sistema nervioso central infantil recidivante en Tratamiento del tumor teratoide rabdoide atípico del sistema nervioso central infantil.
En la mayoría de los niños, el tratamiento es paliativo y el control de la enfermedad es transitorio en los pacientes tratados previamente con radioterapia y quimioterapia; más del 80 % de los pacientes progresan en el transcurso de 2 años.[3]; [7][Nivel de evidencia C1] Los patrones temporales y espaciales de recaída difieren entre los subgrupos moleculares. Los pacientes con meduloblastomas del grupo 4 presentan recaída diferida, en comparación con los pacientes de otros subgrupos. En los niños que presentan recaída de la enfermedad después de estrategias de conservación de la radiación, los pacientes con meduloblastomas del grupo 4 y SHH tienen tasas más altas de recaída local (42 % y 39 %, respectivamente), en comparación con los pacientes con enfermedad del grupo 3 (17 %).[8] Es posible lograr un control a más largo plazo con los niños pequeños, en su mayoría aquellos menores de 3 años en el momento del diagnóstico que nunca recibieron radioterapia, cuando se someten a una nueva cirugía, radioterapia y quimioterapia.[5,8-12]
Los abordajes de tratamiento son los siguientes:
Cirugía
En el momento de la recaída, se indica una evaluación completa de la extensión de la recidiva para todos los tumores embrionarios. Es posible que sea necesaria una biopsia o una resección quirúrgica para confirmar la recaída porque otras entidades, como los tumores secundarios y la necrosis cerebral causada por el tratamiento, a veces son clínicamente indistinguibles de la recidiva tumoral. La necesidad de intervención quirúrgica se debe individualizar de acuerdo con el tipo de tumor inicial, el tiempo entre el tratamiento inicial y la reaparición de la lesión, y la sintomatología clínica.
Radioterapia
Los pacientes con tumores embrionarios recidivantes que ya recibieron radioterapia y quimioterapia quizás sean aptos para recibir más radioterapia, según el sitio y la dosis de la radiación previa. El tratamiento puede incluir reirradiación en el sitio del tumor primario, radioterapia dirigida de áreas focales en sitios de enfermedad diseminada e irradiación craneoespinal (ICE).[13,14] Sin embargo, se observó supervivencia a largo plazo en un subconjunto de pacientes que recibieron quimioterapia sola en el momento del diagnóstico y que presentaron recaída local. Este hallazgo se observó principalmente en niños pequeños que tenían enfermedad con activación de SHH.[8,15] En la mayoría de los casos, este tratamiento es paliativo. También es posible usar radioterapia estereotáctica y quimioterapia de rescate.[16] Para obtener más información, consultar la sección Quimioterapia.
- En un estudio retrospectivo se notificaron los desenlaces de lactantes y niños pequeños con meduloblastoma en recaída que recibieron tratamiento inicial en una variedad de ensayos clínicos de quimioterapia diferentes sin administración de ICE.[8]
- En el momento de la recaída, el 73 % de estos niños se trataron con regímenes a base de ICE.
- La tasa de supervivencia después de la recaída a 3 años fue del 52,4 % en los pacientes tratados con intención curativa.
- Las tasas de supervivencia después de la recaída a 3 años para los niños con meduloblastoma SHH, de grupo 3 y de grupo 4, que recibieron radioterapia de rescate fueron del 61 %, el 40 % y el 79 %, respectivamente. Los pacientes con enfermedad SHH tuvieron menos probabilidad de recibir radioterapia de rescate.
- La edad más avanzada en el momento del diagnóstico, la recaída local y el subtipo infantil de SHH se relacionaron con una mejor supervivencia después de la recaída.
Quimioterapia
Los tumores embrionarios del SNC recidivantes responden a los fármacos quimioterapéuticos que se usan de manera individual o combinada, como ciclofosfamida, cisplatino, carboplatino, lomustina, etopósido, topotecán y temozolomida, así como la combinación de irinotecán y temozolomida con bevacizumab o sin este, y terapia metronómica antiangiogénica.[9,17-27]; [28-30][Nivel de evidencia B4] Cerca del 30 % al 50 % de estos pacientes tienen respuestas objetivas a la quimioterapia convencional, pero el control de la enfermedad a largo plazo es poco frecuente.
En ciertos pacientes con meduloblastoma recidivante, sobre todo lactantes y niños pequeños tratados con quimioterapia sola en el momento del diagnóstico y que presentan recidiva local, es posible lograr el control de la enfermedad a largo plazo luego de someterlos a más tratamiento con quimioterapia y radioterapia local. Este potencial es mayor en los pacientes que pueden someterse a resección completa de la enfermedad recidivante.[31][Nivel de evidencia B4]; [32][Nivel de evidencia C1]
En un estudio del St. Jude Children’s Research Hospital (SJYC07 [NCT00602667]), 29 pacientes con enfermedad progresiva recibieron ICE (mediana de dosis, 36 Gy; intervalo intercuartílico, 36–36). De estos 29 pacientes, 18 (62 %) estaban vivos en el momento de la publicación, en comparación con 6 de 25 pacientes (24 %) que no recibieron ICE.[12][Nivel de evidencia B4]
Dosis altas de quimioterapia con rescate de células madre
En los pacientes que recibieron radioterapia previa, se han utilizado regímenes quimioterapéuticos de dosis más altas, con apoyo de rescate autógeno de médula ósea o de células madre periféricas, con resultados variables.[10,11,33-36][Nivel de evidencia B4]; [37-39][Nivel de evidencia C1]
- El uso de estos regímenes se traduce en respuestas objetivas frecuentes en el 50 % al 75 % de los pacientes. Sin embargo, el control a largo plazo de la enfermedad se obtiene en menos del 30 % de los pacientes y se observa principalmente en pacientes en la primera recaída y aquellos que solo tienen enfermedad localizada en el momento de la recaída.[11]; [36][Nivel de evidencia B4]; [37][Nivel de evidencia C1]
- Además, los resultados de ensayos nacionales sobre el meduloblastoma en recaída en los que se especificó la intención de trasplante como parte de su plan de tratamiento mostraron que solo cerca del 5 % de los pacientes que iniciaron la terapia de recuperación lograron una supervivencia sin enfermedad a largo plazo con esta estrategia.[36,40] Por lo tanto, en los estudios en los que se notifica desde el momento del trasplante se sobreestima el beneficio de los abordajes basados en trasplante para la población total de pacientes en recaída.
- El control a largo plazo de la enfermedad en los pacientes con enfermedad diseminada es infrecuente.[41][Nivel de evidencia C1]
Terapia molecular dirigida
Con el aumento del conocimiento de los cambios moleculares y genéticos relacionados con diferentes subtipos de meduloblastoma, la terapia molecular dirigida, también llamada terapia de precisión, se está explorando de manera activa para usarla en los niños con enfermedad recidivante.
En pacientes con meduloblastomas con activación de SHH recidivantes, el inhibidor de SHH PTCH1 vismodegib demostró respuestas radiográficas en 3 de 12 pacientes pediátricos. De las respuestas, 2 se mantuvieron durante menos de 2 meses y 1 se mantuvo durante más de 6 meses. Solo se observaron respuestas en pacientes con variantes ubicadas secuencia arriba de la vía SHH, a nivel de PTCH1 o SMO.[42] Sin embargo, debido a la aparición de la fusión irreversible del cartílago de crecimiento, el uso de vismodegib se limita a los niños que ya alcanzaron la maduración esquelética.[43]
Opciones de tratamiento en evaluación clínica del meduloblastoma y otros tumores del sistema nervioso central infantil recidivantes
Tal vez haya ensayos clínicos terapéuticos de fase inicial disponibles para pacientes seleccionados. Es posible que estos ensayos estén disponibles a través del Children’s Oncology Group (COG), el Pediatric Brain Tumor Consortium u otras entidades. La información en inglés sobre los ensayos clínicos patrocinados por el Instituto Nacional del Cáncer (NCI) se encuentra en el portal de Internet del NCI. Para obtener información en inglés sobre ensayos clínicos patrocinados por otras organizaciones, consultar el portal de Internet ClinicalTrials.gov.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Taylor RE, Bailey CC, Robinson K, et al.: Results of a randomized study of preradiation chemotherapy versus radiotherapy alone for nonmetastatic medulloblastoma: The International Society of Paediatric Oncology/United Kingdom Children's Cancer Study Group PNET-3 Study. J Clin Oncol 21 (8): 1581-91, 2003. [PUBMED Abstract]
- Packer RJ, Goldwein J, Nicholson HS, et al.: Treatment of children with medulloblastomas with reduced-dose craniospinal radiation therapy and adjuvant chemotherapy: A Children's Cancer Group Study. J Clin Oncol 17 (7): 2127-36, 1999. [PUBMED Abstract]
- Sabel M, Fleischhack G, Tippelt S, et al.: Relapse patterns and outcome after relapse in standard risk medulloblastoma: a report from the HIT-SIOP-PNET4 study. J Neurooncol 129 (3): 515-524, 2016. [PUBMED Abstract]
- Kumar R, Smith KS, Deng M, et al.: Clinical Outcomes and Patient-Matched Molecular Composition of Relapsed Medulloblastoma. J Clin Oncol 39 (7): 807-821, 2021. [PUBMED Abstract]
- Oyharcabal-Bourden V, Kalifa C, Gentet JC, et al.: Standard-risk medulloblastoma treated by adjuvant chemotherapy followed by reduced-dose craniospinal radiation therapy: a French Society of Pediatric Oncology Study. J Clin Oncol 23 (21): 4726-34, 2005. [PUBMED Abstract]
- Mazloom A, Zangeneh AH, Paulino AC: Prognostic factors after extraneural metastasis of medulloblastoma. Int J Radiat Oncol Biol Phys 78 (1): 72-8, 2010. [PUBMED Abstract]
- Johnston DL, Keene D, Strother D, et al.: Survival Following Tumor Recurrence in Children With Medulloblastoma. J Pediatr Hematol Oncol 40 (3): e159-e163, 2018. [PUBMED Abstract]
- Erker C, Mynarek M, Bailey S, et al.: Outcomes of Infants and Young Children With Relapsed Medulloblastoma After Initial Craniospinal Irradiation-Sparing Approaches: An International Cohort Study. J Clin Oncol 41 (10): 1921-1932, 2023. [PUBMED Abstract]
- Gentet JC, Doz F, Bouffet E, et al.: Carboplatin and VP 16 in medulloblastoma: a phase II Study of the French Society of Pediatric Oncology (SFOP). Med Pediatr Oncol 23 (5): 422-7, 1994. [PUBMED Abstract]
- Kadota RP, Mahoney DH, Doyle J, et al.: Dose intensive melphalan and cyclophosphamide with autologous hematopoietic stem cells for recurrent medulloblastoma or germinoma. Pediatr Blood Cancer 51 (5): 675-8, 2008. [PUBMED Abstract]
- Butturini AM, Jacob M, Aguajo J, et al.: High-dose chemotherapy and autologous hematopoietic progenitor cell rescue in children with recurrent medulloblastoma and supratentorial primitive neuroectodermal tumors: the impact of prior radiotherapy on outcome. Cancer 115 (13): 2956-63, 2009. [PUBMED Abstract]
- Robinson GW, Rudneva VA, Buchhalter I, et al.: Risk-adapted therapy for young children with medulloblastoma (SJYC07): therapeutic and molecular outcomes from a multicentre, phase 2 trial. Lancet Oncol 19 (6): 768-784, 2018. [PUBMED Abstract]
- Wetmore C, Herington D, Lin T, et al.: Reirradiation of recurrent medulloblastoma: does clinical benefit outweigh risk for toxicity? Cancer 120 (23): 3731-7, 2014. [PUBMED Abstract]
- Baroni LV, Freytes C, Fernández Ponce N, et al.: Craniospinal irradiation as part of re-irradiation for children with recurrent medulloblastoma. J Neurooncol 155 (1): 53-61, 2021. [PUBMED Abstract]
- Hill RM, Richardson S, Schwalbe EC, et al.: Time, pattern, and outcome of medulloblastoma relapse and their association with tumour biology at diagnosis and therapy: a multicentre cohort study. Lancet Child Adolesc Health 4 (12): 865-874, 2020. [PUBMED Abstract]
- Abe M, Tokumaru S, Tabuchi K, et al.: Stereotactic radiation therapy with chemotherapy in the management of recurrent medulloblastomas. Pediatr Neurosurg 42 (2): 81-8, 2006. [PUBMED Abstract]
- Friedman HS, Oakes WJ: The chemotherapy of posterior fossa tumors in childhood. J Neurooncol 5 (3): 217-29, 1987. [PUBMED Abstract]
- Needle MN, Molloy PT, Geyer JR, et al.: Phase II study of daily oral etoposide in children with recurrent brain tumors and other solid tumors. Med Pediatr Oncol 29 (1): 28-32, 1997. [PUBMED Abstract]
- Gaynon PS, Ettinger LJ, Baum ES, et al.: Carboplatin in childhood brain tumors. A Children's Cancer Study Group Phase II trial. Cancer 66 (12): 2465-9, 1990. [PUBMED Abstract]
- Allen JC, Walker R, Luks E, et al.: Carboplatin and recurrent childhood brain tumors. J Clin Oncol 5 (3): 459-63, 1987. [PUBMED Abstract]
- Ashley DM, Longee D, Tien R, et al.: Treatment of patients with pineoblastoma with high dose cyclophosphamide. Med Pediatr Oncol 26 (6): 387-92, 1996. [PUBMED Abstract]
- Lefkowitz IB, Packer RJ, Siegel KR, et al.: Results of treatment of children with recurrent medulloblastoma/primitive neuroectodermal tumors with lomustine, cisplatin, and vincristine. Cancer 65 (3): 412-7, 1990. [PUBMED Abstract]
- Friedman HS, Mahaley MS, Schold SC, et al.: Efficacy of vincristine and cyclophosphamide in the therapy of recurrent medulloblastoma. Neurosurgery 18 (3): 335-40, 1986. [PUBMED Abstract]
- Castello MA, Clerico A, Deb G, et al.: High-dose carboplatin in combination with etoposide (JET regimen) for childhood brain tumors. Am J Pediatr Hematol Oncol 12 (3): 297-300, 1990. [PUBMED Abstract]
- Cefalo G, Massimino M, Ruggiero A, et al.: Temozolomide is an active agent in children with recurrent medulloblastoma/primitive neuroectodermal tumor: an Italian multi-institutional phase II trial. Neuro Oncol 16 (5): 748-53, 2014. [PUBMED Abstract]
- Le Teuff G, Castaneda-Heredia A, Dufour C, et al.: Phase II study of temozolomide and topotecan (TOTEM) in children with relapsed or refractory extracranial and central nervous system tumors including medulloblastoma with post hoc Bayesian analysis: A European ITCC study. Pediatr Blood Cancer 67 (1): e28032, 2020. [PUBMED Abstract]
- Levy AS, Krailo M, Chi S, et al.: Temozolomide with irinotecan versus temozolomide, irinotecan plus bevacizumab for recurrent medulloblastoma of childhood: Report of a COG randomized Phase II screening trial. Pediatr Blood Cancer 68 (8): e29031, 2021. [PUBMED Abstract]
- Minturn JE, Janss AJ, Fisher PG, et al.: A phase II study of metronomic oral topotecan for recurrent childhood brain tumors. Pediatr Blood Cancer 56 (1): 39-44, 2011. [PUBMED Abstract]
- Peyrl A, Chocholous M, Kieran MW, et al.: Antiangiogenic metronomic therapy for children with recurrent embryonal brain tumors. Pediatr Blood Cancer 59 (3): 511-7, 2012. [PUBMED Abstract]
- Peyrl A, Chocholous M, Sabel M, et al.: Sustained Survival Benefit in Recurrent Medulloblastoma by a Metronomic Antiangiogenic Regimen: A Nonrandomized Controlled Trial. JAMA Oncol 9 (12): 1688-1695, 2023. [PUBMED Abstract]
- Ridola V, Grill J, Doz F, et al.: High-dose chemotherapy with autologous stem cell rescue followed by posterior fossa irradiation for local medulloblastoma recurrence or progression after conventional chemotherapy. Cancer 110 (1): 156-63, 2007. [PUBMED Abstract]
- Bakst RL, Dunkel IJ, Gilheeney S, et al.: Reirradiation for recurrent medulloblastoma. Cancer 117 (21): 4977-82, 2011. [PUBMED Abstract]
- Dunkel IJ, Boyett JM, Yates A, et al.: High-dose carboplatin, thiotepa, and etoposide with autologous stem-cell rescue for patients with recurrent medulloblastoma. Children's Cancer Group. J Clin Oncol 16 (1): 222-8, 1998. [PUBMED Abstract]
- Park JE, Kang J, Yoo KH, et al.: Efficacy of high-dose chemotherapy and autologous stem cell transplantation in patients with relapsed medulloblastoma: a report on the Korean Society for Pediatric Neuro-Oncology (KSPNO)-S-053 study. J Korean Med Sci 25 (8): 1160-6, 2010. [PUBMED Abstract]
- Gilman AL, Jacobsen C, Bunin N, et al.: Phase I study of tandem high-dose chemotherapy with autologous peripheral blood stem cell rescue for children with recurrent brain tumors: a Pediatric Blood and MarrowTransplant Consortium study. Pediatr Blood Cancer 57 (3): 506-13, 2011. [PUBMED Abstract]
- Pizer B, Donachie PH, Robinson K, et al.: Treatment of recurrent central nervous system primitive neuroectodermal tumours in children and adolescents: results of a Children's Cancer and Leukaemia Group study. Eur J Cancer 47 (9): 1389-97, 2011. [PUBMED Abstract]
- Massimino M, Gandola L, Spreafico F, et al.: No salvage using high-dose chemotherapy plus/minus reirradiation for relapsing previously irradiated medulloblastoma. Int J Radiat Oncol Biol Phys 73 (5): 1358-63, 2009. [PUBMED Abstract]
- Gururangan S, Krauser J, Watral MA, et al.: Efficacy of high-dose chemotherapy or standard salvage therapy in patients with recurrent medulloblastoma. Neuro Oncol 10 (5): 745-51, 2008. [PUBMED Abstract]
- Dunkel IJ, Gardner SL, Garvin JH, et al.: High-dose carboplatin, thiotepa, and etoposide with autologous stem cell rescue for patients with previously irradiated recurrent medulloblastoma. Neuro Oncol 12 (3): 297-303, 2010. [PUBMED Abstract]
- Gajjar A, Pizer B: Role of high-dose chemotherapy for recurrent medulloblastoma and other CNS primitive neuroectodermal tumors. Pediatr Blood Cancer 54 (4): 649-51, 2010. [PUBMED Abstract]
- Bowers DC, Gargan L, Weprin BE, et al.: Impact of site of tumor recurrence upon survival for children with recurrent or progressive medulloblastoma. J Neurosurg 107 (1 Suppl): 5-10, 2007. [PUBMED Abstract]
- Robinson GW, Orr BA, Wu G, et al.: Vismodegib Exerts Targeted Efficacy Against Recurrent Sonic Hedgehog-Subgroup Medulloblastoma: Results From Phase II Pediatric Brain Tumor Consortium Studies PBTC-025B and PBTC-032. J Clin Oncol 33 (24): 2646-54, 2015. [PUBMED Abstract]
- Robinson GW, Kaste SC, Chemaitilly W, et al.: Irreversible growth plate fusions in children with medulloblastoma treated with a targeted hedgehog pathway inhibitor. Oncotarget 8 (41): 69295-69302, 2017. [PUBMED Abstract]
Actualizaciones más recientes a este resumen (05/15/2025)
Los resúmenes del PDQ con información sobre el cáncer se revisan con regularidad y se actualizan a medida que se obtiene nueva información. Esta sección describe los cambios más recientes introducidos en este resumen a partir de la fecha arriba indicada.
Este resumen fue objeto de revisión integral.
El Consejo editorial del PDQ sobre el tratamiento pediátrico es responsable de la redacción y actualización de este resumen y mantiene independencia editorial respecto del NCI. El resumen refleja una revisión independiente de la bibliografía médica y no representa las políticas del NCI ni de los NIH. Para obtener más información sobre las políticas relativas a los resúmenes y la función de los consejos editoriales del PDQ responsables de su actualización, consultar Información sobre este resumen del PDQ e Información del PDQ® sobre el cáncer dirigida a profesionales de la salud.
Información sobre este resumen del PDQ
Propósito de este resumen
Este resumen de información del PDQ sobre el cáncer dirigido a profesionales de la salud proporciona información integral revisada por expertos y basada en la evidencia sobre el tratamiento del meduloblastoma y otros tumores embrionarios del sistema nervioso central infantil. El objetivo es servir como fuente de información y ayuda para los profesionales clínicos durante la atención de pacientes. No ofrece pautas ni recomendaciones formales para tomar decisiones relacionadas con la atención sanitaria.
Revisores y actualizaciones
El consejo editorial del PDQ sobre el tratamiento pediátrico, que mantiene independencia editorial respecto del Instituto Nacional del Cáncer (NCI), revisa este resumen de manera periódica y, en caso necesario, lo actualiza. Este resumen es el resultado de una revisión bibliográfica independiente y no constituye una declaración de política del NCI ni de los Institutos Nacionales de la Salud (NIH).
Cada mes, los integrantes de este consejo revisan los artículos publicados recientemente para determinar lo siguiente:
- Si el artículo se debe analizar en una reunión del consejo.
- Si conviene añadir texto acerca del artículo.
- Si se debe reemplazar o actualizar un artículo que ya se citó.
Los cambios en los resúmenes se deciden mediante consenso de los integrantes del consejo después de evaluar la solidez de la evidencia de los artículos publicados y determinar la forma de incorporar el artículo en el resumen.
Los revisores principales del sumario sobre Tratamiento del meduloblastoma y otros tumores embrionarios del sistema nervioso central infantil son:
- Kenneth J. Cohen, MD, MBA (Sidney Kimmel Comprehensive Cancer Center at Johns Hopkins Hospital)
- Louis S. Constine, MD (James P. Wilmot Cancer Center at University of Rochester Medical Center)
- Roger J. Packer, MD (Children's National Hospital)
- Malcolm A. Smith, MD, PhD (National Cancer Institute)
Cualquier comentario o pregunta sobre el contenido de este resumen se debe enviar al Servicio de Información de Cáncer del Instituto Nacional del Cáncer. Por favor, no enviar preguntas o comentarios directamente a los integrantes del consejo, ya que no responderán consultas de manera individual.
Niveles de evidencia
Algunas de las referencias bibliográficas de este resumen se acompañan del nivel de evidencia. El propósito de esto es ayudar al lector a evaluar la solidez de la evidencia que respalda el uso de ciertas intervenciones o abordajes. El consejo editorial del PDQ sobre el tratamiento pediátrico emplea un sistema de jerarquización formal para asignar los niveles de evidencia científica.
Permisos para el uso de este resumen
PDQ (Physician Data Query) es una marca registrada. Se autoriza el uso del texto de los documentos del PDQ; sin embargo, no se podrá identificar como un resumen de información sobre cáncer del PDQ del NCI, salvo que el resumen se reproduzca en su totalidad y se actualice de manera periódica. Por otra parte, se permitirá que un autor escriba una oración como “En el resumen del PDQ del NCI de información sobre la prevención del cáncer de mama se describen, de manera concisa, los siguientes riesgos: [incluir fragmento del resumen]”.
Se sugiere citar la referencia bibliográfica de este resumen del PDQ de la siguiente forma:
PDQ® sobre el tratamiento pediátrico. PDQ Tratamiento del meduloblastoma y otros tumores embrionarios del sistema nervioso central infantil. Bethesda, MD: National Cancer Institute. Actualización: <MM/DD/YYYY>. Disponible en: https://www.cancer.gov/espanol/tipos/cerebro/pro/tratamiento-embrionarios-snc-infantil-pdq. Fecha de acceso: <MM/DD/YYYY>.
Las imágenes en este resumen se reproducen con autorización del autor, el artista o la editorial para uso exclusivo en los resúmenes del PDQ. La utilización de las imágenes fuera del PDQ requiere la autorización del propietario, que el Instituto Nacional del Cáncer no puede otorgar. Para obtener más información sobre el uso de las ilustraciones de este resumen o de otras imágenes relacionadas con el cáncer, consultar Visuals Online, una colección de más de 2000 imágenes científicas.
Cláusula sobre el descargo de responsabilidad
Según la solidez de la evidencia, las opciones de tratamiento se clasifican como “estándar” o “en evaluación clínica”. Estas clasificaciones no se deben utilizar para justificar decisiones sobre reembolsos de seguros. Para obtener más información sobre la cobertura de seguros, consultar la página Manejo de la atención del cáncer en Cancer.gov/espanol.
Comuníquese con el Instituto Nacional del Cáncer
Para obtener más información sobre las opciones para comunicarse con el NCI, incluso la dirección de correo electrónico, el número telefónico o el chat, consultar la página del Servicio de Información de Cáncer del Instituto Nacional del Cáncer.