Tratamiento del linfoma no Hodgkin (PDQ®)–Versión para profesionales de salud
Información general sobre el linfoma no Hodgkin
Los linfomas no Hodgkin (LNH) son un grupo heterogéneo de neoplasias malignas linfoproliferativas con diferentes modelos de comportamiento y respuestas terapéuticas.[1]
Al igual que el linfoma de Hodgkin, el LNH a menudo se origina en los tejidos linfoides y se disemina a otros órganos. Sin embargo, el comportamiento del LNH es mucho menos predecible que el linfoma de Hodgkin y tiene una predilección mucho más alta por la diseminación a sitios extraganglionares. El pronóstico depende del tipo histológico, el estadio y el tratamiento.
Incidencia y mortalidad
Número estimado de casos nuevos y defunciones por LNH en los Estados Unidos para 2023:[2]
- Casos nuevos: 80 550.
- Defunciones: 20 180.
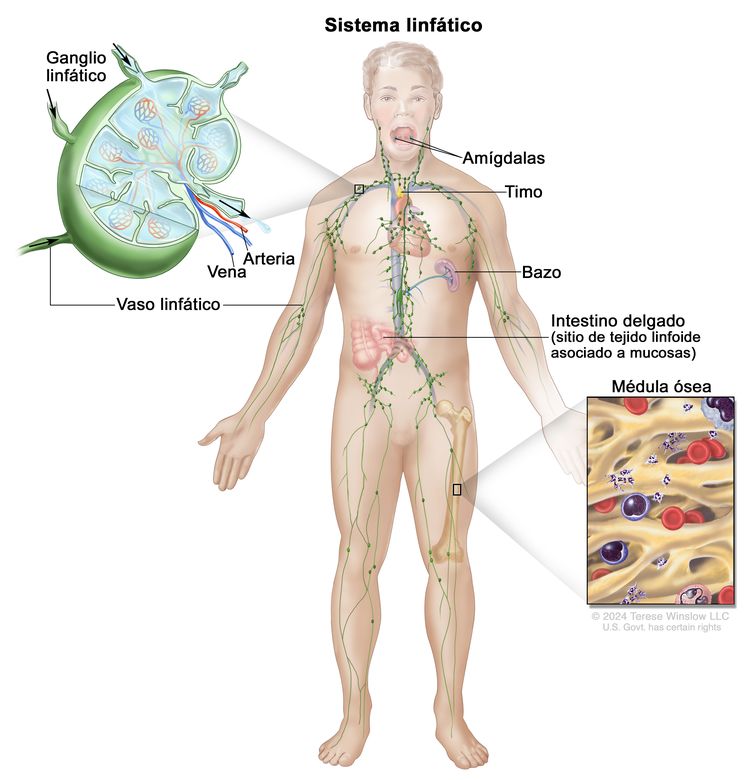
Características anatómicas
El LNH por lo general se origina en los tejidos linfoides.
Pronóstico y supervivencia
El LNH se divide en dos grupos pronósticos: linfomas de crecimiento lento (de escasa malignidad) y linfomas de crecimiento rápido (agresivos o de gran malignidad).
Los LNH de crecimiento lento tienen un pronóstico relativamente bueno, con una mediana de supervivencia de hasta 20 años, pero a menudo son incurables en estadios clínicos avanzados.[3] La radioterapia sola es un tratamiento eficaz para el LNH de crecimiento lento en estadio temprano (estadio I y estadio II). La mayoría de los tipos de crecimiento lento son de tipo morfológico nodular (o folicular).
El LNH de crecimiento rápido tiene una evolución natural más corta, pero un número significativo de estos pacientes se cura con regímenes de quimioterapia combinada intensiva.
Por lo común, los pacientes de LNH que reciben tratamientos modernos logran una tasa de supervivencia general a 5 años de más del 60 %. Más del 50 % de los pacientes con LNH de crecimiento rápido se pueden curar. La mayoría de las recaídas surgen durante los primeros 2 años posteriores al tratamiento. El riesgo de recaída tardía es más alto para los pacientes que presentan ambos tipos histológicos, de crecimiento lento y rápido.[4]
Mientras que el LNH de crecimiento lento es sensible a la inmunoterapia, la radioterapia y la quimioterapia, por lo general, se observa una tasa continua de recaída en los estadios avanzados. Sin embargo, a menudo los pacientes se pueden volver a tratar con bastante éxito si el tipo histológico de la enfermedad permanece de grado bajo. Los pacientes de LNH que presentan desde el inicio un tipo de linfoma de crecimiento rápido o cuyo linfoma se transforma luego en uno de crecimiento rápido a veces exhiben remisiones completas prolongadas con regímenes de quimioterapia combinada o una consolidación intensiva con apoyo de células madre o médula ósea.[5,6]
Bibliografía
- Shankland KR, Armitage JO, Hancock BW: Non-Hodgkin lymphoma. Lancet 380 (9844): 848-57, 2012. [PUBMED Abstract]
- American Cancer Society: Cancer Facts and Figures 2023. American Cancer Society, 2023. Available online. Last accessed Dec. 15, 2023.
- Tan D, Horning SJ, Hoppe RT, et al.: Improvements in observed and relative survival in follicular grade 1-2 lymphoma during 4 decades: the Stanford University experience. Blood 122 (6): 981-7, 2013. [PUBMED Abstract]
- Cabanillas F, Velasquez WS, Hagemeister FB, et al.: Clinical, biologic, and histologic features of late relapses in diffuse large cell lymphoma. Blood 79 (4): 1024-8, 1992. [PUBMED Abstract]
- Bastion Y, Sebban C, Berger F, et al.: Incidence, predictive factors, and outcome of lymphoma transformation in follicular lymphoma patients. J Clin Oncol 15 (4): 1587-94, 1997. [PUBMED Abstract]
- Yuen AR, Kamel OW, Halpern J, et al.: Long-term survival after histologic transformation of low-grade follicular lymphoma. J Clin Oncol 13 (7): 1726-33, 1995. [PUBMED Abstract]
Efectos tardíos del tratamiento del linfoma no Hodgkin
Se han observado efectos tardíos del tratamiento del linfoma no Hodgkin (LNH). Es posible que se produzca una disminución de la fertilidad tras la exposición a alquilantes.[1] Hasta tres décadas después del diagnóstico, los pacientes tienen un riesgo significativamente elevado de formación de segundos cánceres primarios, en especial, de los siguientes tipos:[2-5]
- Cáncer de pulmón.
- Cáncer de encéfalo.
- Cáncer de riñón.
- Cáncer de vejiga.
- Melanoma.
- Linfoma de Hodgkin.
- Leucemia no linfocítica aguda.
La disfunción del ventrículo izquierdo fue uno de los efectos tardíos más importantes en los sobrevivientes a largo plazo de LNH de grado alto que recibieron más de 200 mg/m² de doxorrubicina.[1,6]
El síndrome mielodisplásico y la leucemia mielógena aguda son complicaciones tardías de la terapia mielosupresora con apoyo de médula ósea o células madre de sangre periférica autógenas, al igual que de la quimioterapia convencional con alquilantes.[3,7-14] La mayoría de estos pacientes exhiben hematopoyesis clonal incluso antes del trasplante; esto indica que las lesiones hematológicas a menudo se presentan durante la quimioterapia de inducción o reinducción.[9,15,16] En una serie de 605 pacientes con una mediana de seguimiento de 10 años después de un trasplante autógeno de médula ósea con acondicionamiento de ciclofosfamida y radioterapia corporal total, la incidencia de una segunda neoplasia maligna fue del 21 %, y de estas, el 10 % fueron tumores sólidos.[17]
Se notificaron embarazos fructíferos con recién nacidos sin anomalías congénitas en mujeres jóvenes después de un trasplante autógeno de médula ósea.[18] Es posible que se produzca un tromboembolismo venoso tardío después de un trasplante de médula ósea (TMO) alogénico o autógeno.[19]
El deterioro inmunitario a largo plazo se evaluó en un estudio de cohorte retrospectivo que incluyó 21 690 sobrevivientes de linfoma difuso de células B grandes del California Cancer Registry. Se encontraron tasas de incidencia elevadas de neumonía (10,8 veces mayor), meningitis (5,3 veces mayor), deficiencia de inmunoglobulina (17,6 veces mayor) y citopenias autoinmunitarias (12 veces mayor) hasta 10 años después.[20] Del mismo modo, hay respuestas humorales deficientes a la vacunación contra el virus de la COVID-19 en pacientes con linfoma que reciben terapias dirigidas a las células B.[21,22]
Algunos pacientes tienen osteopenia u osteoporosis al comenzar el tratamiento; la densidad ósea quizás empeore después del tratamiento del linfoma.[23]
Bibliografía
- Haddy TB, Adde MA, McCalla J, et al.: Late effects in long-term survivors of high-grade non-Hodgkin's lymphomas. J Clin Oncol 16 (6): 2070-9, 1998. [PUBMED Abstract]
- Travis LB, Curtis RE, Glimelius B, et al.: Second cancers among long-term survivors of non-Hodgkin's lymphoma. J Natl Cancer Inst 85 (23): 1932-7, 1993. [PUBMED Abstract]
- Mudie NY, Swerdlow AJ, Higgins CD, et al.: Risk of second malignancy after non-Hodgkin's lymphoma: a British Cohort Study. J Clin Oncol 24 (10): 1568-74, 2006. [PUBMED Abstract]
- Hemminki K, Lenner P, Sundquist J, et al.: Risk of subsequent solid tumors after non-Hodgkin's lymphoma: effect of diagnostic age and time since diagnosis. J Clin Oncol 26 (11): 1850-7, 2008. [PUBMED Abstract]
- Major A, Smith DE, Ghosh D, et al.: Risk and subtypes of secondary primary malignancies in diffuse large B-cell lymphoma survivors change over time based on stage at diagnosis. Cancer 126 (1): 189-201, 2020. [PUBMED Abstract]
- Moser EC, Noordijk EM, van Leeuwen FE, et al.: Long-term risk of cardiovascular disease after treatment for aggressive non-Hodgkin lymphoma. Blood 107 (7): 2912-9, 2006. [PUBMED Abstract]
- Darrington DL, Vose JM, Anderson JR, et al.: Incidence and characterization of secondary myelodysplastic syndrome and acute myelogenous leukemia following high-dose chemoradiotherapy and autologous stem-cell transplantation for lymphoid malignancies. J Clin Oncol 12 (12): 2527-34, 1994. [PUBMED Abstract]
- Stone RM, Neuberg D, Soiffer R, et al.: Myelodysplastic syndrome as a late complication following autologous bone marrow transplantation for non-Hodgkin's lymphoma. J Clin Oncol 12 (12): 2535-42, 1994. [PUBMED Abstract]
- Armitage JO, Carbone PP, Connors JM, et al.: Treatment-related myelodysplasia and acute leukemia in non-Hodgkin's lymphoma patients. J Clin Oncol 21 (5): 897-906, 2003. [PUBMED Abstract]
- André M, Mounier N, Leleu X, et al.: Second cancers and late toxicities after treatment of aggressive non-Hodgkin lymphoma with the ACVBP regimen: a GELA cohort study on 2837 patients. Blood 103 (4): 1222-8, 2004. [PUBMED Abstract]
- Oddou S, Vey N, Viens P, et al.: Second neoplasms following high-dose chemotherapy and autologous stem cell transplantation for malignant lymphomas: a report of six cases in a cohort of 171 patients from a single institution. Leuk Lymphoma 31 (1-2): 187-94, 1998. [PUBMED Abstract]
- Lenz G, Dreyling M, Schiegnitz E, et al.: Moderate increase of secondary hematologic malignancies after myeloablative radiochemotherapy and autologous stem-cell transplantation in patients with indolent lymphoma: results of a prospective randomized trial of the German Low Grade Lymphoma Study Group. J Clin Oncol 22 (24): 4926-33, 2004. [PUBMED Abstract]
- McLaughlin P, Estey E, Glassman A, et al.: Myelodysplasia and acute myeloid leukemia following therapy for indolent lymphoma with fludarabine, mitoxantrone, and dexamethasone (FND) plus rituximab and interferon alpha. Blood 105 (12): 4573-5, 2005. [PUBMED Abstract]
- Morton LM, Curtis RE, Linet MS, et al.: Second malignancy risks after non-Hodgkin's lymphoma and chronic lymphocytic leukemia: differences by lymphoma subtype. J Clin Oncol 28 (33): 4935-44, 2010. [PUBMED Abstract]
- Mach-Pascual S, Legare RD, Lu D, et al.: Predictive value of clonality assays in patients with non-Hodgkin's lymphoma undergoing autologous bone marrow transplant: a single institution study. Blood 91 (12): 4496-503, 1998. [PUBMED Abstract]
- Lillington DM, Micallef IN, Carpenter E, et al.: Detection of chromosome abnormalities pre-high-dose treatment in patients developing therapy-related myelodysplasia and secondary acute myelogenous leukemia after treatment for non-Hodgkin's lymphoma. J Clin Oncol 19 (9): 2472-81, 2001. [PUBMED Abstract]
- Brown JR, Yeckes H, Friedberg JW, et al.: Increasing incidence of late second malignancies after conditioning with cyclophosphamide and total-body irradiation and autologous bone marrow transplantation for non-Hodgkin's lymphoma. J Clin Oncol 23 (10): 2208-14, 2005. [PUBMED Abstract]
- Jackson GH, Wood A, Taylor PR, et al.: Early high dose chemotherapy intensification with autologous bone marrow transplantation in lymphoma associated with retention of fertility and normal pregnancies in females. Scotland and Newcastle Lymphoma Group, UK. Leuk Lymphoma 28 (1-2): 127-32, 1997. [PUBMED Abstract]
- Gangaraju R, Chen Y, Hageman L, et al.: Risk of venous thromboembolism in patients with non-Hodgkin lymphoma surviving blood or marrow transplantation. Cancer 125 (24): 4498-4508, 2019. [PUBMED Abstract]
- Shree T, Li Q, Glaser SL, et al.: Impaired Immune Health in Survivors of Diffuse Large B-Cell Lymphoma. J Clin Oncol 38 (15): 1664-1675, 2020. [PUBMED Abstract]
- Ghione P, Gu JJ, Attwood K, et al.: Impaired humoral responses to COVID-19 vaccination in patients with lymphoma receiving B-cell-directed therapies. Blood 138 (9): 811-814, 2021. [PUBMED Abstract]
- Terpos E, Trougakos IP, Gavriatopoulou M, et al.: Low neutralizing antibody responses against SARS-CoV-2 in older patients with myeloma after the first BNT162b2 vaccine dose. Blood 137 (26): 3674-3676, 2021. [PUBMED Abstract]
- Westin JR, Thompson MA, Cataldo VD, et al.: Zoledronic acid for prevention of bone loss in patients receiving primary therapy for lymphomas: a prospective, randomized controlled phase III trial. Clin Lymphoma Myeloma Leuk 13 (2): 99-105, 2013. [PUBMED Abstract]
Clasificación celular del linfoma no Hodgkin
Se debe consultar con un patólogo antes de realizar una biopsia porque algunos estudios exigen una preparación especial del tejido (por ejemplo, tejido congelado). El conocimiento de los marcadores de superficie celular y los reordenamientos de los genes de inmunoglobulinas y del receptor de células T puede ayudar a tomar decisiones diagnósticas y terapéuticas. El exceso clonal de inmunoglobulinas de cadena ligera permite diferenciar las células linfoides malignas de las células reactivas. Es muy importante que un hematopatólogo con experiencia en el diagnóstico de linfomas realice un examen minucioso de las muestras de biopsia porque las características histopatológicas afectan el pronóstico y el abordaje del tratamiento. Aunque se recomienda obtener biopsias de ganglios linfáticos cuando sea posible, a veces los datos inmunofenotípicos son suficientes para establecer un diagnóstico de linfoma si se prefiere hacer un estudio citológico mediante aspiración con aguja fina.[1,2]
Sistemas de clasificación tradicionales
Tradicionalmente, no se podía establecer un tratamiento uniforme para los pacientes de linfoma no Hodgkin (LNH) por la falta de un sistema de clasificación sistemático. En 1982, se publicaron los resultados de un estudio de consenso llamado Working Formulation.[3] En el Working Formulation, se combinaron los resultados de seis sistemas de clasificación principales en una sola clasificación. Esto permitió la comparación de estudios de diferentes instituciones y países. La clasificación de Rappaport, que también aparece a continuación, ya no se usa mucho.
| Working Formulation [3] | Clasificación de Rappaport |
|---|---|
| Grado bajo | |
| A. Linfocítico pequeño, compatible con leucemia linfocítica crónica | Linfocítico difuso, bien diferenciado |
| B. Folicular, predominio de células hendidas pequeñas | Linfocítico nodular, poco diferenciado |
| C. Folicular, mezcla de células hendidas pequeñas y células grandes | Nodular mixto, linfocítico e histiocítico |
| Grado intermedio | |
| D. Folicular, predominio de células grandes | Histiocítico nodular |
| E. Difuso, células hendidas pequeñas | Linfocítico difuso, poco diferenciado |
| F. Difuso mixto, células pequeñas y grandes | Difuso mixto, linfocítico e histiocítico |
| G. Difuso, células grandes hendidas o no hendidas | Histiocítico difuso |
| Grado alto | |
| H. Inmunoblástico, células grandes | Histiocítico difuso |
| I. Linfoblástico, de células cerebriformes o no cerebriformes | Linfoblástico difuso |
| J. Células pequeñas no hendidas, de Burkitt o no Burkitt | Burkitt o no Burkitt difuso indiferenciado |
Sistemas de clasificación actuales
A medida que mejoró la comprensión del LNH y que se volvió más sofisticado el diagnóstico histopatológico gracias a técnicas inmunológicas y genéticas, se empezaron a describir nuevas entidades patológicas.[4] Además, cambió la comprensión y el abordaje de tratamiento para muchos de los subtipos patológicos descritos antes. Como resultado, la Working Formulation se volvió anticuada y obsoleta para los médicos y patólogos. Por este motivo, grupos de patólogos de Europa y Estados Unidos propusieron una clasificación nueva a la que llamaron Revised European American Lymphoma (REAL).[5-8] Desde 1995, los miembros de las sociedades europeas y estadounidenses de hematopatología colaboran para establecer la nueva clasificación de la Organización Mundial de la Salud (OMS), que representa una versión actualizada del sistema REAL.[9,10]
En la modificación que hizo la OMS de la clasificación REAL, se reconocen tres categorías principales de neoplasias malignas linfoides a partir de características morfológicas y de linaje celular: Neoplasias de células B, neoplasias de células T o de células citolíticas naturales (NK), y linfoma de Hodgkin (LH). En esta clasificación se incluyen los linfomas y las leucemias linfoides porque muchas neoplasias linfoides exhiben ambas fases (sólida y circulante), así que la distinción entre ellas es artificial. Por ejemplo, la leucemia linfocítica crónica (LLC) de células B y el linfoma linfocítico pequeño de células B son distintas manifestaciones de la misma neoplasia, al igual que los linfomas linfoblásticos y las leucemias linfocíticas agudas. Dentro de las categorías de células B y de células T, se reconocen dos subdivisiones: neoplasias precursoras, que corresponden a estadios tempranos de diferenciación, y las neoplasias diferenciadas más maduras.[9,10]
Clasificación Revised European American Lymphoma/Organización Mundial de la Salud actualizada
Neoplasias de células B
- Neoplasias de células B precursoras: leucemia linfoblástica aguda de células B precursoras o linfoma linfoblástico de células B precursoras.
- Neoplasias de células B periféricas.
- Leucemia linfocítica crónica de células B o linfoma linfocítico pequeño de células B.
- Leucemia prolinfocítica de células B.
- Linfoma linfoplasmocítico o inmunocitoma.
- Linfoma de células de manto.
- Linfoma folicular.
- Linfoma extraganglionar de células B de zona marginal de tejido linfoide asociado a mucosa.
- Linfoma ganglionar de células B de zona marginal (± células B monocitoides).
- Linfoma esplénico de zona marginal (± linfocitos vellosos).
- Leucemia de células pilosas.
- Plasmocitoma o mieloma de células plasmáticas.
- Linfoma difuso de células B grandes.
- Linfoma de Burkitt.
Neoplasias de células T y presumiblemente derivadas de células NK
- Neoplasias de células T precursoras: leucemia linfoblástica aguda de células T precursoras o linfoma linfoblástico de células T precursoras.
- Neoplasias de células T periféricas y de células NK.
- Leucemia linfocítica crónica de células T o leucemia prolinfocítica de células T.
- Leucemia linfocítica granular de células T.
- Micosis fungoide (incluso el síndrome de Sézary).
- Linfoma de células T periféricas, sin otra indicación.
- Linfoma hepatoesplénico de células T γ-δ.
- Linfoma subcutáneo de células T similar a paniculitis
- Linfoma angioinmunoblástico de células T.
- Linfoma extraganglionar de células T o de células NK de tipo nasal.
- Linfoma intestinal de células T de tipo enteropático.
- Linfoma de células T o leucemia de células T en adultos (virus linfotrópico T humano [VLHT] 1+).
- Linfoma anaplásico de células grandes de tipo sistémico primario.
- Linfoma anaplásico de células grandes de tipo cutáneo primario.
- Leucemia de células NK de crecimiento rápido (agresiva).
Linfoma de Hodgkin
- Linfoma de Hodgkin con predominio linfocítico nodular.
- Linfoma de Hodgkin clásico.
- Linfoma de Hodgkin con esclerosis nodular.
- Linfoma de Hodgkin clásico rico en linfocitos.
- Linfoma de Hodgkin con celularidad mixta.
- Linfoma de Hodgkin con agotamiento linfocítico.
La clasificación Revised European American Lymphoma (REAL) abarca todas las neoplasias linfoproliferativas. Para obtener más información, consultar los siguientes sumarios del PDQ:
- Tratamiento de la leucemia linfoblástica aguda en adultos
- Tratamiento del linfoma de Hodgkin
- Tratamiento del linfoma relacionado con el SIDA
- Tratamiento de la leucemia linfocítica crónica
- Tratamiento de la leucemia de células pilosas
- Tratamiento de la micosis fungoide (incluso el síndrome de Sézary)
- Tratamiento de las neoplasias de células plasmáticas (incluso mieloma múltiple)
- Tratamiento del linfoma primario del sistema nervioso central
Bibliografía
- Zeppa P, Marino G, Troncone G, et al.: Fine-needle cytology and flow cytometry immunophenotyping and subclassification of non-Hodgkin lymphoma: a critical review of 307 cases with technical suggestions. Cancer 102 (1): 55-65, 2004. [PUBMED Abstract]
- Young NA, Al-Saleem T: Diagnosis of lymphoma by fine-needle aspiration cytology using the revised European-American classification of lymphoid neoplasms. Cancer 87 (6): 325-45, 1999. [PUBMED Abstract]
- National Cancer Institute sponsored study of classifications of non-Hodgkin's lymphomas: summary and description of a working formulation for clinical usage. The Non-Hodgkin's Lymphoma Pathologic Classification Project. Cancer 49 (10): 2112-35, 1982. [PUBMED Abstract]
- Pugh WC: Is the working formulation adequate for the classification of the low grade lymphomas? Leuk Lymphoma 10 (Suppl 1): 1-8, 1993.
- Harris NL, Jaffe ES, Stein H, et al.: A revised European-American classification of lymphoid neoplasms: a proposal from the International Lymphoma Study Group. Blood 84 (5): 1361-92, 1994. [PUBMED Abstract]
- Pittaluga S, Bijnens L, Teodorovic I, et al.: Clinical analysis of 670 cases in two trials of the European Organization for the Research and Treatment of Cancer Lymphoma Cooperative Group subtyped according to the Revised European-American Classification of Lymphoid Neoplasms: a comparison with the Working Formulation. Blood 87 (10): 4358-67, 1996. [PUBMED Abstract]
- Armitage JO, Weisenburger DD: New approach to classifying non-Hodgkin's lymphomas: clinical features of the major histologic subtypes. Non-Hodgkin's Lymphoma Classification Project. J Clin Oncol 16 (8): 2780-95, 1998. [PUBMED Abstract]
- A clinical evaluation of the International Lymphoma Study Group classification of non-Hodgkin's lymphoma. The Non-Hodgkin's Lymphoma Classification Project. Blood 89 (11): 3909-18, 1997. [PUBMED Abstract]
- Pileri SA, Milani M, Fraternali-Orcioni G, et al.: From the R.E.A.L. Classification to the upcoming WHO scheme: a step toward universal categorization of lymphoma entities? Ann Oncol 9 (6): 607-12, 1998. [PUBMED Abstract]
- Society for Hematopathology Program: Society for Hematopathology Program. Am J Surg Pathol 21 (1): 114-121, 1997.
Linfoma no Hodgkin de crecimiento lento
El linfoma no Hodgkin (LNH) de crecimiento lento incluye los siguientes subtipos:
Linfoma folicular
El linfoma folicular comprende el 20 % de todos los LNH y hasta el 70 % de los linfomas de crecimiento lento notificados en los ensayos clínicos en América y Europa.[1-3] La mayoría de los pacientes de linfoma folicular tienen 50 años o más y exhiben una enfermedad diseminada en el momento del diagnóstico. El compromiso ganglionar es más común y, con frecuencia, se acompaña de enfermedad en el bazo y la médula ósea. Hay un reordenamiento del gen BCL2 en más del 90 % de los pacientes de linfoma folicular; la sobreexpresión de la proteína BCL2 se relaciona con incapacidad de erradicar el linfoma por inhibición de la apoptosis.[4]
Pronóstico
A pesar del estadio avanzado, la mediana de supervivencia oscila entre 8 y 15 años, motivo por el que se designa como de crecimiento lento.[5-7] Los pacientes con linfoma folicular en estadio avanzado no se curan con las opciones terapéuticas vigentes. La tasa de recaída es bastante constante en el tiempo, aun en pacientes que lograron respuestas completas al tratamiento.[8] La observación cautelosa, es decir, diferir el tratamiento hasta que el paciente presente síntomas, es una opción para los pacientes con linfoma folicular en estadio avanzado.[9,10] En un índice internacional para el linfoma folicular llamado Follicular Lymphoma International Prognostic Index [FLIPI] [11-13] se incluyen los siguientes 5 factores de riesgo significativos para el pronóstico de la supervivencia general (SG):
- Edad (<60 vs. >60 años).
- Concentración sérica (normal vs. elevada) de lactato-deshidrogenasa (LDH).
- Estadio (estadio I o II vs. estadio III o IV).
- Concentración de hemoglobina (≥120 g/l vs. <120 g/l).
- Número de áreas ganglionares (≤4 vs. >4).
Los pacientes sin factores de riesgo o que solo tienen un factor de riesgo presentan una tasa de supervivencia a 10 años del 85 %; los pacientes con 3 o más factores de riesgo tienen una tasa de supervivencia a 10 años del 40 %.[11] En los criterios FLIPI-2 revisados, se propuso el uso de otros factores pronósticos, la concentración elevada de microglobulina β2 y el tamaño de un ganglio linfático de más de 6 cm en lugar de la concentración sérica de LDH y el número de áreas ganglionares.[14] Si bien los índices FLIPI y FLIPI-2 permiten predecir la supervivencia sin progresión (SSP) y la SG, estos puntajes no sirven para determinar la necesidad de tratamiento ni para predecir la respuesta terapéutica.[11,14] La principal utilidad de FLIPI y FLIPI-2 es garantizar el equilibrio de los factores pronósticos o definir los requisitos para participar en ensayos clínicos aleatorizados. Las personas con un puntaje de FLIPI adverso quizás se beneficien de una observación cautelosa o quizás respondan bien al tratamiento inicial. Un índice pronóstico alternativo para el que se usa solo la microglobulina β2 y el compromiso inicial de la médula ósea (PRIMA-PI) tiene la desventaja de exigir el empleo de pruebas invasoras que por lo general no se necesitan fuera del entorno de un ensayo clínico.[15] Un índice pronóstico alternativo que usa variables clínicas no invasivas sobrepasó a los índices FLIPI, FLIPI-2 y PRIMA-PI; se utilizaron datos de ensayos de inmunoquimioterapia.[16]
En 3 análisis retrospectivos, incluso un análisis conjunto de 5225 pacientes de 13 ensayos clínicos aleatorizados, se identificó un grupo de riesgo alto con una tasa de SG a los 5 años del 50 % cuando se presentaron recidivas dentro de los 24 meses de la quimioinmunoterapia de inducción.[17-19] En un cuarto análisis retrospectivo de 296 pacientes que recibieron bendamustina con rituximab se observó una tasa de SG a 2 años del 38 % (intervalo de confianza [IC] 95 %, 20−55 %) en aquellos con progresión de la enfermedad antes de 24 meses (PDE24). La mayoría de estos pacientes (76 %) presentó transformación de la enfermedad (progresión histológica a linfoma difuso de células B grandes [LDCBG]).[20] Estos pacientes de riesgo más alto con PDE24 representan una población de interés para los ensayos clínicos.
No hay diferencias reproducibles en la supervivencia sin enfermedad ni en la SG del linfoma folicular de células hendidas pequeñas y el linfoma folicular mixto de células hendidas pequeñas y grandes.
Abordajes terapéuticos
A menudo el linfoma folicular tiene una evolución clínica de escasa malignidad y algunos pacientes son asintomáticos, esto lleva a que se siga usando la observación cautelosa como estándar de atención inicial después del diagnóstico y para los pacientes con recaída asintomática de crecimiento lento. Cuando se necesita tratamiento, es posible emplear múltiples opciones terapéuticas en diferentes secuencias con resultados equivalentes de SG a 5 y 10 años.[9,21-23] El rituximab se puede administrar solo o en combinación con varias opciones de quimioterapia.[23,24] También es posible combinar el rituximab con el inmunomodulador lenalidomida para evitar los efectos tóxicos a corto y largo plazo de los citotóxicos.[25-27] Otro anticuerpo monoclonal anti-CD20, el obinutuzumab, se puede administrar con quimioterapia combinada.[28] Los inhibidores de la fosfatidilinositol 3–cinasa (PI3K) también son eficaces para los pacientes con enfermedad en recaída o resistente al tratamiento.[29] Las células T con receptor de antígeno quimérico (CAR) dirigido a CD19 pueden utilizarse en pacientes con progresión de la enfermedad tras dos o más líneas de tratamiento previas.[30] También es posible usar mosunetuzumab, un activador biespecífico de células T CD3 dirigido a CD20, en este entorno.[31] Además, se puede considerar la terapia de consolidación para una recaída después de la terapia de reinducción con trasplante de células madre (TCM) autógeno o alogénico.[32]
El linfoma folicular in situ y el linfoma folicular primario de duodeno son variantes de escasa malignidad que muy pocas veces progresan y casi nunca exigen tratamiento.[33,34] El linfoma folicular ganglionar de tipo pediátrico tiene un comportamiento de escasa malignidad y es infrecuente que recidive; en los adultos esta variante histológica se caracteriza por la falta de un reordenamiento de BCL2, un índice de proliferación Ki-67 superior al 30 % y un estadio l localizado en el momento del cuadro clínico inicial.[35]
Los pacientes con linfoma de crecimiento lento a veces recaen con un tipo histológico más maligno. Si el modelo clínico de la recaída indica que la enfermedad es más maligna, se deberá tomar una biopsia si esta es viable.[36] Cuando se documenta una conversión a un tipo histológico más maligno se necesita cambiar el tratamiento por uno adecuado para el tipo histológico.[37] El crecimiento rápido o discordante en diversos sitios de la enfermedad quizás indique una conversión histológica.[36] El riesgo de transformación histológica a los 10 años fue del 30 % en una revisión retrospectiva de 325 pacientes que recibieron el diagnóstico entre 1972 y 1999.[38] En esta serie, los factores de riesgo alto de transformación histológica posterior fueron estadio avanzado, FLIPI de riesgo alto y observación cautelosa (contrario al inicio del tratamiento en el momento del diagnóstico). La tasa de SG a 5 años fue superior al 50 % para los pacientes con transformación a un tipo histológico de gran malignidad en varios estudios multicéntricos de cohortes en los que se usó rituximab y una antraciclina, quimioterapia a base de derivados del platino o una terapia semejante seguida por un TCM autógeno o alogénico.[36,39,40]
En un estudio prospectivo no aleatorizado, después de una mediana de seguimiento de 6,8 años, 379 (14 %) de 2652 pacientes con diagnóstico inicial de linfoma folicular presentaron una transformación a un tipo histológico más maligno.[41][Nivel de evidencia C3] La mediana de SG después de la transformación fue de 5 años; no obstante, en 47 pacientes con indicios de transformación después de un diagnóstico inicial de linfoma folicular, la SG no fue más precaria que la de otros pacientes sin transformación (tasa de SG a 5 años, 88 %; IC 95 %, 74–95 %).
Linfoma linfoplasmocítico (macroglobulinemia de Waldenström)
El linfoma linfoplasmocítico por lo general se relaciona con una paraproteína monoclonal de tipo inmunoglobulina M (IgM) en el suero (macroglobulinemia de Waldenström).[42] La mayoría de los pacientes tiene compromiso de médula ósea, ganglios linfáticos y bazo; algunos pacientes presentan síndrome de hiperviscosidad. La mayoría de los pacientes con macroglobulinemia de Waldenström son portadores de una mutación en MYD88 que algunos patólogos consideran patognomónica de la enfermedad.[43] Otros linfomas también se asocian con paraproteínas séricas. En los pacientes con linfoma linfoplasmocítico se debe evaluar la presencia de infección por el virus de la hepatitis C.
Los pacientes asintomáticos se pueden vigilar para identificar la progresión de la enfermedad, porque no tienen una necesidad inmediata de quimioterapia.[9,44,45]
Los factores pronósticos relacionados con síntomas que exigen tratamiento son los siguientes:
- Edad mayor de 70 años.
- Microglobulina β2 de 3 mg/dl o más.
- Aumento de la concentración sérica de LDH.[44]
Abordajes terapéuticos
El tratamiento del linfoma linfoplasmocítico es similar al de otros linfomas de grado bajo; en especial, el linfoma linfocítico pequeño difuso y la leucemia linfocítica crónica.[46-48] Si la viscosidad relativa con respecto al agua es mayor de 4, el paciente quizás exhiba manifestaciones de hiperviscosidad. La plasmaféresis es útil para síntomas agudos transitorios, como retinopatía, enfermedad cardíaca congestiva y disfunción del sistema nervioso central (SNC), pero se puede combinar con quimioterapia a fin de lograr un control prolongado de la enfermedad. Por lo general, la quimioterapia o las terapias dirigidas de tipo biológico se inician de manera directa para los pacientes sintomáticos con viscosidad sérica de 4 o menos. Es posible que se necesite tratamiento para corregir una anemia hemolítica en los pacientes con enfermedad por crioaglutininas crónica; a menudo se usan rituximab, bendamustina y corticoesteroides.[45] En ocasiones, se necesita una habitación con calefacción para aquellos pacientes cuyas crioaglutininas se activan hasta con el menor escalofrío. Es posible que sutimlimab, un anticuerpo monoclonal de tipo inmunoglobulina G4 que inhibe de manera selectiva la vía del complemento en C15, reduzca la hemólisis cuando las terapias dirigidas al linfoma linfoplasmocítico resultan ineficaces.[49]
Los regímenes de primera línea incluyen rituximab e ibrutinib (inhibidor de la tirosina–cinasa de Bruton [BTK]), rituximab solo, análogos nucleosídicos, y alquilantes, en monoterapia o quimioterapia combinada.[50-54] En un ensayo prospectivo aleatorizado, 150 pacientes asintomáticos (incluso pacientes no tratados o en recaída) recibieron ibrutinib con rituximab o rituximab con un placebo. Después de una mediana de seguimiento de 50 meses, la tasa de SSP a 4,5 años favoreció al grupo de ibrutinib con rituximab (68 %; IC 95 %, 55–78 %) versus el grupo de rituximab con placebo (25 %; IC 95 %, 15–37 %) (cociente de riesgos instantáneos, 0,25; IC 95 %, 0,15–0,42; P < 0,0001), y no hubo diferencias en la tasa de SG a 30 meses entre los dos grupos (92–94 %).[54][Nivel de evidencia B1] El zanubrutinib, otro inhibidor de la BTK, se comparó con el ibrutinib en un ensayo clínico prospectivo aleatorizado de 164 pacientes en recaída y 38 pacientes que no habían sido tratados.[55] Al cabo de una mediana de seguimiento de 18 meses, la tasa de SSP fue igual en los dos grupos, del 84 %. El grupo de zanubrutinib presentó menos casos de fibrilación auricular (11 vs. 1) y un 50 % menos casos de hipertensión (no se notificaron los datos estadísticos).[55][Nivel de evidencia C3] La inhibición de la BTK con ibrutinib permitió que los 13 pacientes con anemia hemolítica autoinmunitaria mediada por anticuerpos fríos y con acrocianosis lograran la remisión clínica con independencia de la patología subyacente o del estado de MYD88.[56][Nivel de evidencia C3]
Los pacientes sin tratamiento previo que recibieron rituximab tuvieron tasas de respuesta del 60 % al 80 %, pero se necesita vigilar de cerca la IgM sérica por un posible aumento repentino de esta paraproteína al comienzo del tratamiento.[50,57,58][Nivel de evidencia C3] El aumento de la IgM al iniciar el rituximab se evita con el uso simultáneo de un alquilante, como ciclofosfamida o los inhibidores del proteosoma, bortezomib o ixazomib.[45,59-61] Una combinación de bortezomib, dexametasona y rituximab se ha usado para evitar que la IgM vuelva a aumentar.[62-64] Los pacientes con linfoma linfoplasmocítico sin tratamiento previo que recibieron los análogos nucleosídicos cladribina y fludarabina obtuvieron tasas de respuesta similares.[53,65,66][Nivel de evidencia C3] También obtienen tasas de respuesta similares los pacientes que recibieron monoterapias de alquilantes, como la bendamustina, el bortezomib o el venetoclax, y una quimioterapia combinada con rituximab o sin este.[53,59,61,67-71][Nivel de evidencia C3] En casos infrecuentes de linfoma linfoplasmocítico con compromiso del SNC (síndrome de Bing-Neel), el ibrutinib produjo una tasa de respuesta del 85 % en una serie anecdótica de 28 pacientes.[72][Nivel de evidencia C3]
La terapia mielosupresora con apoyo de células madre autógenas o alogénicas está en evaluación clínica.[73-76] Los pacientes aptos para recibir este abordaje deben evitar el uso a largo plazo de alquilantes o de análogos de nucleósidos de purina, que pueden reducir las células madre hematopoyéticas o predisponer a los pacientes a una mielodisplasia o leucemia aguda.[50,77] Después de una recaída durante la terapia con alquilantes, 92 pacientes de linfoma linfoplasmocítico se asignaron al azar a recibir fludarabina o ciclofosfamida, doxorrubicina y prednisona. Aunque la fludarabina favoreció la supervivencia sin recaída (mediana de duración de 19 vs. 3 meses, P < 0,01) no se observó diferencia en la SG.[78][Nivel de evidencia B1]
Linfoma de zona marginal
Cuando los linfomas de zona marginal comprometen los ganglios, se llaman linfomas de células B monocitoides o linfomas ganglionares de células B de zona marginal. Cuando comprometen sitios extraganglionares (por ejemplo, tubo digestivo, tiroides, pulmón, mama, órbita y piel), se llaman linfomas de tejido linfoide asociado a mucosa (TLAM).[79,80] El linfoma esplénico de zona marginal es una entidad clínica distinta que suele presentarse con esplenomegalia masiva. Una variante del linfoma TLAM se conoce como enfermedad inmunoproliferativa del intestino delgado (EIPID).[80] Un índice pronóstico de todos los linfomas de la zona marginal incluye 3 factores de pronóstico adverso: edad de 70 años o más, enfermedad en estadio III o estadio IV, y concentración elevada de LDH.[81] Menos del 10 % de los pacientes presentan una transformación a un linfoma de grado más alto; en una revisión retrospectiva, los factores de riesgo incluyeron la concentración elevada de LDH, más de 4 sitios ganglionares en el momento del diagnóstico inicial de linfoma de zona marginal y el fracaso en lograr una respuesta completa después del tratamiento inicial.[82]
Tejido linfoide asociado a mucosa gástrica
Muchos pacientes tienen antecedentes de una enfermedad autoinmunitaria, como la tiroiditis de Hashimoto, el síndrome de Sjögren o una gastritis por Helicobacter. La mayoría de los pacientes presentan una enfermedad extraganglionar en estadio I o estadio II, a menudo en el estómago. La mayoría de los casos de compromiso gástrico localizado quizás se resuelvan con el tratamiento de la infección por Helicobacter pylori.[83,84] Después de administrar regímenes estándar con antibióticos, se observó en la endoscopia resolución del tejido linfoide asociado a mucosa (TLAM) gástrica en un 50 % de los pacientes al cabo de 3 meses. Es posible que otros pacientes se curen después de 12 a 18 meses de observación. Tras una mediana de seguimiento de 5 años, entre los pacientes que logran una remisión completa, el 30 % tienen monoclonalidad asociada con un reordenamiento de la cadena pesada de las inmunoglobulinas detectada en biopsias de estómago.[85] Se desconocen las implicaciones clínicas de este hallazgo. La translocación t(11;18) en pacientes con TLAM gástrica predice una respuesta precaria al tratamiento antibiótico, pruebas negativas para la infección por H. pylori y respuesta precaria a la quimioterapia con alquilantes orales.[86-88] Fue posible seguir con éxito a los pacientes asintomáticos estables que reiteradamente obtienen resultados positivos en las biopsias mediante el abordaje de observación cautelosa hasta el momento que progresa la enfermedad.[84] Los pacientes con progresión de la enfermedad se tratan con radioterapia,[89-93] rituximab,[94] cirugía (gastrectomía total o gastrectomía parcial y radioterapia),[95] quimioterapia,[96] o terapia de modalidad combinada.[97] El uso de ecografía endoscópica quizás sirva para el seguimiento médico de las respuestas en estos pacientes.[98] En 4 series de casos que incluyeron a más de 100 pacientes con LDCBG en estadio IE o IIE con linfoma de TLAM gástrica o sin este (positivo para H. pylori) se notificaron remisiones completas duraderas en más del 50 % de los pacientes después del tratamiento del H. pylori.[99-102]
Tejido linfoide asociado a mucosa extragástrica
El compromiso localizado de otros sitios se puede tratar con radiación o cirugía.[90-92,103-106] En algunas series, los pacientes con tejido linfoide asociado a mucosa (TLAM) extragástrica tienen una tasa de recaída más alta que los pacientes con TLAM gástrica, y presentan recaídas después de muchos años, incluso décadas.[107] La mayoría de estas recidivas comprometen sitios de TLAM diferentes a la ubicación original.[108] Cuando se disemina a los ganglios linfáticos, la médula ósea o la sangre, esta entidad se comporta como otros linfomas de grado bajo.[109,110] En un ensayo prospectivo aleatorizado de 401 pacientes con TLAM extragástrica extraganglionar se comparó el clorambucilo solo versus rituximab y clorambucilo versus rituximab solo.[111] Después de una mediana de seguimiento de 7,4 años, la supervivencia sin complicaciones fue mejor para el grupo de rituximab y clorambucilo (68 %) que para el grupo de rituximab solo (51 %) y el grupo de clorambucilo solo (50 %) (P = 0,0009). No obstante, la tasa de SG a 5 años fue del 90 % en todos los grupos.[111] Para los pacientes con TLAM anexial, la terapia antibiótica con doxiciclina dirigida a Chlamydia psittaci produjo remisiones duraderas para casi la mitad de los pacientes en una revisión de la bibliografía que incluyó a 131 pacientes.[112][Nivel de evidencia C3] Estas reacciones a la doxiciclina se observaron principalmente en ensayos italianos y, con menos frecuencia, en ensayos dirigidos en otros lugares geográficos.[113] Los linfomas de células B grandes de sitios de TLAM se clasifican y se tratan como linfomas difusos de células B grandes.[114] En una revisión retrospectiva numerosa de casos primarios de TLAM de anejos oculares, se encontró que después de 10 años de seguimiento, el 4 % de los pacientes en estadio I tratados con radioterapia presentaron una transformación a un LDCBG, y el 3 % presentaron compromiso del SNC.[115]
Linfoma ganglionar de zona marginal
Los pacientes con linfoma ganglionar de zona marginal (linfoma de células B monocitoides) se tratan con el mismo modelo de observación cautelosa o tratamiento descrito para el linfoma folicular.[116] Al igual que los pacientes de linfoma folicular, los pacientes con PDE24 que tuvieron que comenzar la terapia presentaron un pronóstico más precario (tasa de SG a 3 años de 53 %) que los pacientes sin PDE24 (tasa de SG a 3 años de 95 %).[117] Entre los pacientes con infección simultánea por el virus de la hepatitis C (VHC), entre un 40 % y un 60 % logran una remisión completa o parcial cuando ya no se detecta el ARN del VHC, gracias al tratamiento antivírico.[118,119][Nivel de evidencia C3]
Linfoma abdominal mediterráneo
La enfermedad conocida por varios nombres como linfoma abdominal mediterráneo, enfermedad de cadena pesada o EIPID, que se presenta en adultos jóvenes en los países del Mediterráneo oriental, es otra versión del linfoma TLAM que responde a antibióticos en estadios tempranos.[120] Se identificó que Campylobacter jejuni es una de las especies bacterianas relacionadas con la EIPID y que el tratamiento antibiótico quizás produzca remisión de la enfermedad.[121]
Linfoma esplénico de zona marginal
El linfoma esplénico de zona marginal es un linfoma de crecimiento lento que se caracteriza por esplenomegalia masiva y compromiso de sangre periférica y médula ósea, por lo general, sin adenopatías.[122,123] Este tipo de linfoma también se conoce como linfoma esplénico con linfocitos vellosos. La esplenectomía a veces produce remisión prolongada.[124,125]
El tratamiento es similar al de otros linfomas de grado bajo y por lo general incluye rituximab solo o rituximab en combinación con análogos de las purinas o quimioterapia con alquilantes.[126] El linfoma esplénico de zona marginal no responde tan bien a la quimioterapia, que por lo común es eficaz para la leucemia linfocítica crónica.[122,126,127] En algunos pocos pacientes con linfoma esplénico de zona marginal (linfoma esplénico con linfocitos vellosos) e infección simultánea por el virus de la hepatitis C (VHC), la mayoría logran una remisión completa o parcial cuando ya no se detecta el ARN del VHC, mediante el tratamiento con interferón-α, con ribavirina o sin esta.[118,128]; [129][Nivel de evidencia C3] En contraste, no se observaron respuestas al interferón en 6 pacientes sin infección por el VHC.
Linfoma anaplásico de células grandes de tipo cutáneo primario
El linfoma anaplásico de células grandes de tipo cutáneo primario se presenta solo en la piel de pacientes sin antecedentes de enfermedad linfoproliferativa ni sitios de compromiso extracutáneo.[130-132] Este tipo de linfoma se manifiesta con variantes que abarcan desde una papulosis linfomatoide clínicamente benigna caracterizada por nódulos localizados que a veces desaparecen solos, hasta una enfermedad progresiva y sistémica que exige la administración de quimioterapia combinada intensiva a base de doxorrubicina. El conjunto de estas afecciones se denominan trastorno linfoproliferativo de células T CD30+ de tipo cutáneo primario.
Los pacientes con enfermedad localizada por lo general se someten a radioterapia. Cuando hay compromiso por diseminación, se utiliza la observación cautelosa o quimioterapia combinada a base de doxorrubicina.[130-132]
Para obtener más información, consultar Tratamiento de la leucemia linfocítica crónica, Tratamiento de la micosis fungoide (incluso el síndrome de Sézary), Tratamiento de la leucemia de células pilosas y Tratamiento del linfoma de Hodgkin.
Bibliografía
- Armitage JO, Weisenburger DD: New approach to classifying non-Hodgkin's lymphomas: clinical features of the major histologic subtypes. Non-Hodgkin's Lymphoma Classification Project. J Clin Oncol 16 (8): 2780-95, 1998. [PUBMED Abstract]
- A clinical evaluation of the International Lymphoma Study Group classification of non-Hodgkin's lymphoma. The Non-Hodgkin's Lymphoma Classification Project. Blood 89 (11): 3909-18, 1997. [PUBMED Abstract]
- Society for Hematopathology Program: Society for Hematopathology Program. Am J Surg Pathol 21 (1): 114-121, 1997.
- López-Guillermo A, Cabanillas F, McDonnell TI, et al.: Correlation of bcl-2 rearrangement with clinical characteristics and outcome in indolent follicular lymphoma. Blood 93 (9): 3081-7, 1999. [PUBMED Abstract]
- Peterson BA, Petroni GR, Frizzera G, et al.: Prolonged single-agent versus combination chemotherapy in indolent follicular lymphomas: a study of the cancer and leukemia group B. J Clin Oncol 21 (1): 5-15, 2003. [PUBMED Abstract]
- Swenson WT, Wooldridge JE, Lynch CF, et al.: Improved survival of follicular lymphoma patients in the United States. J Clin Oncol 23 (22): 5019-26, 2005. [PUBMED Abstract]
- Liu Q, Fayad L, Cabanillas F, et al.: Improvement of overall and failure-free survival in stage IV follicular lymphoma: 25 years of treatment experience at The University of Texas M.D. Anderson Cancer Center. J Clin Oncol 24 (10): 1582-9, 2006. [PUBMED Abstract]
- Kahl BS, Yang DT: Follicular lymphoma: evolving therapeutic strategies. Blood 127 (17): 2055-63, 2016. [PUBMED Abstract]
- Ardeshna KM, Smith P, Norton A, et al.: Long-term effect of a watch and wait policy versus immediate systemic treatment for asymptomatic advanced-stage non-Hodgkin lymphoma: a randomised controlled trial. Lancet 362 (9383): 516-22, 2003. [PUBMED Abstract]
- Armitage JO, Longo DL: Is watch and wait still acceptable for patients with low-grade follicular lymphoma? Blood 127 (23): 2804-8, 2016. [PUBMED Abstract]
- Solal-Céligny P, Roy P, Colombat P, et al.: Follicular lymphoma international prognostic index. Blood 104 (5): 1258-65, 2004. [PUBMED Abstract]
- Perea G, Altés A, Montoto S, et al.: Prognostic indexes in follicular lymphoma: a comparison of different prognostic systems. Ann Oncol 16 (9): 1508-13, 2005. [PUBMED Abstract]
- Buske C, Hoster E, Dreyling M, et al.: The Follicular Lymphoma International Prognostic Index (FLIPI) separates high-risk from intermediate- or low-risk patients with advanced-stage follicular lymphoma treated front-line with rituximab and the combination of cyclophosphamide, doxorubicin, vincristine, and prednisone (R-CHOP) with respect to treatment outcome. Blood 108 (5): 1504-8, 2006. [PUBMED Abstract]
- Federico M, Bellei M, Marcheselli L, et al.: Follicular lymphoma international prognostic index 2: a new prognostic index for follicular lymphoma developed by the international follicular lymphoma prognostic factor project. J Clin Oncol 27 (27): 4555-62, 2009. [PUBMED Abstract]
- Bachy E, Maurer MJ, Habermann TM, et al.: A simplified scoring system in de novo follicular lymphoma treated initially with immunochemotherapy. Blood 132 (1): 49-58, 2018. [PUBMED Abstract]
- Mir F, Mattiello F, Grigg A, et al.: Follicular Lymphoma Evaluation Index (FLEX): A new clinical prognostic model that is superior to existing risk scores for predicting progression-free survival and early treatment failure after frontline immunochemotherapy. Am J Hematol 95 (12): 1503-1510, 2020. [PUBMED Abstract]
- Casulo C, Byrtek M, Dawson KL, et al.: Early Relapse of Follicular Lymphoma After Rituximab Plus Cyclophosphamide, Doxorubicin, Vincristine, and Prednisone Defines Patients at High Risk for Death: An Analysis From the National LymphoCare Study. J Clin Oncol 33 (23): 2516-22, 2015. [PUBMED Abstract]
- Shi Q, Flowers CR, Hiddemann W, et al.: Thirty-Month Complete Response as a Surrogate End Point in First-Line Follicular Lymphoma Therapy: An Individual Patient-Level Analysis of Multiple Randomized Trials. J Clin Oncol 35 (5): 552-560, 2017. [PUBMED Abstract]
- Casulo C, Dixon JG, Le-Rademacher J, et al.: Validation of POD24 as a robust early clinical end point of poor survival in FL from 5225 patients on 13 clinical trials. Blood 139 (11): 1684-1693, 2022. [PUBMED Abstract]
- Freeman CL, Kridel R, Moccia AA, et al.: Early progression after bendamustine-rituximab is associated with high risk of transformation in advanced stage follicular lymphoma. Blood 134 (9): 761-764, 2019. [PUBMED Abstract]
- Brice P, Bastion Y, Lepage E, et al.: Comparison in low-tumor-burden follicular lymphomas between an initial no-treatment policy, prednimustine, or interferon alfa: a randomized study from the Groupe d'Etude des Lymphomes Folliculaires. Groupe d'Etude des Lymphomes de l'Adulte. J Clin Oncol 15 (3): 1110-7, 1997. [PUBMED Abstract]
- Young RC, Longo DL, Glatstein E, et al.: The treatment of indolent lymphomas: watchful waiting v aggressive combined modality treatment. Semin Hematol 25 (2 Suppl 2): 11-6, 1988. [PUBMED Abstract]
- Luminari S, Ferrari A, Manni M, et al.: Long-Term Results of the FOLL05 Trial Comparing R-CVP Versus R-CHOP Versus R-FM for the Initial Treatment of Patients With Advanced-Stage Symptomatic Follicular Lymphoma. J Clin Oncol 36 (7): 689-696, 2018. [PUBMED Abstract]
- Lockmer S, Østenstad B, Hagberg H, et al.: Chemotherapy-Free Initial Treatment of Advanced Indolent Lymphoma Has Durable Effect With Low Toxicity: Results From Two Nordic Lymphoma Group Trials With More Than 10 Years of Follow-Up. J Clin Oncol : JCO1800262, 2018. [PUBMED Abstract]
- Morschhauser F, Fowler NH, Feugier P, et al.: Rituximab plus Lenalidomide in Advanced Untreated Follicular Lymphoma. N Engl J Med 379 (10): 934-947, 2018. [PUBMED Abstract]
- Leonard JP, Trnený M, Izutsu K, et al.: Augment: a phase III randomized study of lenalidomide Plus rituximab (R2) vs rituximab/placebo in patients with relapsed/refractory indolent non-Hodgkin lymphoma. [Abstract] Blood 132 (Suppl 1): A-445, 2018.
- Zucca E, Rondeau S, Vanazzi A, et al.: Short regimen of rituximab plus lenalidomide in follicular lymphoma patients in need of first-line therapy. Blood 134 (4): 353-362, 2019. [PUBMED Abstract]
- Marcus R, Davies A, Ando K, et al.: Obinutuzumab for the First-Line Treatment of Follicular Lymphoma. N Engl J Med 377 (14): 1331-1344, 2017. [PUBMED Abstract]
- Dreyling M, Santoro A, Mollica L, et al.: Phosphatidylinositol 3-Kinase Inhibition by Copanlisib in Relapsed or Refractory Indolent Lymphoma. J Clin Oncol 35 (35): 3898-3905, 2017. [PUBMED Abstract]
- Jacobson CA, Chavez JC, Sehgal AR, et al.: Axicabtagene ciloleucel in relapsed or refractory indolent non-Hodgkin lymphoma (ZUMA-5): a single-arm, multicentre, phase 2 trial. Lancet Oncol 23 (1): 91-103, 2022. [PUBMED Abstract]
- Bartlett NL, Sehn LH, Matasar MJ, et al.: Mosunetuzumab monotherapy demonstrates durable efficacy with a manageable safety profile in patients with relapsed/refractory follicular lymphoma who received ≥2 prior therapies: updated results from a pivotal phase II study. [Abstract] Blood 140 (Suppl 1): A-610, 1467-70, 2022.
- Schaaf M, Reiser M, Borchmann P, et al.: High-dose therapy with autologous stem cell transplantation versus chemotherapy or immuno-chemotherapy for follicular lymphoma in adults. Cochrane Database Syst Rev 1: CD007678, 2012. [PUBMED Abstract]
- Schmatz AI, Streubel B, Kretschmer-Chott E, et al.: Primary follicular lymphoma of the duodenum is a distinct mucosal/submucosal variant of follicular lymphoma: a retrospective study of 63 cases. J Clin Oncol 29 (11): 1445-51, 2011. [PUBMED Abstract]
- Jegalian AG, Eberle FC, Pack SD, et al.: Follicular lymphoma in situ: clinical implications and comparisons with partial involvement by follicular lymphoma. Blood 118 (11): 2976-84, 2011. [PUBMED Abstract]
- Louissaint A, Ackerman AM, Dias-Santagata D, et al.: Pediatric-type nodal follicular lymphoma: an indolent clonal proliferation in children and adults with high proliferation index and no BCL2 rearrangement. Blood 120 (12): 2395-404, 2012. [PUBMED Abstract]
- Sarkozy C, Trneny M, Xerri L, et al.: Risk Factors and Outcomes for Patients With Follicular Lymphoma Who Had Histologic Transformation After Response to First-Line Immunochemotherapy in the PRIMA Trial. J Clin Oncol 34 (22): 2575-82, 2016. [PUBMED Abstract]
- Tsimberidou AM, O'Brien S, Khouri I, et al.: Clinical outcomes and prognostic factors in patients with Richter's syndrome treated with chemotherapy or chemoimmunotherapy with or without stem-cell transplantation. J Clin Oncol 24 (15): 2343-51, 2006. [PUBMED Abstract]
- Montoto S, Davies AJ, Matthews J, et al.: Risk and clinical implications of transformation of follicular lymphoma to diffuse large B-cell lymphoma. J Clin Oncol 25 (17): 2426-33, 2007. [PUBMED Abstract]
- Villa D, Crump M, Panzarella T, et al.: Autologous and allogeneic stem-cell transplantation for transformed follicular lymphoma: a report of the Canadian blood and marrow transplant group. J Clin Oncol 31 (9): 1164-71, 2013. [PUBMED Abstract]
- Williams CD, Harrison CN, Lister TA, et al.: High-dose therapy and autologous stem-cell support for chemosensitive transformed low-grade follicular non-Hodgkin's lymphoma: a case-matched study from the European Bone Marrow Transplant Registry. J Clin Oncol 19 (3): 727-35, 2001. [PUBMED Abstract]
- Wagner-Johnston ND, Link BK, Byrtek M, et al.: Outcomes of transformed follicular lymphoma in the modern era: a report from the National LymphoCare Study (NLCS). Blood 126 (7): 851-7, 2015. [PUBMED Abstract]
- Leblond V, Kastritis E, Advani R, et al.: Treatment recommendations from the Eighth International Workshop on Waldenström's Macroglobulinemia. Blood 128 (10): 1321-8, 2016. [PUBMED Abstract]
- Treon SP, Xu L, Yang G, et al.: MYD88 L265P somatic mutation in Waldenström's macroglobulinemia. N Engl J Med 367 (9): 826-33, 2012. [PUBMED Abstract]
- Dhodapkar MV, Hoering A, Gertz MA, et al.: Long-term survival in Waldenstrom macroglobulinemia: 10-year follow-up of Southwest Oncology Group-directed intergroup trial S9003. Blood 113 (4): 793-6, 2009. [PUBMED Abstract]
- Ansell SM, Kyle RA, Reeder CB, et al.: Diagnosis and management of Waldenström macroglobulinemia: Mayo stratification of macroglobulinemia and risk-adapted therapy (mSMART) guidelines. Mayo Clin Proc 85 (9): 824-33, 2010. [PUBMED Abstract]
- Kapoor P, Ansell SM, Fonseca R, et al.: Diagnosis and Management of Waldenström Macroglobulinemia: Mayo Stratification of Macroglobulinemia and Risk-Adapted Therapy (mSMART) Guidelines 2016. JAMA Oncol 3 (9): 1257-1265, 2017. [PUBMED Abstract]
- Dimopoulos MA, Kastritis E: How I treat Waldenström macroglobulinemia. Blood 134 (23): 2022-2035, 2019. [PUBMED Abstract]
- Gertz MA: Waldenstrom Macroglobulinemia: Tailoring Therapy for the Individual. J Clin Oncol 40 (23): 2600-2608, 2022. [PUBMED Abstract]
- Röth A, Berentsen S, Barcellini W, et al.: Sutimlimab in patients with cold agglutinin disease: results of the randomized placebo-controlled phase 3 CADENZA trial. Blood 140 (9): 980-991, 2022. [PUBMED Abstract]
- Gertz MA, Anagnostopoulos A, Anderson K, et al.: Treatment recommendations in Waldenstrom's macroglobulinemia: consensus panel recommendations from the Second International Workshop on Waldenstrom's Macroglobulinemia. Semin Oncol 30 (2): 121-6, 2003. [PUBMED Abstract]
- Dimopoulos MA, Anagnostopoulos A, Kyrtsonis MC, et al.: Primary treatment of Waldenström macroglobulinemia with dexamethasone, rituximab, and cyclophosphamide. J Clin Oncol 25 (22): 3344-9, 2007. [PUBMED Abstract]
- Treon SP, Branagan AR, Ioakimidis L, et al.: Long-term outcomes to fludarabine and rituximab in Waldenström macroglobulinemia. Blood 113 (16): 3673-8, 2009. [PUBMED Abstract]
- Leblond V, Johnson S, Chevret S, et al.: Results of a randomized trial of chlorambucil versus fludarabine for patients with untreated Waldenström macroglobulinemia, marginal zone lymphoma, or lymphoplasmacytic lymphoma. J Clin Oncol 31 (3): 301-7, 2013. [PUBMED Abstract]
- Buske C, Tedeschi A, Trotman J, et al.: Ibrutinib Plus Rituximab Versus Placebo Plus Rituximab for Waldenström's Macroglobulinemia: Final Analysis From the Randomized Phase III iNNOVATE Study. J Clin Oncol 40 (1): 52-62, 2022. [PUBMED Abstract]
- Tam CS, Opat S, D'Sa S, et al.: A randomized phase 3 trial of zanubrutinib vs ibrutinib in symptomatic Waldenström macroglobulinemia: the ASPEN study. Blood 136 (18): 2038-2050, 2020. [PUBMED Abstract]
- Jalink M, Berentsen S, Castillo JJ, et al.: Effect of ibrutinib treatment on hemolytic anemia and acrocyanosis in cold agglutinin disease/cold agglutinin syndrome. Blood 138 (20): 2002-2005, 2021. [PUBMED Abstract]
- Dimopoulos MA, Zervas C, Zomas A, et al.: Treatment of Waldenström's macroglobulinemia with rituximab. J Clin Oncol 20 (9): 2327-33, 2002. [PUBMED Abstract]
- Treon SP, Branagan AR, Hunter Z, et al.: Paradoxical increases in serum IgM and viscosity levels following rituximab in Waldenstrom's macroglobulinemia. Ann Oncol 15 (10): 1481-3, 2004. [PUBMED Abstract]
- Dimopoulos MA, Chen C, Kastritis E, et al.: Bortezomib as a treatment option in patients with Waldenström macroglobulinemia. Clin Lymphoma Myeloma Leuk 10 (2): 110-7, 2010. [PUBMED Abstract]
- Gavriatopoulou M, García-Sanz R, Kastritis E, et al.: BDR in newly diagnosed patients with WM: final analysis of a phase 2 study after a minimum follow-up of 6 years. Blood 129 (4): 456-459, 2017. [PUBMED Abstract]
- Kersten MJ, Amaador K, Minnema MC, et al.: Combining Ixazomib With Subcutaneous Rituximab and Dexamethasone in Relapsed or Refractory Waldenström's Macroglobulinemia: Final Analysis of the Phase I/II HOVON124/ECWM-R2 Study. J Clin Oncol 40 (1): 40-51, 2022. [PUBMED Abstract]
- Treon SP, Ioakimidis L, Soumerai JD, et al.: Primary therapy of Waldenström macroglobulinemia with bortezomib, dexamethasone, and rituximab: WMCTG clinical trial 05-180. J Clin Oncol 27 (23): 3830-5, 2009. [PUBMED Abstract]
- Dimopoulos MA, García-Sanz R, Gavriatopoulou M, et al.: Primary therapy of Waldenstrom macroglobulinemia (WM) with weekly bortezomib, low-dose dexamethasone, and rituximab (BDR): long-term results of a phase 2 study of the European Myeloma Network (EMN). Blood 122 (19): 3276-82, 2013. [PUBMED Abstract]
- Treon SP, Tripsas CK, Meid K, et al.: Carfilzomib, rituximab, and dexamethasone (CaRD) treatment offers a neuropathy-sparing approach for treating Waldenström's macroglobulinemia. Blood 124 (4): 503-10, 2014. [PUBMED Abstract]
- Dimopoulos MA, Alexanian R: Waldenstrom's macroglobulinemia. Blood 83 (6): 1452-9, 1994. [PUBMED Abstract]
- Laszlo D, Andreola G, Rigacci L, et al.: Rituximab and subcutaneous 2-chloro-2'-deoxyadenosine combination treatment for patients with Waldenstrom macroglobulinemia: clinical and biologic results of a phase II multicenter study. J Clin Oncol 28 (13): 2233-8, 2010. [PUBMED Abstract]
- García-Sanz R, Montoto S, Torrequebrada A, et al.: Waldenström macroglobulinaemia: presenting features and outcome in a series with 217 cases. Br J Haematol 115 (3): 575-82, 2001. [PUBMED Abstract]
- Buske C, Hoster E, Dreyling M, et al.: The addition of rituximab to front-line therapy with CHOP (R-CHOP) results in a higher response rate and longer time to treatment failure in patients with lymphoplasmacytic lymphoma: results of a randomized trial of the German Low-Grade Lymphoma Study Group (GLSG). Leukemia 23 (1): 153-61, 2009. [PUBMED Abstract]
- Ghobrial IM, Hong F, Padmanabhan S, et al.: Phase II trial of weekly bortezomib in combination with rituximab in relapsed or relapsed and refractory Waldenstrom macroglobulinemia. J Clin Oncol 28 (8): 1422-8, 2010. [PUBMED Abstract]
- Rummel MJ, Niederle N, Maschmeyer G, et al.: Bendamustine plus rituximab versus CHOP plus rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: an open-label, multicentre, randomised, phase 3 non-inferiority trial. Lancet 381 (9873): 1203-10, 2013. [PUBMED Abstract]
- Castillo JJ, Allan JN, Siddiqi T, et al.: Venetoclax in Previously Treated Waldenström Macroglobulinemia. J Clin Oncol 40 (1): 63-71, 2022. [PUBMED Abstract]
- Castillo JJ, Itchaki G, Paludo J, et al.: Ibrutinib for the treatment of Bing-Neel syndrome: a multicenter study. Blood 133 (4): 299-305, 2019. [PUBMED Abstract]
- Dreger P, Glass B, Kuse R, et al.: Myeloablative radiochemotherapy followed by reinfusion of purged autologous stem cells for Waldenström's macroglobulinaemia. Br J Haematol 106 (1): 115-8, 1999. [PUBMED Abstract]
- Desikan R, Dhodapkar M, Siegel D, et al.: High-dose therapy with autologous haemopoietic stem cell support for Waldenström's macroglobulinaemia. Br J Haematol 105 (4): 993-6, 1999. [PUBMED Abstract]
- Martin P, Chadburn A, Christos P, et al.: Intensive treatment strategies may not provide superior outcomes in mantle cell lymphoma: overall survival exceeding 7 years with standard therapies. Ann Oncol 19 (7): 1327-30, 2008. [PUBMED Abstract]
- Kyriakou C, Canals C, Cornelissen JJ, et al.: Allogeneic stem-cell transplantation in patients with Waldenström macroglobulinemia: report from the Lymphoma Working Party of the European Group for Blood and Marrow Transplantation. J Clin Oncol 28 (33): 4926-34, 2010. [PUBMED Abstract]
- Leleu X, Soumerai J, Roccaro A, et al.: Increased incidence of transformation and myelodysplasia/acute leukemia in patients with Waldenström macroglobulinemia treated with nucleoside analogs. J Clin Oncol 27 (2): 250-5, 2009. [PUBMED Abstract]
- Leblond V, Lévy V, Maloisel F, et al.: Multicenter, randomized comparative trial of fludarabine and the combination of cyclophosphamide-doxorubicin-prednisone in 92 patients with Waldenström macroglobulinemia in first relapse or with primary refractory disease. Blood 98 (9): 2640-4, 2001. [PUBMED Abstract]
- Zucca E, Bertoni F: The spectrum of MALT lymphoma at different sites: biological and therapeutic relevance. Blood 127 (17): 2082-92, 2016. [PUBMED Abstract]
- Rossi D, Bertoni F, Zucca E: Marginal-Zone Lymphomas. N Engl J Med 386 (6): 568-581, 2022. [PUBMED Abstract]
- Thieblemont C, Cascione L, Conconi A, et al.: A MALT lymphoma prognostic index. Blood 130 (12): 1409-1417, 2017. [PUBMED Abstract]
- Alderuccio JP, Zhao W, Desai A, et al.: Risk Factors for Transformation to Higher-Grade Lymphoma and Its Impact on Survival in a Large Cohort of Patients With Marginal Zone Lymphoma From a Single Institution. J Clin Oncol : JCO1800138, 2018. [PUBMED Abstract]
- Zullo A, Hassan C, Andriani A, et al.: Eradication therapy for Helicobacter pylori in patients with gastric MALT lymphoma: a pooled data analysis. Am J Gastroenterol 104 (8): 1932-7; quiz 1938, 2009. [PUBMED Abstract]
- Nakamura S, Sugiyama T, Matsumoto T, et al.: Long-term clinical outcome of gastric MALT lymphoma after eradication of Helicobacter pylori: a multicentre cohort follow-up study of 420 patients in Japan. Gut 61 (4): 507-13, 2012. [PUBMED Abstract]
- Wündisch T, Thiede C, Morgner A, et al.: Long-term follow-up of gastric MALT lymphoma after Helicobacter pylori eradication. J Clin Oncol 23 (31): 8018-24, 2005. [PUBMED Abstract]
- Ye H, Liu H, Raderer M, et al.: High incidence of t(11;18)(q21;q21) in Helicobacter pylori-negative gastric MALT lymphoma. Blood 101 (7): 2547-50, 2003. [PUBMED Abstract]
- Lévy M, Copie-Bergman C, Gameiro C, et al.: Prognostic value of translocation t(11;18) in tumoral response of low-grade gastric lymphoma of mucosa-associated lymphoid tissue type to oral chemotherapy. J Clin Oncol 23 (22): 5061-6, 2005. [PUBMED Abstract]
- Nakamura S, Ye H, Bacon CM, et al.: Clinical impact of genetic aberrations in gastric MALT lymphoma: a comprehensive analysis using interphase fluorescence in situ hybridisation. Gut 56 (10): 1358-63, 2007. [PUBMED Abstract]
- Schechter NR, Yahalom J: Low-grade MALT lymphoma of the stomach: a review of treatment options. Int J Radiat Oncol Biol Phys 46 (5): 1093-103, 2000. [PUBMED Abstract]
- Tsang RW, Gospodarowicz MK, Pintilie M, et al.: Stage I and II MALT lymphoma: results of treatment with radiotherapy. Int J Radiat Oncol Biol Phys 50 (5): 1258-64, 2001. [PUBMED Abstract]
- Tsang RW, Gospodarowicz MK, Pintilie M, et al.: Localized mucosa-associated lymphoid tissue lymphoma treated with radiation therapy has excellent clinical outcome. J Clin Oncol 21 (22): 4157-64, 2003. [PUBMED Abstract]
- Tsai HK, Li S, Ng AK, et al.: Role of radiation therapy in the treatment of stage I/II mucosa-associated lymphoid tissue lymphoma. Ann Oncol 18 (4): 672-8, 2007. [PUBMED Abstract]
- De Leo AN, Bates JE, Lockney NA, et al.: Radiotherapy in Early-stage Gastric MALT: Improved Survival Without Increased Cardiac Death. Am J Clin Oncol 43 (11): 770-775, 2020. [PUBMED Abstract]
- Martinelli G, Laszlo D, Ferreri AJ, et al.: Clinical activity of rituximab in gastric marginal zone non-Hodgkin's lymphoma resistant to or not eligible for anti-Helicobacter pylori therapy. J Clin Oncol 23 (9): 1979-83, 2005. [PUBMED Abstract]
- Cogliatti SB, Schmid U, Schumacher U, et al.: Primary B-cell gastric lymphoma: a clinicopathological study of 145 patients. Gastroenterology 101 (5): 1159-70, 1991. [PUBMED Abstract]
- Zinzani PL, Magagnoli M, Galieni P, et al.: Nongastrointestinal low-grade mucosa-associated lymphoid tissue lymphoma: analysis of 75 patients. J Clin Oncol 17 (4): 1254, 1999. [PUBMED Abstract]
- Thieblemont C, Bastion Y, Berger F, et al.: Mucosa-associated lymphoid tissue gastrointestinal and nongastrointestinal lymphoma behavior: analysis of 108 patients. J Clin Oncol 15 (4): 1624-30, 1997. [PUBMED Abstract]
- Pavlick AC, Gerdes H, Portlock CS: Endoscopic ultrasound in the evaluation of gastric small lymphocytic mucosa-associated lymphoid tumors. J Clin Oncol 15 (5): 1761-6, 1997. [PUBMED Abstract]
- Morgner A, Miehlke S, Fischbach W, et al.: Complete remission of primary high-grade B-cell gastric lymphoma after cure of Helicobacter pylori infection. J Clin Oncol 19 (7): 2041-8, 2001. [PUBMED Abstract]
- Chen LT, Lin JT, Shyu RY, et al.: Prospective study of Helicobacter pylori eradication therapy in stage I(E) high-grade mucosa-associated lymphoid tissue lymphoma of the stomach. J Clin Oncol 19 (22): 4245-51, 2001. [PUBMED Abstract]
- Chen LT, Lin JT, Tai JJ, et al.: Long-term results of anti-Helicobacter pylori therapy in early-stage gastric high-grade transformed MALT lymphoma. J Natl Cancer Inst 97 (18): 1345-53, 2005. [PUBMED Abstract]
- Kuo SH, Yeh KH, Wu MS, et al.: Helicobacter pylori eradication therapy is effective in the treatment of early-stage H pylori-positive gastric diffuse large B-cell lymphomas. Blood 119 (21): 4838-44; quiz 5057, 2012. [PUBMED Abstract]
- Uno T, Isobe K, Shikama N, et al.: Radiotherapy for extranodal, marginal zone, B-cell lymphoma of mucosa-associated lymphoid tissue originating in the ocular adnexa: a multiinstitutional, retrospective review of 50 patients. Cancer 98 (4): 865-71, 2003. [PUBMED Abstract]
- Bayraktar S, Bayraktar UD, Stefanovic A, et al.: Primary ocular adnexal mucosa-associated lymphoid tissue lymphoma (MALT): single institution experience in a large cohort of patients. Br J Haematol 152 (1): 72-80, 2011. [PUBMED Abstract]
- Stefanovic A, Lossos IS: Extranodal marginal zone lymphoma of the ocular adnexa. Blood 114 (3): 501-10, 2009. [PUBMED Abstract]
- Vazquez A, Khan MN, Sanghvi S, et al.: Extranodal marginal zone lymphoma of mucosa-associated lymphoid tissue of the salivary glands: a population-based study from 1994 to 2009. Head Neck 37 (1): 18-22, 2015. [PUBMED Abstract]
- Raderer M, Streubel B, Woehrer S, et al.: High relapse rate in patients with MALT lymphoma warrants lifelong follow-up. Clin Cancer Res 11 (9): 3349-52, 2005. [PUBMED Abstract]
- Sretenovic M, Colovic M, Jankovic G, et al.: More than a third of non-gastric malt lymphomas are disseminated at diagnosis: a single center survey. Eur J Haematol 82 (5): 373-80, 2009. [PUBMED Abstract]
- Nathwani BN, Drachenberg MR, Hernandez AM, et al.: Nodal monocytoid B-cell lymphoma (nodal marginal-zone B-cell lymphoma). Semin Hematol 36 (2): 128-38, 1999. [PUBMED Abstract]
- Raderer M, Wöhrer S, Streubel B, et al.: Assessment of disease dissemination in gastric compared with extragastric mucosa-associated lymphoid tissue lymphoma using extensive staging: a single-center experience. J Clin Oncol 24 (19): 3136-41, 2006. [PUBMED Abstract]
- Zucca E, Conconi A, Martinelli G, et al.: Final Results of the IELSG-19 Randomized Trial of Mucosa-Associated Lymphoid Tissue Lymphoma: Improved Event-Free and Progression-Free Survival With Rituximab Plus Chlorambucil Versus Either Chlorambucil or Rituximab Monotherapy. J Clin Oncol 35 (17): 1905-1912, 2017. [PUBMED Abstract]
- Kiesewetter B, Raderer M: Antibiotic therapy in nongastrointestinal MALT lymphoma: a review of the literature. Blood 122 (8): 1350-7, 2013. [PUBMED Abstract]
- Grünberger B, Hauff W, Lukas J, et al.: 'Blind' antibiotic treatment targeting Chlamydia is not effective in patients with MALT lymphoma of the ocular adnexa. Ann Oncol 17 (3): 484-7, 2006. [PUBMED Abstract]
- Kuo SH, Chen LT, Yeh KH, et al.: Nuclear expression of BCL10 or nuclear factor kappa B predicts Helicobacter pylori-independent status of early-stage, high-grade gastric mucosa-associated lymphoid tissue lymphomas. J Clin Oncol 22 (17): 3491-7, 2004. [PUBMED Abstract]
- Desai A, Joag MG, Lekakis L, et al.: Long-term course of patients with primary ocular adnexal MALT lymphoma: a large single-institution cohort study. Blood 129 (3): 324-332, 2017. [PUBMED Abstract]
- Thieblemont C, Molina T, Davi F: Optimizing therapy for nodal marginal zone lymphoma. Blood 127 (17): 2064-71, 2016. [PUBMED Abstract]
- Luminari S, Merli M, Rattotti S, et al.: Early progression as a predictor of survival in marginal zone lymphomas: an analysis from the FIL-NF10 study. Blood 134 (10): 798-801, 2019. [PUBMED Abstract]
- Vallisa D, Bernuzzi P, Arcaini L, et al.: Role of anti-hepatitis C virus (HCV) treatment in HCV-related, low-grade, B-cell, non-Hodgkin's lymphoma: a multicenter Italian experience. J Clin Oncol 23 (3): 468-73, 2005. [PUBMED Abstract]
- Merli M, Rattotti S, Spina M, et al.: Direct-Acting Antivirals as Primary Treatment for Hepatitis C Virus-Associated Indolent Non-Hodgkin Lymphomas: The BArT Study of the Fondazione Italiana Linfomi. J Clin Oncol 40 (35): 4060-4070, 2022. [PUBMED Abstract]
- Isaacson PG: Gastrointestinal lymphoma. Hum Pathol 25 (10): 1020-9, 1994. [PUBMED Abstract]
- Lecuit M, Abachin E, Martin A, et al.: Immunoproliferative small intestinal disease associated with Campylobacter jejuni. N Engl J Med 350 (3): 239-48, 2004. [PUBMED Abstract]
- Arcaini L, Paulli M, Boveri E, et al.: Splenic and nodal marginal zone lymphomas are indolent disorders at high hepatitis C virus seroprevalence with distinct presenting features but similar morphologic and phenotypic profiles. Cancer 100 (1): 107-15, 2004. [PUBMED Abstract]
- Arcaini L, Rossi D, Paulli M: Splenic marginal zone lymphoma: from genetics to management. Blood 127 (17): 2072-81, 2016. [PUBMED Abstract]
- Bertoni F, Zucca E: State-of-the-art therapeutics: marginal-zone lymphoma. J Clin Oncol 23 (26): 6415-20, 2005. [PUBMED Abstract]
- Parry-Jones N, Matutes E, Gruszka-Westwood AM, et al.: Prognostic features of splenic lymphoma with villous lymphocytes: a report on 129 patients. Br J Haematol 120 (5): 759-64, 2003. [PUBMED Abstract]
- Arcaini L, Lazzarino M, Colombo N, et al.: Splenic marginal zone lymphoma: a prognostic model for clinical use. Blood 107 (12): 4643-9, 2006. [PUBMED Abstract]
- Iannitto E, Ambrosetti A, Ammatuna E, et al.: Splenic marginal zone lymphoma with or without villous lymphocytes. Hematologic findings and outcomes in a series of 57 patients. Cancer 101 (9): 2050-7, 2004. [PUBMED Abstract]
- Hermine O, Lefrère F, Bronowicki JP, et al.: Regression of splenic lymphoma with villous lymphocytes after treatment of hepatitis C virus infection. N Engl J Med 347 (2): 89-94, 2002. [PUBMED Abstract]
- Kelaidi C, Rollot F, Park S, et al.: Response to antiviral treatment in hepatitis C virus-associated marginal zone lymphomas. Leukemia 18 (10): 1711-6, 2004. [PUBMED Abstract]
- de Bruin PC, Beljaards RC, van Heerde P, et al.: Differences in clinical behaviour and immunophenotype between primary cutaneous and primary nodal anaplastic large cell lymphoma of T-cell or null cell phenotype. Histopathology 23 (2): 127-35, 1993. [PUBMED Abstract]
- Willemze R, Beljaards RC: Spectrum of primary cutaneous CD30 (Ki-1)-positive lymphoproliferative disorders. A proposal for classification and guidelines for management and treatment. J Am Acad Dermatol 28 (6): 973-80, 1993. [PUBMED Abstract]
- Kempf W, Pfaltz K, Vermeer MH, et al.: EORTC, ISCL, and USCLC consensus recommendations for the treatment of primary cutaneous CD30-positive lymphoproliferative disorders: lymphomatoid papulosis and primary cutaneous anaplastic large-cell lymphoma. Blood 118 (15): 4024-35, 2011. [PUBMED Abstract]
Linfoma no Hodgkin de crecimiento rápido
El linfoma no Hodgkin (LNH) de crecimiento rápido incluye los siguientes subtipos:
- Linfoma difuso de células B grandes.
- Linfoma mediastínico de células B grandes (linfoma mediastínico primario de células B grandes).
- Linfoma folicular de células grandes.
- Linfoma anaplásico de células grandes.
- Linfoma extraganglionar de células T o de células NK.
- Granulomatosis linfomatoide.
- Linfoma angioinmunoblástico de células T.
- Linfoma de células T periféricas.
- Linfoma intestinal de células T de tipo enteropático.
- Linfoma intravascular de células B grandes (linfomatosis intravascular).
- Linfoma de Burkitt o linfoma de células pequeñas no hendidas.
- Linfoma linfoblástico.
- Leucemia de células T o linfoma de células T en adultos.
- Linfoma de células de manto.
- Trastorno linfoproliferativo postrasplante polimórfico.
- Linfoma histiocítico verdadero.
- Linfoma de efusión primaria.
- Linfoma plasmoblástico.
Linfoma difuso de células B grandes
El linfoma difuso de células B grandes (LDCBG) es el tipo de LNH más común y comprende el 30 % de los casos recién diagnosticados.[1] La mayoría de los pacientes presentan masas que crecen rápido, a menudo con síntomas locales y sistémicos (designados como síntomas B, con fiebre, sudores nocturnos o pérdida de peso). Para obtener más información sobre la pérdida de peso, consultar La nutrición en el tratamiento del cáncer.
Algunos casos de linfoma de células B grandes tienen un fondo de células T reactivas y a menudo histiocitos, en este caso se denomina linfoma de células T y de células B grandes rico en histiocitos. Este subtipo de linfoma de células grandes a menudo compromete el hígado, el bazo y la médula ósea; sin embargo, el desenlace es equivalente al de pacientes con LDCBG en estadios similares.[2-4] En el momento del diagnóstico, algunos pacientes con LDCBG presentan de manera simultánea un componente de células B pequeñas de escasa malignidad; si bien la supervivencia general (SG) es similar después de la quimioterapia multifarmacológica, hay un riesgo más alto de recaída de enfermedad con escasa malignidad.[5]
Pronóstico
La mayoría de los pacientes con enfermedad localizada se curan con una terapia de modalidad combinada o quimioterapia combinada sola.[6] Entre los pacientes con enfermedad en estadio avanzado, el 50 % se curan con quimioterapia combinada a base de doxorrubicina y rituximab, por lo general, R-CHOP (rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona).[7-9]
En el National Comprehensive Cancer Network International Prognostic Index (IPI) para el LNH de crecimiento rápido (linfoma difuso de células grades) se incluyen los siguientes 5 factores de riesgo significativos para el pronóstico de la SG y los puntajes de riesgo relacionado:[10]
- Edad.
- <40 años: 0.
- 41–60 años: 1.
- 61–75 años: 2.
- >75 años: 3.
- Estadio III/IV: 1.
- Estado funcional 2, 3 o 4: 1.
- Concentración sérica de lactato-deshidrogenasa (LDH).
- Normalizada: 0.
- >1x–3x: 1.
- >3x: 2.
- Número de sitios extraganglionares ≥2: 1.
Puntaje de riesgo:
- Bajo (0 o 1): tasa de SG a 5 años de 96 %; tasa de supervivencia sin progresión (SSP) de 91 %.
- Intermedio bajo (2 o 3): tasa de SG a 5 años de 82 %; tasa de SSP de 74 %.
- Intermedio alto (4 o 5): tasa de SG a 5 años de 64 %; tasa de SSP de 51 %.
- Alto (>6): tasa de SG a 5 años de 33 %; tasa de SSP de 30 %.
Se utilizan modificaciones del IPI ajustadas por edad y estadio para los pacientes más jóvenes con enfermedad localizada.[11] Según parece, los intervalos de tiempo más cortos entre el diagnóstico y el tratamiento son marcadores indirectos de factores biológicos de pronóstico precario.[12]
La identificación de reordenamientos de los genes BCL2 y MYC, una sobreexpresión dual del gen MYC, o ambos, confieren un pronóstico particularmente desfavorable.[13-15] En este grupo de pacientes de riesgo alto se explora el uso de las terapias de dosis intensivas, las terapias de infusión, y la consolidación con trasplante de células madre (TCM).[16,17] En un análisis retrospectivo, se evaluaron 159 pacientes de LDCBG sin tratamiento previo sometidos a pruebas genéticas para detectar mutación doble (double-hit) mediante hibridación fluorescente in situ (FISH), que lograron una respuesta completa (RC).[18] La terapia de inducción no cambió la tasa de supervivencia sin recaída a 3 años ni la SG cuando se usó un TCM autógeno.
En una revisión retrospectiva con 117 pacientes de LDCBG en recaída o resistente al tratamiento sometidos a TCM autógeno, se encontró que la tasa de SG a 4 años fue del 25 % para los linfomas con mutación doble (reordenamientos de BCL2 y MYC), del 61 % para los linfomas con expresión doble (sin reordenamientos, pero con aumento de la expresión de BCL2 y MYC) y del 70 % para los pacientes sin estas características.[19] Los pacientes en riesgo alto de recaída se consideran aptos para participar en ensayos clínicos.[20]
La obtención de perfiles moleculares de expresión génica mediante micromatrices de ADN quizás sirva en el futuro para ayudar a estratificar a los pacientes en grupos de tratamiento dirigido a dianas específicas y para mejorar la predicción de la supervivencia después de la quimioterapia estándar.[21] Por ejemplo, los linfomas de células B grandes positivos para la cinasa del linfoma anaplásico (ALK) son extremadamente raros y no responden bien al tratamiento convencional con R-CHOP. Se han descrito respuestas anecdóticas a inhibidores de ALK como lorlatinib o alectinib.[22][Nivel de evidencia C3] Es probable que los pacientes de LDCBG con coexpresión de CD20 y CD30 definan un subgrupo con una firma molecular única, un pronóstico más favorable y una posible indicación terapéutica para el uso de una terapia anti-CD30 específica, como brentuximab vedotina.[23] Los pacientes de LDCBG sin complicaciones después de 2 años tienen una SG subsiguiente equivalente a la de la población general emparejada por edad y sexo.[24]
Profilaxis del sistema nervioso central
El CNS-IPI es un instrumento usado para predecir qué pacientes tienen un riesgo mayor del 10 % de recidiva en el sistema nervioso central (SNC). El German Lymphoma Study Group formuló este instrumento y se validó en la base de datos de British Columbia Cancer Agency. Se usó la presencia de 4 a 6 de los factores de riesgo del CNS-IPI (edad >60 años, estado funcional ≥2, concentración elevada de LDH, enfermedad en estadio III o IV, >1 sitio extraganglionar o compromiso renal o suprarrenal) para definir el grupo de riesgo alto para la recaída en el SNC (un riesgo del 12 % de compromiso del SNC al cabo de 2 años).[25]
Por lo general, se recomienda la profilaxis del SNC (a menudo con 4 a 6 dosis de metotrexato intratecal) para los pacientes con compromiso testicular.[26-28][Nivel de evidencia C3] En un análisis retrospectivo de los estudios alemanes RICOVER, se comparó el metotrexato intratecal con la ausencia de profilaxis en los pacientes con LDCBG. Este estudio se llevó a cabo durante la era del tratamiento con R-CHOP. Con la posible excepción de los pacientes con compromiso testicular, el análisis mostró que el metotrexato intratecal no disminuyó el riesgo de enfermedad en el SNC.[29][Nivel de evidencia C3] Algunos médicos emplean dosis altas intravenosas (IV) (a menudo 4 dosis) de metotrexato en lugar del tratamiento intratecal porque esto mejora la administración del fármaco y reduce la morbilidad del paciente.[30] En un estudio retrospectivo se evaluaron 1162 pacientes de 21 centros académicos de los Estados Unidos que recibieron metotrexato, el 77 % por vía intratecal, el 20 % dosis altas intravenosas y el 3 % por ambas vías de administración en forma secuencial (debido a los efectos tóxicos).[31] No se observó diferencia en las tasas de recaída en el SNC entre los pacientes que recibieron metotrexato por vía intratecal y los que recibieron dosis altas intravenosas (5,4 vs. 6,8 %, P = 0,40). El compromiso testicular, el subtipo no centro germinal y el compromiso extraganglionar alto fueron factores pronósticos del aumento de la recaída en el SNC con independencia de la vía de administración de la profilaxis.[31] En 2 estudios retrospectivos, en los que se evaluaron las dosis altas de metotrexato en pacientes con riesgo alto de LDCBG, tampoco se indicó una mejora de la tasa de recidiva en el SNC.[32,33][Nivel de evidencia C3] Los pacientes que se consideran de riesgo alto para la recidiva en el SNC (por ejemplo, pacientes con 4 a 6 factores de riesgo del CNS-IPI) con frecuencia reciben metotrexato intratecal o dosis altas IV de metotrexato, pero la falta de estudios aleatorizados confirmatorios pone en entredicho este estándar y refleja una necesidad importante de tratamientos mejor verificados en los ensayos clínicos. Los pacientes con compromiso testicular son una excepción, ya que en ellos se observa un beneficio con el metotrexato intratecal o las dosis altas IV de metotrexato.[26-28][Nivel de evidencia C3]
En análisis retrospectivos, la adición de rituximab a los regímenes a base de ciclofosfamida, doxorrubicina, vincristina y prednisona (CHOP) redujo de modo significativo el riesgo de recaída en el SNC.[29,34][Nivel de evidencia C3] Los pacientes con diseminación al SNC en el momento del diagnóstico o de una recaída, a menudo reciben rituximab y dosis altas de metotrexato solo o con citarabina, seguidas por TCM autógeno, pero este abordaje no se ha evaluado en ensayos aleatorizados.[35,36][Nivel de evidencia C3]
Linfoma mediastínico primario de células B grandes
El linfoma mediastínico (tímico) primario de células B grandes (LMPCBG) es un subtipo de LDCBG con características moleculares que son más similares al linfoma de Hodgkin (LH) con esclerosis nodular.[37] Los linfomas mediastínicos con características intermedias entre linfoma mediastínico primario de células B y LH con esclerosis nodular se llaman linfomas mediastínicos de la zona gris.[38,39] Por lo general, los pacientes son mujeres jóvenes (mediana de edad, 30–40 años). Los pacientes presentan una masa mediastínica anterior localmente invasiva que a veces produce síntomas respiratorios o síndrome de la vena cava superior.
El pronóstico y el tratamiento son los mismos que para otros pacientes de LDCBG en estadio comparable. En estudios no controlados de fase II en los que se emplean dosis ajustadas de R-EPOCH (etopósido, prednisona, vincristina, ciclofosfamida y doxorrubicina con rituximab) o R-CHOP, se observaron tasas de curación altas y se evitó la irradiación mediastínica.[39-45]Nivel de evidencia C1] Estos resultados indican que los pacientes que reciben regímenes a base de R-CHOP quizás eviten las complicaciones graves y a largo plazo de la radioterapia cuando se administra con quimioterapia. El uso de tomografía por emisión de positrones con flúor F 18-fludesoxiglucosa (18F-FDG)y tomografía computarizada (TEP-TC) es polémico; todavía no está claro si la TEP permite identificar de manera confiable a los pacientes que deben recibir radioterapia de consolidación o que deben omitirla.[40,46-48]
En una revisión retrospectiva de 109 pacientes con LMPCBG se indicó que el 63 % de ellos tenía una TEP-TC negativa al final del tratamiento (puntaje de Deauville 1–3).[49] No se ofreció radioterapia, la tasa de tiempo hasta la progresión a 5 años (similar a la supervivencia sin enfermedad, pero restringida a la recaída del linfoma) fue del 90 % y la tasa de SG a 5 años fue del 97 %.[49][Nivel de evidencia C3] Los pacientes con una TEP-TC positiva al final del tratamiento recibieron radioterapia de consolidación. En este estudio, no está claro si esos pacientes hubieran evolucionado igual de bien sin radioterapia. Los médicos tienen la posibilidad de seguir la mejora con el transcurso del tiempo de los puntajes de Deauville 4 en las imágenes de TEP-TC al final del tratamiento como alternativa a la radioterapia, pero esto no se ha estudiado en ningún ensayo clínico.
Cuando la radioterapia mediastínica abarcará el lado izquierdo del corazón o se sabe que aumentará el riesgo de cáncer de mama en pacientes jóvenes, es posible considerar el uso de terapia con protones para reducir la dosis de radiación dirigida a los órganos en riesgo.[50] Para obtener más información, consultar la sección Síndrome de la vena cava superior en Síndromes cardiopulmonares.
Debido a que el LMPCBG se caracteriza por una expresión alta del ligando 1 de muerte programada (PD-L1) y una expresión variable de CD30, en un estudio de fase II se evaluó nivolumab con brentuximab vedotina en 30 pacientes con recaída de la enfermedad. Al cabo de una mediana de seguimiento de 11,1 meses, la tasa de respuesta objetiva fue del 73 % (IC 95 %, 54−88 %).[51][Nivel de evidencia C3] De manera similar, en los ensayos de fase I y II sobre pembrolizumab en 74 pacientes con enfermedad recidivante o resistente al tratamiento, se observó una tasa de respuesta objetiva del 45 % al 48 %. La mediana de duración de la respuesta no se alcanzó en 21 pacientes después de una mediana de seguimiento de 29 meses, ni en 53 pacientes después de una mediana de seguimiento de 12,5 meses.[52][Nivel de evidencia C3]
Entre los pacientes que habían recibido dos líneas de tratamiento previas, más de la mitad de los que recibieron terapia de células T con CAR con lisocabtagén maraleucel presentaron respuesta de la enfermedad.[53][Nivel de evidencia C3]
Linfoma folicular de células grandes
Pronóstico
La evolución natural del linfoma folicular de células grandes es polémica.[54] Si bien hay acuerdo acerca del número significativo de sobrevivientes sin enfermedad a largo plazo que tenían una enfermedad en estadio temprano, la posibilidad de curación de los pacientes con enfermedad avanzada (estadio III o estadio IV) permanece incierta. Algunos grupos notifican una tasa de recaída continua semejante a la de otros linfomas foliculares (patrón de un linfoma de crecimiento lento).[55] Otros investigadores notifican una estabilización del tiempo sin progresión hasta los niveles previstos para un linfoma de crecimiento rápido (40 % a 10 años).[56,57] Las causas de esta discrepancia quizás sean las variaciones en la clasificación histológica entre diferentes instituciones y el número escaso de pacientes con linfoma folicular de células grandes. En una revisión retrospectiva de 252 pacientes, todos tratados con quimioterapia combinada con antraciclinas, se observó que los pacientes con más del 50 % de componentes difusos en la biopsia tuvieron una SG mucho más precaria que otros pacientes de linfoma folicular de células grandes.[58]
Abordajes terapéuticos
El tratamiento del linfoma folicular de células grandes se parece más al tratamiento del LNH de crecimiento rápido que al tratamiento del LNH de crecimiento lento. Este abordaje se sustenta en el hecho de que el tratamiento con dosis altas de quimioterapia y trasplante de células madre hematopoyéticas periféricas autógenas tiene el mismo potencial curativo en pacientes que recaen con linfoma folicular de células grandes o linfoma difuso de células grandes.[59][Nivel de evidencia C1]
Entre los pacientes que habían recibido dos líneas de tratamiento previas, más de la mitad de los que recibieron terapia de células T con CAR con lisocabtagén maraleucel presentaron respuesta de la enfermedad.[53][Nivel de evidencia C3]
Linfoma anaplásico de células grandes
Los linfomas anaplásicos de células grandes (LACG) es un tipo de linfoma de células T que se relacionan con el antígeno Ki-1 (CD30). La translocación de los cromosomas 2 y 5 crea una proteína de fusión única de nucleofosmina y ALK.[60,61] Los pacientes con linfomas que expresan ALK en pruebas inmunohistoquímicas a menudo son más jóvenes y a veces tienen síntomas sistémicos, enfermedad extraganglionar y enfermedad en estadio avanzado. Sin embargo, presentan una tasa de supervivencia más favorable que los pacientes que no expresan ALK.[62,63]
En un ensayo prospectivo aleatorizado con 452 pacientes de linfoma de células T CD30+ (70 % LACG: 22 % positivo para ALK y 48 % negativo para ALK). En el ensayo se comparó el régimen estándar de uso tradicional CHOP con un régimen de brentuximab vedotina (un anticuerpo monoclonal anti-CD30 conjugado con un citotóxico) combinado con ciclofosfamida, doxorrubicina y prednisona.[64] Luego de una mediana de seguimiento de 35 meses, la tasa de SG a 3 años fue del 77 % para el grupo de brentuximab vedotina y del 68 % para el grupo de CHOP (cociente de riesgos instantáneos [CRI], 0,66; IC 95 %, 0,46–0,95; P = 0,02).[64][Nivel de evidencia A1] Esto permitió establecer una nueva opción de tratamiento con brentuximab vedotina, ciclofosfamida, doxorrubicina y prednisona para los pacientes con LACG y otros linfomas de células T CD30+, como el linfoma angioinmunoblástico de células T y el linfoma de células T periféricas, sin otra indicación. Para los pacientes en recaída, hay informes anecdóticos de respuesta con brentuximab vedotina,[65-68] romidepsina [69] y pralatrexato.[70][Nivel de evidencia C3]
En un estudio de fase II (NCT00866047), el 66 % de 58 pacientes alcanzaron una respuesta completa con brentuximab vedotina. Al cabo de una mediana de seguimiento de 58 meses, la tasa de SSP a 5 años fue del 57 % (IC 95 %, 41–74 %) y la tasa de SG a 5 años fue del 79 % (IC 95 %, 65–92 %). De los pacientes que lograron una respuesta completa, el 42 % se sometieron a trasplante de células madre hematopoyéticas.[68][Nivel de evidencia C3] Para los pacientes en recaída, el TCM autógeno o alogénico produjo una tasa de SSP a 3 años del 50 % en 39 pacientes de una revisión retrospectiva.[71][Nivel de evidencia C2] En una revisión retrospectiva de 84 pacientes con LACG negativo para ALK se indicó un beneficio en la supervivencia con el TCM autógeno. Esta hipótesis requiere confirmación en un ensayo prospectivo aleatorizado.[72]
El LACG en niños por lo general se caracteriza por enfermedad sistémica y cutánea con tasas de respuesta elevadas y una SG buena cuando se usa quimioterapia combinada a base de doxorrubicina.[73] Los pacientes de LACG relacionado con implante de mama a veces evolucionan bien sin quimioterapia después de someterse a capsulectomía y extracción del implante si la enfermedad está confinada a la cápsula fibrosa y no hay masas ni linfadenopatías relacionadas.[74-77] La mayoría de los pacientes con LACG relacionado con implante de mama tienen una deleción característica en 20Q13.13 que quizás sea útil para el diagnóstico porque ayuda a diferenciarlo del LACG cutáneo o sistémico.[78]
El LACG cutáneo primario es una entidad distinta que es, por lo general, negativo para ALK y tiene un curso clínico de crecimiento lento y de grado bajo.
Linfoma extraganglionar de células T o de células citolíticas naturales
El linfoma extraganglionar de células T o de células citolíticas naturales (NK) de tipo nasal es un linfoma de crecimiento rápido caracterizado por necrosis extensa y angioinvasión, que a menudo se presenta en sitios extraganglionares, en particular en la región de la nariz y los senos paranasales.[79] Otros sitios extraganglionares incluyen el paladar, la tráquea, la piel y el tubo gastrointestinal. Es posible que se presente un síndrome hemofagocítico; tradicionalmente estos tumores se consideraban parte de un granuloma de línea media mortal.[80] En la mayoría de los casos, se detectan genomas del virus de Epstein-Barr (VEB) en las células tumorales y un resultado positivo para CD56 en el análisis inmunofenotípico. Los casos que tienen compromiso de la sangre y la médula se consideran leucemia de células NK.
El aumento en el riesgo de compromiso del SNC y de recidiva local llevó a que se recomiende la administración de radioterapia local antes, de manera simultánea o después de la quimioterapia, o entre el ciclo 2 y 3 de la quimioterapia; además de profilaxis intratecal y radioterapia craneal profiláctica.[81-88]
En una revisión retrospectiva, 1273 pacientes en estadio temprano se estratificaron en grupos de riesgo bajo y riesgo alto a partir del estadio, la edad, la LDH, el estado funcional y la invasión del tumor primario. Los pacientes de riesgo bajo evolucionaron mejor con radioterapia sola,[89] mientras que los pacientes de riesgo alto evolucionaron mejor con una estrategia de radioterapia combinada con quimioterapia.[87,90,91]
En una revisión retrospectiva de 303 pacientes sin tratamiento previo de un consorcio internacional que habían recibido quimioterapia sin antraciclinas, las tasas de SG fueron idénticas en los pacientes en estadio temprano (72−74 % a los 5 años) que recibieron quimioterapia y radioterapia simultáneas o quimioterapia seguida de radioterapia.[92][Nivel de evidencia C3]
El uso de dosis más altas de radioterapia, superiores a 50 Gy, se relacionó con mejoría de los desenlaces de acuerdo con informes anecdóticos.[87] La evolución muy maligna con respuesta precaria y supervivencia corta cuando se usan terapias estándar, en especial, en pacientes con enfermedad en estadio avanzado o presentación inicial extranasal, llevó a algunos investigadores a recomendar la consolidación con un TCM de sangre periférica autógeno o alogénico.[88,93-97] En informes anecdóticos se observó que los regímenes que contienen L-asparaginasa produjeron tasas de respuesta superiores al 50 % en pacientes con enfermedad en recaída, resistente al tratamiento o de diagnóstico reciente.[88,98-101][Nivel de evidencia C3] Debido a la ausencia de ensayos clínicos aleatorizados con más de 100 pacientes para este tipo raro de linfoma de células T, los regímenes que contienen pegaspargasa se han convertido en el tratamiento sistémico estándar. La pegaspargasa es una formulación de asparaginasa menos tóxica que produce menos reacciones de hipersensibilidad y que tiene una semivida más prolongada.[102,103] El linfoma de células T o de células NK que solo se presenta en la piel tiene un pronóstico más favorable, en especial, en pacientes con coexpresión de CD30 y CD56.[104] Una enteropatía benigna de células NK (negativa para VEB) se puede diferenciar del linfoma de células T o de células NK mediante una biopsia endoscópica.[105] En un ensayo de fase II se administró el anticuerpo anti-PD-L1 avelumab a 21 pacientes con enfermedad en recaída o resistente al tratamiento. La tasa de RC fue del 24 %, la tasa de respuesta objetiva fue del 38 % y las respuestas se correlacionaron con la expresión de PD-L1 del tumor.[106][Nivel de evidencia C3] El tratamiento con pembrolizumab, un anticuerpo contra la proteína de muerte celular programada 1 (PD-1), produjo respuestas similares en pacientes con enfermedad en recaída o resistente al tratamiento.[107][Nivel de evidencia C3]
Granulomatosis linfomatoide
La granulomatosis linfomatoide es un linfoma de células B grandes positivo para VEB sobre un fondo con predominio de células T.[108,109] En el examen histológico se observa angioinvasión y vasculitis que a menudo se manifiestan como lesiones pulmonares o compromiso de los senos paranasales.
Los pacientes se tratan como los de linfoma difuso de células grandes y necesitan quimioterapia combinada a base de doxorrubicina.
Linfoma angioinmunoblástico de células T
El linfoma angioinmunoblástico de células T (LACT) se llamaba antes linfadenopatía angioinmunoblástica con disproteinemia. Esta entidad se caracteriza por un reordenamiento clonal del gen del receptor de células T y se trata como un linfoma difuso de células grandes.[110-113] Los pacientes presentan gran linfadenopatía, fiebre, sudores nocturnos, pérdida de peso, exantema, prueba de Coombs positiva e hipergammaglobulinemia policlonal.[80] Las infecciones oportunistas son frecuentes debido a una inmunodeficiencia subyacente. En la mayoría de los pacientes afectados se detectan genomas del VEB en las células B.[114] Para obtener más información sobre la pérdida de peso, consultar La nutrición en el tratamiento del cáncer y, para obtener más información sobre el exantema, consultar Prurito.
Se recomienda la quimioterapia combinada a base de doxorrubicina, como en el régimen CHOP, de igual forma que para otros linfomas de crecimiento rápido.[110,113] Para los casos CD30+, el estándar de atención es brentuximab combinado con ciclofosfamida, doxorrubicina y prednisona.[64][Nivel de evidencia B1] Para obtener más información, consultar la sección Linfoma anaplásico de células grandes. En el International Peripheral T-Cell Lymphoma Project, llevado a cabo en 22 centros internacionales, se identificaron 243 pacientes de LACT; la tasa de SG a 5 años fue del 33 % y la tasa de supervivencia sin fracaso terapéutico a 5 años fue de 18 %.[115] En informes anecdóticos se describió el uso de quimioterapia mielosupresora y radioterapia con apoyo de células madre periféricas autógenas o alogénicas.[72,96,116-118] Hay informes anecdóticos de respuestas a la ciclosporina,[119] el pralatrexato,[120] la bendamustina,[121] el inhibidor de la histona–desacetilasa romidepsina, y el brentuximab vedotina (incluso si el linfoma no tiene expresión de CD30 o la expresión es baja).[69,122][Nivel de evidencia C3] De manera ocasional se han notificado remisiones espontáneas y respuestas prolongadas a los corticoesteroides.
Linfoma de células T periféricas
Los pacientes con linfoma de células T periféricas tienen un linfoma difuso de células grandes o un linfoma difuso mixto que exhibe en la superficie celular un fenotipo postímico (periférico) de célula T que expresa CD4 o CD8, pero que no expresa ambos.[123] Los linfoma de células T periféricas abarcan un grupo heterogéneo de linfomas ganglionares de células T que necesitan mejor descripción en el futuro.[80,124] Estos incluyen el denominado linfoma de Lennert, un linfoma mixto de células T con predominio de células linfoepitelioides.
Pronóstico
La mayoría de los investigadores notifican respuestas y tasas de supervivencia más precarias para los pacientes con linfomas de células T periféricas que para otros pacientes con linfomas de células B de crecimiento rápido en estadio comparable.[124,125] La mayoría de los pacientes presentan múltiples factores de pronóstico adverso (es decir, edad avanzada, estadio IV, varios sitios extraganglionares y LDH elevada), y tienen tasas bajas (<20 %) de supervivencia sin fracaso terapéutico y SG a 5 años.[124,125] Al igual que para otros linfomas (por ejemplo, LDCBG o linfoma folicular), la supervivencia sin complicaciones a 24 meses predice una SG a 5 años de 78 %.[126]
Abordajes terapéuticos
El tratamiento incluye quimioterapia combinada a base de doxorrubicina (como CHOP o CHOPE [CHOP y etopósido]), que también se usa para el LDCBG.[127] Para los casos CD30+, el estándar de atención es brentuximab combinado con ciclofosfamida, doxorrubicina y prednisona.[64][Nivel de evidencia B1] Para obtener más información, consultar la sección Linfoma anaplásico de células grandes. En los pacientes en estadio temprano, los resultados anecdóticos de series retrospectivas son contradictorios en cuanto a la importancia de la radioterapia de consolidación después de la quimioterapia combinada.[128][Nivel de evidencia C3] La terapia de consolidación de dosis altas de quimioterapia y apoyo de células madre hematopoyéticas autógenas o alogénicas se ha administrado a los pacientes con linfoma de células T periféricas en estadio avanzado después de la terapia de inducción en múltiples ensayos de fase II o retrospectivos. La evidencia que respalda este abordaje es de carácter anecdótico.[72,96,116,118,129-131][Nivel de evidencia C3]
En un ensayo prospectivo aleatorizado se incluyó a 104 pacientes menores de 61 años con linfoma de células T periféricas en estadio II, III o IV (excepto el LACG positivo para ALK). Los pacientes recibieron TCM autógeno o TCM alogénico como terapia de consolidación tras la inducción con CHOEP (ciclofosfamida, doxorrubicina, vincristina, etopósido y prednisona) seguido de DHAP (dexametasona, citarabina y cisplatino).[132][Nivel de evidencia C3] Al cabo de una mediana de seguimiento de 42 meses, la tasa de SSC a 3 años fue del 43 % para los pacientes que recibieron TCM alogénico y del 38 % para los pacientes que recibieron TCM autógeno. La tasa de SG a 3 años fue del 57 % para los pacientes que recibieron TCM alogénico y del 70 % para los pacientes que recibieron TCM autógeno (P = no significativo). Ninguno de los 21 pacientes que respondieron y continuaron con TCM alogénico tuvieron recaída; el 36 % de los pacientes que continuaron con TCM autógeno tuvieron recaída. Ocho de los 26 pacientes (31 %) que recibieron TCM alogénico murieron por la enfermedad de injerto contra huésped; ninguno de los 41 pacientes que recibieron TCM autógeno murió por toxicidad. El aumento de la mortalidad relacionada con el trasplante anuló el beneficio del efecto injerto contra linfoma.
En un ensayo prospectivo, el pralatrexato indujo una tasa de respuesta del 30 % y una mediana de duración de la respuesta de 10 meses en 109 pacientes en recaída evaluables.[69,133][Nivel de evidencia C3] También se observaron tasas de respuesta semejantes cuando se administró romidepsina a 130 pacientes evaluables en un ensayo prospectivo.[69][Nivel de evidencia C3] Hay informes anecdóticos que indican que se observaron respuestas con una combinación de pralatrexato y romidepsina,[120] bendamustina en monoterapia,[121] belinostat,[134] y brentuximab vedotina (incluso si el linfoma no expresa CD30 o la expresión es baja).[122][Nivel de evidencia C3] La incorporación de estos nuevos fármacos a la quimioterapia CHOP está en evaluación clínica.[64,124]
Un tipo poco común de linfoma de células T periféricas que se presenta en hombres jóvenes, el linfoma hepatoesplénico de células T, surge en los sinusoides hepáticos y esplénicos y expresa en la superficie celular el receptor de células T γ-δ.[135-137] Otra variante, el linfoma subcutáneo de células T similar a paniculitis, se ubica en el tejido subcutáneo y se relaciona con el síndrome hemofagocítico.[138-141] Estos pacientes tienen células que expresan un fenotipo α-β. Los linfomas con fenotipo γ-δ presentan una evolución clínica más maligna y se clasifican como linfomas cutáneos de células T γ-δ.[142-144] Estos pacientes pueden tener compromiso de la epidermis, la dermis, la región subcutánea o la mucosa. Estas entidades tienen un pronóstico sumamente desfavorable con una evolución clínica muy maligna y se han tratado con el mismo modelo terapéutico que se usa para los grupos con LDCBG de riesgo más alto.[96,137] La enfermedad linfoproliferativa de células T de crecimiento lento en el tubo gastrointestinal se debe diferenciar del linfoma de células T periféricas porque es posible que no necesite tratamiento.[145]
Linfoma intestinal de células T de tipo enteropático
El linfoma intestinal de células T de tipo enteropático afecta el intestino delgado de pacientes con enteropatía por intolerancia al gluten (celiaquía).[80,146-148] Debido a que una alimentación sin gluten evita la formación del linfoma, los pacientes que reciben el diagnóstico de celiaquía durante la niñez pocas veces presentan un linfoma. El diagnóstico de celiaquía se suele hacer cuando se encuentra atrofia vellosa en el intestino resecado. A menudo se necesita una cirugía para establecer el diagnóstico y para evitar la perforación durante el tratamiento.
El tratamiento incluye quimioterapia combinada a base de doxorrubicina, pero las tasas de recaída son más altas que para los pacientes con linfoma difuso de células B grandes en estadio comparable.[147-149] Las complicaciones del tratamiento son hemorragia gastrointestinal, perforación del intestino delgado y fístula enterocólica; a menudo los pacientes necesitan nutrición parenteral. Para obtener más información sobre la nutrición parenteral, consultar La nutrición en el tratamiento del cáncer. En el momento de la recaída se observan perforaciones intestinales multifocales y compromiso de vísceras abdominales. El tratamiento con dosis altas y el rescate de células madre hematopoyéticas se han usado en el momento de la primera remisión o recaída.[96,147,150][Nivel de evidencia C2] La evidencia que respalda este abordaje es de carácter anecdótico.
Linfoma intravascular de células B grandes (linfomatosis intravascular)
La linfomatosis intravascular se caracteriza como un linfoma de células grandes limitado al lumen intravascular. En la linfomatosis intravascular, los órganos que más a menudo están comprometidos son el encéfalo, los riñones, los pulmones y la piel.
El pronóstico es similar al del linfoma difuso de células B grandes (LDCBG) convencional en estadio IV cuando se administra una quimioterapia combinada intensiva a base de R-CHOP, como se usa en casos de LDCBG.[151-153]
Linfoma de Burkitt o linfoma difuso de células pequeñas no hendidas
El linfoma de Burkitt o el linfoma difuso de células pequeñas no hendidas por lo general afecta a pacientes más jóvenes y es el tipo más común de LNH infantil.[154] Estos tipos de linfomas extraganglionares de células B de crecimiento rápido se caracterizan por una translocación y desregulación del gen MYC en el cromosoma 8.[155] Un subgrupo de pacientes que tiene una translocación doble de MYC y BCL2 presenta un desenlace muy desfavorable a pesar del tratamiento intensivo (mediana de SG, 5 meses).[156][Nivel de evidencia C1]
En algunos pacientes con células B más grandes hay una superposición morfológica con el LDCBG. Estos linfomas de células grandes de tipo Burkitt exhiben una desregulación de MYC, tasas de proliferación muy altas y un perfil de expresión génica compatible con el linfoma de Burkitt clásico.[157-159] En casos endémicos, a menudo en África, hay compromiso de los huesos faciales o los maxilares en los niños, y en su mayoría contienen genomas del VEB. Los casos esporádicos suelen afectar el sistema gastrointestinal, los ovarios o los riñones. Los pacientes que presentan masas de crecimiento rápido y una concentración muy alta de LDH, se podrían curar con quimioterapia combinada intensiva a base de doxorrubicina.
Abordajes terapéuticos
El tratamiento del linfoma de Burkitt o el linfoma difuso de células pequeñas no hendidas incluye regímenes multifarmacológicos intensivos en combinación con rituximab, similares a los que se usan para los linfomas de crecimiento rápido en estadios avanzados (linfomas difusos de células grades).[160-163] Una quimioterapia combinada intensiva, como la que se utiliza para el linfoma de Burkitt infantil resultó muy exitosa para los pacientes adultos con enfermedad en estadio avanzado que lograron una supervivencia sin enfermedad a 5 años de más de 60 %.[164-167] Los factores de pronóstico adverso son la enfermedad con gran masa tumoral abdominal y una concentración sérica alta de LDH. Los pacientes con linfoma de Burkitt tienen un riesgo de por vida del 20 % al 30 % de compromiso del SNC. Se necesita profilaxis con quimioterapia intratecal durante la terapia de inducción.[168] Los pacientes con linfoma de Burkitt relacionado con el virus de la inmunodeficiencia humana (VIH) también se benefician de una modificación menos tóxica de los regímenes multifarmacológicos intensivos en combinación con rituximab.[169][Nivel de evidencia C3] Para obtener más información, consultar Tratamiento del linfoma primario del sistema nervioso central y Tratamiento del linfoma relacionado con el SIDA.
Linfoma linfoblástico
El linfoma linfoblástico (células T precursoras) es una forma muy maligna de LNH. A menudo, pero no siempre, se presenta en pacientes jóvenes.[170] Por lo común, este linfoma produce masas mediastínicas grandes y tiene una gran predilección por diseminarse a la médula ósea y el sistema nervioso central (SNC).
El tratamiento por lo general se estructura como el de la leucemia linfoblástica aguda. El tratamiento estándar para este tipo histológico de LNH crecimiento rápido es la quimioterapia combinada intensiva con profilaxis del SNC.[171-173] A veces, se administra radioterapia dirigida a las masas tumorales voluminosas. Debido a que estas formas de LNH tienden a progresar rápido, la quimioterapia combinada se administra de inmediato una vez que se confirma el diagnóstico. Los aspectos más importantes de la evaluación de estadificación antes del tratamiento incluyen una revisión minuciosa de las piezas patológicas, las muestras de aspirado de la médula ósea, las muestras de la biopsia, las pruebas citológicas del líquido cefalorraquídeo y de los marcadores de linfocitos. Para obtener más información, consultar Tratamiento de la leucemia linfoblástica aguda en adultos.
Leucemia de células T o linfoma de células T en adultos
La infección por un retrovirus humano llamado virus linfotrópico T humano de tipo 1 es la causa de la leucemia o el linfoma de células T en adultos (LTA) que con frecuencia produce linfadenopatía, hipercalcemia, células leucémicas circulantes, compromiso óseo y cutáneo, hepatoesplenomegalia, progresión rápida y respuesta precaria a la quimioterapia combinada.[174,175] El LTA se dividió en cuatro subtipos clínicos:[176,177]
- Tipo agudo (evolución muy maligna con leucemia y compromiso extraganglionar o ganglionar, o sin este).
- Tipo linfoma (evolución muy maligna con linfadenopatía y sin leucemia).
- Tipo crónico (evolución de escasa malignidad con leucemia y linfadenopatía).
- Tipo quiescente (evolución de escasa malignidad solo con leucemia).
El LTA de tipo agudo y de tipo linfoma evolucionan mal cuando se usan estrategias de quimioterapia combinada y TCM alogénico: la mediana de SG es inferior a 1 año.[178-180] Cuando se usó quimioterapia combinada, menos del 10 % de 807 pacientes estaban vivos a los 4 años.[180] Hay informes anecdóticos de remisiones duraderas después de un TCM alogénico, incluso tras una infusión de linfocitos de un donante para recaídas posteriores al trasplante.[181][Nivel de evidencia C3] En 2 revisiones retrospectivas, la tasa de supervivencia a 3 años fue del 36 % y el 26 % entre 815 pacientes sometidos a TCM alogénico.[182,183][Nivel de evidencia C1]
La combinación de zidovudina e interferón α es eficaz contra el LTA, incluso en pacientes con fracaso del tratamiento citotóxico previo. Se han observado remisiones duraderas en la mayoría de pacientes que reciben esta combinación, pero no en los pacientes de LTA con subtipo linfoma.[184-188] En un estudio multicéntrico de fase II con 26 pacientes en recaída, el 42 % respondieron a lenalidomida (incluso se presentó una RC).[189][Nivel de evidencia C3] La progresión local sintomática de todos los subtipos responde bien a la radioterapia paliativa.[190] En el entorno de una recaída, se observa una tasa de respuesta objetiva del 50 % o superior cuando se usa mogamulizumab, un anticuerpo monoclonal humanizado contra el receptor 4 de quimiocinas C-C (CCR4).[191][Nivel de evidencia C3] En los casos CD30+, el estándar de atención es brentuximab combinado con ciclofosfamida, doxorrubicina y prednisona.[64][Nivel de evidencia B1] Para obtener más información, consultar la sección Linfoma anaplásico de células grandes.
Linfoma de células de manto
El linfoma de células de manto (LCM) se encuentra en los ganglios linfáticos, el bazo, la médula ósea, la sangre, y a veces en el tubo gastrointestinal (poliposis linfomatosa).[192] El LCM se caracteriza por células B foliculares de manto CD5+, una translocación de los cromosomas 11 y 14, así como la sobreexpresión de la proteína ciclina D1.[192] El LCM se divide en dos subtipos clínicos: una versión clásica con linfadenopatía y expresión alta de SOX-11 que se manifiesta con una evolución clínica de gran malignidad y un pronóstico más precario; una versión leucémica no ganglionar con expresión baja de SOX-11, una evolución clínica menos maligna y un mejor pronóstico.[193] Con un cariotipo complejo se predicen respuestas precarias a la terapia de inducción y una supervivencia inferior.[194] Con frecuencia hay superposición del cuadro clínico inicial de estos subtipos, y las implicaciones terapéuticas no son evidentes. Sin embargo, ambas versiones pueden converger en la evolución y convertirse en un fenotipo blastoide o resistente al tratamiento debido a la inestabilidad y selección genómica.[195,196]
Al igual que los linfomas de grado bajo, el LCM es incurable con quimioterapia a base de antraciclinas y se presenta en pacientes de más edad con una enfermedad en estadio avanzada que por lo general es asintomática. Sin embargo, la mediana de supervivencia es mucho más corta (5–7 años) que la de otros linfomas; en la actualidad, este tipo histológico se considera un linfoma de gran malignidad.[197] El patrón difuso y la variante blastoide indican una evolución más maligna y una supervivencia más corta; mientras que el tipo de la zona de manto quizás tenga una evolución menos maligna.[196,198] Es posible que una tasa de proliferación celular elevada (aumento de Ki-67, índice mitótico y microglobulina β2) se relacione con un pronóstico más precario.[199,200]
Abordajes terapéuticos
Los pacientes asintomáticos con puntajes de riesgo bajo en el IPI quizás evolucionen bien cuando se difiere el tratamiento inicial.[201,202][Nivel de evidencia C3] No hay un abordaje estándar para el LCM. Se han empleado varios regímenes de quimioterapia de inducción para la enfermedad progresiva sintomática. Estos regímenes varían en intensidad: rituximab solo, rituximab con ibrutinib, rituximab con bendamustina, R-CHOP o regímenes intensivos de dosis altas, como ciclofosfamida, vincristina, doxorrubicina y dexametasona alternada con metotrexato y citarabina (R-hyper C-VAD). Después de estos regímenes, algunos médicos usan un TCM autógeno o alogénico para la consolidación, mientras que otros prefieren el mantenimiento con rituximab y reservan la consolidación con dosis altas para otro momento.[203] Ibrutinib, lenalidomida y bortezomib demostraron ser activos en pacientes en recaída y ahora estos medicamentos se incorporan al tratamiento inicial.[204-209]
No está claro qué abordaje terapéutico se traduce en la mejor supervivencia a largo plazo para esta entidad clinicopatológica.
En un ensayo de fase II con pacientes de 64 años de edad con LCM sin tratamiento previo, 50 pacientes recibieron el inhibidor del receptor de células B ibrutinib con rituximab. Al cabo de una mediana de seguimiento de 45 meses, la tasa de respuesta objetiva fue del 96 %, la tasa de RC fue del 76 %, la tasa de SSP a 3 años fue del 87 % y la tasa de SG a 3 años fue del 94 %.[209][Nivel de evidencia C3] En un ensayo de fase II de 131 pacientes de 65 años o menos con LCM sin tratamiento previo, 1 año de ibrutinib y 4 semanas de rituximab, dio lugar a una tasa de RC del 89 % antes de cualquier consolidación con quimioterapia.[210][Nivel de evidencia C3] En otro ensayo de fase II con ibrutinib y rituximab se incluyó a pacientes asintomáticos con LCM sin tratamiento previo; la tasa de RC fue del 87 %.[211][Nivel de evidencia C3] Los pacientes con tratamiento previo que recibieron ibrutinib tuvieron una tasa de respuesta del 86 % (tasa de RC, 21 %) y una mediana de SSP de 14 meses.[206][Nivel de evidencia C3] En un ensayo prospectivo aleatorizado, 280 pacientes de LCM en recaída o resistente al tratamiento recibieron ibrutinib o temsirólimus.[212] Después de una mediana de seguimiento de 15 meses, la mediana de SSP favoreció al ibrutinib (14,6 vs. 6,2 meses; CRI, 0,43; IC 95 %, 0,32–0,58; P < 0,001).[212][Nivel de evidencia B1] En un estudio de fase II con 23 pacientes de LCM en recaída o resistente al tratamiento se combinó el ibrutinib con otro fármaco activo, venetoclax.[213] Se obtuvieron resultados sin precedentes: un 71 % de los pacientes tuvo una RC y, de ellos, el 78 % mantuvo la respuesta al cabo de 15 meses.[213][Nivel de evidencia C3]
Un ensayo prospectivo y aleatorizado incluyó a 523 pacientes de 65 años o más con LCM. Los pacientes fueron asignados al azar para recibir ibrutinib, bendamustina y rituximab, o solo bendamustina y rituximab.[214] Al cabo de una mediana de seguimiento de 84,7 meses, la mediana de la SSP fue de 80,6 meses para los pacientes que recibieron ibrutinib, y de 52,9 meses para los pacientes que recibieron solo bendamustina y rituximab (CRI, 0,75; IC 95 %, 0,59–0,96; P = 0,01). No hubo diferencias en la tasa de SG a 7 años (55,0 vs. 56,8 %; CRI, 1,07; IC 95 %, 0,81–1,40).[214][Nivel de evidencia B1] No está claro si los pacientes que reciban ibrutinib solo podrían conseguir estos mismos resultados sin la quimioterapia convencional. La magnitud del beneficio que se observó en los resultados para la SSP contrastaron con el beneficio insuficiente para la SG después de 7 años lo que podría poner en duda la inocuidad a largo plazo de esta combinación.
En un ensayo prospectivo aleatorizado, 560 pacientes mayores de 60 años que no eran aptos para un TCM recibieron R-CHOP o rituximab, fludarabina y ciclofosfamida (R-FC) durante 6 a 8 ciclos, luego los pacientes que respondieron se asignaron al azar a un régimen de mantenimiento con rituximab o interferón α.[215] Al cabo de una mediana de seguimiento de 7,6 años, la mediana de SG fue significativamente más corta después de R-FC que después de R-CHOP (3,9 años versus 6,4 años; P = 0,0054).[215][Nivel de evidencia A1] En el mismo ensayo, al cabo de una mediana de seguimiento de 8 años para los 316 pacientes que respondieron al tratamiento, el mantenimiento con rituximab mejoró la SG en comparación con el mantenimiento con interferón (mediana de SG, 9,8 años vs. 7,1 años; P = 0,009).[215][Nivel de evidencia A1] Los pacientes que respondieron a R-CHOP fueron los que más se beneficiaron con rituximab en la SG (mediana 9,8 años vs. 6,4 años; P = 0,0026).[215][Nivel de evidencia C1] En un ensayo aleatorizado en el que se comparó bendamustina y rituximab (BR) con R-CHOP se observó una mejora de la SSP (35 vs. 22 meses; CRI, 0,49; IC 95 %, 0,28–0,79; P = 0,004), pero ninguna diferencia en la SG.[216][Nivel de evidencia B1] No obstante, en este ensayo no se logró mostrar ningún beneficio para el mantenimiento con rituximab después de BR. En un ensayo prospectivo aleatorizado con 487 pacientes, se comparó un régimen de bortezomib, rituximab, ciclofosfamida, doxorrubicina y prednisona (VR-CAP) con R-CHOP.[217] Al cabo de una mediana de seguimiento de 82 meses, la mediana de SG fue superior para VR-CAP (90,7 meses) en comparación con R-CHOP (55,7 meses) (CRI, 0,66; IC 95 %, 0,51−0,85; P = 0,001).[217][Nivel de evidencia A1]
En un ensayo prospectivo aleatorizado con 497 pacientes menores de 65 años se compararon 6 ciclos de R-CHOP y 6 ciclos alternados de R-CHOP con rituximab, dexametasona, citarabina y cisplatino (R-DHAP); ambos grupos se sometieron a TCM autógeno.[218,219][Nivel de evidencia B1] Al cabo de una mediana de seguimiento de 10,6 años, la tasa de SSP a 10 años fue del 73 % en los pacientes que recibieron R-DHAP y del 57 % en los que recibieron R-CHOP (CRI, 0,56; P = 0,038), pero no hubo diferencias en las tasas de SG a 10 años (60 % [R-DHAP] vs. 55 % [R-CHOP]; CRI, 0,80; 0,61–1,06; P = 0,12).[220][Nivel de evidencia B1] Este es el ensayo aleatorizado al que hacen referencia todos los artículos posteriores en los que se establece el papel de la citarabina en el tratamiento de inducción; la falta final de ventaja en la supervivencia pone en duda esta afirmación.
En los ensayos aleatorizados no se han confirmado los beneficios para la SG en los pacientes que reciben terapia de consolidación con TCM autógeno o alogénico.[221-226]
En un ensayo prospectivo (NCT00921414) con 299 pacientes sin tratamiento previo para un LCM, 257 respondieron al tratamiento con 4 ciclos de R-DHAP y TCM autógeno. Los pacientes se asignaron al azar a terapia de mantenimiento con rituximab por 3 años versus ninguna terapia de mantenimiento. Después de la aleatorización y tras una mediana de seguimiento de 50,2 meses, se observó una tasa de SSP a 4 años del 83 % (IC 95 %, 73–88 %), que favoreció al grupo de tratamiento con rituximab versus una tasa del 64 % (IC 95 %, 55–73 %; P < 0,001) en el grupo que no recibió mantenimiento. La tasa de SG a 4 años del 89 % (IC 95 %, 81–94 %) también favoreció al grupo de mantenimiento con rituximab versus una tasa del 80 % (IC 95 %, 72–88 %; P = 0,04) en el grupo que no recibió mantenimiento.[227][Nivel de evidencia A1]
La lenalidomida con rituximab o sin este también produce tasas de respuesta en torno al 50 % en pacientes en recaída, y tasas de respuesta incluso más altas en pacientes sin tratamiento previo.[205,208,228,229][Nivel de evidencia C3]
El acalabrutinib (otro inhibidor del receptor de células B de la vía de la tirosina–cinasa de Bruton [BTK]) se estudió en 124 pacientes con LCM en recaída o resistente al tratamiento.[230] En un estudio de fase II, la tasa de respuesta objetiva fue del 81 %, la RC del 40 %, y la SSP a 1 año fue del 67 %.[230][Nivel de evidencia C3] Asimismo, en un estudio de fase II con 86 pacientes de LCM en recaída o resistente al tratamiento, se evaluó el inhibidor de BTK zanubrutinib.[231] Al cabo de una mediana de seguimiento de 35,3 meses, la tasa de respuesta objetiva fue del 84 %, la tasa de RC fue del 78 % y la mediana de SSP fue 33,0 meses.[231][Nivel de evidencia C3]
Los pacientes con LCM en recaída o resistente al tratamiento cuya enfermedad no respondió al ibrutinib o al acalabrutinib se inscribieron en un ensayo de fase II que utilizó brexucabtagén autoleucel, una terapia de células T con CAR anti-CD19.[232] Al cabo de una mediana de seguimiento de 36 meses, 74 pacientes tuvieron una tasa de respuesta objetiva del 91 % (IC 95 %, 82−97 %) y una tasa de RC del 68 % (IC 95 %, 55−78 %).[232][Nivel de evidencia C3] De los pacientes, el 15 % presentaron un síndrome de liberación de citocinas de grado 3 o superior, y el 31 % de los pacientes presentaron complicaciones neurológicas.
En resumen, la mejor secuenciación de estos tratamientos no está clara y es el tema central de un ensayo clínico intergrupal. El rituximab, la lenalidomida, el ibrutinib, el acalabrutinib, el venetoclax, y el zanubrutinib son fármacos biológicos directos que quizás conduzcan a estrategias de tratamiento sin quimioterapia para los pacientes con LCM.[233]
Nunca se ha estudiado en un ensayo prospectivo aleatorizado la administración rutinaria de profilaxis del SNC para el LCM de riesgo alto. El uso de metotrexato intratecal o de dosis altas y el uso de terapias sistémicas con penetración en el SNC, como el ibrutinib, la citarabina en dosis altas o el venetoclax, no se ha estudiado ni se ha comprobado su eficacia en esta situación.[196]
Trastorno linfoproliferativo postrasplante
Los pacientes sometidos a trasplante de corazón, pulmón, hígado, riñón o páncreas suelen necesitar inmunodepresión de por vida. La inmunodepresión produce un trastorno linfoproliferativo postrasplante (TLPT) en el 1 % al 3 % de los receptores; esta enfermedad es similar a un linfoma de crecimiento rápido.[234] Los patólogos pueden diferenciar la hiperplasia policlonal de células B y el linfoma monoclonal de células B que casi siempre se relacionan con el VEB.[235]
Pronóstico
Los factores de pronóstico precario del TLPT son el estado funcional deficiente, el compromiso del órgano injertado, un IPI alto, una LDH elevada y enfermedad en múltiples sitios.[236,237]
Opciones de tratamiento
En algunos casos la interrupción del tratamiento inmunodepresor lleva a la erradicación del linfoma.[238,239] Cuando esto no es posible, se considera el uso de rituximab, porque demostró que produce remisiones duraderas en alrededor de un 60 % de los pacientes y tiene un perfil de toxicidad favorable.[238,240,241] Si estas medidas fracasan, se recomienda una quimioterapia combinada a base de doxorrubicina (R-CHOP), aunque algunos pacientes pueden evitar la terapia citotóxica.[241,242] Las presentaciones localizadas se pueden controlar con cirugía o radioterapia sola. Estas masas localizadas, que a veces crecen durante meses, a menudo tienen un fenotipo policlonal y tienden a surgir en el transcurso de semanas o pocos meses después del trasplante.[235] La enfermedad multifocal rápidamente progresiva se presenta de manera más tardía después del trasplante (>1 año), a menudo tiene un fenotipo monoclonal y se relaciona con el VEB.[243] Estos pacientes pueden presentar remisiones prolongadas con los regímenes de quimioterapia estándar que se usan para el linfoma de crecimiento rápido.[243-245] Los casos de TLPT negativo para VEB se presentan todavía más tarde (mediana de 5 años después del trasplante) y tienen un pronóstico más precario; en estas circunstancias se puede usar de manera directa quimioterapia R-CHOP.[246] Se obtuvo una respuesta clínica sostenida con una inmunotoxina (un antígeno de superficie de las células B anti-CD22 unido a ricina, una toxina vegetal) después del fracaso de la quimioterapia.[247] También está en evaluación clínica un anticuerpo monoclonal anti-interleucina 6.[248]
Linfoma histiocítico verdadero
Este tipo de linfoma produce tumores muy poco frecuentes que exhiben diferenciación histiocítica y expresan marcadores histiocíticos en ausencia de marcadores inmunitarios de linaje específico de células B o T.[249,250] Se debe tener cuidado con las pruebas inmunofenotípicas para excluir el LACG o los síndromes hemofagocíticos debidos a infecciones víricas, en especial por el VEB.
Opciones de tratamiento
El tratamiento sigue el modelo terapéutico de los linfomas difusos de células grandes en estadio comparable, pero todavía queda por definir el abordaje óptimo.
Linfoma de efusión primaria
El linfoma de efusión primaria casi siempre ocurre en la cavidad pleural, pericárdica o abdominal en ausencia de una masa tumoral identificable.[251] A menudo los pacientes son seropositivos para el VIH y, por lo general, el tumor contiene el virus del herpes relacionado con el sarcoma de Kaposi y el virus del herpes humano de tipo 8.[252]
Pronóstico
El pronóstico para el linfoma de efusión primaria es muy precario.
Abordajes terapéuticos
El tratamiento suele seguir el modelo terapéutico de los linfomas difusos de células grandes en estadio comparable.
Linfoma plasmoblástico
El linfoma plasmoblástico se observa con más frecuencia en pacientes con infección por el VIH y presenta células B grandes CD20 con características plasmocitarias. Este tipo de linfoma tiene una evolución clínica muy maligna, con respuestas precarias y remisiones cortas a la quimioterapia estándar.[253] Hay informes anecdóticos en los que se indica que a veces es posible administrar la quimioterapia intensiva que se usa para el linfoma de Burkitt o el linfoma linfoblástico, seguida de consolidación con TCM en los pacientes que responden a esta.[253-255]
Bibliografía
- Sehn LH, Salles G: Diffuse Large B-Cell Lymphoma. N Engl J Med 384 (9): 842-858, 2021. [PUBMED Abstract]
- Delabie J, Vandenberghe E, Kennes C, et al.: Histiocyte-rich B-cell lymphoma. A distinct clinicopathologic entity possibly related to lymphocyte predominant Hodgkin's disease, paragranuloma subtype. Am J Surg Pathol 16 (1): 37-48, 1992. [PUBMED Abstract]
- Achten R, Verhoef G, Vanuytsel L, et al.: T-cell/histiocyte-rich large B-cell lymphoma: a distinct clinicopathologic entity. J Clin Oncol 20 (5): 1269-77, 2002. [PUBMED Abstract]
- Bouabdallah R, Mounier N, Guettier C, et al.: T-cell/histiocyte-rich large B-cell lymphomas and classical diffuse large B-cell lymphomas have similar outcome after chemotherapy: a matched-control analysis. J Clin Oncol 21 (7): 1271-7, 2003. [PUBMED Abstract]
- Ghesquières H, Berger F, Felman P, et al.: Clinicopathologic characteristics and outcome of diffuse large B-cell lymphomas presenting with an associated low-grade component at diagnosis. J Clin Oncol 24 (33): 5234-41, 2006. [PUBMED Abstract]
- Miller TP, Dahlberg S, Cassady JR, et al.: Chemotherapy alone compared with chemotherapy plus radiotherapy for localized intermediate- and high-grade non-Hodgkin's lymphoma. N Engl J Med 339 (1): 21-6, 1998. [PUBMED Abstract]
- Coiffier B, Lepage E, Briere J, et al.: CHOP chemotherapy plus rituximab compared with CHOP alone in elderly patients with diffuse large-B-cell lymphoma. N Engl J Med 346 (4): 235-42, 2002. [PUBMED Abstract]
- Coiffier B: State-of-the-art therapeutics: diffuse large B-cell lymphoma. J Clin Oncol 23 (26): 6387-93, 2005. [PUBMED Abstract]
- Habermann TM, Weller EA, Morrison VA, et al.: Rituximab-CHOP versus CHOP alone or with maintenance rituximab in older patients with diffuse large B-cell lymphoma. J Clin Oncol 24 (19): 3121-7, 2006. [PUBMED Abstract]
- Zhou Z, Sehn LH, Rademaker AW, et al.: An enhanced International Prognostic Index (NCCN-IPI) for patients with diffuse large B-cell lymphoma treated in the rituximab era. Blood 123 (6): 837-42, 2014. [PUBMED Abstract]
- Møller MB, Christensen BE, Pedersen NT: Prognosis of localized diffuse large B-cell lymphoma in younger patients. Cancer 98 (3): 516-21, 2003. [PUBMED Abstract]
- Maurer MJ, Ghesquières H, Link BK, et al.: Diagnosis-to-Treatment Interval Is an Important Clinical Factor in Newly Diagnosed Diffuse Large B-Cell Lymphoma and Has Implication for Bias in Clinical Trials. J Clin Oncol 36 (16): 1603-1610, 2018. [PUBMED Abstract]
- Scott DW, King RL, Staiger AM, et al.: High-grade B-cell lymphoma with MYC and BCL2 and/or BCL6 rearrangements with diffuse large B-cell lymphoma morphology. Blood 131 (18): 2060-2064, 2018. [PUBMED Abstract]
- Horn H, Ziepert M, Becher C, et al.: MYC status in concert with BCL2 and BCL6 expression predicts outcome in diffuse large B-cell lymphoma. Blood 121 (12): 2253-63, 2013. [PUBMED Abstract]
- Staiger AM, Ziepert M, Horn H, et al.: Clinical Impact of the Cell-of-Origin Classification and the MYC/ BCL2 Dual Expresser Status in Diffuse Large B-Cell Lymphoma Treated Within Prospective Clinical Trials of the German High-Grade Non-Hodgkin's Lymphoma Study Group. J Clin Oncol 35 (22): 2515-2526, 2017. [PUBMED Abstract]
- Howlett C, Snedecor SJ, Landsburg DJ, et al.: Front-line, dose-escalated immunochemotherapy is associated with a significant progression-free survival advantage in patients with double-hit lymphomas: a systematic review and meta-analysis. Br J Haematol 170 (4): 504-14, 2015. [PUBMED Abstract]
- Sesques P, Johnson NA: Approach to the diagnosis and treatment of high-grade B-cell lymphomas with MYC and BCL2 and/or BCL6 rearrangements. Blood 129 (3): 280-288, 2017. [PUBMED Abstract]
- Landsburg DJ, Falkiewicz MK, Maly J, et al.: Outcomes of Patients With Double-Hit Lymphoma Who Achieve First Complete Remission. J Clin Oncol 35 (20): 2260-2267, 2017. [PUBMED Abstract]
- Herrera AF, Mei M, Low L, et al.: Relapsed or Refractory Double-Expressor and Double-Hit Lymphomas Have Inferior Progression-Free Survival After Autologous Stem-Cell Transplantation. J Clin Oncol 35 (1): 24-31, 2017. [PUBMED Abstract]
- Canellos GP: CHOP may have been part of the beginning but certainly not the end: issues in risk-related therapy of large-cell lymphoma. J Clin Oncol 15 (5): 1713-6, 1997. [PUBMED Abstract]
- Sha C, Barrans S, Cucco F, et al.: Molecular High-Grade B-Cell Lymphoma: Defining a Poor-Risk Group That Requires Different Approaches to Therapy. J Clin Oncol 37 (3): 202-212, 2019. [PUBMED Abstract]
- Soumerai JD, Rosenthal A, Harkins S, et al.: Next-generation ALK inhibitors are highly active in ALK-positive large B-cell lymphoma. Blood 140 (16): 1822-1826, 2022. [PUBMED Abstract]
- Hu S, Xu-Monette ZY, Balasubramanyam A, et al.: CD30 expression defines a novel subgroup of diffuse large B-cell lymphoma with favorable prognosis and distinct gene expression signature: a report from the International DLBCL Rituximab-CHOP Consortium Program Study. Blood 121 (14): 2715-24, 2013. [PUBMED Abstract]
- Maurer MJ, Ghesquières H, Jais JP, et al.: Event-free survival at 24 months is a robust end point for disease-related outcome in diffuse large B-cell lymphoma treated with immunochemotherapy. J Clin Oncol 32 (10): 1066-73, 2014. [PUBMED Abstract]
- Schmitz N, Zeynalova S, Nickelsen M, et al.: CNS International Prognostic Index: A Risk Model for CNS Relapse in Patients With Diffuse Large B-Cell Lymphoma Treated With R-CHOP. J Clin Oncol 34 (26): 3150-6, 2016. [PUBMED Abstract]
- Zucca E, Conconi A, Mughal TI, et al.: Patterns of outcome and prognostic factors in primary large-cell lymphoma of the testis in a survey by the International Extranodal Lymphoma Study Group. J Clin Oncol 21 (1): 20-7, 2003. [PUBMED Abstract]
- Vitolo U, Chiappella A, Ferreri AJ, et al.: First-line treatment for primary testicular diffuse large B-cell lymphoma with rituximab-CHOP, CNS prophylaxis, and contralateral testis irradiation: final results of an international phase II trial. J Clin Oncol 29 (20): 2766-72, 2011. [PUBMED Abstract]
- Cheah CY, Wirth A, Seymour JF: Primary testicular lymphoma. Blood 123 (4): 486-93, 2014. [PUBMED Abstract]
- Boehme V, Schmitz N, Zeynalova S, et al.: CNS events in elderly patients with aggressive lymphoma treated with modern chemotherapy (CHOP-14) with or without rituximab: an analysis of patients treated in the RICOVER-60 trial of the German High-Grade Non-Hodgkin Lymphoma Study Group (DSHNHL). Blood 113 (17): 3896-902, 2009. [PUBMED Abstract]
- Glantz MJ, Cole BF, Recht L, et al.: High-dose intravenous methotrexate for patients with nonleukemic leptomeningeal cancer: is intrathecal chemotherapy necessary? J Clin Oncol 16 (4): 1561-7, 1998. [PUBMED Abstract]
- Orellana-Noia VM, Reed DR, McCook AA, et al.: Single-route CNS prophylaxis for aggressive non-Hodgkin lymphomas: real-world outcomes from 21 US academic institutions. Blood 139 (3): 413-423, 2022. [PUBMED Abstract]
- Puckrin R, El Darsa H, Ghosh S, et al.: Ineffectiveness of high-dose methotrexate for prevention of CNS relapse in diffuse large B-cell lymphoma. Am J Hematol 96 (7): 764-771, 2021. [PUBMED Abstract]
- Jeong H, Cho H, Kim H, et al.: Efficacy and safety of prophylactic high-dose MTX in high-risk DLBCL: a treatment intent-based analysis. Blood Adv 5 (8): 2142-2152, 2021. [PUBMED Abstract]
- Villa D, Connors JM, Shenkier TN, et al.: Incidence and risk factors for central nervous system relapse in patients with diffuse large B-cell lymphoma: the impact of the addition of rituximab to CHOP chemotherapy. Ann Oncol 21 (5): 1046-52, 2010. [PUBMED Abstract]
- Ferreri AJ, Donadoni G, Cabras MG, et al.: High Doses of Antimetabolites Followed by High-Dose Sequential Chemoimmunotherapy and Autologous Stem-Cell Transplantation in Patients With Systemic B-Cell Lymphoma and Secondary CNS Involvement: Final Results of a Multicenter Phase II Trial. J Clin Oncol 33 (33): 3903-10, 2015. [PUBMED Abstract]
- Schmitz N, Wu HS: Advances in the Treatment of Secondary CNS Lymphoma. J Clin Oncol 33 (33): 3851-3, 2015. [PUBMED Abstract]
- Savage KJ: Primary mediastinal large B-cell lymphoma. Blood 140 (9): 955-970, 2022. [PUBMED Abstract]
- van Besien K, Kelta M, Bahaguna P: Primary mediastinal B-cell lymphoma: a review of pathology and management. J Clin Oncol 19 (6): 1855-64, 2001. [PUBMED Abstract]
- Dunleavy K, Wilson WH: Primary mediastinal B-cell lymphoma and mediastinal gray zone lymphoma: do they require a unique therapeutic approach? Blood 125 (1): 33-9, 2015. [PUBMED Abstract]
- Dunleavy K, Pittaluga S, Maeda LS, et al.: Dose-adjusted EPOCH-rituximab therapy in primary mediastinal B-cell lymphoma. N Engl J Med 368 (15): 1408-16, 2013. [PUBMED Abstract]
- Savage KJ, Yenson PR, Shenkier T, et al.: The outcome of primary mediastinal large B-cell lymphoma in the R-CHOP treatment era. [Abstract] Blood 120 (21): A-303, 2012.
- Vassilakopoulos TP, Pangalis GA, Katsigiannis A, et al.: Rituximab, cyclophosphamide, doxorubicin, vincristine, and prednisone with or without radiotherapy in primary mediastinal large B-cell lymphoma: the emerging standard of care. Oncologist 17 (2): 239-49, 2012. [PUBMED Abstract]
- Rieger M, Osterborg A, Pettengell R, et al.: Primary mediastinal B-cell lymphoma treated with CHOP-like chemotherapy with or without rituximab: results of the Mabthera International Trial Group study. Ann Oncol 22 (3): 664-70, 2011. [PUBMED Abstract]
- Gleeson M, Hawkes EA, Cunningham D, et al.: Rituximab, cyclophosphamide, doxorubicin, vincristine and prednisolone (R-CHOP) in the management of primary mediastinal B-cell lymphoma: a subgroup analysis of the UK NCRI R-CHOP 14 versus 21 trial. Br J Haematol 175 (4): 668-672, 2016. [PUBMED Abstract]
- Held G, Thurner L, Poeschel V, et al.: Role of radiotherapy and dose-densification of R-CHOP in primary mediastinal B-cell lymphoma: A subgroup analysis of the unfolder trial of the German Lymphoma Alliance (GLA). [Abstract] J Clin Oncol 38 (Suppl 15): A-8041, 2021.
- Martelli M, Ceriani L, Zucca E, et al.: [18F]fluorodeoxyglucose positron emission tomography predicts survival after chemoimmunotherapy for primary mediastinal large B-cell lymphoma: results of the International Extranodal Lymphoma Study Group IELSG-26 Study. J Clin Oncol 32 (17): 1769-75, 2014. [PUBMED Abstract]
- Zinzani PL, Broccoli A, Casadei B, et al.: The role of rituximab and positron emission tomography in the treatment of primary mediastinal large B-cell lymphoma: experience on 74 patients. Hematol Oncol 33 (4): 145-50, 2015. [PUBMED Abstract]
- Ceriani L, Martelli M, Conconi A, et al.: Prognostic models for primary mediastinal (thymic) B-cell lymphoma derived from 18-FDG PET/CT quantitative parameters in the International Extranodal Lymphoma Study Group (IELSG) 26 study. Br J Haematol 178 (4): 588-591, 2017. [PUBMED Abstract]
- Hayden AR, Tonseth P, Lee DG, et al.: Outcome of primary mediastinal large B-cell lymphoma using R-CHOP: impact of a PET-adapted approach. Blood 136 (24): 2803-2811, 2020. [PUBMED Abstract]
- Dabaja BS, Hoppe BS, Plastaras JP, et al.: Proton therapy for adults with mediastinal lymphomas: the International Lymphoma Radiation Oncology Group guidelines. Blood 132 (16): 1635-1646, 2018. [PUBMED Abstract]
- Zinzani PL, Santoro A, Gritti G, et al.: Nivolumab Combined With Brentuximab Vedotin for Relapsed/Refractory Primary Mediastinal Large B-Cell Lymphoma: Efficacy and Safety From the Phase II CheckMate 436 Study. J Clin Oncol 37 (33): 3081-3089, 2019. [PUBMED Abstract]
- Armand P, Rodig S, Melnichenko V, et al.: Pembrolizumab in Relapsed or Refractory Primary Mediastinal Large B-Cell Lymphoma. J Clin Oncol 37 (34): 3291-3299, 2019. [PUBMED Abstract]
- Abramson JS, Palomba ML, Gordon LI, et al.: Lisocabtagene maraleucel for patients with relapsed or refractory large B-cell lymphomas (TRANSCEND NHL 001): a multicentre seamless design study. Lancet 396 (10254): 839-852, 2020. [PUBMED Abstract]
- Longo DL: What's the deal with follicular lymphomas? J Clin Oncol 11 (2): 202-8, 1993. [PUBMED Abstract]
- Anderson JR, Vose JM, Bierman PJ, et al.: Clinical features and prognosis of follicular large-cell lymphoma: a report from the Nebraska Lymphoma Study Group. J Clin Oncol 11 (2): 218-24, 1993. [PUBMED Abstract]
- Bartlett NL, Rizeq M, Dorfman RF, et al.: Follicular large-cell lymphoma: intermediate or low grade? J Clin Oncol 12 (7): 1349-57, 1994. [PUBMED Abstract]
- Wendum D, Sebban C, Gaulard P, et al.: Follicular large-cell lymphoma treated with intensive chemotherapy: an analysis of 89 cases included in the LNH87 trial and comparison with the outcome of diffuse large B-cell lymphoma. Groupe d'Etude des Lymphomes de l'Adulte. J Clin Oncol 15 (4): 1654-63, 1997. [PUBMED Abstract]
- Hans CP, Weisenburger DD, Vose JM, et al.: A significant diffuse component predicts for inferior survival in grade 3 follicular lymphoma, but cytologic subtypes do not predict survival. Blood 101 (6): 2363-7, 2003. [PUBMED Abstract]
- Vose JM, Bierman PJ, Lynch JC, et al.: Effect of follicularity on autologous transplantation for large-cell non-Hodgkin's lymphoma. J Clin Oncol 16 (3): 844-9, 1998. [PUBMED Abstract]
- Bai RY, Ouyang T, Miething C, et al.: Nucleophosmin-anaplastic lymphoma kinase associated with anaplastic large-cell lymphoma activates the phosphatidylinositol 3-kinase/Akt antiapoptotic signaling pathway. Blood 96 (13): 4319-27, 2000. [PUBMED Abstract]
- Hapgood G, Savage KJ: The biology and management of systemic anaplastic large cell lymphoma. Blood 126 (1): 17-25, 2015. [PUBMED Abstract]
- Gascoyne RD, Aoun P, Wu D, et al.: Prognostic significance of anaplastic lymphoma kinase (ALK) protein expression in adults with anaplastic large cell lymphoma. Blood 93 (11): 3913-21, 1999. [PUBMED Abstract]
- Sibon D, Fournier M, Brière J, et al.: Long-term outcome of adults with systemic anaplastic large-cell lymphoma treated within the Groupe d'Etude des Lymphomes de l'Adulte trials. J Clin Oncol 30 (32): 3939-46, 2012. [PUBMED Abstract]
- Horwitz S, O'Connor OA, Pro B, et al.: Brentuximab vedotin with chemotherapy for CD30-positive peripheral T-cell lymphoma (ECHELON-2): a global, double-blind, randomised, phase 3 trial. Lancet 393 (10168): 229-240, 2019. [PUBMED Abstract]
- Younes A, Bartlett NL, Leonard JP, et al.: Brentuximab vedotin (SGN-35) for relapsed CD30-positive lymphomas. N Engl J Med 363 (19): 1812-21, 2010. [PUBMED Abstract]
- Pro B, Advani R, Brice P, et al.: Brentuximab vedotin (SGN-35) in patients with relapsed or refractory systemic anaplastic large-cell lymphoma: results of a phase II study. J Clin Oncol 30 (18): 2190-6, 2012. [PUBMED Abstract]
- Prince HM, Kim YH, Horwitz SM, et al.: Brentuximab vedotin or physician's choice in CD30-positive cutaneous T-cell lymphoma (ALCANZA): an international, open-label, randomised, phase 3, multicentre trial. Lancet 390 (10094): 555-566, 2017. [PUBMED Abstract]
- Pro B, Advani R, Brice P, et al.: Five-year results of brentuximab vedotin in patients with relapsed or refractory systemic anaplastic large cell lymphoma. Blood 130 (25): 2709-2717, 2017. [PUBMED Abstract]
- Coiffier B, Pro B, Prince HM, et al.: Results from a pivotal, open-label, phase II study of romidepsin in relapsed or refractory peripheral T-cell lymphoma after prior systemic therapy. J Clin Oncol 30 (6): 631-6, 2012. [PUBMED Abstract]
- O'Connor OA, Horwitz S, Hamlin P, et al.: Phase II-I-II study of two different doses and schedules of pralatrexate, a high-affinity substrate for the reduced folate carrier, in patients with relapsed or refractory lymphoma reveals marked activity in T-cell malignancies. J Clin Oncol 27 (26): 4357-64, 2009. [PUBMED Abstract]
- Smith SM, Burns LJ, van Besien K, et al.: Hematopoietic cell transplantation for systemic mature T-cell non-Hodgkin lymphoma. J Clin Oncol 31 (25): 3100-9, 2013. [PUBMED Abstract]
- Brink M, Meeuwes FO, van der Poel MWM, et al.: Impact of etoposide and ASCT on survival among patients aged <65 years with stage II to IV PTCL: a population-based cohort study. Blood 140 (9): 1009-1019, 2022. [PUBMED Abstract]
- Seidemann K, Tiemann M, Schrappe M, et al.: Short-pulse B-non-Hodgkin lymphoma-type chemotherapy is efficacious treatment for pediatric anaplastic large cell lymphoma: a report of the Berlin-Frankfurt-Münster Group Trial NHL-BFM 90. Blood 97 (12): 3699-706, 2001. [PUBMED Abstract]
- Miranda RN, Aladily TN, Prince HM, et al.: Breast implant-associated anaplastic large-cell lymphoma: long-term follow-up of 60 patients. J Clin Oncol 32 (2): 114-20, 2014. [PUBMED Abstract]
- Clemens MW, Medeiros LJ, Butler CE, et al.: Complete Surgical Excision Is Essential for the Management of Patients With Breast Implant-Associated Anaplastic Large-Cell Lymphoma. J Clin Oncol 34 (2): 160-8, 2016. [PUBMED Abstract]
- Mehta-Shah N, Clemens MW, Horwitz SM: How I treat breast implant-associated anaplastic large cell lymphoma. Blood 132 (18): 1889-1898, 2018. [PUBMED Abstract]
- Jaffe ES, Ashar BS, Clemens MW, et al.: Best Practices Guideline for the Pathologic Diagnosis of Breast Implant-Associated Anaplastic Large-Cell Lymphoma. J Clin Oncol 38 (10): 1102-1111, 2020. [PUBMED Abstract]
- Los-de Vries GT, de Boer M, van Dijk E, et al.: Chromosome 20 loss is characteristic of breast implant-associated anaplastic large cell lymphoma. Blood 136 (25): 2927-2932, 2020. [PUBMED Abstract]
- Tse E, Kwong YL: How I treat NK/T-cell lymphomas. Blood 121 (25): 4997-5005, 2013. [PUBMED Abstract]
- Rizvi MA, Evens AM, Tallman MS, et al.: T-cell non-Hodgkin lymphoma. Blood 107 (4): 1255-64, 2006. [PUBMED Abstract]
- Li YX, Yao B, Jin J, et al.: Radiotherapy as primary treatment for stage IE and IIE nasal natural killer/T-cell lymphoma. J Clin Oncol 24 (1): 181-9, 2006. [PUBMED Abstract]
- Lee J, Suh C, Park YH, et al.: Extranodal natural killer T-cell lymphoma, nasal-type: a prognostic model from a retrospective multicenter study. J Clin Oncol 24 (4): 612-8, 2006. [PUBMED Abstract]
- Li CC, Tien HF, Tang JL, et al.: Treatment outcome and pattern of failure in 77 patients with sinonasal natural killer/T-cell or T-cell lymphoma. Cancer 100 (2): 366-75, 2004. [PUBMED Abstract]
- Yamaguchi M, Tobinai K, Oguchi M, et al.: Phase I/II study of concurrent chemoradiotherapy for localized nasal natural killer/T-cell lymphoma: Japan Clinical Oncology Group Study JCOG0211. J Clin Oncol 27 (33): 5594-600, 2009. [PUBMED Abstract]
- Kim SJ, Kim K, Kim BS, et al.: Phase II trial of concurrent radiation and weekly cisplatin followed by VIPD chemotherapy in newly diagnosed, stage IE to IIE, nasal, extranodal NK/T-Cell Lymphoma: Consortium for Improving Survival of Lymphoma study. J Clin Oncol 27 (35): 6027-32, 2009. [PUBMED Abstract]
- Li YX, Fang H, Liu QF, et al.: Clinical features and treatment outcome of nasal-type NK/T-cell lymphoma of Waldeyer ring. Blood 112 (8): 3057-64, 2008. [PUBMED Abstract]
- Vargo JA, Patel A, Glaser SM, et al.: The impact of the omission or inadequate dosing of radiotherapy in extranodal natural killer T-cell lymphoma, nasal type, in the United States. Cancer 123 (16): 3176-3185, 2017. [PUBMED Abstract]
- Yamaguchi M, Suzuki R, Oguchi M: Advances in the treatment of extranodal NK/T-cell lymphoma, nasal type. Blood 131 (23): 2528-2540, 2018. [PUBMED Abstract]
- Yang Y, Cao JZ, Lan SM, et al.: Association of Improved Locoregional Control With Prolonged Survival in Early-Stage Extranodal Nasal-Type Natural Killer/T-Cell Lymphoma. JAMA Oncol 3 (1): 83-91, 2017. [PUBMED Abstract]
- Yang Y, Zhu Y, Cao JZ, et al.: Risk-adapted therapy for early-stage extranodal nasal-type NK/T-cell lymphoma: analysis from a multicenter study. Blood 126 (12): 1424-32; quiz 1517, 2015. [PUBMED Abstract]
- Yamaguchi M, Suzuki R, Oguchi M, et al.: Treatments and Outcomes of Patients With Extranodal Natural Killer/T-Cell Lymphoma Diagnosed Between 2000 and 2013: A Cooperative Study in Japan. J Clin Oncol 35 (1): 32-39, 2017. [PUBMED Abstract]
- Kwong YL, Kim SJ, Tse E, et al.: Sequential chemotherapy/radiotherapy was comparable with concurrent chemoradiotherapy for stage I/II NK/T-cell lymphoma. Ann Oncol 29 (1): 256-263, 2018. [PUBMED Abstract]
- Liang R, Todd D, Chan TK, et al.: Treatment outcome and prognostic factors for primary nasal lymphoma. J Clin Oncol 13 (3): 666-70, 1995. [PUBMED Abstract]
- Cheung MM, Chan JK, Lau WH, et al.: Primary non-Hodgkin's lymphoma of the nose and nasopharynx: clinical features, tumor immunophenotype, and treatment outcome in 113 patients. J Clin Oncol 16 (1): 70-7, 1998. [PUBMED Abstract]
- Hausdorff J, Davis E, Long G, et al.: Non-Hodgkin's lymphoma of the paranasal sinuses: clinical and pathological features, and response to combined-modality therapy. Cancer J Sci Am 3 (5): 303-11, 1997 Sep-Oct. [PUBMED Abstract]
- Le Gouill S, Milpied N, Buzyn A, et al.: Graft-versus-lymphoma effect for aggressive T-cell lymphomas in adults: a study by the Société Francaise de Greffe de Moëlle et de Thérapie Cellulaire. J Clin Oncol 26 (14): 2264-71, 2008. [PUBMED Abstract]
- Au WY, Weisenburger DD, Intragumtornchai T, et al.: Clinical differences between nasal and extranasal natural killer/T-cell lymphoma: a study of 136 cases from the International Peripheral T-Cell Lymphoma Project. Blood 113 (17): 3931-7, 2009. [PUBMED Abstract]
- Jaccard A, Gachard N, Marin B, et al.: Efficacy of L-asparaginase with methotrexate and dexamethasone (AspaMetDex regimen) in patients with refractory or relapsing extranodal NK/T-cell lymphoma, a phase 2 study. Blood 117 (6): 1834-9, 2011. [PUBMED Abstract]
- Yamaguchi M, Kwong YL, Kim WS, et al.: Phase II study of SMILE chemotherapy for newly diagnosed stage IV, relapsed, or refractory extranodal natural killer (NK)/T-cell lymphoma, nasal type: the NK-Cell Tumor Study Group study. J Clin Oncol 29 (33): 4410-6, 2011. [PUBMED Abstract]
- Li JW, Li YJ, Zhong MZ, et al.: Efficacy and tolerance of GELOXD/P-GEMOXD in newly diagnosed nasal-type extranodal NK/T-cell lymphoma: A multicenter retrospective study. Eur J Haematol 100 (3): 247-256, 2018. [PUBMED Abstract]
- Wei L, Wang L, Cong J, et al.: SVILE regimen, a combination of dexamethasone, vindesine, ifosfamide, pegaspargase, and etoposide, for treating relapsed/refractory extranodal natural killer/T-cell lymphoma, nasal type. Leuk Res 96: 106422, 2020. [PUBMED Abstract]
- Liang R, Gao GX, Chen JP, et al.: A phase 2 study of methotrexate, etoposide, dexamethasone, and pegaspargase chemotherapy for newly diagnosed, relapsed, or refractory extranodal natural killer/T-cell lymphoma, nasal type: a multicenter trial in Northwest China. Hematol Oncol 35 (4): 619-629, 2017. [PUBMED Abstract]
- Wang X, Zhang L, Liu X, et al.: Efficacy and Safety of a Pegasparaginase-Based Chemotherapy Regimen vs an L-asparaginase-Based Chemotherapy Regimen for Newly Diagnosed Advanced Extranodal Natural Killer/T-Cell Lymphoma: A Randomized Clinical Trial. JAMA Oncol 8 (7): 1035-1041, 2022. [PUBMED Abstract]
- Mraz-Gernhard S, Natkunam Y, Hoppe RT, et al.: Natural killer/natural killer-like T-cell lymphoma, CD56+, presenting in the skin: an increasingly recognized entity with an aggressive course. J Clin Oncol 19 (8): 2179-88, 2001. [PUBMED Abstract]
- Mansoor A, Pittaluga S, Beck PL, et al.: NK-cell enteropathy: a benign NK-cell lymphoproliferative disease mimicking intestinal lymphoma: clinicopathologic features and follow-up in a unique case series. Blood 117 (5): 1447-52, 2011. [PUBMED Abstract]
- Kim SJ, Lim JQ, Laurensia Y, et al.: Avelumab for the treatment of relapsed or refractory extranodal NK/T-cell lymphoma: an open-label phase 2 study. Blood 136 (24): 2754-2763, 2020. [PUBMED Abstract]
- Kwong YL, Chan TSY, Tan D, et al.: PD1 blockade with pembrolizumab is highly effective in relapsed or refractory NK/T-cell lymphoma failing l-asparaginase. Blood 129 (17): 2437-2442, 2017. [PUBMED Abstract]
- Guinee D, Jaffe E, Kingma D, et al.: Pulmonary lymphomatoid granulomatosis. Evidence for a proliferation of Epstein-Barr virus infected B-lymphocytes with a prominent T-cell component and vasculitis. Am J Surg Pathol 18 (8): 753-64, 1994. [PUBMED Abstract]
- Myers JL, Kurtin PJ, Katzenstein AL, et al.: Lymphomatoid granulomatosis. Evidence of immunophenotypic diversity and relationship to Epstein-Barr virus infection. Am J Surg Pathol 19 (11): 1300-12, 1995. [PUBMED Abstract]
- Siegert W, Agthe A, Griesser H, et al.: Treatment of angioimmunoblastic lymphadenopathy (AILD)-type T-cell lymphoma using prednisone with or without the COPBLAM/IMVP-16 regimen. A multicenter study. Kiel Lymphoma Study Group. Ann Intern Med 117 (5): 364-70, 1992. [PUBMED Abstract]
- Jaffe ES: Angioimmunoblastic T-cell lymphoma: new insights, but the clinical challenge remains. Ann Oncol 6 (7): 631-2, 1995. [PUBMED Abstract]
- Siegert W, Nerl C, Agthe A, et al.: Angioimmunoblastic lymphadenopathy (AILD)-type T-cell lymphoma: prognostic impact of clinical observations and laboratory findings at presentation. The Kiel Lymphoma Study Group. Ann Oncol 6 (7): 659-64, 1995. [PUBMED Abstract]
- Lunning MA, Vose JM: Angioimmunoblastic T-cell lymphoma: the many-faced lymphoma. Blood 129 (9): 1095-1102, 2017. [PUBMED Abstract]
- Bräuninger A, Spieker T, Willenbrock K, et al.: Survival and clonal expansion of mutating "forbidden" (immunoglobulin receptor-deficient) epstein-barr virus-infected b cells in angioimmunoblastic t cell lymphoma. J Exp Med 194 (7): 927-40, 2001. [PUBMED Abstract]
- Federico M, Rudiger T, Bellei M, et al.: Clinicopathologic characteristics of angioimmunoblastic T-cell lymphoma: analysis of the international peripheral T-cell lymphoma project. J Clin Oncol 31 (2): 240-6, 2013. [PUBMED Abstract]
- Reimer P, Rüdiger T, Geissinger E, et al.: Autologous stem-cell transplantation as first-line therapy in peripheral T-cell lymphomas: results of a prospective multicenter study. J Clin Oncol 27 (1): 106-13, 2009. [PUBMED Abstract]
- Kyriakou C, Canals C, Finke J, et al.: Allogeneic stem cell transplantation is able to induce long-term remissions in angioimmunoblastic T-cell lymphoma: a retrospective study from the lymphoma working party of the European group for blood and marrow transplantation. J Clin Oncol 27 (24): 3951-8, 2009. [PUBMED Abstract]
- Park SI, Horwitz SM, Foss FM, et al.: The role of autologous stem cell transplantation in patients with nodal peripheral T-cell lymphomas in first complete remission: Report from COMPLETE, a prospective, multicenter cohort study. Cancer 125 (9): 1507-1517, 2019. [PUBMED Abstract]
- Advani R, Horwitz S, Zelenetz A, et al.: Angioimmunoblastic T cell lymphoma: treatment experience with cyclosporine. Leuk Lymphoma 48 (3): 521-5, 2007. [PUBMED Abstract]
- Amengual JE, Lichtenstein R, Lue J, et al.: A phase 1 study of romidepsin and pralatrexate reveals marked activity in relapsed and refractory T-cell lymphoma. Blood 131 (4): 397-407, 2018. [PUBMED Abstract]
- Damaj G, Gressin R, Bouabdallah K, et al.: Results from a prospective, open-label, phase II trial of bendamustine in refractory or relapsed T-cell lymphomas: the BENTLY trial. J Clin Oncol 31 (1): 104-10, 2013. [PUBMED Abstract]
- Fanale MA, Horwitz SM, Forero-Torres A, et al.: Five-year outcomes for frontline brentuximab vedotin with CHP for CD30-expressing peripheral T-cell lymphomas. Blood 131 (19): 2120-2124, 2018. [PUBMED Abstract]
- Rüdiger T, Weisenburger DD, Anderson JR, et al.: Peripheral T-cell lymphoma (excluding anaplastic large-cell lymphoma): results from the Non-Hodgkin's Lymphoma Classification Project. Ann Oncol 13 (1): 140-9, 2002. [PUBMED Abstract]
- Weisenburger DD, Savage KJ, Harris NL, et al.: Peripheral T-cell lymphoma, not otherwise specified: a report of 340 cases from the International Peripheral T-cell Lymphoma Project. Blood 117 (12): 3402-8, 2011. [PUBMED Abstract]
- Sonnen R, Schmidt WP, Müller-Hermelink HK, et al.: The International Prognostic Index determines the outcome of patients with nodal mature T-cell lymphomas. Br J Haematol 129 (3): 366-72, 2005. [PUBMED Abstract]
- Maurer MJ, Ellin F, Srour L, et al.: International Assessment of Event-Free Survival at 24 Months and Subsequent Survival in Peripheral T-Cell Lymphoma. J Clin Oncol 35 (36): 4019-4026, 2017. [PUBMED Abstract]
- Carson KR, Horwitz SM, Pinter-Brown LC, et al.: A prospective cohort study of patients with peripheral T-cell lymphoma in the United States. Cancer 123 (7): 1174-1183, 2017. [PUBMED Abstract]
- Briski R, Feldman AL, Bailey NG, et al.: Survival in patients with limited-stage peripheral T-cell lymphomas. Leuk Lymphoma 56 (6): 1665-70, 2015. [PUBMED Abstract]
- Rodriguez J, Munsell M, Yazji S, et al.: Impact of high-dose chemotherapy on peripheral T-cell lymphomas. J Clin Oncol 19 (17): 3766-70, 2001. [PUBMED Abstract]
- d'Amore F, Relander T, Lauritzsen GF, et al.: Up-front autologous stem-cell transplantation in peripheral T-cell lymphoma: NLG-T-01. J Clin Oncol 30 (25): 3093-9, 2012. [PUBMED Abstract]
- Schmitz N, Lenz G, Stelljes M: Allogeneic hematopoietic stem cell transplantation for T-cell lymphomas. Blood 132 (3): 245-253, 2018. [PUBMED Abstract]
- Schmitz N, Truemper L, Bouabdallah K, et al.: A randomized phase 3 trial of autologous vs allogeneic transplantation as part of first-line therapy in poor-risk peripheral T-NHL. Blood 137 (19): 2646-2656, 2021. [PUBMED Abstract]
- O'Connor OA, Pro B, Pinter-Brown L, et al.: Pralatrexate in patients with relapsed or refractory peripheral T-cell lymphoma: results from the pivotal PROPEL study. J Clin Oncol 29 (9): 1182-9, 2011. [PUBMED Abstract]
- O'Connor OA, Horwitz S, Masszi T, et al.: Belinostat in Patients With Relapsed or Refractory Peripheral T-Cell Lymphoma: Results of the Pivotal Phase II BELIEF (CLN-19) Study. J Clin Oncol 33 (23): 2492-9, 2015. [PUBMED Abstract]
- Belhadj K, Reyes F, Farcet JP, et al.: Hepatosplenic gammadelta T-cell lymphoma is a rare clinicopathologic entity with poor outcome: report on a series of 21 patients. Blood 102 (13): 4261-9, 2003. [PUBMED Abstract]
- Chanan-Khan A, Islam T, Alam A, et al.: Long-term survival with allogeneic stem cell transplant and donor lymphocyte infusion following salvage therapy with anti-CD52 monoclonal antibody (Campath) in a patient with alpha/beta hepatosplenic T-cell non-Hodgkin's lymphoma. Leuk Lymphoma 45 (8): 1673-5, 2004. [PUBMED Abstract]
- Pro B, Allen P, Behdad A: Hepatosplenic T-cell lymphoma: a rare but challenging entity. Blood 136 (18): 2018-2026, 2020. [PUBMED Abstract]
- Go RS, Wester SM: Immunophenotypic and molecular features, clinical outcomes, treatments, and prognostic factors associated with subcutaneous panniculitis-like T-cell lymphoma: a systematic analysis of 156 patients reported in the literature. Cancer 101 (6): 1404-13, 2004. [PUBMED Abstract]
- Marzano AV, Berti E, Paulli M, et al.: Cytophagic histiocytic panniculitis and subcutaneous panniculitis-like T-cell lymphoma: report of 7 cases. Arch Dermatol 136 (7): 889-96, 2000. [PUBMED Abstract]
- Hoque SR, Child FJ, Whittaker SJ, et al.: Subcutaneous panniculitis-like T-cell lymphoma: a clinicopathological, immunophenotypic and molecular analysis of six patients. Br J Dermatol 148 (3): 516-25, 2003. [PUBMED Abstract]
- Salhany KE, Macon WR, Choi JK, et al.: Subcutaneous panniculitis-like T-cell lymphoma: clinicopathologic, immunophenotypic, and genotypic analysis of alpha/beta and gamma/delta subtypes. Am J Surg Pathol 22 (7): 881-93, 1998. [PUBMED Abstract]
- Massone C, Chott A, Metze D, et al.: Subcutaneous, blastic natural killer (NK), NK/T-cell, and other cytotoxic lymphomas of the skin: a morphologic, immunophenotypic, and molecular study of 50 patients. Am J Surg Pathol 28 (6): 719-35, 2004. [PUBMED Abstract]
- Arnulf B, Copie-Bergman C, Delfau-Larue MH, et al.: Nonhepatosplenic gammadelta T-cell lymphoma: a subset of cytotoxic lymphomas with mucosal or skin localization. Blood 91 (5): 1723-31, 1998. [PUBMED Abstract]
- Toro JR, Liewehr DJ, Pabby N, et al.: Gamma-delta T-cell phenotype is associated with significantly decreased survival in cutaneous T-cell lymphoma. Blood 101 (9): 3407-12, 2003. [PUBMED Abstract]
- Perry AM, Warnke RA, Hu Q, et al.: Indolent T-cell lymphoproliferative disease of the gastrointestinal tract. Blood 122 (22): 3599-606, 2013. [PUBMED Abstract]
- Egan LJ, Walsh SV, Stevens FM, et al.: Celiac-associated lymphoma. A single institution experience of 30 cases in the combination chemotherapy era. J Clin Gastroenterol 21 (2): 123-9, 1995. [PUBMED Abstract]
- Gale J, Simmonds PD, Mead GM, et al.: Enteropathy-type intestinal T-cell lymphoma: clinical features and treatment of 31 patients in a single center. J Clin Oncol 18 (4): 795-803, 2000. [PUBMED Abstract]
- Di Sabatino A, Biagi F, Gobbi PG, et al.: How I treat enteropathy-associated T-cell lymphoma. Blood 119 (11): 2458-68, 2012. [PUBMED Abstract]
- Daum S, Ullrich R, Heise W, et al.: Intestinal non-Hodgkin's lymphoma: a multicenter prospective clinical study from the German Study Group on Intestinal non-Hodgkin's Lymphoma. J Clin Oncol 21 (14): 2740-6, 2003. [PUBMED Abstract]
- Sieniawski M, Angamuthu N, Boyd K, et al.: Evaluation of enteropathy-associated T-cell lymphoma comparing standard therapies with a novel regimen including autologous stem cell transplantation. Blood 115 (18): 3664-70, 2010. [PUBMED Abstract]
- Shimada K, Matsue K, Yamamoto K, et al.: Retrospective analysis of intravascular large B-cell lymphoma treated with rituximab-containing chemotherapy as reported by the IVL study group in Japan. J Clin Oncol 26 (19): 3189-95, 2008. [PUBMED Abstract]
- Ponzoni M, Ferreri AJ, Campo E, et al.: Definition, diagnosis, and management of intravascular large B-cell lymphoma: proposals and perspectives from an international consensus meeting. J Clin Oncol 25 (21): 3168-73, 2007. [PUBMED Abstract]
- Shimada K, Yamaguchi M, Atsuta Y, et al.: Rituximab, cyclophosphamide, doxorubicin, vincristine, and prednisolone combined with high-dose methotrexate plus intrathecal chemotherapy for newly diagnosed intravascular large B-cell lymphoma (PRIMEUR-IVL): a multicentre, single-arm, phase 2 trial. Lancet Oncol 21 (4): 593-602, 2020. [PUBMED Abstract]
- Blum KA, Lozanski G, Byrd JC: Adult Burkitt leukemia and lymphoma. Blood 104 (10): 3009-20, 2004. [PUBMED Abstract]
- Onciu M, Schlette E, Zhou Y, et al.: Secondary chromosomal abnormalities predict outcome in pediatric and adult high-stage Burkitt lymphoma. Cancer 107 (5): 1084-92, 2006. [PUBMED Abstract]
- Macpherson N, Lesack D, Klasa R, et al.: Small noncleaved, non-Burkitt's (Burkit-Like) lymphoma: cytogenetics predict outcome and reflect clinical presentation. J Clin Oncol 17 (5): 1558-67, 1999. [PUBMED Abstract]
- Dave SS, Fu K, Wright GW, et al.: Molecular diagnosis of Burkitt's lymphoma. N Engl J Med 354 (23): 2431-42, 2006. [PUBMED Abstract]
- Hummel M, Bentink S, Berger H, et al.: A biologic definition of Burkitt's lymphoma from transcriptional and genomic profiling. N Engl J Med 354 (23): 2419-30, 2006. [PUBMED Abstract]
- Salaverria I, Siebert R: The gray zone between Burkitt's lymphoma and diffuse large B-cell lymphoma from a genetics perspective. J Clin Oncol 29 (14): 1835-43, 2011. [PUBMED Abstract]
- Thomas DA, Faderl S, O'Brien S, et al.: Chemoimmunotherapy with hyper-CVAD plus rituximab for the treatment of adult Burkitt and Burkitt-type lymphoma or acute lymphoblastic leukemia. Cancer 106 (7): 1569-80, 2006. [PUBMED Abstract]
- Dunleavy K, Pittaluga S, Shovlin M, et al.: Low-intensity therapy in adults with Burkitt's lymphoma. N Engl J Med 369 (20): 1915-25, 2013. [PUBMED Abstract]
- Hoelzer D, Walewski J, Döhner H, et al.: Improved outcome of adult Burkitt lymphoma/leukemia with rituximab and chemotherapy: report of a large prospective multicenter trial. Blood 124 (26): 3870-9, 2014. [PUBMED Abstract]
- Ribrag V, Koscielny S, Bosq J, et al.: Rituximab and dose-dense chemotherapy for adults with Burkitt's lymphoma: a randomised, controlled, open-label, phase 3 trial. Lancet 387 (10036): 2402-11, 2016. [PUBMED Abstract]
- Magrath I, Adde M, Shad A, et al.: Adults and children with small non-cleaved-cell lymphoma have a similar excellent outcome when treated with the same chemotherapy regimen. J Clin Oncol 14 (3): 925-34, 1996. [PUBMED Abstract]
- Hoelzer D, Ludwig WD, Thiel E, et al.: Improved outcome in adult B-cell acute lymphoblastic leukemia. Blood 87 (2): 495-508, 1996. [PUBMED Abstract]
- Lee EJ, Petroni GR, Schiffer CA, et al.: Brief-duration high-intensity chemotherapy for patients with small noncleaved-cell lymphoma or FAB L3 acute lymphocytic leukemia: results of cancer and leukemia group B study 9251. J Clin Oncol 19 (20): 4014-22, 2001. [PUBMED Abstract]
- Mead GM, Sydes MR, Walewski J, et al.: An international evaluation of CODOX-M and CODOX-M alternating with IVAC in adult Burkitt's lymphoma: results of United Kingdom Lymphoma Group LY06 study. Ann Oncol 13 (8): 1264-74, 2002. [PUBMED Abstract]
- Rizzieri DA, Johnson JL, Niedzwiecki D, et al.: Intensive chemotherapy with and without cranial radiation for Burkitt leukemia and lymphoma: final results of Cancer and Leukemia Group B Study 9251. Cancer 100 (7): 1438-48, 2004. [PUBMED Abstract]
- Noy A, Lee JY, Cesarman E, et al.: AMC 048: modified CODOX-M/IVAC-rituximab is safe and effective for HIV-associated Burkitt lymphoma. Blood 126 (2): 160-6, 2015. [PUBMED Abstract]
- Morel P, Lepage E, Brice P, et al.: Prognosis and treatment of lymphoblastic lymphoma in adults: a report on 80 patients. J Clin Oncol 10 (7): 1078-85, 1992. [PUBMED Abstract]
- Verdonck LF, Dekker AW, de Gast GC, et al.: Autologous bone marrow transplantation for adult poor-risk lymphoblastic lymphoma in first remission. J Clin Oncol 10 (4): 644-6, 1992. [PUBMED Abstract]
- Thomas DA, O'Brien S, Cortes J, et al.: Outcome with the hyper-CVAD regimens in lymphoblastic lymphoma. Blood 104 (6): 1624-30, 2004. [PUBMED Abstract]
- Sweetenham JW, Santini G, Qian W, et al.: High-dose therapy and autologous stem-cell transplantation versus conventional-dose consolidation/maintenance therapy as postremission therapy for adult patients with lymphoblastic lymphoma: results of a randomized trial of the European Group for Blood and Marrow Transplantation and the United Kingdom Lymphoma Group. J Clin Oncol 19 (11): 2927-36, 2001. [PUBMED Abstract]
- Höllsberg P, Hafler DA: Seminars in medicine of the Beth Israel Hospital, Boston. Pathogenesis of diseases induced by human lymphotropic virus type I infection. N Engl J Med 328 (16): 1173-82, 1993. [PUBMED Abstract]
- Foss FM, Aquino SL, Ferry JA: Case records of the Massachusetts General Hospital. Weekly clinicopathological exercises. Case 10-2003. A 72-year-old man with rapidly progressive leukemia, rash, and multiorgan failure. N Engl J Med 348 (13): 1267-75, 2003. [PUBMED Abstract]
- Shimoyama M: Diagnostic criteria and classification of clinical subtypes of adult T-cell leukaemia-lymphoma. A report from the Lymphoma Study Group (1984-87). Br J Haematol 79 (3): 428-37, 1991. [PUBMED Abstract]
- Takasaki Y, Iwanaga M, Imaizumi Y, et al.: Long-term study of indolent adult T-cell leukemia-lymphoma. Blood 115 (22): 4337-43, 2010. [PUBMED Abstract]
- Yamada Y, Tomonaga M, Fukuda H, et al.: A new G-CSF-supported combination chemotherapy, LSG15, for adult T-cell leukaemia-lymphoma: Japan Clinical Oncology Group Study 9303. Br J Haematol 113 (2): 375-82, 2001. [PUBMED Abstract]
- Fukushima T, Miyazaki Y, Honda S, et al.: Allogeneic hematopoietic stem cell transplantation provides sustained long-term survival for patients with adult T-cell leukemia/lymphoma. Leukemia 19 (5): 829-34, 2005. [PUBMED Abstract]
- Katsuya H, Yamanaka T, Ishitsuka K, et al.: Prognostic index for acute- and lymphoma-type adult T-cell leukemia/lymphoma. J Clin Oncol 30 (14): 1635-40, 2012. [PUBMED Abstract]
- Itonaga H, Tsushima H, Taguchi J, et al.: Treatment of relapsed adult T-cell leukemia/lymphoma after allogeneic hematopoietic stem cell transplantation: the Nagasaki Transplant Group experience. Blood 121 (1): 219-25, 2013. [PUBMED Abstract]
- Ishida T, Hishizawa M, Kato K, et al.: Allogeneic hematopoietic stem cell transplantation for adult T-cell leukemia-lymphoma with special emphasis on preconditioning regimen: a nationwide retrospective study. Blood 120 (8): 1734-41, 2012. [PUBMED Abstract]
- Katsuya H, Ishitsuka K, Utsunomiya A, et al.: Treatment and survival among 1594 patients with ATL. Blood 126 (24): 2570-7, 2015. [PUBMED Abstract]
- Gill PS, Harrington W, Kaplan MH, et al.: Treatment of adult T-cell leukemia-lymphoma with a combination of interferon alfa and zidovudine. N Engl J Med 332 (26): 1744-8, 1995. [PUBMED Abstract]
- Matutes E, Taylor GP, Cavenagh J, et al.: Interferon alpha and zidovudine therapy in adult T-cell leukaemia lymphoma: response and outcome in 15 patients. Br J Haematol 113 (3): 779-84, 2001. [PUBMED Abstract]
- Hermine O, Allard I, Lévy V, et al.: A prospective phase II clinical trial with the use of zidovudine and interferon-alpha in the acute and lymphoma forms of adult T-cell leukemia/lymphoma. Hematol J 3 (6): 276-82, 2002. [PUBMED Abstract]
- Bazarbachi A, Plumelle Y, Carlos Ramos J, et al.: Meta-analysis on the use of zidovudine and interferon-alfa in adult T-cell leukemia/lymphoma showing improved survival in the leukemic subtypes. J Clin Oncol 28 (27): 4177-83, 2010. [PUBMED Abstract]
- Bazarbachi A, Suarez F, Fields P, et al.: How I treat adult T-cell leukemia/lymphoma. Blood 118 (7): 1736-45, 2011. [PUBMED Abstract]
- Ishida T, Fujiwara H, Nosaka K, et al.: Multicenter Phase II Study of Lenalidomide in Relapsed or Recurrent Adult T-Cell Leukemia/Lymphoma: ATLL-002. J Clin Oncol 34 (34): 4086-4093, 2016. [PUBMED Abstract]
- Simone CB, Morris JC, Stewart DM, et al.: Radiation therapy for the management of patients with HTLV-1-associated adult T-cell leukemia/lymphoma. Blood 120 (9): 1816-9, 2012. [PUBMED Abstract]
- Ureshino H, Kamachi K, Kimura S: Mogamulizumab for the Treatment of Adult T-cell Leukemia/Lymphoma. Clin Lymphoma Myeloma Leuk 19 (6): 326-331, 2019. [PUBMED Abstract]
- Cohen JB, Zain JM, Kahl BS: Current Approaches to Mantle Cell Lymphoma: Diagnosis, Prognosis, and Therapies. Am Soc Clin Oncol Educ Book 37: 512-525, 2017. [PUBMED Abstract]
- Clot G, Jares P, Giné E, et al.: A gene signature that distinguishes conventional and leukemic nonnodal mantle cell lymphoma helps predict outcome. Blood 132 (4): 413-422, 2018. [PUBMED Abstract]
- Greenwell IB, Staton AD, Lee MJ, et al.: Complex karyotype in patients with mantle cell lymphoma predicts inferior survival and poor response to intensive induction therapy. Cancer 124 (11): 2306-2315, 2018. [PUBMED Abstract]
- Dreyling M, Klapper W, Rule S: Blastoid and pleomorphic mantle cell lymphoma: still a diagnostic and therapeutic challenge! Blood 132 (26): 2722-2729, 2018. [PUBMED Abstract]
- Jain P, Dreyling M, Seymour JF, et al.: High-Risk Mantle Cell Lymphoma: Definition, Current Challenges, and Management. J Clin Oncol 38 (36): 4302-4316, 2020. [PUBMED Abstract]
- Herrmann A, Hoster E, Zwingers T, et al.: Improvement of overall survival in advanced stage mantle cell lymphoma. J Clin Oncol 27 (4): 511-8, 2009. [PUBMED Abstract]
- Majlis A, Pugh WC, Rodriguez MA, et al.: Mantle cell lymphoma: correlation of clinical outcome and biologic features with three histologic variants. J Clin Oncol 15 (4): 1664-71, 1997. [PUBMED Abstract]
- Tiemann M, Schrader C, Klapper W, et al.: Histopathology, cell proliferation indices and clinical outcome in 304 patients with mantle cell lymphoma (MCL): a clinicopathological study from the European MCL Network. Br J Haematol 131 (1): 29-38, 2005. [PUBMED Abstract]
- Campo E, Raffeld M, Jaffe ES: Mantle-cell lymphoma. Semin Hematol 36 (2): 115-27, 1999. [PUBMED Abstract]
- Martin P, Chadburn A, Christos P, et al.: Outcome of deferred initial therapy in mantle-cell lymphoma. J Clin Oncol 27 (8): 1209-13, 2009. [PUBMED Abstract]
- Cohen JB, Han X, Jemal A, et al.: Deferred therapy is associated with improved overall survival in patients with newly diagnosed mantle cell lymphoma. Cancer 122 (15): 2356-63, 2016. [PUBMED Abstract]
- Gerson JN, Handorf E, Villa D, et al.: Survival Outcomes of Younger Patients With Mantle Cell Lymphoma Treated in the Rituximab Era. J Clin Oncol 37 (6): 471-480, 2019. [PUBMED Abstract]
- Goy A, Kalayoglu Besisik S, Drach J, et al.: Longer-term follow-up and outcome by tumour cell proliferation rate (Ki-67) in patients with relapsed/refractory mantle cell lymphoma treated with lenalidomide on MCL-001(EMERGE) pivotal trial. Br J Haematol 170 (4): 496-503, 2015. [PUBMED Abstract]
- Ruan J, Martin P, Shah B, et al.: Lenalidomide plus Rituximab as Initial Treatment for Mantle-Cell Lymphoma. N Engl J Med 373 (19): 1835-44, 2015. [PUBMED Abstract]
- Wang ML, Rule S, Martin P, et al.: Targeting BTK with ibrutinib in relapsed or refractory mantle-cell lymphoma. N Engl J Med 369 (6): 507-16, 2013. [PUBMED Abstract]
- Wang ML, Blum KA, Martin P, et al.: Long-term follow-up of MCL patients treated with single-agent ibrutinib: updated safety and efficacy results. Blood 126 (6): 739-45, 2015. [PUBMED Abstract]
- Ruan J, Martin P, Christos P, et al.: Five-year follow-up of lenalidomide plus rituximab as initial treatment of mantle cell lymphoma. Blood 132 (19): 2016-2025, 2018. [PUBMED Abstract]
- Jain P, Zhao S, Lee HJ, et al.: Ibrutinib With Rituximab in First-Line Treatment of Older Patients With Mantle Cell Lymphoma. J Clin Oncol 40 (2): 202-212, 2022. [PUBMED Abstract]
- Wang ML, Jain P, Zhao S, et al.: Ibrutinib-rituximab followed by R-HCVAD as frontline treatment for young patients (≤65 years) with mantle cell lymphoma (WINDOW-1): a single-arm, phase 2 trial. Lancet Oncol 23 (3): 406-415, 2022. [PUBMED Abstract]
- Giné E, de la Cruz F, Jiménez Ubieto A, et al.: Ibrutinib in Combination With Rituximab for Indolent Clinical Forms of Mantle Cell Lymphoma (IMCL-2015): A Multicenter, Open-Label, Single-Arm, Phase II Trial. J Clin Oncol 40 (11): 1196-1205, 2022. [PUBMED Abstract]
- Dreyling M, Jurczak W, Jerkeman M, et al.: Ibrutinib versus temsirolimus in patients with relapsed or refractory mantle-cell lymphoma: an international, randomised, open-label, phase 3 study. Lancet 387 (10020): 770-8, 2016. [PUBMED Abstract]
- Tam CS, Anderson MA, Pott C, et al.: Ibrutinib plus Venetoclax for the Treatment of Mantle-Cell Lymphoma. N Engl J Med 378 (13): 1211-1223, 2018. [PUBMED Abstract]
- Wang ML, Jurczak W, Jerkeman M, et al.: Ibrutinib plus Bendamustine and Rituximab in Untreated Mantle-Cell Lymphoma. N Engl J Med 386 (26): 2482-2494, 2022. [PUBMED Abstract]
- Kluin-Nelemans HC, Hoster E, Hermine O, et al.: Treatment of Older Patients With Mantle Cell Lymphoma (MCL): Long-Term Follow-Up of the Randomized European MCL Elderly Trial. J Clin Oncol 38 (3): 248-256, 2020. [PUBMED Abstract]
- Rummel MJ, Niederle N, Maschmeyer G, et al.: Bendamustine plus rituximab versus CHOP plus rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: an open-label, multicentre, randomised, phase 3 non-inferiority trial. Lancet 381 (9873): 1203-10, 2013. [PUBMED Abstract]
- Robak T, Jin J, Pylypenko H, et al.: Frontline bortezomib, rituximab, cyclophosphamide, doxorubicin, and prednisone (VR-CAP) versus rituximab, cyclophosphamide, doxorubicin, vincristine, and prednisone (R-CHOP) in transplantation-ineligible patients with newly diagnosed mantle cell lymphoma: final overall survival results of a randomised, open-label, phase 3 study. Lancet Oncol 19 (11): 1449-1458, 2018. [PUBMED Abstract]
- Hermine O, Hoster E, Walewski J, et al.: Addition of high-dose cytarabine to immunochemotherapy before autologous stem-cell transplantation in patients aged 65 years or younger with mantle cell lymphoma (MCL Younger): a randomised, open-label, phase 3 trial of the European Mantle Cell Lymphoma Network. Lancet 388 (10044): 565-75, 2016. [PUBMED Abstract]
- Hermine O, Jiang L, Walewski J, et al.: Addition of high-dose cytarabine to immunochemotherapy before autologous stem-cell transplantation in patients aged 65 years or younger with mantle cell lymphoma (MCL younger): a long-term follow-up of the randomized, open-label, phase 3 trial of the European Mantle Cell Lymphoma Network. [Abstract] Blood 138 (Suppl 1); A-380, 2021.
- Hermine O, Jiang L, Walewski J, et al.: High-Dose Cytarabine and Autologous Stem-Cell Transplantation in Mantle Cell Lymphoma: Long-Term Follow-Up of the Randomized Mantle Cell Lymphoma Younger Trial of the European Mantle Cell Lymphoma Network. J Clin Oncol 41 (3): 479-484, 2023. [PUBMED Abstract]
- Khouri IF, Lee MS, Saliba RM, et al.: Nonablative allogeneic stem-cell transplantation for advanced/recurrent mantle-cell lymphoma. J Clin Oncol 21 (23): 4407-12, 2003. [PUBMED Abstract]
- Dreyling M, Lenz G, Hoster E, et al.: Early consolidation by myeloablative radiochemotherapy followed by autologous stem cell transplantation in first remission significantly prolongs progression-free survival in mantle-cell lymphoma: results of a prospective randomized trial of the European MCL Network. Blood 105 (7): 2677-84, 2005. [PUBMED Abstract]
- Geisler CH, Kolstad A, Laurell A, et al.: Long-term progression-free survival of mantle cell lymphoma after intensive front-line immunochemotherapy with in vivo-purged stem cell rescue: a nonrandomized phase 2 multicenter study by the Nordic Lymphoma Group. Blood 112 (7): 2687-93, 2008. [PUBMED Abstract]
- Tam CS, Bassett R, Ledesma C, et al.: Mature results of the M. D. Anderson Cancer Center risk-adapted transplantation strategy in mantle cell lymphoma. Blood 113 (18): 4144-52, 2009. [PUBMED Abstract]
- Damon LE, Johnson JL, Niedzwiecki D, et al.: Immunochemotherapy and autologous stem-cell transplantation for untreated patients with mantle-cell lymphoma: CALGB 59909. J Clin Oncol 27 (36): 6101-8, 2009. [PUBMED Abstract]
- Fenske TS, Zhang MJ, Carreras J, et al.: Autologous or reduced-intensity conditioning allogeneic hematopoietic cell transplantation for chemotherapy-sensitive mantle-cell lymphoma: analysis of transplantation timing and modality. J Clin Oncol 32 (4): 273-81, 2014. [PUBMED Abstract]
- Le Gouill S, Thieblemont C, Oberic L, et al.: Rituximab after Autologous Stem-Cell Transplantation in Mantle-Cell Lymphoma. N Engl J Med 377 (13): 1250-1260, 2017. [PUBMED Abstract]
- Wang M, Fayad L, Wagner-Bartak N, et al.: Lenalidomide in combination with rituximab for patients with relapsed or refractory mantle-cell lymphoma: a phase 1/2 clinical trial. Lancet Oncol 13 (7): 716-23, 2012. [PUBMED Abstract]
- Trněný M, Lamy T, Walewski J, et al.: Lenalidomide versus investigator's choice in relapsed or refractory mantle cell lymphoma (MCL-002; SPRINT): a phase 2, randomised, multicentre trial. Lancet Oncol 17 (3): 319-31, 2016. [PUBMED Abstract]
- Wang M, Rule S, Zinzani PL, et al.: Acalabrutinib in relapsed or refractory mantle cell lymphoma (ACE-LY-004): a single-arm, multicentre, phase 2 trial. Lancet 391 (10121): 659-667, 2018. [PUBMED Abstract]
- Song Y, Zhou K, Zou D, et al.: Zanubrutinib in relapsed/refractory mantle cell lymphoma: long-term efficacy and safety results from a phase 2 study. Blood 139 (21): 3148-3158, 2022. [PUBMED Abstract]
- Wang M, Munoz J, Goy A, et al.: Three-Year Follow-Up of KTE-X19 in Patients With Relapsed/Refractory Mantle Cell Lymphoma, Including High-Risk Subgroups, in the ZUMA-2 Study. J Clin Oncol 41 (3): 555-567, 2023. [PUBMED Abstract]
- Martin P, Ruan J, Leonard JP: The potential for chemotherapy-free strategies in mantle cell lymphoma. Blood 130 (17): 1881-1888, 2017. [PUBMED Abstract]
- Morrison VA, Dunn DL, Manivel JC, et al.: Clinical characteristics of post-transplant lymphoproliferative disorders. Am J Med 97 (1): 14-24, 1994. [PUBMED Abstract]
- Knowles DM, Cesarman E, Chadburn A, et al.: Correlative morphologic and molecular genetic analysis demonstrates three distinct categories of posttransplantation lymphoproliferative disorders. Blood 85 (2): 552-65, 1995. [PUBMED Abstract]
- Leblond V, Dhedin N, Mamzer Bruneel MF, et al.: Identification of prognostic factors in 61 patients with posttransplantation lymphoproliferative disorders. J Clin Oncol 19 (3): 772-8, 2001. [PUBMED Abstract]
- Ghobrial IM, Habermann TM, Maurer MJ, et al.: Prognostic analysis for survival in adult solid organ transplant recipients with post-transplantation lymphoproliferative disorders. J Clin Oncol 23 (30): 7574-82, 2005. [PUBMED Abstract]
- Evens AM, David KA, Helenowski I, et al.: Multicenter analysis of 80 solid organ transplantation recipients with post-transplantation lymphoproliferative disease: outcomes and prognostic factors in the modern era. J Clin Oncol 28 (6): 1038-46, 2010. [PUBMED Abstract]
- Dierickx D, Tousseyn T, Gheysens O: How I treat posttransplant lymphoproliferative disorders. Blood 126 (20): 2274-83, 2015. [PUBMED Abstract]
- Kuehnle I, Huls MH, Liu Z, et al.: CD20 monoclonal antibody (rituximab) for therapy of Epstein-Barr virus lymphoma after hemopoietic stem-cell transplantation. Blood 95 (4): 1502-5, 2000. [PUBMED Abstract]
- Trappe RU, Dierickx D, Zimmermann H, et al.: Response to Rituximab Induction Is a Predictive Marker in B-Cell Post-Transplant Lymphoproliferative Disorder and Allows Successful Stratification Into Rituximab or R-CHOP Consolidation in an International, Prospective, Multicenter Phase II Trial. J Clin Oncol 35 (5): 536-543, 2017. [PUBMED Abstract]
- Leblond V, Sutton L, Dorent R, et al.: Lymphoproliferative disorders after organ transplantation: a report of 24 cases observed in a single center. J Clin Oncol 13 (4): 961-8, 1995. [PUBMED Abstract]
- Mamzer-Bruneel MF, Lomé C, Morelon E, et al.: Durable remission after aggressive chemotherapy for very late post-kidney transplant lymphoproliferation: A report of 16 cases observed in a single center. J Clin Oncol 18 (21): 3622-32, 2000. [PUBMED Abstract]
- Swinnen LJ: Durable remission after aggressive chemotherapy for post-cardiac transplant lymphoproliferation. Leuk Lymphoma 28 (1-2): 89-101, 1997. [PUBMED Abstract]
- McCarthy M, Ramage J, McNair A, et al.: The clinical diversity and role of chemotherapy in lymphoproliferative disorder in liver transplant recipients. J Hepatol 27 (6): 1015-21, 1997. [PUBMED Abstract]
- Leblond V, Davi F, Charlotte F, et al.: Posttransplant lymphoproliferative disorders not associated with Epstein-Barr virus: a distinct entity? J Clin Oncol 16 (6): 2052-9, 1998. [PUBMED Abstract]
- Senderowicz AM, Vitetta E, Headlee D, et al.: Complete sustained response of a refractory, post-transplantation, large B-cell lymphoma to an anti-CD22 immunotoxin. Ann Intern Med 126 (11): 882-5, 1997. [PUBMED Abstract]
- Haddad E, Paczesny S, Leblond V, et al.: Treatment of B-lymphoproliferative disorder with a monoclonal anti-interleukin-6 antibody in 12 patients: a multicenter phase 1-2 clinical trial. Blood 97 (6): 1590-7, 2001. [PUBMED Abstract]
- Soslow RA, Davis RE, Warnke RA, et al.: True histiocytic lymphoma following therapy for lymphoblastic neoplasms. Blood 87 (12): 5207-12, 1996. [PUBMED Abstract]
- Kamel OW, Gocke CD, Kell DL, et al.: True histiocytic lymphoma: a study of 12 cases based on current definition. Leuk Lymphoma 18 (1-2): 81-6, 1995. [PUBMED Abstract]
- Nador RG, Cesarman E, Chadburn A, et al.: Primary effusion lymphoma: a distinct clinicopathologic entity associated with the Kaposi's sarcoma-associated herpes virus. Blood 88 (2): 645-56, 1996. [PUBMED Abstract]
- Shimada K, Hayakawa F, Kiyoi H: Biology and management of primary effusion lymphoma. Blood 132 (18): 1879-1888, 2018. [PUBMED Abstract]
- Castillo JJ, Bibas M, Miranda RN: The biology and treatment of plasmablastic lymphoma. Blood 125 (15): 2323-30, 2015. [PUBMED Abstract]
- Al-Malki MM, Castillo JJ, Sloan JM, et al.: Hematopoietic cell transplantation for plasmablastic lymphoma: a review. Biol Blood Marrow Transplant 20 (12): 1877-84, 2014. [PUBMED Abstract]
- Cattaneo C, Re A, Ungari M, et al.: Plasmablastic lymphoma among human immunodeficiency virus-positive patients: results of a single center's experience. Leuk Lymphoma 56 (1): 267-9, 2015. [PUBMED Abstract]
Información sobre los estadios del linfoma no Hodgkin
El estadio es importante para la selección del tratamiento en pacientes con linfoma no Hodgkin (LNH). Por lo general, las tomografías computarizadas (TC) del tórax y el abdomen forman parte de la evaluación para la estadificación de todos los pacientes de linfoma. El sistema de estadificación es similar al que se usa para el linfoma de Hodgkin (LH).
Es común que los pacientes de LNH presenten compromiso en las siguientes partes:
- Ganglios linfáticos no contiguos.
- Anillo de Waldeyer.
- Ganglios epitrocleares.
- Tubo gastrointestinal.
- Sitios extraganglionares. (En ocasiones, una localización extraganglionar es el único sitio comprometido en pacientes de linfoma difuso).
- Médula ósea.
- Hígado (muy común en pacientes con linfomas de grado bajo).
El examen citológico del líquido cefalorraquídeo a veces da un resultado positivo en pacientes con LNH de crecimiento rápido. El compromiso de los ganglios linfáticos hiliares y mediastínicos es menos común que en el LH. Sin embargo, las adenopatías mediastínicas son una característica destacada del linfoma linfoblástico y del linfoma mediastínico primario de células B, que se presentan sobre todo en adultos jóvenes.
La mayoría de los pacientes de LNH presentan una enfermedad avanzada (estadio III o estadio IV) que, a menudo, se puede identificar con procedimientos de estadificación limitados, como TC y biopsias de la médula ósea y de otros sitios comprometidos accesibles. En una revisión retrospectiva de más de 32 000 casos de linfoma en Francia, hasta el 40 % de los diagnósticos se realizaron mediante biopsia con aguja gruesa, y el 60 % mediante biopsia por escisión.[1] Tras la revisión por expertos, la biopsia con aguja gruesa proporcionó un diagnóstico definitivo en el 92,3 % de los casos, pero fue menos concluyente que la biopsia por escisión, que proporcionó un diagnóstico definitivo en el 98,1 % de los casos (P < 0,0001). La biopsia laparoscópica o la laparotomía no son necesarias para la estadificación, pero a veces son necesarias para establecer el diagnóstico o el tipo histológico.[2] La tomografía por emisión de positrones (TEP) con flúor F 18-fludesoxiglucosa se puede usar para la estadificación inicial y como complemento de la TC para el seguimiento después del tratamiento.[3] El uso de una TEP intermedia después de 2 a 4 ciclos de terapia no aportó información pronóstica confiable debido a problemas de reproducibilidad entre los observadores de un ensayo grupal cooperativo grande (ECOG-E344 [NCT00274924]) y por la escasa diferenciación en el desenlace de los pacientes con resultados positivos o negativos en la TEP que además tenían resultados negativos en la biopsia, en dos ensayos prospectivos [4-6] y en un metanálisis.[7] Para los pacientes con linfoma folicular, obtener un resultado positivo en una TEP después del tratamiento inicial acarrea un pronóstico más precario; sin embargo, no está claro si un resultado positivo en una TEP es predictivo cuando se usa tratamiento adicional o se usa otro tipo de tratamiento.[8]
En un estudio retrospectivo con 130 pacientes de linfoma difuso de células B grandes, la TEP permitió identificar el compromiso de la médula ósea de importancia clínica; la biopsia de médula ósea no llevó a la sobreestadificación del linfoma de ningún paciente.[9] En un estudio retrospectivo de 580 pacientes con linfoma folicular de 7 ensayos patrocinados por el Instituto Nacional del Cáncer no se observó ninguna mejora en la evaluación de la respuesta al tratamiento cuando se añadió la biopsia de médula ósea a las imágenes radiológicas.[10] El estudio del LNH debe incluir una biopsia de médula ósea cuando cambie el tratamiento (por ejemplo, para determinar el estadio limitado frente al avanzado) o cuando se evalúen las citopenias.
Sistema de estadificación en subtipos
Clasificación de Lugano
El American Joint Committee on Cancer (AJCC) adoptó la clasificación de Lugano para evaluar y estadificar el linfoma.[11] El sistema de clasificación de Lugano reemplaza el sistema de clasificación de Ann Arbor, que se adoptó en 1971 durante la conferencia de Ann Arbor,[12] con algunas modificaciones que se introdujeron 18 años después en la reunión de Cotswolds.[13,14]
| Estadio | Descripción del estadio | Imagen |
|---|---|---|
| LCR = líquido cefalorraquídeo; LDCBG = linfoma difuso de células B grandes; LNH = linfoma no Hodgkin; TC = tomografía computarizada. | ||
| aHodgkin and Non-Hodgkin Lymphomas. En: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer, 2017, pp. 937–58. | ||
| bEs posible que el estadio II con masa tumoral voluminosa antes se considerara un estadio temprano o avanzado de acuerdo con las características histológicas del linfoma y los factores pronósticos. | ||
| cLa definición de una masa tumoral voluminosa varía de acuerdo con el tipo histológico del linfoma. En la clasificación de Lugano, la masa tumoral voluminosa en el linfoma de Hodgkin se define como una masa que mide más de un tercio del diámetro torácico en la TC del tórax, o una masa que mide >10 cm. Las definiciones recomendadas para la masa tumoral voluminosa en el LNH varían de acuerdo con el tipo histológico del linfoma. En el linfoma folicular, se sugirió la medida de 6 cm a partir de la validación del Follicular Lymphoma International Prognostic Index-2. En el LDCBG, se han usado límites que oscilan entre 5 y 10 cm, si bien se recomienda el límite de 10 cm. | ||
| Estadio limitado | ||
| I | Compromiso en un solo sitio linfático (es decir, región ganglionar, anillo de Waldeyer, timo o bazo). | 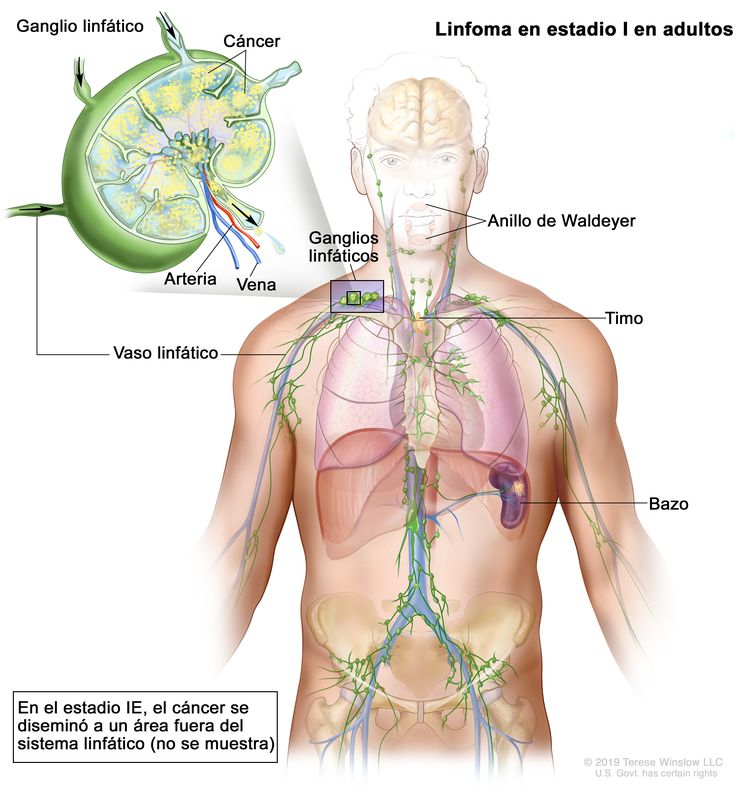 |
| IE | Compromiso de 1 solo sitio extralinfático sin compromiso ganglionar (infrecuente en el linfoma de Hodgkin). | |
| II | Compromiso de 2 o más regiones ganglionares en el mismo lado del diafragma. | 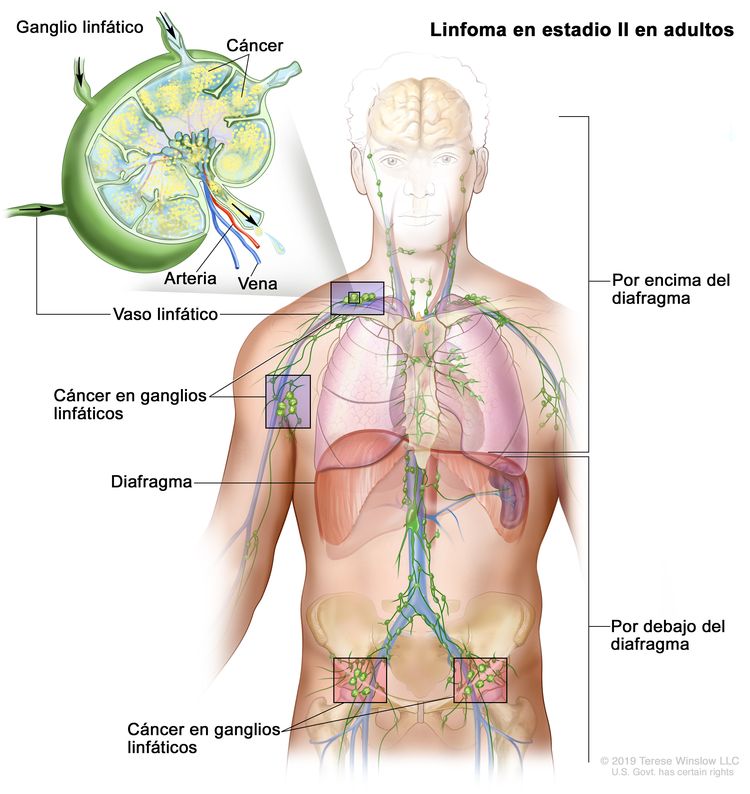 |
| IIE | Diseminación contigua extralinfática desde un sitio ganglionar, con compromiso de otras regiones ganglionares en el mismo lado del diafragma, o sin esta. | 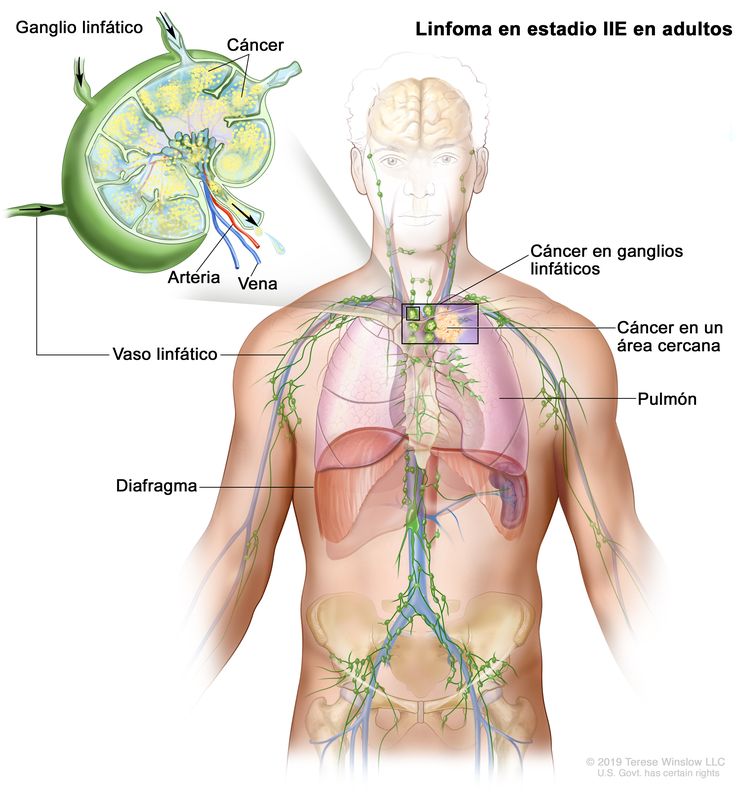 |
| II con masa voluminosab | Estadio II con una gran masa tumoral.c | |
| Estadio avanzado | ||
| III | Compromiso de regiones ganglionares en ambos lados del diafragma; ganglios supradiafragmáticos y compromiso esplénico. | 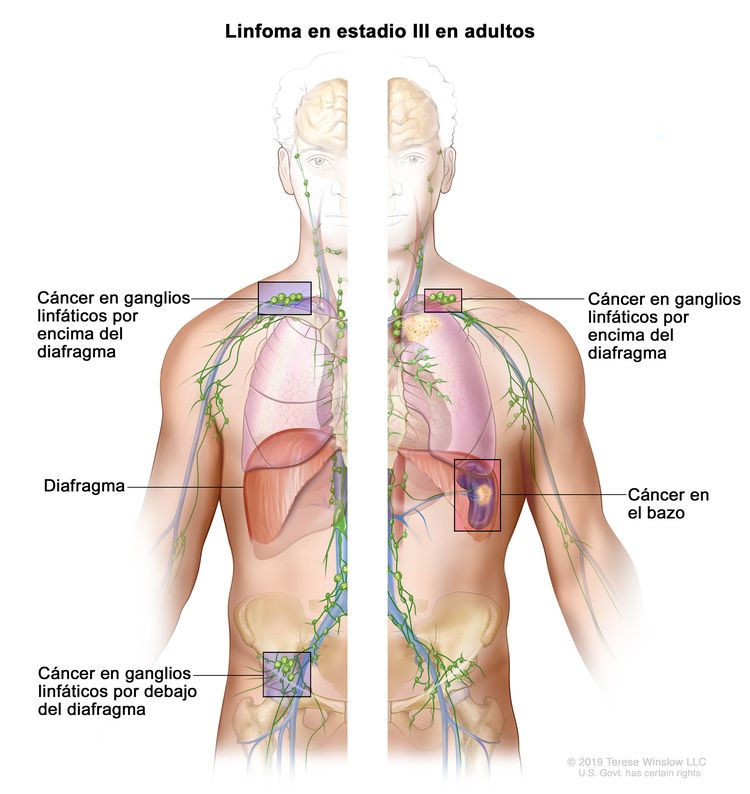 |
| IV | Compromiso difuso o diseminado de uno o más órganos extralinfáticos con compromiso ganglionar relacionado o sin este; compromiso de órgano extralinfático no contiguo con enfermedad ganglionar en estadio II; o compromiso de cualquier órgano extralinfático con enfermedad ganglionar en estadio III. El estadio IV incluye cualquier compromiso del LCR, la médula ósea y el hígado, o la presencia de lesiones pulmonares múltiples (diferentes a las lesiones por diseminación directa en una enfermedad en estadio IIE). | 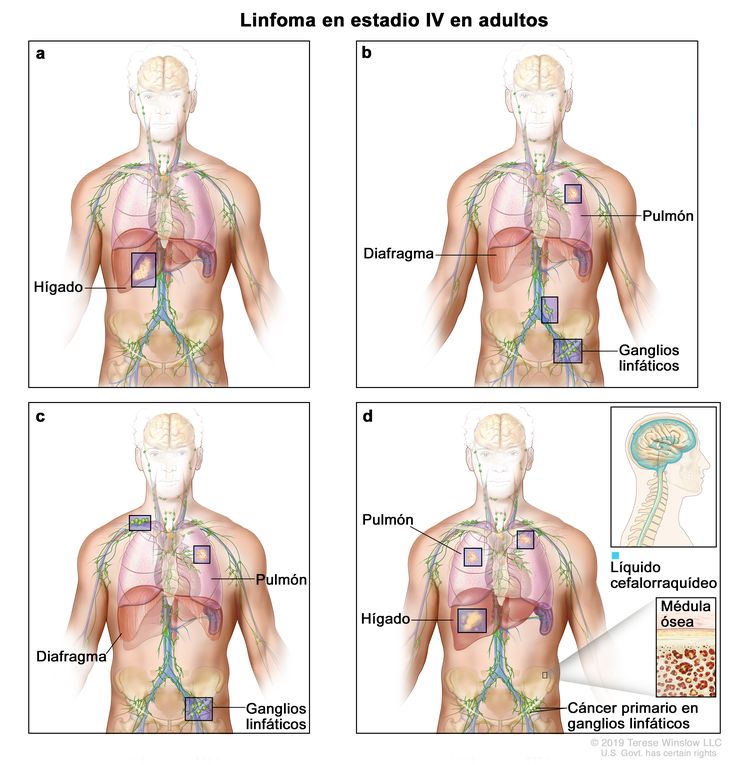 |
| Nota: Se utiliza la designación A o B junto con el grupo de estadio para el linfoma de Hodgkin. Ya no se utiliza la designación A o B para el LNH. | ||
En ocasiones, se usan sistemas de estadificación especializados. El médico debe estar al tanto del sistema que se usa en el informe.
La designación E se usa cuando aparecen neoplasias linfoides extraganglionares malignas en tejidos separados de los conglomerados linfáticos principales pero cercanos a estos. El estadio IV se refiere a la enfermedad con diseminación difusa por todo un sitio extraganglionar, como el hígado. Si el compromiso de uno o más sitios extralinfáticos se documentó mediante estudio patológico, se usa el símbolo del sitio comprometido seguido por el signo más (+).
| N = ganglios | H = hígado | L = pulmón | M = médula ósea |
| S = bazo | P = pleura | O = hueso | D = piel |
En la práctica actual se asigna un estadio clínico a partir de los hallazgos de la evaluación clínica y un estadio patológico a partir de los hallazgos de los procedimientos invasores adicionales a la biopsia inicial.
Por ejemplo, es posible que se detecte un compromiso del hígado y la médula ósea mediante una biopsia percutánea en un paciente con adenopatía inguinal sin síntomas sistémicos que tiene un resultado positivo en el linfangiograma. El estadio preciso para dicho paciente sería estadio clínico IIA, estado patológico IVA(H+)(M+).
Hay varios factores adicionales que no se incluyen en el sistema de estadificación anterior, pero que son importantes para la estadificación y el pronóstico de los pacientes con LNH. Estos factores son los siguientes:
- Edad.
- Estado funcional (EF).
- Tamaño del tumor.
- Valores de lactato-deshidrogenasa (LDH).
- Número de sitios con compromiso extraganglionar.
En el National Comprehensive Cancer Network International Prognostic Index (IPI) para el LNH de crecimiento rápido (linfoma difuso de células grades) se incluyen los siguientes 5 factores de riesgo significativos para el pronóstico de la supervivencia general (SG) y los puntajes de riesgo relacionado:[15]
- Edad.
- <40 años: 0.
- 41–60 años: 1.
- 61–75 años: 2.
- >75 años: 3.
- Estadio III/IV: 1.
- EF 2, 3 o 4: 1.
- Concentración sérica de LDH.
- Normalizada: 0.
- >1x–3x: 1.
- >3x: 2.
- Número de sitios extraganglionares ≥2: 1.
Puntaje de riesgo:
- Bajo (0 o 1): tasa de SG a 5 años de 96 %; tasa de supervivencia sin progresión (SSP) de 91 %.
- Intermedio bajo (2 o 3): tasa de SG a 5 años de 82 %; tasa de SSP de 74 %.
- Intermedio alto (4 o 5): tasa de SG a 5 años de 64 %; tasa de SSP de 51 %.
- Alto (>6): tasa de SG a 5 años de 33 %; tasa de SSP de 30 %.
Se utilizan modificaciones del IPI ajustadas por edad y estadio para los pacientes más jóvenes con enfermedad localizada.[16] Según parece, los intervalos de tiempo más cortos entre el diagnóstico y el tratamiento son marcadores indirectos de factores biológicos de pronóstico precario.[17]
Un reordenamiento del gen BCL2 o del gen MYC, la sobreexpresión dual del gen MYC o ambas cosas confieren un pronóstico particularmente desfavorable.[18,19] Los pacientes en riesgo alto de recaída quizás se beneficien de terapia de consolidación u otros abordajes en evaluación clínica.[20] La obtención de perfiles moleculares de expresión génica mediante micromatrices de ADN quizás sirva en el futuro para ayudar a estratificar a los pacientes en grupos de tratamiento dirigido a dianas específicas y para mejorar la predicción de la supervivencia después de la quimioterapia estándar.[21]
Bibliografía
- Syrykh C, Chaouat C, Poullot E, et al.: Lymph node excisions provide more precise lymphoma diagnoses than core biopsies: a French Lymphopath network survey. Blood 140 (24): 2573-2583, 2022. [PUBMED Abstract]
- Mann GB, Conlon KC, LaQuaglia M, et al.: Emerging role of laparoscopy in the diagnosis of lymphoma. J Clin Oncol 16 (5): 1909-15, 1998. [PUBMED Abstract]
- Barrington SF, Mikhaeel NG, Kostakoglu L, et al.: Role of imaging in the staging and response assessment of lymphoma: consensus of the International Conference on Malignant Lymphomas Imaging Working Group. J Clin Oncol 32 (27): 3048-58, 2014. [PUBMED Abstract]
- Horning SJ, Juweid ME, Schöder H, et al.: Interim positron emission tomography scans in diffuse large B-cell lymphoma: an independent expert nuclear medicine evaluation of the Eastern Cooperative Oncology Group E3404 study. Blood 115 (4): 775-7; quiz 918, 2010. [PUBMED Abstract]
- Moskowitz CH, Schöder H, Teruya-Feldstein J, et al.: Risk-adapted dose-dense immunochemotherapy determined by interim FDG-PET in Advanced-stage diffuse large B-Cell lymphoma. J Clin Oncol 28 (11): 1896-903, 2010. [PUBMED Abstract]
- Pregno P, Chiappella A, Bellò M, et al.: Interim 18-FDG-PET/CT failed to predict the outcome in diffuse large B-cell lymphoma patients treated at the diagnosis with rituximab-CHOP. Blood 119 (9): 2066-73, 2012. [PUBMED Abstract]
- Sun N, Zhao J, Qiao W, et al.: Predictive value of interim PET/CT in DLBCL treated with R-CHOP: meta-analysis. Biomed Res Int 2015: 648572, 2015. [PUBMED Abstract]
- Pyo J, Won Kim K, Jacene HA, et al.: End-therapy positron emission tomography for treatment response assessment in follicular lymphoma: a systematic review and meta-analysis. Clin Cancer Res 19 (23): 6566-77, 2013. [PUBMED Abstract]
- Khan AB, Barrington SF, Mikhaeel NG, et al.: PET-CT staging of DLBCL accurately identifies and provides new insight into the clinical significance of bone marrow involvement. Blood 122 (1): 61-7, 2013. [PUBMED Abstract]
- Rutherford SC, Yin J, Pederson L, et al.: Relevance of Bone Marrow Biopsies for Response Assessment in US National Cancer Institute National Clinical Trials Network Follicular Lymphoma Clinical Trials. J Clin Oncol 41 (2): 336-342, 2023. [PUBMED Abstract]
- Hodgkin and non-Hodgkin lymphoma. In: Amin MB, Edge SB, Greene FL, et al., eds.: AJCC Cancer Staging Manual. 8th ed. Springer; 2017, pp. 937–58.
- Carbone PP, Kaplan HS, Musshoff K, et al.: Report of the Committee on Hodgkin's Disease Staging Classification. Cancer Res 31 (11): 1860-1, 1971. [PUBMED Abstract]
- Lister TA, Crowther D, Sutcliffe SB, et al.: Report of a committee convened to discuss the evaluation and staging of patients with Hodgkin's disease: Cotswolds meeting. J Clin Oncol 7 (11): 1630-6, 1989. [PUBMED Abstract]
- National Cancer Institute sponsored study of classifications of non-Hodgkin's lymphomas: summary and description of a working formulation for clinical usage. The Non-Hodgkin's Lymphoma Pathologic Classification Project. Cancer 49 (10): 2112-35, 1982. [PUBMED Abstract]
- Zhou Z, Sehn LH, Rademaker AW, et al.: An enhanced International Prognostic Index (NCCN-IPI) for patients with diffuse large B-cell lymphoma treated in the rituximab era. Blood 123 (6): 837-42, 2014. [PUBMED Abstract]
- Møller MB, Christensen BE, Pedersen NT: Prognosis of localized diffuse large B-cell lymphoma in younger patients. Cancer 98 (3): 516-21, 2003. [PUBMED Abstract]
- Maurer MJ, Ghesquières H, Link BK, et al.: Diagnosis-to-Treatment Interval Is an Important Clinical Factor in Newly Diagnosed Diffuse Large B-Cell Lymphoma and Has Implication for Bias in Clinical Trials. J Clin Oncol 36 (16): 1603-1610, 2018. [PUBMED Abstract]
- Scott DW, King RL, Staiger AM, et al.: High-grade B-cell lymphoma with MYC and BCL2 and/or BCL6 rearrangements with diffuse large B-cell lymphoma morphology. Blood 131 (18): 2060-2064, 2018. [PUBMED Abstract]
- Horn H, Ziepert M, Becher C, et al.: MYC status in concert with BCL2 and BCL6 expression predicts outcome in diffuse large B-cell lymphoma. Blood 121 (12): 2253-63, 2013. [PUBMED Abstract]
- A predictive model for aggressive non-Hodgkin's lymphoma. The International Non-Hodgkin's Lymphoma Prognostic Factors Project. N Engl J Med 329 (14): 987-94, 1993. [PUBMED Abstract]
- Sha C, Barrans S, Cucco F, et al.: Molecular High-Grade B-Cell Lymphoma: Defining a Poor-Risk Group That Requires Different Approaches to Therapy. J Clin Oncol 37 (3): 202-212, 2019. [PUBMED Abstract]
Aspectos generales de las opciones de tratamiento del linfoma no Hodgkin
El tratamiento del linfoma no Hodgkin (LNH) depende del tipo histológico y el estadio. Muchas de las mejorías en la supervivencia se han logrado mediante ensayos clínicos (terapia experimental) en los que se intentó perfeccionar el mejor tratamiento aceptado disponible (tratamiento convencional o estándar).
En los pacientes asintomáticos con formas de LNH de crecimiento lento en estadio avanzado, es posible diferir el tratamiento hasta que el paciente presente síntomas o la enfermedad progrese. Cuando se difiere el tratamiento, la progresión clínica de los pacientes con LNH de crecimiento lento es variable; se necesita una observación frecuente y cuidadosa para poder iniciar un tratamiento eficaz cuando se acelera la evolución clínica de la enfermedad. Algunos pacientes tienen un período prolongado de enfermedad de crecimiento lento, pero en otros la enfermedad evoluciona rápido a tipos más malignos de LNH, lo que exige un tratamiento inmediato.
Las técnicas de radioterapia son un poco diferentes de las que se utilizan para el tratamiento del linfoma de Hodgkin. La dosis de radioterapia por lo habitual oscila entre 25 Gy y 50 Gy, y depende de factores como el tipo histológico de linfoma, el estadio, el estado general del paciente, el objetivo del tratamiento (curativo o paliativo), la proximidad a órganos circundantes sensibles, y si se usa radioterapia sola o combinada con quimioterapia. Debido a la variedad de presentaciones clínicas de la enfermedad y de la recaída, a veces se incluyen en el tratamiento sitios no habituales, como el anillo de Waldeyer, los ganglios epitrocleares o los ganglios mesentéricos. La morbilidad relacionada con el tratamiento se debe considerar en detalle. La mayoría de los pacientes que reciben radiación se tratan solo en un lado del diafragma. Las presentaciones localizadas del LNH extraganglionar se pueden tratar con técnicas dirigidas al campo comprometido con éxito significativo (>50 %).
Aunque los tratamientos existentes son curativos en una proporción significativa de los pacientes con linfoma, se están llevando a cabo numerosos ensayos clínicos para mejorar el tratamiento. En lo posible, los pacientes se deben incluir en estos estudios. Se propusieron pautas estandarizadas para evaluar la respuesta en los ensayos clínicos.[1]
En varias revisiones retrospectivas se indicó que la vigilancia rutinaria mediante imágenes aporta poco o ningún valor a los pacientes con linfoma difuso de células B grandes (LDCBG) que logran una remisión clínica completa después del tratamiento de inducción. Además, resulta difícil determinar el valor pronóstico de la tomografía por emisión de positrones con tomografía computarizada provisional para el tratamiento de inducción del LDCBG.[2-5]
Cada vez se observan más linfomas de crecimiento rápido en pacientes con infección por el virus de la inmunodeficiencia humana (VIH). El tratamiento de estos pacientes exige consideraciones especiales. Para obtener más información, consultar Tratamiento del linfoma relacionado con el SIDA.
En los pacientes con linfomas de crecimiento rápido, además de los exámenes de detección para el VIH, también se evalúa la presencia de hepatitis B o hepatitis C activas antes del tratamiento con rituximab o quimioterapia.[6,7] Hay beneficio de usar profilaxis con entecavir en el entorno del tratamiento con rituximab para los pacientes con carga vírica detectable del virus de la hepatitis B.[8,9] Los pacientes con infección por el virus de la hepatitis B (VHB) no resuelta (negativos para el antígeno de superficie de la hepatitis B, pero positivos para el anticuerpo del núcleo de la hepatitis B) presentan riesgo de reactivación del VHB y necesitan vigilancia del ADN del VHB. El tratamiento profiláctico con nucleósidos redujo la reactivación del VHB del 10,8 % al 2,1 % en un estudio retrospectivo de 326 pacientes.[10] De manera similar, cuando se usa rituximab con quimioterapia combinada o sin esta, por lo general se administra profilaxis con aciclovir o valaciclovir para el herpes zóster, y profilaxis con trimetoprim-sulfametoxazol o dapsona para la infección por Pneumocystis. El deterioro inmunitario a largo plazo se evaluó en un estudio de cohorte retrospectivo que incluyó 21 690 sobrevivientes de LDCBG del California Cancer Registry. Se encontraron tasas de incidencia elevadas de neumonía (10,8 veces mayor), meningitis (5,3 veces mayor), deficiencia de inmunoglobulina (17,6 veces mayor) y citopenias autoinmunitarias (12 veces mayor) hasta 10 años después.[11]
Entre 2508 pacientes en un registro danés, la incidencia de insuficiencia cardíaca congestiva inducida por la doxorrubicina aumentó en 115 sobrevivientes de LNH con antecedentes de enfermedad cardíaca (coeficiente de riesgos instantáneos [CRI], 2,71; intervalo de confianza [IC] 95 % , 1,15−6,36) y múltiples factores de riesgo cardiovascular (CRI, 2,86; IC 95 %, 1,56−5,23).[12]
Hay varias presentaciones clínicas poco habituales de linfoma que a menudo exigen abordajes modificados para la estadificación y el tratamiento. El lector puede remitirse a otras revisiones para obtener descripciones más detalladas de otras presentaciones extraganglionares en el aparato digestivo,[13-21] la tiroides,[22,23] el bazo,[24] los testículos,[25-27] los senos paranasales,[28-31] los huesos,[32,33] las órbitas[34-38] y la piel.[39-48]
Para obtener más información, consultar Tratamiento del linfoma primario del sistema nervioso central.
Enfermedad de Castleman
Es posible que el resultado de una biopsia de las acumulaciones localizadas o multifocales de los ganglios linfáticos conduzca a un diagnóstico de la enfermedad de Castleman (EC), aunque es un diagnóstico poco frecuente. En sentido estricto, no se trata de un linfoma, ni siquiera de una neoplasia maligna. Sin embargo, muchos pacientes con EC son atendidos y tratados por hematólogos u oncólogos.
La EC localizada o unicéntrica suele ser asintomática y se produce en el mediastino, que es la presentación más común de la EC.[49] Para esta forma de crecimiento lento se utiliza la observación cautelosa, la cirugía o la radioterapia. La EC multicéntrica (30 % de los pacientes con EC) se presenta con linfadenopatía en múltiples sitios; síntomas como fiebre, sudoración nocturna, pérdida de peso y fatiga; y anomalías de las pruebas de laboratorio como anemia, albúmina baja, proteína C reactiva elevada y fibrinógeno alto.[49] La EC multicéntrica (ECM) se subdivide en ECM relacionada con el virus del herpes humano 8 (normalmente con VIH o con inmunodeficiencia grave) o ECM idiopática. Las citopenias y la hipercitocinemia se atribuyen a la sobreproducción de interleucina 6 (IL-6). La ECM es una característica observada en el síndrome POEMS (polineuropatía, organomegalia, endocrinopatía, gammapatía monoclonal y anomalías cutáneas) [50] y el síndrome TAFRO (trombocitopenia, anasarca, fiebre, reticulinofibrosis y organomegalia).[51,52] El tratamiento con siltuximab (un anticuerpo monoclonal anti-IL-6), rituximab (un anticuerpo monoclonal anti-CD20) o fármacos quimioterapéuticos se ha notificado en series anecdóticas no aleatorias.[53-56]
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Cheson BD, Horning SJ, Coiffier B, et al.: Report of an international workshop to standardize response criteria for non-Hodgkin's lymphomas. NCI Sponsored International Working Group. J Clin Oncol 17 (4): 1244, 1999. [PUBMED Abstract]
- Mamot C, Klingbiel D, Hitz F, et al.: Final Results of a Prospective Evaluation of the Predictive Value of Interim Positron Emission Tomography in Patients With Diffuse Large B-Cell Lymphoma Treated With R-CHOP-14 (SAKK 38/07). J Clin Oncol 33 (23): 2523-9, 2015. [PUBMED Abstract]
- Thompson CA, Ghesquieres H, Maurer MJ, et al.: Utility of routine post-therapy surveillance imaging in diffuse large B-cell lymphoma. J Clin Oncol 32 (31): 3506-12, 2014. [PUBMED Abstract]
- El-Galaly TC, Jakobsen LH, Hutchings M, et al.: Routine Imaging for Diffuse Large B-Cell Lymphoma in First Complete Remission Does Not Improve Post-Treatment Survival: A Danish-Swedish Population-Based Study. J Clin Oncol 33 (34): 3993-8, 2015. [PUBMED Abstract]
- Huntington SF, Svoboda J, Doshi JA: Cost-effectiveness analysis of routine surveillance imaging of patients with diffuse large B-cell lymphoma in first remission. J Clin Oncol 33 (13): 1467-74, 2015. [PUBMED Abstract]
- Niitsu N, Hagiwara Y, Tanae K, et al.: Prospective analysis of hepatitis B virus reactivation in patients with diffuse large B-cell lymphoma after rituximab combination chemotherapy. J Clin Oncol 28 (34): 5097-100, 2010. [PUBMED Abstract]
- Dong HJ, Ni LN, Sheng GF, et al.: Risk of hepatitis B virus (HBV) reactivation in non-Hodgkin lymphoma patients receiving rituximab-chemotherapy: a meta-analysis. J Clin Virol 57 (3): 209-14, 2013. [PUBMED Abstract]
- Huang YH, Hsiao LT, Hong YC, et al.: Randomized controlled trial of entecavir prophylaxis for rituximab-associated hepatitis B virus reactivation in patients with lymphoma and resolved hepatitis B. J Clin Oncol 31 (22): 2765-72, 2013. [PUBMED Abstract]
- Li H, Zhang HM, Chen LF, et al.: Prophylactic lamivudine to improve the outcome of HBsAg-positive lymphoma patients during chemotherapy: a systematic review and meta-analysis. Clin Res Hepatol Gastroenterol 39 (1): 80-92, 2015. [PUBMED Abstract]
- Kusumoto S, Arcaini L, Hong X, et al.: Risk of HBV reactivation in patients with B-cell lymphomas receiving obinutuzumab or rituximab immunochemotherapy. Blood 133 (2): 137-146, 2019. [PUBMED Abstract]
- Shree T, Li Q, Glaser SL, et al.: Impaired Immune Health in Survivors of Diffuse Large B-Cell Lymphoma. J Clin Oncol 38 (15): 1664-1675, 2020. [PUBMED Abstract]
- Salz T, Zabor EC, de Nully Brown P, et al.: Preexisting Cardiovascular Risk and Subsequent Heart Failure Among Non-Hodgkin Lymphoma Survivors. J Clin Oncol 35 (34): 3837-3843, 2017. [PUBMED Abstract]
- Maor MH, Velasquez WS, Fuller LM, et al.: Stomach conservation in stages IE and IIE gastric non-Hodgkin's lymphoma. J Clin Oncol 8 (2): 266-71, 1990. [PUBMED Abstract]
- Salles G, Herbrecht R, Tilly H, et al.: Aggressive primary gastrointestinal lymphomas: review of 91 patients treated with the LNH-84 regimen. A study of the Groupe d'Etude des Lymphomes Agressifs. Am J Med 90 (1): 77-84, 1991. [PUBMED Abstract]
- Taal BG, Burgers JM, van Heerde P, et al.: The clinical spectrum and treatment of primary non-Hodgkin's lymphoma of the stomach. Ann Oncol 4 (10): 839-46, 1993. [PUBMED Abstract]
- Tondini C, Giardini R, Bozzetti F, et al.: Combined modality treatment for primary gastrointestinal non-Hodgkin's lymphoma: the Milan Cancer Institute experience. Ann Oncol 4 (10): 831-7, 1993. [PUBMED Abstract]
- d'Amore F, Brincker H, Grønbaek K, et al.: Non-Hodgkin's lymphoma of the gastrointestinal tract: a population-based analysis of incidence, geographic distribution, clinicopathologic presentation features, and prognosis. Danish Lymphoma Study Group. J Clin Oncol 12 (8): 1673-84, 1994. [PUBMED Abstract]
- Haim N, Leviov M, Ben-Arieh Y, et al.: Intermediate and high-grade gastric non-Hodgkin's lymphoma: a prospective study of non-surgical treatment with primary chemotherapy, with or without radiotherapy. Leuk Lymphoma 17 (3-4): 321-6, 1995. [PUBMED Abstract]
- Koch P, del Valle F, Berdel WE, et al.: Primary gastrointestinal non-Hodgkin's lymphoma: I. Anatomic and histologic distribution, clinical features, and survival data of 371 patients registered in the German Multicenter Study GIT NHL 01/92. J Clin Oncol 19 (18): 3861-73, 2001. [PUBMED Abstract]
- Koch P, del Valle F, Berdel WE, et al.: Primary gastrointestinal non-Hodgkin's lymphoma: II. Combined surgical and conservative or conservative management only in localized gastric lymphoma--results of the prospective German Multicenter Study GIT NHL 01/92. J Clin Oncol 19 (18): 3874-83, 2001. [PUBMED Abstract]
- Koch P, Probst A, Berdel WE, et al.: Treatment results in localized primary gastric lymphoma: data of patients registered within the German multicenter study (GIT NHL 02/96). J Clin Oncol 23 (28): 7050-9, 2005. [PUBMED Abstract]
- Blair TJ, Evans RG, Buskirk SJ, et al.: Radiotherapeutic management of primary thyroid lymphoma. Int J Radiat Oncol Biol Phys 11 (2): 365-70, 1985. [PUBMED Abstract]
- Junor EJ, Paul J, Reed NS: Primary non-Hodgkin's lymphoma of the thyroid. Eur J Surg Oncol 18 (4): 313-21, 1992. [PUBMED Abstract]
- Morel P, Dupriez B, Gosselin B, et al.: Role of early splenectomy in malignant lymphomas with prominent splenic involvement (primary lymphomas of the spleen). A study of 59 cases. Cancer 71 (1): 207-15, 1993. [PUBMED Abstract]
- Zucca E, Conconi A, Mughal TI, et al.: Patterns of outcome and prognostic factors in primary large-cell lymphoma of the testis in a survey by the International Extranodal Lymphoma Study Group. J Clin Oncol 21 (1): 20-7, 2003. [PUBMED Abstract]
- Vitolo U, Chiappella A, Ferreri AJ, et al.: First-line treatment for primary testicular diffuse large B-cell lymphoma with rituximab-CHOP, CNS prophylaxis, and contralateral testis irradiation: final results of an international phase II trial. J Clin Oncol 29 (20): 2766-72, 2011. [PUBMED Abstract]
- Cheah CY, Wirth A, Seymour JF: Primary testicular lymphoma. Blood 123 (4): 486-93, 2014. [PUBMED Abstract]
- Liang R, Todd D, Chan TK, et al.: Treatment outcome and prognostic factors for primary nasal lymphoma. J Clin Oncol 13 (3): 666-70, 1995. [PUBMED Abstract]
- Cheung MM, Chan JK, Lau WH, et al.: Primary non-Hodgkin's lymphoma of the nose and nasopharynx: clinical features, tumor immunophenotype, and treatment outcome in 113 patients. J Clin Oncol 16 (1): 70-7, 1998. [PUBMED Abstract]
- Hausdorff J, Davis E, Long G, et al.: Non-Hodgkin's lymphoma of the paranasal sinuses: clinical and pathological features, and response to combined-modality therapy. Cancer J Sci Am 3 (5): 303-11, 1997 Sep-Oct. [PUBMED Abstract]
- Sasai K, Yamabe H, Kokubo M, et al.: Head-and-neck stages I and II extranodal non-Hodgkin's lymphomas: real classification and selection for treatment modality. Int J Radiat Oncol Biol Phys 48 (1): 153-60, 2000. [PUBMED Abstract]
- Ferreri AJ, Reni M, Ceresoli GL, et al.: Therapeutic management with adriamycin-containing chemotherapy and radiotherapy of monostotic and polyostotic primary non-Hodgkin's lymphoma of bone in adults. Cancer Invest 16 (8): 554-61, 1998. [PUBMED Abstract]
- Dubey P, Ha CS, Besa PC, et al.: Localized primary malignant lymphoma of bone. Int J Radiat Oncol Biol Phys 37 (5): 1087-93, 1997. [PUBMED Abstract]
- Martinet S, Ozsahin M, Belkacémi Y, et al.: Outcome and prognostic factors in orbital lymphoma: a Rare Cancer Network study on 90 consecutive patients treated with radiotherapy. Int J Radiat Oncol Biol Phys 55 (4): 892-8, 2003. [PUBMED Abstract]
- Uno T, Isobe K, Shikama N, et al.: Radiotherapy for extranodal, marginal zone, B-cell lymphoma of mucosa-associated lymphoid tissue originating in the ocular adnexa: a multiinstitutional, retrospective review of 50 patients. Cancer 98 (4): 865-71, 2003. [PUBMED Abstract]
- Sjö LD, Ralfkiaer E, Juhl BR, et al.: Primary lymphoma of the lacrimal sac: an EORTC ophthalmic oncology task force study. Br J Ophthalmol 90 (8): 1004-9, 2006. [PUBMED Abstract]
- Stefanovic A, Lossos IS: Extranodal marginal zone lymphoma of the ocular adnexa. Blood 114 (3): 501-10, 2009. [PUBMED Abstract]
- Sjö LD: Ophthalmic lymphoma: epidemiology and pathogenesis. Acta Ophthalmol 87 Thesis 1: 1-20, 2009. [PUBMED Abstract]
- Geelen FA, Vermeer MH, Meijer CJ, et al.: bcl-2 protein expression in primary cutaneous large B-cell lymphoma is site-related. J Clin Oncol 16 (6): 2080-5, 1998. [PUBMED Abstract]
- Pandolfino TL, Siegel RS, Kuzel TM, et al.: Primary cutaneous B-cell lymphoma: review and current concepts. J Clin Oncol 18 (10): 2152-68, 2000. [PUBMED Abstract]
- Sarris AH, Braunschweig I, Medeiros LJ, et al.: Primary cutaneous non-Hodgkin's lymphoma of Ann Arbor stage I: preferential cutaneous relapses but high cure rate with doxorubicin-based therapy. J Clin Oncol 19 (2): 398-405, 2001. [PUBMED Abstract]
- Grange F, Bekkenk MW, Wechsler J, et al.: Prognostic factors in primary cutaneous large B-cell lymphomas: a European multicenter study. J Clin Oncol 19 (16): 3602-10, 2001. [PUBMED Abstract]
- Mirza I, Macpherson N, Paproski S, et al.: Primary cutaneous follicular lymphoma: an assessment of clinical, histopathologic, immunophenotypic, and molecular features. J Clin Oncol 20 (3): 647-55, 2002. [PUBMED Abstract]
- Smith BD, Glusac EJ, McNiff JM, et al.: Primary cutaneous B-cell lymphoma treated with radiotherapy: a comparison of the European Organization for Research and Treatment of Cancer and the WHO classification systems. J Clin Oncol 22 (4): 634-9, 2004. [PUBMED Abstract]
- Willemze R, Jaffe ES, Burg G, et al.: WHO-EORTC classification for cutaneous lymphomas. Blood 105 (10): 3768-85, 2005. [PUBMED Abstract]
- El-Helw L, Goodwin S, Slater D, et al.: Primary B-cell lymphoma of the skin: the Sheffield Lymphoma Group Experience (1984-2003). Int J Oncol 25 (5): 1453-8, 2004. [PUBMED Abstract]
- Zinzani PL, Quaglino P, Pimpinelli N, et al.: Prognostic factors in primary cutaneous B-cell lymphoma: the Italian Study Group for Cutaneous Lymphomas. J Clin Oncol 24 (9): 1376-82, 2006. [PUBMED Abstract]
- Senff NJ, Noordijk EM, Kim YH, et al.: European Organization for Research and Treatment of Cancer and International Society for Cutaneous Lymphoma consensus recommendations for the management of cutaneous B-cell lymphomas. Blood 112 (5): 1600-9, 2008. [PUBMED Abstract]
- van Rhee F, Voorhees P, Dispenzieri A, et al.: International, evidence-based consensus treatment guidelines for idiopathic multicentric Castleman disease. Blood 132 (20): 2115-2124, 2018. [PUBMED Abstract]
- Dispenzieri A: POEMS Syndrome: 2019 Update on diagnosis, risk-stratification, and management. Am J Hematol 94 (7): 812-827, 2019. [PUBMED Abstract]
- Zhang Y, Suo SS, Yang HJ, et al.: Clinical features and treatment of 7 Chinese TAFRO syndromes from 96 de novo Castleman diseases: a 10-year retrospective study. J Cancer Res Clin Oncol 146 (2): 357-365, 2020. [PUBMED Abstract]
- Fujimoto S, Sakai T, Kawabata H, et al.: Is TAFRO syndrome a subtype of idiopathic multicentric Castleman disease? Am J Hematol 94 (9): 975-983, 2019. [PUBMED Abstract]
- Tonialini L, Bonfichi M, Ferrero S, et al.: Siltuximab in relapsed/refractory multicentric Castleman disease: Experience of the Italian NPP program. Hematol Oncol 36 (4): 689-692, 2018. [PUBMED Abstract]
- Dong Y, Zhang L, Nong L, et al.: Effectiveness of rituximab-containing treatment regimens in idiopathic multicentric Castleman disease. Ann Hematol 97 (9): 1641-1647, 2018. [PUBMED Abstract]
- Zhang L, Zhao AL, Duan MH, et al.: Phase 2 study using oral thalidomide-cyclophosphamide-prednisone for idiopathic multicentric Castleman disease. Blood 133 (16): 1720-1728, 2019. [PUBMED Abstract]
- van Rhee F, Wong RS, Munshi N, et al.: Siltuximab for multicentric Castleman's disease: a randomised, double-blind, placebo-controlled trial. Lancet Oncol 15 (9): 966-74, 2014. [PUBMED Abstract]
Tratamiento del linfoma no Hodgkin de crecimiento lento en estadio I y del linfoma no Hodgkin de crecimiento lento y contiguo en estadio II
Aunque es poco común observar presentaciones localizadas del linfoma no Hodgkin (LNH), el objetivo del tratamiento es curarlo en los pacientes en los que se confirme la enfermedad muy localizada después de haberse sometido a procedimientos de estadificación apropiados.
Opciones de tratamiento para el linfoma no Hodgkin de crecimiento lento en estadio I y el linfoma no Hodgkin de crecimiento lento y contiguo en estadio II
Las opciones de tratamiento para el linfoma no Hodgkin de crecimiento lento en estadio I y el linfoma no Hodgkin de crecimiento lento y contiguo en estadio II son las siguientes:
En un ensayo prospectivo aleatorizado, 150 pacientes de linfoma folicular en estadio I o estadio II se asignaron al azar a recibir 30 Gy de radioterapia sola dirigida al campo comprometido o radioterapia con 6 ciclos de R-CVP (rituximab, ciclofosfamida, vincristina y prednisona). Al cabo de una mediana de seguimiento de 9,6 años, la tasa de supervivencia sin progresión (SSP) a 10 años que favoreció al grupo de terapia de modalidad combinada fue del 59 % (intervalo de confianza [IC] 95 %, 46–74 %) versus el 41 % para la radioterapia sola (IC 95 %, 30–57 %) (P = 0,033). No se encontraron diferencias en la supervivencia general (SG) (87 y 95 %, P = 0,40).[1][Nivel de evidencia B1]
En el National Lymphocare Study se identificaron 471 pacientes con linfoma folicular en estadio I. De estos pacientes, 206 se estadificaron de manera cuidadosa mediante aspirado y biopsia de médula ósea, tomografía computarizada (TC) o tomografía por emisión de positrones con tomografía computarizada (TEP-TC).[2] El tratamiento no aleatorizado incluyó radioterapia (27 %), quimioterapia con rituximab (quimioterapia R) (28 %), observación cautelosa (17 %), quimioterapia R con radioterapia (13 %) y rituximab solo (12%), aunque más de un tercio de los pacientes comenzó el estudio en el grupo de terapia diferida. Tras una mediana de seguimiento de 57 meses, la SSP favoreció la quimioterapia R o la quimioterapia R con radioterapia, pero la SG fue casi idéntica, superior al 90 % para todos los pacientes.[2][Nivel de evidencia C2] Se necesitan ensayos clínicos para responder a preguntas como las siguientes:[3]
- ¿Se prefiere la observación cautelosa o la radioterapia después de una TEP-TC normal tras la biopsia por escisión?
- ¿Se debería agregar rituximab a la radioterapia para el linfoma folicular en estadio I?
- ¿La quimioterapia R con radioterapia cumple alguna función en el tratamiento?
Radioterapia
Se puede lograr el control a largo plazo de los campos de radiación en un número significativo de pacientes con LNH de crecimiento lento en estadio I o estadio II mediante el uso de dosificaciones de radiación que oscilan entre 25 y 40 Gy dirigidas a los sitios comprometidos o a campos extendidos que cubren sitios ganglionares adyacentes.[1,4-6] Casi la mitad de todos los pacientes tratados con radioterapia sola presentan recaídas fuera del campo de radiación en un plazo de 10 años.[1,6,7]
En una revisión retrospectiva de 512 pacientes de un consorcio internacional, se evaluó a pacientes con linfoma folicular en estadio temprano que habían recibido al menos 24 Gy de radioterapia localizada en el momento de la presentación inicial. Al cabo de una mediana de seguimiento de 52 meses, el 29,1 % de los pacientes presentaron linfoma recidivante después de una mediana de 23 meses (intervalo, 1–143 meses).[8] Al cabo de una mediana de seguimiento de 33 meses después de la recidiva, la tasa de SG a 3 años fue del 91,4 % una vez que los pacientes recibieron quimioterapia sistémica subsiguiente que incluía rituximab, por lo general con quimioterapia.[8]
El uso de dosis muy bajas de radioterapia de 4 Gy (2 Gy en 2 fracciones) lleva a tasas de remisión en el 50 % de los pacientes que no toleran dosis más altas.[9] En un ensayo prospectivo aleatorizado multicéntrico de 548 pacientes con linfoma de la zona marginal o folicular recibieron radioterapia: 4 Gy en 2 fracciones o 24 Gy en 12 fracciones.[10]
- Al cabo de una mediana de seguimiento de 73,8 meses, la tasa de respuesta completa local a 5 años fue del 89,9 % (85,5–93,1 %) después de 24 Gy y del 70,4 % (64,7–75,4 %) después de 4 Gy (CRI, 3,46; IC 95 %, 2,25–5,33, P < 0,0001).[10]
- A pesar de que el control local duradero fue superior en los pacientes que recibieron 24 Gy en 12 fracciones, el régimen de 4 Gy (2 Gy en 2 fracciones) fue casi similar con una exposición a la radiación, una duración del tratamiento y un costo inferiores.
Es posible considerar el uso de terapia con protones para reducir la dosis de radiación dirigida a los órganos en riesgo, cuando la radiación mediastínica abarca el lado izquierdo del corazón o se sabe que aumentará el riesgo de cáncer de mama en mujeres jóvenes.[11]
Rituximab con quimioterapia o sin esta
Cuando se contraindica la radioterapia para los pacientes sintomáticos que necesitan tratamiento, o cuando se prefiere un tratamiento alternativo, se puede administrar rituximab con quimioterapia o sin esta (como se indica a continuación para los pacientes en estadios más avanzados). La utilidad de disminuir la recaída del tratamiento adyuvante mediante radioterapia y rituximab (un anticuerpo monoclonal anti-CD20), solo o en combinación con quimioterapia, se extrapoló de ensayos con pacientes de enfermedad en estadio avanzado y no se ha confirmado.[12,13]
Observación cautelosa
Se puede considerar la observación cautelosa para pacientes asintomáticos.[14] La observación cautelosa nunca se ha comparado con la radioterapia inicial en ningún ensayo prospectivo aleatorizado; en un análisis retrospectivo de 30 años de la base de datos del Surveillance, Epidemiology and End Results Program (SEER), se observaron mejores desenlaces con la administración de radioterapia inicial.[15]
Otros tratamientos indicados para pacientes con enfermedad en estadio avanzado
Los pacientes con sitios de compromiso que no se pueden alcanzar mediante radioterapia se tratan como los pacientes con linfoma de grado bajo en estadio III o en estadio IV.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- MacManus M, Fisher R, Roos D, et al.: Randomized Trial of Systemic Therapy After Involved-Field Radiotherapy in Patients With Early-Stage Follicular Lymphoma: TROG 99.03. J Clin Oncol 36 (29): 2918-2925, 2018. [PUBMED Abstract]
- Friedberg JW, Byrtek M, Link BK, et al.: Effectiveness of first-line management strategies for stage I follicular lymphoma: analysis of the National LymphoCare Study. J Clin Oncol 30 (27): 3368-75, 2012. [PUBMED Abstract]
- Montoto S: Management of localized-stage follicular lymphoma: changing the paradigm? J Clin Oncol 30 (27): 3328-9, 2012. [PUBMED Abstract]
- Haas RL, Poortmans P, de Jong D, et al.: High response rates and lasting remissions after low-dose involved field radiotherapy in indolent lymphomas. J Clin Oncol 21 (13): 2474-80, 2003. [PUBMED Abstract]
- Guckenberger M, Alexandrow N, Flentje M: Radiotherapy alone for stage I-III low grade follicular lymphoma: long-term outcome and comparison of extended field and total nodal irradiation. Radiat Oncol 7: 103, 2012. [PUBMED Abstract]
- Brady JL, Binkley MS, Hajj C, et al.: Definitive radiotherapy for localized follicular lymphoma staged by 18F-FDG PET-CT: a collaborative study by ILROG. Blood 133 (3): 237-245, 2019. [PUBMED Abstract]
- Guadagnolo BA, Li S, Neuberg D, et al.: Long-term outcome and mortality trends in early-stage, Grade 1-2 follicular lymphoma treated with radiation therapy. Int J Radiat Oncol Biol Phys 64 (3): 928-34, 2006. [PUBMED Abstract]
- Binkley MS, Brady JL, Hajj C, et al.: Salvage Treatment and Survival for Relapsed Follicular Lymphoma Following Primary Radiation Therapy: A Collaborative Study on Behalf of ILROG. Int J Radiat Oncol Biol Phys 104 (3): 522-529, 2019. [PUBMED Abstract]
- Hoskin PJ, Kirkwood AA, Popova B, et al.: 4 Gy versus 24 Gy radiotherapy for patients with indolent lymphoma (FORT): a randomised phase 3 non-inferiority trial. Lancet Oncol 15 (4): 457-63, 2014. [PUBMED Abstract]
- Hoskin P, Popova B, Schofield O, et al.: 4 Gy versus 24 Gy radiotherapy for follicular and marginal zone lymphoma (FoRT): long-term follow-up of a multicentre, randomised, phase 3, non-inferiority trial. Lancet Oncol 22 (3): 332-340, 2021. [PUBMED Abstract]
- Dabaja BS, Hoppe BS, Plastaras JP, et al.: Proton therapy for adults with mediastinal lymphomas: the International Lymphoma Radiation Oncology Group guidelines. Blood 132 (16): 1635-1646, 2018. [PUBMED Abstract]
- Kelsey SM, Newland AC, Hudson GV, et al.: A British National Lymphoma Investigation randomised trial of single agent chlorambucil plus radiotherapy versus radiotherapy alone in low grade, localised non-Hodgkins lymphoma. Med Oncol 11 (1): 19-25, 1994. [PUBMED Abstract]
- Seymour JF, Pro B, Fuller LM, et al.: Long-term follow-up of a prospective study of combined modality therapy for stage I-II indolent non-Hodgkin's lymphoma. J Clin Oncol 21 (11): 2115-22, 2003. [PUBMED Abstract]
- Advani R, Rosenberg SA, Horning SJ: Stage I and II follicular non-Hodgkin's lymphoma: long-term follow-up of no initial therapy. J Clin Oncol 22 (8): 1454-9, 2004. [PUBMED Abstract]
- Pugh TJ, Ballonoff A, Newman F, et al.: Improved survival in patients with early stage low-grade follicular lymphoma treated with radiation: a Surveillance, Epidemiology, and End Results database analysis. Cancer 116 (16): 3843-51, 2010. [PUBMED Abstract]
Tratamiento del linfoma no Hodgkin de crecimiento lento no contiguo en estadios II, III y IV
El tratamiento óptimo para el linfoma no Hodgkin (LNH) de grado bajo en estadios avanzados es polémico debido a las tasas bajas de curación que se obtienen con las opciones terapéuticas vigentes. Hay numerosos ensayos clínicos en curso para evaluar los asuntos relacionados con el tratamiento y se insta a los pacientes a que participen en estos. La tasa de recaída es muy constante en el tiempo, incluso en pacientes que lograron una respuesta completa al tratamiento. De hecho, a veces se producen recaídas muchos años después del tratamiento. Por el momento, no hay ensayos aleatorizados que orienten a los médicos acerca de la elección inicial de observación cautelosa o el uso de rituximab, análogos de nucleósidos, alquilantes, quimioterapia combinada, anticuerpos monoclonales radiomarcados o combinaciones de estas opciones.[1];[2][Nivel de evidencia B1]
Para los pacientes con LNH de crecimiento lento no contiguo en estadios II y III, se propuso la radioterapia linfática central, pero no se recomienda su uso habitual como método de tratamiento.[3,4]
Los pacientes con infección por el virus de la hepatitis B (VHB) no resuelta (negativos para el antígeno de superficie de la hepatitis B, pero positivos para el anticuerpo del núcleo de la hepatitis B) presentan riesgo de reactivación del VHB y necesitan vigilancia del ADN del VHB. El tratamiento profiláctico con nucleósidos redujo la reactivación del VHB del 10,8 % al 2,1 % en un estudio retrospectivo de 326 pacientes.[5]
Opciones de tratamiento para el linfoma no Hodgkin de crecimiento lento no contiguo en estadios II, III y IV
Las opciones de tratamiento para el linfoma no Hodgkin de crecimiento lento no contiguo en estadios II, III y IV son las siguientes:
- Observación cautelosa para pacientes asintomáticos.
- Rituximab solo o en combinación con los citotóxicos utilizados en la terapia de primera línea.
- Lenalidomida y rituximab.
- Mantenimiento con rituximab.
- Obinutuzumab solo o en combinación con los citotóxicos utilizados en la terapia de primera línea.
- Inhibidor de la fosfatidilinositol 3–cinasa (PI3K).
- Inhibidor de EZH2.
- Anticuerpos monoclonales anti-CD20 radiomarcados.
- Tratamiento intensivo con quimioterapia, con irradiación corporal total o sin esta, o con dosis altas de radioinmunoterapia, seguidas de trasplantes de médula ósea autógenos o alogénicos o de células madre periféricas (en evaluación clínica).[6-15]
- Ensayos clínicos de fase III en los que se compara la quimioterapia sola con la quimioterapia seguida de una vacuna anti-idiotipo.[16-18]
- Radioterapia de campo extendido (solo para pacientes en estadio III) (en evaluación clínica).[19]
- Ofatumumab, un anticuerpo monoclonal humano anti-CD20 (en evaluación clínica).[20]
- Ciclo corto de dosis bajas de radioterapia paliativa (2 × 2 Gy) (en evaluación clínica).[21,22]
Debido a que ninguno de los tratamientos enumerados antes son curativos para la enfermedad en estadio avanzado, se encuentran en evaluación clínica varios abordajes innovadores.
Observación cautelosa para pacientes asintomáticos
La tasa de recaída es muy constante en el tiempo, incluso en pacientes que lograron una respuesta completa (RC) al tratamiento. De hecho, a veces se producen recaídas muchos años después del tratamiento. Para esta categoría, se puede considerar el tratamiento diferido (es decir, observación cautelosa hasta que el paciente presente síntomas).[2,23-25] El Follicular Lymphoma International Prognostic Index (FLIPI) y el FLIPI-2 revisado permiten predecir la supervivencia sin progresión (SSP) y la supervivencia general (SG), pero los puntajes no sirven para establecer la necesidad de tratamiento en pacientes asintomáticos.[26,27]
Evidencia (observación cautelosa):
- En tres ensayos aleatorizados se comparó la observación cautelosa y la administración inmediata de quimioterapia.[24,28]; [29][Nivel de evidencia A1]
- En ninguno de los tres ensayos se observó una diferencia en la SG ni en la supervivencia específica.
- En los pacientes asignados al azar a la observación cautelosa, la mediana de tiempo hasta la necesidad de tratamiento fue de 2 a 3 años; un tercio de los pacientes del grupo de observación cautelosa nunca necesitaron tratamiento (la mitad murió por otras causas y la otra mitad permaneció sin progresión después de 10 años).
- Un grupo seleccionado de 107 pacientes con linfoma folicular en estadio avanzado se siguió mediante observación cautelosa inicial seguida de tratamiento después de mediana de retraso de inicio del tratamiento de 55 meses, y se comparó con una cohorte similar de pacientes que recibieron tratamiento inmediato con rituximab. Se encontró equivalencia en la ausencia de fracaso de tratamiento y la SG.[30][Nivel de evidencia C2] Esto denota que la observación cautelosa es un abordaje apropiado incluso en la era del rituximab.
Rituximab solo o en combinación con los citotóxicos utilizados en la terapia de primera línea
El tratamiento estándar incluye rituximab, un anticuerpo monoclonal anti-CD20, solo como se usó en el ensayo ECOG-E4402 (NCT00075946),[31-35] o en combinación con análogos de nucleósidos de purina como la fludarabina o la cladribina, alquilantes (con corticoesteroides o sin estos) o quimioterapia combinada. El rituximab se puede considerar como tratamiento de primera línea, solo o en combinación con otros medicamentos. El rituximab se puede administrar por vía intravenosa o subcutánea; versiones biosimilares, como CT-P10 y GP2013, tienen eficacia y tolerabilidad semejantes.[36-38] Las combinaciones son las siguientes:
- R-bendamustina: rituximab y bendamustina.[39-41]
- R-F: rituximab y fludarabina.[42]
- R-CVP: rituximab, ciclofosfamida, vincristina y prednisona.[43-46]
- R-CHOP: rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona.[45-49] En un metanálisis de Cochrane, no se pudo identificar un beneficio para la SG al añadir doxorrubicina a los regímenes quimioterapéuticos con rituximab o sin este.[50][Nivel de evidencia A1]
- R-FM: rituximab, fludarabina y mitoxantrona.[45,46,51]
- R-FCM: rituximab, fludarabina, ciclofosfamida y mitoxantrona.[52]
Evidencia (rituximab con o sin quimioterapia):
- En un ensayo prospectivo aleatorizado con 534 pacientes de linfoma folicular en estadio avanzado sin tratamiento previo, se compararon R-CHOP, R-FM y R-CVP.[45]
- Luego de una mediana de seguimiento de 84 meses, no hubo diferencia en la tasa de SG (SG a 8 años 83 %, intervalo de confianza [IC] de 95 %, 79–87 %), pero las tasas de SSP a 8 años favoreció el tratamiento con R-CHOP (52 %) y R-FM (49 %) en comparación con R-CVP (42 %) (P para los 3 regímenes = 0,037).[45][Nivel de evidencia B1]
- En cuatro estudios prospectivos aleatorizados con pacientes sin tratamiento previo (que incluyeron a más de 1300 pacientes) y en un metanálisis de la Cochrane que incluyó a pacientes con y sin tratamiento previo (casi 1000 pacientes), el rituximab con quimioterapia combinada se comparó con la quimioterapia sola.[44,49,53]; [54,55][Nivel de evidencia A1]
- El rituximab con quimioterapia fue superior en términos de supervivencia sin complicaciones (SSC) o SSP (2–3 años) en todos los estudios; esta combinación también fue superior en términos de SG en todos menos uno de los estudios (beneficio absoluto 6–13 % a los 4 años, P < 0,04; cociente de riesgos instantáneos [CRI] para el metanálisis = 0,63 [0,51–0,79]).
- En todos los ensayos participaron pacientes sintomáticos que necesitaban tratamiento. Estos resultados no se oponen a la observación cautelosa cuando resulte apropiada.
- El resultado de la tomografía por emisión de positrones con flúor F 18-fludesoxiglucosa y tomografía computarizada al finalizar el tratamiento con rituximab y quimioterapia es muy predictivo del desenlace. Todavía no se sabe si decidir el tratamiento a partir del resultado de estas imágenes conduce a mejores desenlaces.[56,57]
- En un ensayo prospectivo aleatorizado, NCT00991211, 527 pacientes con linfoma de crecimiento lento y linfoma de células de manto se asignaron al azar a un grupo de bendamustina y rituximab versus un grupo de R-CHOP.[40][Nivel de evidencia B1]
- Después de una mediana de seguimiento de 45 meses, la mediana de SSP favoreció al grupo de bendamustina (69 vs. 31 meses [CRI, 0,58; IC 95%, 0,44–0,74; P < 0,0001]), pero no hubo diferencia en la SG.
- El grupo de bendamustina presentó tasas significativamente más bajas de alopecia, hematotoxicidad, estomatitis, neuropatía periférica e infecciones que el grupo de R-CHOP.
- En un ensayo aleatorizado prospectivo similar, 447 pacientes con linfoma de células de manto se asignaron a bendamustina y rituximab versus R-CHOP o R-CVP.[41][Nivel de evidencia B1]
- Al cabo de una mediana de seguimiento de 65 meses, la tasa de SSP a 5 años favoreció al grupo de bendamustina y rituximab, 65,5 % versus 55,8 % (CRI, 0,61; IC 95 %, 0,45–0,85; P = 0,0025), pero no hubo diferencia en la SG.
- En el grupo de bendamustina y rituximab el aumento en las muertes por causas cardiovasculares (7 vs. 1) y por segundas neoplasias malignas diferentes al linfoma (5 vs. 3) quizás contribuyó a la falta de ventaja de SG.
Lenalidomida y rituximab
La combinación del inmunomodulador lenalidomida y rituximab (régimen R2) se propuso como un régimen alternativo a las combinaciones de citotóxicos, que acarrean toxicidad a corto y largo plazo.
Evidencia (lenalidomida y rituximab):
- En un ensayo prospectivo aleatorizado (RELEVANCE) con 1030 pacientes de linfoma folicular sin tratamiento previo, se comparó el uso de rituximab y lenalidomida durante 18 meses con el uso de rituximab y quimioterapia (por lo general, R-CHOP).[58,59] Todos los pacientes recibieron mantenimiento con rituximab hasta un máximo de 2 años.
- Al cabo de una mediana de seguimiento de 72 meses, la SSP a 6 años (60 y 59 %) y la SG a 3 años (89 %) fueron idénticas (CRI, 1,03; IC 95 %, 0,84–1,27; P = 0,78 para SSP (no se notificó el CRI para la SG).[58,59][Nivel de evidencia A1]
- En el ensayo se determinó que el régimen R2 es tan eficaz como el rituximab combinado con opciones de quimioterapia citotóxica. La tasa de transformación a linfoma de crecimiento rápido por año fue del 0,68 % en el grupo de régimen R2 y del 0,45 % en el grupo de quimioterapia R. Al cabo de una mediana de seguimiento de 72 meses, no hubo nuevas señales de seguridad.[59]
- En un ensayo prospectivo aleatorizado con 358 pacientes de linfoma de crecimiento lento en recaída o resistente al tratamiento (por lo general, linfoma folicular), el régimen R2 se comparó con el uso de rituximab solo.[60]
- Al cabo de una mediana de seguimiento de 28 meses, la mediana de SSP fue de 39,4 meses para el régimen R2 y de 14,1 meses para el rituximab solo (P < 0,0001), sin diferencias en la SG.[60][Nivel de evidencia B1]
Mantenimiento con rituximab
Luego de la terapia de inducción con rituximab solo o con rituximab y quimioterapia, es posible usar el rituximab 1 vez cada 2 o 3 meses. Este abordaje se evaluó en varios estudios.
Evidencia (mantenimiento con rituximab en pacientes sin tratamiento previo):
- En el estudio PRIMA (NCT00140582), 1018 pacientes sintomáticos de riesgo alto sin tratamiento previo que alcanzaron una respuesta completa o una respuesta parcial (RP) después de la terapia de inducción con inmunoquimioterapia (por lo general, R-CHOP), se asignaron al azar a 2 años de mantenimiento con rituximab o a no recibir mantenimiento.[61][Nivel de evidencia B1]
- Al cabo de una mediana de seguimiento de 9 años, la mediana de SSP favoreció al grupo de mantenimiento con rituximab, (10,5 años) en comparación con la observación (4,1 años) (CRI 0,61; IC 95 %, 0,52–0,73, P < 0,0001), pero no hubo diferencia en la SG.
- En el estudio United Kingdom/International Study (NCT00112931), 379 pacientes asintomáticos no tratados con carga de enfermedad baja se asignaron al azar a observación cautelosa versus inducción con rituximab solo, seguido de 2 años de mantenimiento con rituximab.[62][Nivel de evidencia A3]
- Si bien la SG y las tasas de transformación histológica no fueron diferentes a los 3 años, el mantenimiento con rituximab fue mejor según el análisis por escalas de calidad de vida (CV) (Mental Adjustment to Cancer Scale, P = 0,0004 a los 7 meses, Illness Coping Score, P = 0,0012 a los 7 meses) y del tiempo transcurrido hasta el inicio de un tratamiento nuevo durante 3 años (54 % para la observación cautelosa vs. 12 % para el mantenimiento con rituximab [CRI, 0,21; IC 95 %, 0,14–0,31, P < 0,0001]).[62][Nivel de evidencia A3]
- En este estudio se indicó que para algunos pacientes la espera durante la observación cautelosa significó esperar preocupados.[63] Sin embargo, desde la perspectiva de la SG y las tasas de transformación histológica, no se observó beneficio del mantenimiento con rituximab.
- En el estudio RESORT (NCT00075946), 289 pacientes asintomáticos con carga de enfermedad baja y sin tratamiento previo se asignaron al azar a inducción con rituximab solo, con una estrategia de reiterar el tratamiento con rituximab en el momento de la recaída, o inducción con rituximab y mantenimiento con rituximab cada 13 semanas hasta el fracaso terapéutico.[34][Nivel de evidencia A3]
- Después de una mediana de seguimiento de 4,5 años, no hubo diferencia en la mediana de tiempo hasta el fracaso terapéutico (definido como el fracaso con rituximab solo) o en la CV relacionada con la salud. Cuando se usó una estrategia de reiterar el tratamiento con dosis significativamente más bajas de rituximab, se logró un control similar de la enfermedad.
En estos 3 ensayos aleatorizados de pacientes sin tratamiento previo, no se observó una ventaja del mantenimiento con rituximab en comparación con la observación y la terapia de reinducción en el momento de la recaída. En los ensayos se indica que hay un beneficio del mantenimiento con rituximab después de la reinducción para una recaída. Quedan muchas preguntas sin resolver sobre del mantenimiento con rituximab; en particular, aquellas relacionadas con la interrupción del tratamiento a los 2 años, así como su inocuidad y eficacia a largo plazo. En un ensayo en el que se prolongó el mantenimiento con rituximab a 5 años, se observaron SSC y SG equivalentes en comparación con 1 año de mantenimiento después de la terapia de inducción con rituximab en pacientes sin tratamiento previo.[64][Nivel de evidencia A1]
- En el estudio FOLL12 (NCT02063685) participaron 807 pacientes de linfoma folicular con carga tumoral alta sin tratamiento previo. Los pacientes recibieron rituximab con inducción de quimioterapia y se asignaron al azar para recibir mantenimiento con rituximab estándar (cada 8 semanas por 2 años) o tratamiento posinducción (vigilancia, mantenimiento con rituximab o radioinmunoterapia) según la respuesta metabólica completa y el estado negativo para la enfermedad residual medible.[65]
- Al cabo de una mediana de seguimiento de 53 meses, la tasa de SSP a 3 años fue del 86 % para los pacientes que recibieron el mantenimiento estándar y del 72 % para los pacientes que recibieron el tratamiento relacionado con la respuesta (P < 0,001). La SG a 3 años fue igual en ambos grupos (98 vs. 97 %; P = 0,238).[65][Nivel de evidencia B1]
- En este ensayo no se respalda el uso de una TEP-TC al final del tratamiento para orientar el mantenimiento con rituximab.
En todos los estudios de pacientes sin tratamiento previo, se observaron mejorías de la SSP sin cambio en la SG.
Evidencia (mantenimiento con rituximab en pacientes con tratamiento previo):
- En un ensayo prospectivo aleatorizado con 465 pacientes de linfoma folicular en recaída, aquellos que respondieron al tratamiento con R-CHOP o CHOP se asignaron al azar a recibir mantenimiento con rituximab (1 dosis cada 3 meses durante 2 años) o a no recibir mantenimiento.[66][Nivel de evidencia B1]
- Al cabo de una mediana de seguimiento de 6 años, el mantenimiento con rituximab produjo mejoría de la mediana de SSP (44 vs. 16 meses; P <0,001), pero el beneficio para la SG a 5 años fue marginal (74 vs. 64 %, P = 0,07).
- El beneficio del mantenimiento fue evidente incluso para los pacientes que recibieron rituximab durante la terapia de inducción. La mayoría de los pacientes de ambos grupos recibieron más rituximab durante el tratamiento de rescate posterior al protocolo.
- En un ensayo prospectivo aleatorizado de 280 pacientes con linfoma folicular en recaída, aquellos que respondieron a la quimioterapia con consolidación de trasplante autógeno de células madre se asignaron al azar a recibir 4 dosis de rituximab de mantenimiento o a no recibir mantenimiento.[67][Nivel de evidencia B1]
- Al cabo de una mediana de seguimiento de 8,3 años, las tasas de SSP a 10 años favoreció al grupo de mantenimiento (54 vs. 37 % [CRI 0,66; IC 95 %, 0,47–0,91, P 0,012]), pero no hubo diferencia en la SG.
- En un metanálisis de 9 ensayos aleatorizados con 2586 pacientes de linfoma folicular, la mayoría en recaída, el mantenimiento con rituximab se comparó con la ausencia de mantenimiento y se observó mejoría de la SG con el uso del mantenimiento de rituximab en pacientes con tratamiento previo (CRIde muerte 0,72; IC 95 %, 0,57-0,91).[68][Nivel de evidencia A1]
En pacientes con tratamiento previo hay más evidencia que indica una ventaja de la SG cuando se usa el mantenimiento de rituximab.
Obinutuzumab solo o en combinación con los citotóxicos utilizados en la terapia de primera línea
El obinutuzumab es un anticuerpo monoclonal glucomodificado anti-CD20 de tipo II que produce más citotoxicidad celular dependiente de anticuerpos que el rituximab.
Evidencia (obinutuzumab):
- En un ensayo prospectivo aleatorizado (NCT01332968) con 1202 pacientes de linfoma folicular sin tratamiento previo, se comparó el uso de combinaciones de obinutuzumab o de rituximab con una de tres opciones de quimioterapia según la elección del investigador: el 50 % con bendamustina; el 33 % con ciclofosfamida, doxorrubicina, vincristina y prednisona (CHOP); el 10 % con ciclofosfamida, vincristina y prednisona (CVP).[69] Después de 6 ciclos de terapia combinada, los pacientes que recibieron 2 años de terapia de mantenimiento continuaron recibiendo el mismo anticuerpo cada 2 meses.
- Al cabo de una mediana de seguimiento de 34,5 meses, la tasa de SSP a 3 años en el grupo de obinutuzumab fue del 80 %, y del 73,3 % en el grupo de rituximab (73,3 %) (CRI, 0,66; IC 95 %, 0,51–0,85, P = 0,01).[69][Nivel de evidencia B1]
- No hubo diferencia en la SG.
- La mortalidad por toxicidad fue más alta en los pacientes que usaron bendamustina en el grupo de obinutuzumab (5,6 %) y en el grupo de rituximab (4,4 %) en comparación con los resultados históricos. El número de muertes por toxicidad durante la terapia de primera línea parece excesivo en pacientes con linfoma de crecimiento lento de grado bajo y medianas de supervivencia que exceden los 15 años. En cambio, la mortalidad por toxicidad fue del 1 % al 2 % cuando cualquiera de los anticuerpos se combinó con CHOP o CVP.
Se han planteado varios problemas sobre este estudio:
- Los efectos secundarios (reacciones a la infusión y efectos adversos posteriores) fueron significativamente más altos con obinutuzumab.
- El obinutuzumab cuesta mucho más que el rituximab.
En resumen, en ausencia de modificaciones en la SG, resulta complicado decidir si se cambia el rituximab por obinutuzumab para combinarlo con quimioterapia en pacientes con linfoma folicular sin tratamiento previo. Las diferencias en la SSP quizás se pueden atribuir al desequilibrio en la dosificación del anticuerpo monoclonal; y el aumento de los efectos secundarios y del costo son factores mitigantes. En este ensayo, la bendamustina combinada con cualquier anticuerpo condujo a tasas de mortalidad tóxica inaceptables.
Inhibidor de la fosfatidilinositol 3–cinasa
Copanlisib
Evidencia (copanlisib):
- En un estudio aleatorizado, con doble enmascaramiento y controlado con placebo, se asignaron 307 pacientes con linfoma de crecimiento lento en recaída a recibir copanlisib con rituximab y a 151 pacientes a recibir placebo con rituximab (aleatorización de 2:1).[70]
- Al cabo de una mediana de seguimiento de 19,2 meses, la mediana de SSP fue de 21,5 meses en los pacientes del grupo de copanlisib con rituximab (IC 95 %, 17,8–33,0) versus 13,8 meses (IC 95 %, 10,2–17,5) en los pacientes del grupo de placebo con rituximab (CRI, 0,52; IC 95 %, 0,39–0,69; P < 0,0001).[70][Nivel de evidencia B1]
- Los efectos adversos de grado 3 a 4 más comunes fueron la hiperglicemia y la hipertensión, los cuales se presentaron en la mitad de los pacientes que recibieron copanlisib.
Los inhibidores de PI3K tienen efectos adversos significativos que incluyen neumonitis, colitis, transaminitis, hipertensión, hiperglucemia, exantema y aumento del riesgo de infecciones. Los efectos adversos han afectado el uso de estos medicamentos como tratamiento hasta que los resultados del ensayo confirmatorio establezcan su eficacia e inocuidad.[71] Estos medicamentos están aprobados para el tratamiento del linfoma folicular en recaída o resistente al tratamiento después de 2 líneas de terapia previas.
Inhibidor de EZH2
Tazemetostat
El tazemetostat es un inhibidor de EZH2, una histona–metiltransferasa necesaria para la formación de los centros germinales de los ganglios linfáticos, en especial, cuando hay mutaciones activadoras en EZH2.
Evidencia (tazemetostat):
- En un estudio de fase II, participaron 99 pacientes con linfoma folicular en recaída o resistente al tratamiento, 45 se presentaron con mutaciones activadoras en EZH2, y 54 con EZH2 natural normal.[72]
- El tratamiento con tazemetostat produjo una tasa de respuesta objetiva del 69 % (IC 95 %, 53–82 %) en los pacientes con mutaciones activadoras versus un 35 % (IC 95 %, 23–49%) en los pacientes con EZH2 natural.[72]
- Al cabo de una mediana de seguimiento de 22 meses, la mediana de SSP fue de 13,8 meses (IC 95 %, 10,7–22,0) en los pacientes con mutaciones activadoras y de 11,1 meses (IC 95 %, 3,7–14,6) en los pacientes con EZH2 natural.[72][Nivel de evidencia C3]
- Se observaron efectos adversos relacionados con el tratamiento de grado 3 o 4 en el 4 % de los pacientes.
Anticuerpos monoclonales anti-CD20 radiomarcados
El itrio Y 90 (90Y)-ibritumomab tiuxetán (Zevalin) está disponible para pacientes con linfoma sin tratamiento previo y para pacientes en recaída con compromiso mínimo de la médula ósea (<25 %) o sin compromiso de la médula ósea (el yodo I 131 [131I]-tositumomab [Bexxar] ya no está disponible por una retirada de tipo comercial).[73,74]
Evidencia (anticuerpos monoclonales anti-CD20 radiomarcados):
- En un ensayo prospectivo aleatorizado, 554 pacientes de linfoma folicular en estadio avanzado con tratamiento previo recibieron 6 ciclos de R-CHOP o 6 ciclos de CHOP seguidos de radioinmunoterapia (RIT) con 131I-tositumomab.[75]
- Tras una mediana de seguimiento de 10,3 años, mejoró la SSP con el uso de RIT (56 vs. 42 %, P = 0,01); pero no hubo diferencia significativa en la SG a 10 años (SG con R-CHOP de 81 %; SG con CHOP-RIT de 75 %, P = 0,13).[75][Nivel de evidencia B1]
- En este ensayo, la mortalidad acumulada por síndrome mielodisplásico o leucemia mieloide aguda fue más alta para el grupo de RIT (4 vs. 1 %, P = 0,02).
El 131I-tositumomab se retiró del mercado en 2013.
- En un ensayo aleatorizado con 409 pacientes de linfoma folicular en estadios III o IV que lograron una RC o RP, se evaluó la consolidación con 90Y-ibritumomab tiuxetán versus ninguna consolidación.[76]
- La consolidación con el anticuerpo radiomarcado aumentó 3 años la mediana de SSP (P < 0,001) y la mediana de tiempo hasta el siguiente tratamiento mejoró en 5,1 años (P < 0,001); sin embargo, no hubo cambio en la SG.[76][Nivel de evidencia B1]
También se notificaron respuestas duraderas con anticuerpos monoclonales radiomarcados, como 90Y-ibritumomab tiuxetán (se comercializa) y el yodo I 131-tositumomab (no se comercializa) administrados antes y después de quimioterapia citotóxica.[75,77,78][Nivel de evidencia B1] Sin embargo, la mortalidad acumulada por síndrome mielodisplásico o leucemia mieloide aguda es más alta (4 vs. 1 %; P = 0,02) es uno de los ensayos aleatorizados de comparación con un anticuerpo no radiomarcado y quimioterapia.[75]
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Hagenbeek A, Eghbali H, Monfardini S, et al.: Phase III intergroup study of fludarabine phosphate compared with cyclophosphamide, vincristine, and prednisone chemotherapy in newly diagnosed patients with stage III and IV low-grade malignant Non-Hodgkin's lymphoma. J Clin Oncol 24 (10): 1590-6, 2006. [PUBMED Abstract]
- Gribben JG: How I treat indolent lymphoma. Blood 109 (11): 4617-26, 2007. [PUBMED Abstract]
- Jacobs JP, Murray KJ, Schultz CJ, et al.: Central lymphatic irradiation for stage III nodular malignant lymphoma: long-term results. J Clin Oncol 11 (2): 233-8, 1993. [PUBMED Abstract]
- Mendenhall NP, Million RR: Comprehensive lymphatic irradiation for stage II-III non-Hodgkin's lymphoma. Am J Clin Oncol 12 (3): 190-4, 1989. [PUBMED Abstract]
- Kusumoto S, Arcaini L, Hong X, et al.: Risk of HBV reactivation in patients with B-cell lymphomas receiving obinutuzumab or rituximab immunochemotherapy. Blood 133 (2): 137-146, 2019. [PUBMED Abstract]
- van Besien K, Sobocinski KA, Rowlings PA, et al.: Allogeneic bone marrow transplantation for low-grade lymphoma. Blood 92 (5): 1832-6, 1998. [PUBMED Abstract]
- van Besien K, Loberiza FR, Bajorunaite R, et al.: Comparison of autologous and allogeneic hematopoietic stem cell transplantation for follicular lymphoma. Blood 102 (10): 3521-9, 2003. [PUBMED Abstract]
- Deconinck E, Foussard C, Milpied N, et al.: High-dose therapy followed by autologous purged stem-cell transplantation and doxorubicin-based chemotherapy in patients with advanced follicular lymphoma: a randomized multicenter study by GOELAMS. Blood 105 (10): 3817-23, 2005. [PUBMED Abstract]
- Sebban C, Mounier N, Brousse N, et al.: Standard chemotherapy with interferon compared with CHOP followed by high-dose therapy with autologous stem cell transplantation in untreated patients with advanced follicular lymphoma: the GELF-94 randomized study from the Groupe d'Etude des Lymphomes de l'Adulte (GELA). Blood 108 (8): 2540-4, 2006. [PUBMED Abstract]
- Lenz G, Dreyling M, Schiegnitz E, et al.: Myeloablative radiochemotherapy followed by autologous stem cell transplantation in first remission prolongs progression-free survival in follicular lymphoma: results of a prospective, randomized trial of the German Low-Grade Lymphoma Study Group. Blood 104 (9): 2667-74, 2004. [PUBMED Abstract]
- Rohatiner AZ, Nadler L, Davies AJ, et al.: Myeloablative therapy with autologous bone marrow transplantation for follicular lymphoma at the time of second or subsequent remission: long-term follow-up. J Clin Oncol 25 (18): 2554-9, 2007. [PUBMED Abstract]
- Gopal AK, Rajendran JG, Gooley TA, et al.: High-dose [131I]tositumomab (anti-CD20) radioimmunotherapy and autologous hematopoietic stem-cell transplantation for adults > or = 60 years old with relapsed or refractory B-cell lymphoma. J Clin Oncol 25 (11): 1396-402, 2007. [PUBMED Abstract]
- Gyan E, Foussard C, Bertrand P, et al.: High-dose therapy followed by autologous purged stem cell transplantation and doxorubicin-based chemotherapy in patients with advanced follicular lymphoma: a randomized multicenter study by the GOELAMS with final results after a median follow-up of 9 years. Blood 113 (5): 995-1001, 2009. [PUBMED Abstract]
- Al Khabori M, de Almeida JR, Guyatt GH, et al.: Autologous stem cell transplantation in follicular lymphoma: a systematic review and meta-analysis. J Natl Cancer Inst 104 (1): 18-28, 2012. [PUBMED Abstract]
- Schaaf M, Reiser M, Borchmann P, et al.: High-dose therapy with autologous stem cell transplantation versus chemotherapy or immuno-chemotherapy for follicular lymphoma in adults. Cochrane Database Syst Rev 1: CD007678, 2012. [PUBMED Abstract]
- Bendandi M, Gocke CD, Kobrin CB, et al.: Complete molecular remissions induced by patient-specific vaccination plus granulocyte-monocyte colony-stimulating factor against lymphoma. Nat Med 5 (10): 1171-7, 1999. [PUBMED Abstract]
- Neelapu SS, Gause BL, Nikcevich DA, et al.: Phase III randomized trial of patient-specific vaccination for previously untreated patients with follicular lymphoma in first complete remission: protocol summary and interim report. Clin Lymphoma 6 (1): 61-4, 2005. [PUBMED Abstract]
- Inogès S, Rodrìguez-Calvillo M, Zabalegui N, et al.: Clinical benefit associated with idiotypic vaccination in patients with follicular lymphoma. J Natl Cancer Inst 98 (18): 1292-301, 2006. [PUBMED Abstract]
- Ha CS, Kong JS, Tucker SL, et al.: Central lymphatic irradiation for stage I-III follicular lymphoma: report from a single-institutional prospective study. Int J Radiat Oncol Biol Phys 57 (2): 316-20, 2003. [PUBMED Abstract]
- Czuczman MS, Fayad L, Delwail V, et al.: Ofatumumab monotherapy in rituximab-refractory follicular lymphoma: results from a multicenter study. Blood 119 (16): 3698-704, 2012. [PUBMED Abstract]
- Chan EK, Fung S, Gospodarowicz M, et al.: Palliation by low-dose local radiation therapy for indolent non-Hodgkin lymphoma. Int J Radiat Oncol Biol Phys 81 (5): e781-6, 2011. [PUBMED Abstract]
- Rossier C, Schick U, Miralbell R, et al.: Low-dose radiotherapy in indolent lymphoma. Int J Radiat Oncol Biol Phys 81 (3): e1-6, 2011. [PUBMED Abstract]
- Eek R, Falkson G: The low-grade lymphoproliferative disorders. Oncology 54 (6): 441-58, 1997 Nov-Dec. [PUBMED Abstract]
- Ardeshna KM, Smith P, Norton A, et al.: Long-term effect of a watch and wait policy versus immediate systemic treatment for asymptomatic advanced-stage non-Hodgkin lymphoma: a randomised controlled trial. Lancet 362 (9383): 516-22, 2003. [PUBMED Abstract]
- Portlock CS, Rosenberg SA: No initial therapy for stage III and IV non-Hodgkin's lymphomas of favorable histologic types. Ann Intern Med 90 (1): 10-13, 1979.
- Solal-Céligny P, Roy P, Colombat P, et al.: Follicular lymphoma international prognostic index. Blood 104 (5): 1258-65, 2004. [PUBMED Abstract]
- Federico M, Bellei M, Marcheselli L, et al.: Follicular lymphoma international prognostic index 2: a new prognostic index for follicular lymphoma developed by the international follicular lymphoma prognostic factor project. J Clin Oncol 27 (27): 4555-62, 2009. [PUBMED Abstract]
- Brice P, Bastion Y, Lepage E, et al.: Comparison in low-tumor-burden follicular lymphomas between an initial no-treatment policy, prednimustine, or interferon alfa: a randomized study from the Groupe d'Etude des Lymphomes Folliculaires. Groupe d'Etude des Lymphomes de l'Adulte. J Clin Oncol 15 (3): 1110-7, 1997. [PUBMED Abstract]
- Young RC, Longo DL, Glatstein E, et al.: The treatment of indolent lymphomas: watchful waiting v aggressive combined modality treatment. Semin Hematol 25 (2 Suppl 2): 11-6, 1988. [PUBMED Abstract]
- Solal-Céligny P, Bellei M, Marcheselli L, et al.: Watchful waiting in low-tumor burden follicular lymphoma in the rituximab era: results of an F2-study database. J Clin Oncol 30 (31): 3848-53, 2012. [PUBMED Abstract]
- Ghielmini M, Schmitz SF, Cogliatti SB, et al.: Prolonged treatment with rituximab in patients with follicular lymphoma significantly increases event-free survival and response duration compared with the standard weekly x 4 schedule. Blood 103 (12): 4416-23, 2004. [PUBMED Abstract]
- Witzig TE, Vukov AM, Habermann TM, et al.: Rituximab therapy for patients with newly diagnosed, advanced-stage, follicular grade I non-Hodgkin's lymphoma: a phase II trial in the North Central Cancer Treatment Group. J Clin Oncol 23 (6): 1103-8, 2005. [PUBMED Abstract]
- Hainsworth JD, Litchy S, Shaffer DW, et al.: Maximizing therapeutic benefit of rituximab: maintenance therapy versus re-treatment at progression in patients with indolent non-Hodgkin's lymphoma--a randomized phase II trial of the Minnie Pearl Cancer Research Network. J Clin Oncol 23 (6): 1088-95, 2005. [PUBMED Abstract]
- Kahl BS, Hong F, Williams ME, et al.: Rituximab extended schedule or re-treatment trial for low-tumor burden follicular lymphoma: eastern cooperative oncology group protocol e4402. J Clin Oncol 32 (28): 3096-102, 2014. [PUBMED Abstract]
- Buske C, Hiddemann W: Rituximab maintenance therapy in indolent NHL: a clinical review. Leuk Res 30 (Suppl 1): S11-5, 2006. [PUBMED Abstract]
- Kim WS, Buske C, Ogura M, et al.: Efficacy, pharmacokinetics, and safety of the biosimilar CT-P10 compared with rituximab in patients with previously untreated advanced-stage follicular lymphoma: a randomised, double-blind, parallel-group, non-inferiority phase 3 trial. Lancet Haematol 4 (8): e362-e373, 2017. [PUBMED Abstract]
- Davies A, Merli F, Mihaljević B, et al.: Efficacy and safety of subcutaneous rituximab versus intravenous rituximab for first-line treatment of follicular lymphoma (SABRINA): a randomised, open-label, phase 3 trial. Lancet Haematol 4 (6): e272-e282, 2017. [PUBMED Abstract]
- Jurczak W, Moreira I, Kanakasetty GB, et al.: Rituximab biosimilar and reference rituximab in patients with previously untreated advanced follicular lymphoma (ASSIST-FL): primary results from a confirmatory phase 3, double-blind, randomised, controlled study. Lancet Haematol 4 (8): e350-e361, 2017. [PUBMED Abstract]
- Robinson KS, Williams ME, van der Jagt RH, et al.: Phase II multicenter study of bendamustine plus rituximab in patients with relapsed indolent B-cell and mantle cell non-Hodgkin's lymphoma. J Clin Oncol 26 (27): 4473-9, 2008. [PUBMED Abstract]
- Rummel MJ, Niederle N, Maschmeyer G, et al.: Bendamustine plus rituximab versus CHOP plus rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: an open-label, multicentre, randomised, phase 3 non-inferiority trial. Lancet 381 (9873): 1203-10, 2013. [PUBMED Abstract]
- Flinn IW, van der Jagt R, Kahl B, et al.: First-Line Treatment of Patients With Indolent Non-Hodgkin Lymphoma or Mantle-Cell Lymphoma With Bendamustine Plus Rituximab Versus R-CHOP or R-CVP: Results of the BRIGHT 5-Year Follow-Up Study. J Clin Oncol 37 (12): 984-991, 2019. [PUBMED Abstract]
- Czuczman MS, Koryzna A, Mohr A, et al.: Rituximab in combination with fludarabine chemotherapy in low-grade or follicular lymphoma. J Clin Oncol 23 (4): 694-704, 2005. [PUBMED Abstract]
- Marcus R, Imrie K, Belch A, et al.: CVP chemotherapy plus rituximab compared with CVP as first-line treatment for advanced follicular lymphoma. Blood 105 (4): 1417-23, 2005. [PUBMED Abstract]
- Marcus R, Imrie K, Solal-Celigny P, et al.: Phase III study of R-CVP compared with cyclophosphamide, vincristine, and prednisone alone in patients with previously untreated advanced follicular lymphoma. J Clin Oncol 26 (28): 4579-86, 2008. [PUBMED Abstract]
- Federico M, Luminari S, Dondi A, et al.: R-CVP versus R-CHOP versus R-FM for the initial treatment of patients with advanced-stage follicular lymphoma: results of the FOLL05 trial conducted by the Fondazione Italiana Linfomi. J Clin Oncol 31 (12): 1506-13, 2013. [PUBMED Abstract]
- Luminari S, Ferrari A, Manni M, et al.: Long-Term Results of the FOLL05 Trial Comparing R-CVP Versus R-CHOP Versus R-FM for the Initial Treatment of Patients With Advanced-Stage Symptomatic Follicular Lymphoma. J Clin Oncol 36 (7): 689-696, 2018. [PUBMED Abstract]
- Czuczman MS, Weaver R, Alkuzweny B, et al.: Prolonged clinical and molecular remission in patients with low-grade or follicular non-Hodgkin's lymphoma treated with rituximab plus CHOP chemotherapy: 9-year follow-up. J Clin Oncol 22 (23): 4711-6, 2004. [PUBMED Abstract]
- Hainsworth JD, Litchy S, Morrissey LH, et al.: Rituximab plus short-duration chemotherapy as first-line treatment for follicular non-Hodgkin's lymphoma: a phase II trial of the Minnie Pearl Cancer Research Network. J Clin Oncol 23 (7): 1500-6, 2005. [PUBMED Abstract]
- Hiddemann W, Kneba M, Dreyling M, et al.: Frontline therapy with rituximab added to the combination of cyclophosphamide, doxorubicin, vincristine, and prednisone (CHOP) significantly improves the outcome for patients with advanced-stage follicular lymphoma compared with therapy with CHOP alone: results of a prospective randomized study of the German Low-Grade Lymphoma Study Group. Blood 106 (12): 3725-32, 2005. [PUBMED Abstract]
- Itchaki G, Gafter-Gvili A, Lahav M, et al.: Anthracycline-containing regimens for treatment of follicular lymphoma in adults. Cochrane Database Syst Rev 7: CD008909, 2013. [PUBMED Abstract]
- Zinzani PL, Pulsoni A, Perrotti A, et al.: Fludarabine plus mitoxantrone with and without rituximab versus CHOP with and without rituximab as front-line treatment for patients with follicular lymphoma. J Clin Oncol 22 (13): 2654-61, 2004. [PUBMED Abstract]
- Forstpointner R, Dreyling M, Repp R, et al.: The addition of rituximab to a combination of fludarabine, cyclophosphamide, mitoxantrone (FCM) significantly increases the response rate and prolongs survival as compared with FCM alone in patients with relapsed and refractory follicular and mantle cell lymphomas: results of a prospective randomized study of the German Low-Grade Lymphoma Study Group. Blood 104 (10): 3064-71, 2004. [PUBMED Abstract]
- Herold M, Haas A, Srock S, et al.: Rituximab added to first-line mitoxantrone, chlorambucil, and prednisolone chemotherapy followed by interferon maintenance prolongs survival in patients with advanced follicular lymphoma: an East German Study Group Hematology and Oncology Study. J Clin Oncol 25 (15): 1986-92, 2007. [PUBMED Abstract]
- Salles GA, Mounier N, de Guibert S, et al.: Rituximab combined with chemotherapy and interferon in follicular lymphoma patients: final analysis of the GELA-GOELAMS FL2000 study with a 5-year follow-up. [Abstract] Blood 110 (11): A-792, 2007.
- Schulz H, Bohlius J, Skoetz N, et al.: Combined immunochemotherapy with rituximab improves overall survival in patients with follicular and mantle cell lymphoma: updated meta-analysis results. [Abstract] Blood 108 (11): A-2760, 2006.
- Dupuis J, Berriolo-Riedinger A, Julian A, et al.: Impact of [(18)F]fluorodeoxyglucose positron emission tomography response evaluation in patients with high-tumor burden follicular lymphoma treated with immunochemotherapy: a prospective study from the Groupe d'Etudes des Lymphomes de l'Adulte and GOELAMS. J Clin Oncol 30 (35): 4317-22, 2012. [PUBMED Abstract]
- Trotman J, Fournier M, Lamy T, et al.: Positron emission tomography-computed tomography (PET-CT) after induction therapy is highly predictive of patient outcome in follicular lymphoma: analysis of PET-CT in a subset of PRIMA trial participants. J Clin Oncol 29 (23): 3194-200, 2011. [PUBMED Abstract]
- Morschhauser F, Fowler NH, Feugier P, et al.: Rituximab plus Lenalidomide in Advanced Untreated Follicular Lymphoma. N Engl J Med 379 (10): 934-947, 2018. [PUBMED Abstract]
- Morschhauser F, Nastoupil L, Feugier P, et al.: Six-Year Results From RELEVANCE: Lenalidomide Plus Rituximab (R2) Versus Rituximab-Chemotherapy Followed by Rituximab Maintenance in Untreated Advanced Follicular Lymphoma. J Clin Oncol 40 (28): 3239-3245, 2022. [PUBMED Abstract]
- Leonard JP, Trneny M, Izutsu K, et al.: AUGMENT: A Phase III Study of Lenalidomide Plus Rituximab Versus Placebo Plus Rituximab in Relapsed or Refractory Indolent Lymphoma. J Clin Oncol 37 (14): 1188-1199, 2019. [PUBMED Abstract]
- Bachy E, Seymour JF, Feugier P, et al.: Sustained Progression-Free Survival Benefit of Rituximab Maintenance in Patients With Follicular Lymphoma: Long-Term Results of the PRIMA Study. J Clin Oncol 37 (31): 2815-2824, 2019. [PUBMED Abstract]
- Ardeshna KM, Qian W, Smith P, et al.: Rituximab versus a watch-and-wait approach in patients with advanced-stage, asymptomatic, non-bulky follicular lymphoma: an open-label randomised phase 3 trial. Lancet Oncol 15 (4): 424-35, 2014. [PUBMED Abstract]
- Ansell SM: Follicular lymphoma: watch and wait is watch and worry. Lancet Oncol 15 (4): 368-9, 2014. [PUBMED Abstract]
- Taverna C, Martinelli G, Hitz F, et al.: Rituximab Maintenance for a Maximum of 5 Years After Single-Agent Rituximab Induction in Follicular Lymphoma: Results of the Randomized Controlled Phase III Trial SAKK 35/03. J Clin Oncol 34 (5): 495-500, 2016. [PUBMED Abstract]
- Luminari S, Manni M, Galimberti S, et al.: Response-Adapted Postinduction Strategy in Patients With Advanced-Stage Follicular Lymphoma: The FOLL12 Study. J Clin Oncol 40 (7): 729-739, 2022. [PUBMED Abstract]
- van Oers MH, Tönnissen E, Van Glabbeke M, et al.: BCL-2/IgH polymerase chain reaction status at the end of induction treatment is not predictive for progression-free survival in relapsed/resistant follicular lymphoma: results of a prospective randomized EORTC 20981 phase III intergroup study. J Clin Oncol 28 (13): 2246-52, 2010. [PUBMED Abstract]
- Pettengell R, Schmitz N, Gisselbrecht C, et al.: Rituximab purging and/or maintenance in patients undergoing autologous transplantation for relapsed follicular lymphoma: a prospective randomized trial from the lymphoma working party of the European group for blood and marrow transplantation. J Clin Oncol 31 (13): 1624-30, 2013. [PUBMED Abstract]
- Vidal L, Gafter-Gvili A, Salles G, et al.: Rituximab maintenance for the treatment of patients with follicular lymphoma: an updated systematic review and meta-analysis of randomized trials. J Natl Cancer Inst 103 (23): 1799-806, 2011. [PUBMED Abstract]
- Marcus R, Davies A, Ando K, et al.: Obinutuzumab for the First-Line Treatment of Follicular Lymphoma. N Engl J Med 377 (14): 1331-1344, 2017. [PUBMED Abstract]
- Matasar MJ, Capra M, Özcan M, et al.: Copanlisib plus rituximab versus placebo plus rituximab in patients with relapsed indolent non-Hodgkin lymphoma (CHRONOS-3): a double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Oncol 22 (5): 678-689, 2021. [PUBMED Abstract]
- Richardson NC, Kasamon Y, Pazdur R, et al.: The saga of PI3K inhibitors in haematological malignancies: survival is the ultimate safety endpoint. Lancet Oncol 23 (5): 563-566, 2022. [PUBMED Abstract]
- Morschhauser F, Tilly H, Chaidos A, et al.: Tazemetostat for patients with relapsed or refractory follicular lymphoma: an open-label, single-arm, multicentre, phase 2 trial. Lancet Oncol 21 (11): 1433-1442, 2020. [PUBMED Abstract]
- Press OW, Unger JM, Braziel RM, et al.: Phase II trial of CHOP chemotherapy followed by tositumomab/iodine I-131 tositumomab for previously untreated follicular non-Hodgkin's lymphoma: five-year follow-up of Southwest Oncology Group Protocol S9911. J Clin Oncol 24 (25): 4143-9, 2006. [PUBMED Abstract]
- Scholz CW, Pinto A, Linkesch W, et al.: (90)Yttrium-ibritumomab-tiuxetan as first-line treatment for follicular lymphoma: 30 months of follow-up data from an international multicenter phase II clinical trial. J Clin Oncol 31 (3): 308-13, 2013. [PUBMED Abstract]
- Shadman M, Li H, Rimsza L, et al.: Continued Excellent Outcomes in Previously Untreated Patients With Follicular Lymphoma After Treatment With CHOP Plus Rituximab or CHOP Plus 131I-Tositumomab: Long-Term Follow-Up of Phase III Randomized Study SWOG-S0016. J Clin Oncol 36 (7): 697-703, 2018. [PUBMED Abstract]
- Morschhauser F, Radford J, Van Hoof A, et al.: 90Yttrium-ibritumomab tiuxetan consolidation of first remission in advanced-stage follicular non-Hodgkin lymphoma: updated results after a median follow-up of 7.3 years from the International, Randomized, Phase III First-LineIndolent trial. J Clin Oncol 31 (16): 1977-83, 2013. [PUBMED Abstract]
- Fisher RI, Kaminski MS, Wahl RL, et al.: Tositumomab and iodine-131 tositumomab produces durable complete remissions in a subset of heavily pretreated patients with low-grade and transformed non-Hodgkin's lymphomas. J Clin Oncol 23 (30): 7565-73, 2005. [PUBMED Abstract]
- Leahy MF, Seymour JF, Hicks RJ, et al.: Multicenter phase II clinical study of iodine-131-rituximab radioimmunotherapy in relapsed or refractory indolent non-Hodgkin's lymphoma. J Clin Oncol 24 (27): 4418-25, 2006. [PUBMED Abstract]
Tratamiento del linfoma no Hodgkin de crecimiento lento recidivante
El tratamiento con fármacos estándar casi nunca produce la curación de pacientes en recaída. A menudo se obtienen remisiones sostenidas después de una recaída en pacientes con linfomas de crecimiento lento, pero por lo general vuelven a recaer. Una supervivencia favorable después de la recaída se relacionó con una edad menor de 60 años, remisión completa en lugar de remisión parcial y una respuesta con más de 2 años de duración.[1] Sin embargo, incluso en el subconjunto más favorable, la mortalidad 10 veces mayor que las tasas de la población de los Estados Unidos ajustadas por edad.[2]
Los pacientes con linfoma de crecimiento lento que recaen, a menudo logran controlar su enfermedad con quimioterapia en monoterapia o quimioterapia combinada, rituximab (un anticuerpo monoclonal anti-CD20), lenalidomida, anticuerpos monoclonales anti-CD20 radiomarcados o radioterapia paliativa.[3,4] No obstante, la supervivencia a largo plazo sin una segunda recaída es poco común y por lo general se presentan múltiples recaídas. Los pacientes con linfoma de crecimiento lento a veces recaen con un tipo histológico más maligno. Si el modelo clínico de recaída indica que la enfermedad tiene un comportamiento más maligno, se obtiene una biopsia. Si se documenta una conversión a un tipo histológico más maligno se necesita cambiar el tratamiento por uno apropiado para el tipo histológico.[5] El crecimiento rápido o discordante en diversos sitios de la enfermedad quizás indique una conversión histológica.
En una revisión retrospectiva de 325 pacientes atendidos entre 1972 y 1999, el riesgo de transformación histológica fue del 30 % a los 10 años del diagnóstico.[6] En esta serie, los factores de riesgo alto de transformación histológica posterior fueron estadio avanzado, riesgo alto en el Follicular Lymphoma International Prognostic Index y observación cautelosa. La mediana de supervivencia después de la transformación osciló entre 1 y 2 años, el 25 % de los pacientes estaban vivos a los 5 años, y del 10 % al 20 % estaban vivos después de 10 años del segundo tratamiento.[7]
En un ensayo prospectivo con 631 pacientes de linfoma folicular, al cabo de una mediana de seguimiento de 60 meses en la era de rituximab (2002–2009), se encontró que la tasa de transformación a un tipo histológico de grado más alto fue del 11 % a los 5 años.[8] La mediana de supervivencia general (SG) después de la transformación fue de 50 meses y la tasa de SG a 5 años fue del 66 % cuando la transformación se produjo más de 18 meses después del diagnóstico de linfoma folicular. En esta serie, se describe un pronóstico mejor para los pacientes con transformación que para los pacientes tratados antes de la era del rituximab.
Para obtener información sobre los regímenes utilizados para tratar las conversiones histológicas, consultar la sección Tratamiento del linfoma no Hodgkin de crecimiento rápido recidivante. La duración de la segunda remisión a veces es breve y se debe considerar la participación en ensayos clínicos.
Opciones de tratamiento para el linfoma no Hodgkin de crecimiento lento recidivante
Las opciones de tratamiento para el linfoma no Hodgkin (LNH) de crecimiento lento recidivante son las siguientes:
- Rituximab solo o en combinación con los citotóxicos utilizados en la terapia de primera línea.
- Obinutuzumab solo o en combinación con los citotóxicos utilizados en la terapia de primera línea.
- Lenalidomida y rituximab.
- Inhibidor de la fosfatidilinositol 3–cinasa (PI3K).
- Inhibidor de EZH2.
- Radioterapia paliativa.
- Quimioterapia (en monoterapia o combinada).
- Anticuerpos monoclonales anti-CD20 radiomarcados.
- Terapia de células T con receptor de antígeno quimérico.
- Activadores biespecíficos de células T.
- Trasplante de células madre (TCM).
Rituximab solo o en combinación con los citotóxicos utilizados en la terapia de primera línea
El rituximab produce una tasa de respuesta del 40 al 50 % en los pacientes que recaen con un linfoma de células B de crecimiento lento.[9-13] El rituximab también se puede administrar con quimioterapia combinada.[14,15]
Evidencia (rituximab):
- En tres estudios prospectivos aleatorizados con pacientes tratados antes por un linfoma de crecimiento lento recidivante, los pacientes se asignaron al azar a recibir mantenimiento con rituximab después de un segundo tratamiento con quimioterapia combinada (con rituximab o sin este durante la inducción) o rituximab solo.[16-18]
- En todos los ensayos se observó una prolongación de la duración de la respuesta,[16-18] y en un ensayo se observó una mejoría de la mediana de supervivencia sin progresión (SSP) (3,7 vs. 1,3 años, P < 0,001) y de la tasa de SG a 5 años (74 vs. 64 %, P = 0,07) con una mediana de seguimiento de 39 meses que favoreció el mantenimiento con rituximab.[17]
Obinutuzumab solo o en combinación con los citotóxicos utilizados en la terapia de primera línea
El obinutuzumab es un anticuerpo monoclonal que se une a CD20 y tiene un epítopo alternativo de unión.
Evidencia (obinutuzumab):
- En un ensayo prospectivo aleatorizado (NCT01059630) con 396 pacientes de linfoma de crecimiento lento resistente al tratamiento con rituximab (en su mayoría linfoma folicular), los pacientes recibieron obinutuzumab con bendamustina seguido de terapia de mantenimiento con obinutuzumab durante 2 años versus bendamustina sola sin terapia de mantenimiento.[19,20][Nivel de evidencia A1]
- Después de una mediana de seguimiento de 31,8 meses, la combinación de obinutuzumab favoreció la tasa de SG a 2 años (74,5 vs. 65,1 %) (cociente de riesgos instantáneos [CRI], 0,67; intervalo de confianza [IC] 95 %, 0,47–0,96; P = 0,027). La mediana de SSP también favoreció la combinación de obinutuzumab (25,8 meses [IC 95 %, 19,5–41,1 meses] vs. 14,1 meses [IC 95 %, 12,6–16,0 meses]) (CRI, 0,57; IC 95 %, 0,44–0,73; P < 0,001).[20][Nivel de evidencia A1]
- Este diseño no permitió evaluar la contribución de la terapia de mantenimiento al desenlace.
Lenalidomida y rituximab
Se notificaron respuestas a la lenalidomida del 20 % al 56 % de los pacientes; en particular para los pacientes de linfoma folicular y linfoma linfocítico de células pequeñas; se observaron respuestas aún mayores para la combinación de lenalidomida y rituximab.[21,22][Nivel de evidencia C3]
Inhibidor de la fosfatidilinositol 3–cinasa
Copanlisib
Evidencia (copanlisib):
- En un estudio aleatorizado, con doble enmascaramiento y controlado con placebo, se asignaron 307 pacientes con linfoma de crecimiento lento en recaída a recibir copanlisib con rituximab y a 151 pacientes a recibir placebo con rituximab (aleatorización de 2:1).[23]
- Al cabo de una mediana de seguimiento de 19,2 meses, la mediana de SSP fue de 21,5 meses en los pacientes del grupo de copanlisib con rituximab (IC 95 %, 17,8–33,0) versus 13,8 meses (IC 95 %, 10,2–17,5) en los pacientes del grupo de placebo con rituximab (CRI, 0,52; IC 95 %, 0,39–0,69; P < 0,0001).[23][Nivel de evidencia B1]
- Los efectos adversos de grado 3 a 4 más comunes fueron la hiperglicemia y la hipertensión, los cuales se presentaron en la mitad de los pacientes que recibieron copanlisib.
- En un estudio de fase II se incluyeron 142 pacientes con linfoma de crecimiento lento en recaída o resistente al tratamiento.[24]
- El tratamiento con copanlisib intravenoso produjo una tasa de respuesta objetiva del 59 % (RC de 12 %) y una mediana de duración de la respuesta de 22,6 meses.[24][Nivel de evidencia C3]
Los inhibidores de PI3K tienen efectos adversos significativos que incluyen neumonitis, colitis, transaminitis, hipertensión, hiperglucemia, exantema y aumento del riesgo de infecciones. Los efectos adversos han afectado el uso de estos medicamentos hasta que en ensayos confirmatorios se pueda establecer su eficacia cuando se usan en combinaciones terapéuticas. Estos medicamentos están aprobados para el tratamiento del linfoma folicular en recaída o resistente al tratamiento después de dos líneas de terapia previas.
Inhibidor de EZH2
Tazemetostat
El tazemetostat es un inhibidor de EZH2, una histona–metiltransferasa necesaria para la formación de los centros germinales de los ganglios linfáticos, en especial, cuando hay mutaciones activadoras en EZH2.
Evidencia (tazemetostat):
- En un estudio de fase II participaron 99 pacientes con linfoma folicular en recaída o resistente al tratamiento, 45 se presentaron con mutaciones activadoras en EZH2, y 54 con EZH2 natural normal.[25]
- El tratamiento con tazemetostat produjo una tasa de respuesta objetiva del 69 % (IC 95 %, 53–82 %) en los pacientes con mutaciones activadoras versus un 35 % (IC 95 %, 23–49%) en los pacientes con EZH2 natural.[25]
- Al cabo de una mediana de seguimiento de 22 meses, la mediana de SSP fue de 13,8 meses (IC 95 %, 10,7–22,0) en los pacientes con mutaciones activadoras y de 11,1 meses (IC 95 %, 3,7–14,6) en los pacientes con EZH2 natural.[25][Nivel de evidencia C3]
- Se observaron efectos adversos relacionados con el tratamiento de grado 3 o 4 en el 4 % de los pacientes.
Radioterapia paliativa
Se puede lograr paliación con dosis muy bajas (4 Gy) de radioterapia dirigida al campo comprometido en 2 fracciones en pacientes con recaídas de baja malignidad y de gran malignidad.[26] En un ensayo prospectivo aleatorizado, la SSP del tratamiento con 4 Gy fue inferior al tratamiento con 24 Gy en 12 fracciones (77 vs. 92 %, P < 0,0001).[27][Nivel de evidencia B1]
Quimioterapia (monoterapia o combinada)
Es posible que los pacientes respondan de nuevo al régimen de inducción original, en especial, si la remisión duró más de 1 año. Para los pacientes que recaen, el rituximab solo o combinado con otros fármacos que no se utilizaron antes puede inducir remisiones. Para obtener más información, consultar la sección Rituximab solo o en combinación con los citotóxicos utilizados en la terapia de primera línea.
Anticuerpos monoclonales anti-CD20 radiomarcados
También se notificaron respuestas duraderas con anticuerpos monoclonales radiomarcados, como el itrio Y 90 (90Y)-ibritumomab tiuxetán (disponible para la venta) y el yodo I 131-tositumomab (no disponible para la venta) administrados antes y después de quimioterapia citotóxica.[28-30][Nivel de evidencia B1] Sin embargo, la mortalidad acumulada por síndrome mielodisplásico o leucemia mieloide aguda es más alta (4 vs. 1 %; P+/02) es uno de los ensayos aleatorizados de comparación con un anticuerpo no radiomarcado y quimioterapia.[30]
Evidencia (anticuerpos monoclonales anti-CD20 radiomarcados):
- En un ensayo prospectivo, se asignó al azar a 409 pacientes de linfoma folicular que respondieron a la quimioterapia de inducción para recibir 90Y-ibritumomab tiuxetán o para no someterse a consolidación.[31]
- Después de una mediana de seguimiento de 7,3 años, se observó una mejora de la tasa de SSP a 8 años con el uso de 90Y-ibritumomab tiuxetán (41 vs. 22 % [cociente de riesgos instantáneos 0,47; P < 0,001]), pero no hubo diferencia en la SG.[31][Nivel de evidencia B1]
Terapia de células T con receptor de antígeno quimérico
La terapia de células T con receptor de antígeno quimérico (CAR), con la terapia autógena anti-CD19 de axicabtagén ciloleucel, lisocabtagén maraleucel o tisagenlecleucel, ha sido aprobada para pacientes con linfoma folicular recidivante tras dos o más líneas de tratamiento previo.
Evidencia (terapia de células T con CAR):
- En un ensayo de fase II, 153 pacientes con linfoma folicular o linfoma de zona marginal en recaída o resistente al tratamiento recibieron axicabtagén ciloleucel.[32]
- Al cabo de una mediana de seguimiento de 17,5 meses, la tasa de respuesta objetiva fue del 92 % (IC 95 %, 85–97 %) y la tasa de RC fue del 74 %.
- La tasa de SSP a los 18 meses fue del 64,8 % (IC 95 %, 54,2–73,5%).[32][Nivel de evidencia C3]
- El síndrome de liberación de citoquinas se produjo en el 78 % de los pacientes y fue de grado 3 o 4 en el 6 % de los pacientes.
- El 50 % de los pacientes necesitó tocilizumab y el 5 % vasopresores. Se produjeron eventos neurológicos de grado 3 o 4 en el 15 % de los pacientes.
- En un ensayo de fase II, 98 pacientes con linfoma folicular en recaída o resistente al tratamiento tras dos o más líneas de tratamiento previo recibieron terapia de células T con CAR anti-CD19 con tisagenlecleucel.[33]
- Al cabo de una mediana de seguimiento de 16,6 meses, la tasa de respuesta completa fue del 69,1 % (IC 95 %, 58,8–78,3 %), y la tasa de respuesta general fue del 86,2 % (77,5–92,4 %).[33][Nivel de evidencia C3]
- El síndrome de liberación de citoquinas de grado 3 o 4 se produjo en el 48,5 % de los pacientes, y el 37,1 % presentó neurotoxicidad de grado 3 o 4.
Las células T CAR se utilizan en pacientes de riesgo alto que presentaron recaída de la enfermedad de forma rápida tras la quimioinmunoterapia. Este abordaje se considera en el contexto de otros numerosos fármacos disponibles.
Activadores biespecíficos de células T
Los activadores biespecíficos de células T se unen a CD20 (o CD19) y a CD3 para dirigir a las células T a eliminar los linfocitos B malignos.[34,35] De forma similar a la terapia con células T con CAR, casi la mitad de los pacientes que reciben esta terapia presentan síndrome de liberación de citoquinas.
Mosunetuzumab
Evidencia (mosunetuzumab):
- En un estudio de fase II, multicéntrico y de un solo grupo, 90 pacientes con linfoma folicular en recaída o resistente al tratamiento tras dos o más líneas previas de tratamiento (incluso una terapia anti-CD20 y un alquilante) recibieron mosunetuzumab.[34]
- Al cabo de una mediana de seguimiento de 27 meses, la tasa de respuesta objetiva fue del 77,8 % (IC 95 %, 67,8–85,9 %), y la tasa de respuesta completa fue del 60,0 % (IC 95 %, 49,1–70,2 %), según la evaluación de los investigadores. No se alcanzó la mediana de la SSP según la evaluación del investigador. La SSP a 24 meses fue de 51,4 meses (IC 95 %, 39,4–63,3) después de recibir mosunetuzumab, en comparación con 23,5 meses (IC 95 %, 14,5–32,5) para el último tratamiento previo de los pacientes (63 % quimioinmunoterapia, 8 % inhibidor de PI3K, 2 % terapia con células T con CAR, 2 % anticuerpo anti-CD20 con lenalidomida y otros).
- El síndrome de liberación de citoquinas se produjo en el 44,4 % de los pacientes; la gravedad del 97,2 % de los casos fue de grado 1 o 2.[36][Nivel de evidencia C3]
Trasplante de células madre
En muchas instituciones, se están utilizando TCM autógenos o alogénicos en pacientes de riesgo alto que presentaron recaída de la enfermedad de forma rápida tras la quimioinmunoterapia. Este abordaje se considera en el contexto de otros numerosos fármacos disponibles.[37-41]
Evidencia (TCM):
- En el German Low-Grade Lymphoma Study Group se administró a 307 pacientes de linfoma folicular 2 ciclos de quimioterapia de inducción con ciclofosfamida, doxorrubicina, vincristina y prednisona (parecida al CHOP) y luego se los asignó de manera aleatoria a TCM autógeno o mantenimiento con interferón.[42]
- Después de una mediana de seguimiento de 4,2 meses, la SSP a 5 años fue del 65 % en los pacientes que recibieron trasplante versus el 33 % en los pacientes que recibieron el interferón (P < 0,001). No hubo diferencia en la SG.[42][Nivel de evidencia B1]
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Casulo C, Byrtek M, Dawson KL, et al.: Early Relapse of Follicular Lymphoma After Rituximab Plus Cyclophosphamide, Doxorubicin, Vincristine, and Prednisone Defines Patients at High Risk for Death: An Analysis From the National LymphoCare Study. J Clin Oncol 33 (23): 2516-22, 2015. [PUBMED Abstract]
- Weisdorf DJ, Andersen JW, Glick JH, et al.: Survival after relapse of low-grade non-Hodgkin's lymphoma: implications for marrow transplantation. J Clin Oncol 10 (6): 942-7, 1992. [PUBMED Abstract]
- Peterson BA: Current treatment of follicular low-grade lymphomas. Semin Oncol 26 (5 Suppl 14): 2-11, 1999. [PUBMED Abstract]
- Haas RL, Poortmans P, de Jong D, et al.: High response rates and lasting remissions after low-dose involved field radiotherapy in indolent lymphomas. J Clin Oncol 21 (13): 2474-80, 2003. [PUBMED Abstract]
- Tsimberidou AM, O'Brien S, Khouri I, et al.: Clinical outcomes and prognostic factors in patients with Richter's syndrome treated with chemotherapy or chemoimmunotherapy with or without stem-cell transplantation. J Clin Oncol 24 (15): 2343-51, 2006. [PUBMED Abstract]
- Montoto S, Davies AJ, Matthews J, et al.: Risk and clinical implications of transformation of follicular lymphoma to diffuse large B-cell lymphoma. J Clin Oncol 25 (17): 2426-33, 2007. [PUBMED Abstract]
- Yuen AR, Kamel OW, Halpern J, et al.: Long-term survival after histologic transformation of low-grade follicular lymphoma. J Clin Oncol 13 (7): 1726-33, 1995. [PUBMED Abstract]
- Link BK, Maurer MJ, Nowakowski GS, et al.: Rates and outcomes of follicular lymphoma transformation in the immunochemotherapy era: a report from the University of Iowa/MayoClinic Specialized Program of Research Excellence Molecular Epidemiology Resource. J Clin Oncol 31 (26): 3272-8, 2013. [PUBMED Abstract]
- Davis TA, White CA, Grillo-López AJ, et al.: Single-agent monoclonal antibody efficacy in bulky non-Hodgkin's lymphoma: results of a phase II trial of rituximab. J Clin Oncol 17 (6): 1851-7, 1999. [PUBMED Abstract]
- Piro LD, White CA, Grillo-López AJ, et al.: Extended Rituximab (anti-CD20 monoclonal antibody) therapy for relapsed or refractory low-grade or follicular non-Hodgkin's lymphoma. Ann Oncol 10 (6): 655-61, 1999. [PUBMED Abstract]
- Davis TA, Grillo-López AJ, White CA, et al.: Rituximab anti-CD20 monoclonal antibody therapy in non-Hodgkin's lymphoma: safety and efficacy of re-treatment. J Clin Oncol 18 (17): 3135-43, 2000. [PUBMED Abstract]
- Hainsworth JD, Litchy S, Shaffer DW, et al.: Maximizing therapeutic benefit of rituximab: maintenance therapy versus re-treatment at progression in patients with indolent non-Hodgkin's lymphoma--a randomized phase II trial of the Minnie Pearl Cancer Research Network. J Clin Oncol 23 (6): 1088-95, 2005. [PUBMED Abstract]
- Lockmer S, Østenstad B, Hagberg H, et al.: Chemotherapy-Free Initial Treatment of Advanced Indolent Lymphoma Has Durable Effect With Low Toxicity: Results From Two Nordic Lymphoma Group Trials With More Than 10 Years of Follow-Up. J Clin Oncol : JCO1800262, 2018. [PUBMED Abstract]
- Forstpointner R, Dreyling M, Repp R, et al.: The addition of rituximab to a combination of fludarabine, cyclophosphamide, mitoxantrone (FCM) significantly increases the response rate and prolongs survival as compared with FCM alone in patients with relapsed and refractory follicular and mantle cell lymphomas: results of a prospective randomized study of the German Low-Grade Lymphoma Study Group. Blood 104 (10): 3064-71, 2004. [PUBMED Abstract]
- Canellos GP: CHOP may have been part of the beginning but certainly not the end: issues in risk-related therapy of large-cell lymphoma. J Clin Oncol 15 (5): 1713-6, 1997. [PUBMED Abstract]
- van Oers MH, Van Glabbeke M, Giurgea L, et al.: Rituximab maintenance treatment of relapsed/resistant follicular non-Hodgkin's lymphoma: long-term outcome of the EORTC 20981 phase III randomized intergroup study. J Clin Oncol 28 (17): 2853-8, 2010. [PUBMED Abstract]
- van Oers MH, Klasa R, Marcus RE, et al.: Rituximab maintenance improves clinical outcome of relapsed/resistant follicular non-Hodgkin lymphoma in patients both with and without rituximab during induction: results of a prospective randomized phase 3 intergroup trial. Blood 108 (10): 3295-301, 2006. [PUBMED Abstract]
- Martinelli G, Schmitz SF, Utiger U, et al.: Long-term follow-up of patients with follicular lymphoma receiving single-agent rituximab at two different schedules in trial SAKK 35/98. J Clin Oncol 28 (29): 4480-4, 2010. [PUBMED Abstract]
- Sehn LH, Chua N, Mayer J, et al.: Obinutuzumab plus bendamustine versus bendamustine monotherapy in patients with rituximab-refractory indolent non-Hodgkin lymphoma (GADOLIN): a randomised, controlled, open-label, multicentre, phase 3 trial. Lancet Oncol 17 (8): 1081-93, 2016. [PUBMED Abstract]
- Cheson BD, Chua N, Mayer J, et al.: Overall Survival Benefit in Patients With Rituximab-Refractory Indolent Non-Hodgkin Lymphoma Who Received Obinutuzumab Plus Bendamustine Induction and Obinutuzumab Maintenance in the GADOLIN Study. J Clin Oncol 36 (22): 2259-2266, 2018. [PUBMED Abstract]
- Witzig TE, Wiernik PH, Moore T, et al.: Lenalidomide oral monotherapy produces durable responses in relapsed or refractory indolent non-Hodgkin's Lymphoma. J Clin Oncol 27 (32): 5404-9, 2009. [PUBMED Abstract]
- Leonard JP, Jung SH, Johnson J, et al.: Randomized Trial of Lenalidomide Alone Versus Lenalidomide Plus Rituximab in Patients With Recurrent Follicular Lymphoma: CALGB 50401 (Alliance). J Clin Oncol 33 (31): 3635-40, 2015. [PUBMED Abstract]
- Matasar MJ, Capra M, Özcan M, et al.: Copanlisib plus rituximab versus placebo plus rituximab in patients with relapsed indolent non-Hodgkin lymphoma (CHRONOS-3): a double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Oncol 22 (5): 678-689, 2021. [PUBMED Abstract]
- Dreyling M, Santoro A, Mollica L, et al.: Phosphatidylinositol 3-Kinase Inhibition by Copanlisib in Relapsed or Refractory Indolent Lymphoma. J Clin Oncol 35 (35): 3898-3905, 2017. [PUBMED Abstract]
- Morschhauser F, Tilly H, Chaidos A, et al.: Tazemetostat for patients with relapsed or refractory follicular lymphoma: an open-label, single-arm, multicentre, phase 2 trial. Lancet Oncol 21 (11): 1433-1442, 2020. [PUBMED Abstract]
- Haas RL, Poortmans P, de Jong D, et al.: Effective palliation by low dose local radiotherapy for recurrent and/or chemotherapy refractory non-follicular lymphoma patients. Eur J Cancer 41 (12): 1724-30, 2005. [PUBMED Abstract]
- Hoskin PJ, Kirkwood AA, Popova B, et al.: 4 Gy versus 24 Gy radiotherapy for patients with indolent lymphoma (FORT): a randomised phase 3 non-inferiority trial. Lancet Oncol 15 (4): 457-63, 2014. [PUBMED Abstract]
- Fisher RI, Kaminski MS, Wahl RL, et al.: Tositumomab and iodine-131 tositumomab produces durable complete remissions in a subset of heavily pretreated patients with low-grade and transformed non-Hodgkin's lymphomas. J Clin Oncol 23 (30): 7565-73, 2005. [PUBMED Abstract]
- Leahy MF, Seymour JF, Hicks RJ, et al.: Multicenter phase II clinical study of iodine-131-rituximab radioimmunotherapy in relapsed or refractory indolent non-Hodgkin's lymphoma. J Clin Oncol 24 (27): 4418-25, 2006. [PUBMED Abstract]
- Shadman M, Li H, Rimsza L, et al.: Continued Excellent Outcomes in Previously Untreated Patients With Follicular Lymphoma After Treatment With CHOP Plus Rituximab or CHOP Plus 131I-Tositumomab: Long-Term Follow-Up of Phase III Randomized Study SWOG-S0016. J Clin Oncol 36 (7): 697-703, 2018. [PUBMED Abstract]
- Morschhauser F, Radford J, Van Hoof A, et al.: 90Yttrium-ibritumomab tiuxetan consolidation of first remission in advanced-stage follicular non-Hodgkin lymphoma: updated results after a median follow-up of 7.3 years from the International, Randomized, Phase III First-LineIndolent trial. J Clin Oncol 31 (16): 1977-83, 2013. [PUBMED Abstract]
- Jacobson CA, Chavez JC, Sehgal AR, et al.: Axicabtagene ciloleucel in relapsed or refractory indolent non-Hodgkin lymphoma (ZUMA-5): a single-arm, multicentre, phase 2 trial. Lancet Oncol 23 (1): 91-103, 2022. [PUBMED Abstract]
- Fowler NH, Dickinson M, Dreyling M, et al.: Tisagenlecleucel in adult relapsed or refractory follicular lymphoma: the phase 2 ELARA trial. Nat Med 28 (2): 325-332, 2022. [PUBMED Abstract]
- Budde LE, Sehn LH, Matasar M, et al.: Safety and efficacy of mosunetuzumab, a bispecific antibody, in patients with relapsed or refractory follicular lymphoma: a single-arm, multicentre, phase 2 study. Lancet Oncol 23 (8): 1055-1065, 2022. [PUBMED Abstract]
- Hutchings M, Mous R, Clausen MR, et al.: Dose escalation of subcutaneous epcoritamab in patients with relapsed or refractory B-cell non-Hodgkin lymphoma: an open-label, phase 1/2 study. Lancet 398 (10306): 1157-1169, 2021. [PUBMED Abstract]
- Bartlett NL, Sehn LH, Matasar MJ, et al.: Mosunetuzumab monotherapy demonstrates durable efficacy with a manageable safety profile in patients with relapsed/refractory follicular lymphoma who received ≥2 prior therapies: updated results from a pivotal phase II study. [Abstract] Blood 140 (Suppl 1): A-610, 1467-70, 2022.
- Freedman A, Friedberg JW, Gribben J: High-dose therapy for follicular lymphoma. Oncology (Huntingt) 14 (3): 321-6, 329; discussion 330-2, 338, 2000. [PUBMED Abstract]
- Brice P, Simon D, Bouabdallah R, et al.: High-dose therapy with autologous stem-cell transplantation (ASCT) after first progression prolonged survival of follicular lymphoma patients included in the prospective GELF 86 protocol. Ann Oncol 11 (12): 1585-90, 2000. [PUBMED Abstract]
- Khouri IF, McLaughlin P, Saliba RM, et al.: Eight-year experience with allogeneic stem cell transplantation for relapsed follicular lymphoma after nonmyeloablative conditioning with fludarabine, cyclophosphamide, and rituximab. Blood 111 (12): 5530-6, 2008. [PUBMED Abstract]
- Sebban C, Brice P, Delarue R, et al.: Impact of rituximab and/or high-dose therapy with autotransplant at time of relapse in patients with follicular lymphoma: a GELA study. J Clin Oncol 26 (21): 3614-20, 2008. [PUBMED Abstract]
- Thomson KJ, Morris EC, Milligan D, et al.: T-cell-depleted reduced-intensity transplantation followed by donor leukocyte infusions to promote graft-versus-lymphoma activity results in excellent long-term survival in patients with multiply relapsed follicular lymphoma. J Clin Oncol 28 (23): 3695-700, 2010. [PUBMED Abstract]
- Lenz G, Dreyling M, Schiegnitz E, et al.: Myeloablative radiochemotherapy followed by autologous stem cell transplantation in first remission prolongs progression-free survival in follicular lymphoma: results of a prospective, randomized trial of the German Low-Grade Lymphoma Study Group. Blood 104 (9): 2667-74, 2004. [PUBMED Abstract]
Tratamiento del linfoma no Hodgkin de crecimiento rápido en estadio I y del linfoma no Hodgkin de crecimiento rápido y contiguo en estadio II
Los pacientes con linfoma difuso de células B grandes (LDCBG) de crecimiento rápido en estadio I o linfoma de crecimiento rápido y contiguo en estadio II son aptos para recibir quimioterapia combinada con radioterapia dirigida al campo comprometido (RTCC) o sin esta.
Los pacientes con infección por el virus de la hepatitis B (VHB) no resuelta (negativos para el antígeno de superficie de la hepatitis B, pero positivos para el anticuerpo del núcleo de la hepatitis B) presentan riesgo de reactivación del VHB y necesitan vigilancia del ADN del VHB. El tratamiento profiláctico con nucleósidos redujo la reactivación del VHB del 10,8 % al 2,1 % en un estudio retrospectivo de 326 pacientes.[1]
Opciones de tratamiento para el linfoma no Hodgkin de crecimiento rápido en estadio I y el linfoma no Hodgkin de crecimiento rápido y contiguo en estadio II
Las opciones de tratamiento para el linfoma no Hodgkin de crecimiento rápido en estadio I y el linfoma no Hodgkin de crecimiento rápido y contiguo en estadio II son las siguientes:
- Rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona con radioterapia dirigida al campo comprometido o sin esta.
- Rituximab, doxorrubicina, ciclofosfamida, vindesina, bleomicina y prednisona (R-ACVBP) (en evaluación clínica).[2,3]
Rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona con radioterapia dirigida al campo comprometido o sin esta
A partir de la confirmación de la eficacia del rituximab para la enfermedad en estadio avanzado se planteó el uso de rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona (R-CHOP) con radioterapia o sin esta, pero este uso solo se respalda en comparaciones retrospectivas.[4][Nivel de evidencia C2]
- R-CHOP (4 a 6 ciclos).
- R-CHOP (3 a 6 ciclos) y RTCC.
Evidencia (Rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona con radioterapia dirigida al campo comprometido o sin esta):
- En un ensayo prospectivo aleatorizado con 334 pacientes de LDCBG sin gran masa tumoral (≤7 cm) en estadio I o estadio II, los pacientes recibieron 4 a 6 ciclos de R-CHOP-14 (R-CHOP administrado cada 2 semanas) y luego se asignaron al azar a recibir 40 Gy de radioterapia o a no recibir radioterapia.[5]
- Después de una mediana de seguimiento de 64 meses, la supervivencia sin complicaciones a 5 años (89–92 %; P = 0,18) y la supervivencia general (SG) a 5 años (92–96 %; P = 0,32) fueron equivalentes.[5][Nivel de evidencia A1]
De manera semejante a los resultados de los estudios aleatorizados de radioterapia antes de la era de rituximab, es posible diferir la radioterapia para los pacientes sin grandes masas tumorales en estadios tempranos. Para los pacientes que no toleran un curso prolongado de quimioterapia, se obtienen resultados equivalentes con 3 ciclos de R-CHOP y radioterapia de acuerdo a ensayos retrospectivos de un solo grupo.[4]
- En un ensayo prospectivo aleatorizado (NCT00278421) de 592 pacientes menores de 60 años de LDCBG sin gran masa tumoral (<7,5 cm) en estadio I o estadio II, los pacientes se asignaron al azar a recibir 4 o 6 ciclos de R-CHOP (con 2 ciclos más de rituximab después de 4 ciclos).[6]
- Al cabo de una mediana de seguimiento de 66 meses, la tasa de supervivencia sin progresión (SSP) a 3 años fue del 96 % (IC 95 %, 94−99 %) para los pacientes que recibieron 4 ciclos de R-CHOP, esta fue un 3 % mejor (el límite inferior del valor unilateral de IC 95 % fue cero) que la tasa de SSP de los pacientes que recibieron 6 ciclos, lo que estableció una ausencia de inferioridad para el régimen de 4 ciclos.[6][Nivel de evidencia B1]
- En un análisis retrospectivo realizado en el Memorial Sloan Kettering Cancer Center entre 2001 y 2015 se incluyó a 341 pacientes con enfermedad en estadio I. En el análisis se observó que el 66 % de los pacientes tenían una presentación extraganglionar. Después de R-CHOP (o un régimen similar), con o sin radioterapia, la tasa de supervivencia sin enfermedad a 5 años fue del 77 %, y la tasa de SG a 5 años fue del 94 %.[7][Nivel de evidencia C3] En un análisis multivariante se indicó que la radioterapia puede mejorar los desenlaces de los pacientes con enfermedad extraganglionar y positiva en la tomografía por emisión de positrones (TEP) al final del tratamiento. Esta hipótesis debe confirmarse en un ensayo prospectivo aleatorizado.[7]
En resumen, para los pacientes de LDCBG sin gran masa tumoral (<7 cm) en estadio I o estadio II y con pronóstico favorable, 4 ciclos de R-CHOP son suficientes. En los pacientes con pronóstico desfavorable, se pueden administrar 6 ciclos de R-CHOP o 3 ciclos de R-CHOP y 40 Gy de radioterapia. Los pacientes con una enfermedad en estadio temprano con una gran masa tumoral (>7,5 cm) no se han estudiado en ensayos aleatorizados; por lo general se usa una terapia de modalidad combinada con 4 a 6 ciclos de R-CHOP y radioterapia. Aunque en un estudio retrospectivo se indicó que es posible que los pacientes con enfermedad extraganglionar en estadio I y un resultado positivo en una TEP al final del tratamiento se beneficien de la radioterapia, esta hipótesis debe confirmarse en un ensayo prospectivo aleatorizado.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Kusumoto S, Arcaini L, Hong X, et al.: Risk of HBV reactivation in patients with B-cell lymphomas receiving obinutuzumab or rituximab immunochemotherapy. Blood 133 (2): 137-146, 2019. [PUBMED Abstract]
- Reyes F, Lepage E, Ganem G, et al.: ACVBP versus CHOP plus radiotherapy for localized aggressive lymphoma. N Engl J Med 352 (12): 1197-205, 2005. [PUBMED Abstract]
- Ketterer N, Coiffier B, Thieblemont C, et al.: Phase III study of ACVBP versus ACVBP plus rituximab for patients with localized low-risk diffuse large B-cell lymphoma (LNH03-1B). Ann Oncol 24 (4): 1032-7, 2013. [PUBMED Abstract]
- Persky DO, Unger JM, Spier CM, et al.: Phase II study of rituximab plus three cycles of CHOP and involved-field radiotherapy for patients with limited-stage aggressive B-cell lymphoma: Southwest Oncology Group study 0014. J Clin Oncol 26 (14): 2258-63, 2008. [PUBMED Abstract]
- Lamy T, Damaj G, Soubeyran P, et al.: R-CHOP 14 with or without radiotherapy in nonbulky limited-stage diffuse large B-cell lymphoma. Blood 131 (2): 174-181, 2018. [PUBMED Abstract]
- Poeschel V, Held G, Ziepert M, et al.: Four versus six cycles of CHOP chemotherapy in combination with six applications of rituximab in patients with aggressive B-cell lymphoma with favourable prognosis (FLYER): a randomised, phase 3, non-inferiority trial. Lancet 394 (10216): 2271-2281, 2019. [PUBMED Abstract]
- Bobillo S, Joffe E, Lavery JA, et al.: Clinical characteristics and outcomes of extranodal stage I diffuse large B-cell lymphoma in the rituximab era. Blood 137 (1): 39-48, 2021. [PUBMED Abstract]
Tratamiento del linfoma no Hodgkin de crecimiento rápido no contiguo en estadios II, III y IV
El tratamiento preferido para los pacientes con linfoma no Hodgkin (LNH) de crecimiento rápido en estadios avanzados es la quimioterapia combinada, sola o que se complementa con radioterapia dirigida al campo local.[1]
En esta sección se mencionan las siguientes combinaciones farmacológicas:
- Rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona (R-CHOP).
- Rituximab, un anticuerpo monoclonal anti-CD20, doxorrubicina, ciclofosfamida, vindesina, bleomicina y prednisona (R-ACVBP).
Opciones de tratamiento para el linfoma no Hodgkin de crecimiento rápido no contiguo en estadios II, III y IV en adultos
Las opciones de tratamiento para el linfoma no Hodgkin de crecimiento rápido no contiguo en estadios II, III y IV en adultos son las siguientes:
- Rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona.
- Otra quimioterapia combinada.
- Trasplante de médula ósea o trasplante de células madre (en evaluación clínica).
- Consolidación con radioterapia dirigida a los sitios de enfermedad con gran masa tumoral (en evaluación clínica).
Rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona
En los siguientes estudios, R-CHOP se estableció como el régimen estándar para pacientes de linfoma difuso de células B grandes (LDCBG) recién diagnosticado.[2] La intensificación de la dosis de R-CHOP en un ciclo de 14 días versus un ciclo de 21 días no produjo mejores resultados.[3]
Evidencia (R-CHOP):
- R-CHOP mostró una mejora en la supervivencia sin complicaciones (SSC) y la supervivencia general (SG) en comparación con CHOP (ciclofosfamida, doxorubicina, vincristina y prednisona) solo en 399 pacientes mayores de 60 años con LDCBG en estadio avanzado (tasa de SSC de 57 vs. 38 %, P = 0,002 y tasa de SG de 70 vs. 57 %, P = 0,007 a los 2 años).[4][Nivel de evidencia A1] En el momento de una mediana de seguimiento de 10 años, la tasa de SG de los pacientes que recibieron R-CHOP comparada con la de los pacientes que recibieron CHOP fue de 44 versus 28% (P < 0,001).[5]
- De la misma manera, en 326 pacientes evaluables menores de 61 años, el régimen R-CHOP mostró una mejoría en la SSC y la SG en comparación con el régimen CHOP solo (tasa de SSC de 79 vs. 59 %, P = 0,001 y tasa de SG de 93 vs. 84%, P = 0,001 a los 3 años).[6][Nivel de evidencia A1]
- En un estudio aleatorizado (DSHNHL-1999-1A [NCT00052936]) con 1222 pacientes mayores de 60 años se comparó R-CHOP administrado cada 2 semanas durante 6 u 8 ciclos con CHOP administrado cada 2 semanas durante 6 u 8 ciclos.[7] Luego de una mediana de seguimiento de 72 meses, la SSC favoreció a R-CHOP administrado cada 2 semanas durante 6 u 8 ciclos (tasa de SSC a 6 años, 74 vs. 56 %; P < 0,0001). La SG favoreció a R-CHOP administrado durante solo 6 ciclos debido al aumento de toxicidad en el grupo de 8 ciclos (tasa de SG a 6 años, 90 vs. 80 %; P = 0,0004).[7][Nivel de evidencia A1] No hubo una comparación entre los regímenes estándar de R-CHOP o CHOP administrados cada 3 semanas.
- En un ensayo (NCT00140595) con 380 pacientes menores de 60 años de LDCBG y un puntaje de 1 ajustado por edad en el International Prognostic Index (IPI), los pacientes se asignaron al azar a un tratamiento con ACVBP y R-ACVBP acompañado de consolidación con metotrexato, ifosfamida, etopósido y citarabina versus CHOP y rituximab.[8] Luego de una mediana de seguimiento de 44 meses, la tasa de SG a 3 años favoreció R-ACVBP (92 vs 84 %; cociente de riesgos instantáneos [CRI], 0,44; intervalo de confianza [IC] 95 %, 0,28–0,81; P = 0,007).[8][Nivel de evidencia A1] La toxicidad significativamente peor de R-ACVBP, la población destinataria tan limitada (<60 años, lactato-deshidrogenasa [LDH] elevada o enfermedad en estadio III o IV, pero no ambas) y la falta de un ensayo confirmatorio quizás impidan la adopción de R-ACVBP como nuevo estándar de atención.[9]
En los ensayos clínicos se siguen explorando modificaciones del R-CHOP para lograr una mayor eficacia. Durante más de 2 décadas, ninguna modificación ha reemplazado a R-CHOP, ya que este ha sido el tratamiento de inducción estándar en todo el mundo.[10]
Pola-R-CHP
El R-CHOP se ha comparado con el Pola-R-CHP (polatuzumab vedotina, rituximab, ciclofosfamida, doxorrubicina y prednisona). El polatuzumab es un conjugado anticuerpo-fármaco compuesto por un anticuerpo monoclonal anti-CD79B unido a la vedotina (monometil auristatina E), un inhibidor de los microtúbulos.
Evidencia (Pola-R-CHP):
- Un estudio provocativo, prospectivo y aleatorizado de 879 pacientes con LDCV no tratados previamente comparó R-CHOP con Pola-R-CHP.[11] Polatuzumab vedotina fue sustituido por vincristina para mitigar la toxicidad neurológica.
- Al cabo de una mediana de seguimiento de 28,2 meses, la tasa de SSP a los 2 años fue significativamente mayor en el grupo Pola-R-CHP que en el grupo R-CHOP: 76,7 % (IC 95 %, 72,7–80,0 %) versus 70,2 % (IC 95 %, 65,8–74,6 %) (CRI, 0,73; IC 95 %, 0,57–0,95; P = 0,02).[11][Nivel de evidencia B1]
- La tasa de SG a 2 años fue del 88,7 % (IC 95 %, 85,7–91,6 %) en los pacientes que recibieron Pola-R-CHP y del 88,6 % (IC 95 %, 85,6–91,6 %) en los pacientes que recibieron R-CHOP (CRI, 0,94; IC 95 %, 0,65–1,37); P = 0,75).
El intervalo de seguimiento fue demasiado corto para establecer si la mejora del 6 % en la tasa de SSP se estabilizará o mejorará después de 2 años, y no hay evidencia de la ventaja en la SG. No obstante, los paneles consultivos de médicos están considerando si esto representa un nuevo régimen estándar para sustituir al R-CHOP. El nuevo régimen cuesta más del doble que el R-CHOP según los precios de adquisición de 2022.
No hay estudios validados para la intensificación del tratamiento de acuerdo con la tomografía por emisión de positrones interina.[12] R-CHOP tiene potencial curativo incluso en pacientes de más de 80 años, que están débiles y requieren una dosis reducida de los componentes de R-CHOP. En una revisión retrospectiva de 239 pacientes, la tasa de supervivencia a 5 años de causa específica fue del 48 % (IC 95 %, 41−55 %).[13][Nivel de evidencia C3]
Menos del 10 % de los pacientes con LDCBG presentaron un linfoma de crecimiento lento simultáneo en el momento del diagnóstico, y fueron en su mayoría del fenotipo de célula B de centro germinal. En una revisión retrospectiva de 1324 pacientes se observaron SSC (CRI, 1,19) y SG (CRI, 1,09) similares.[14][Nivel de evidencia C3] En 847 pacientes tratados con R-CHOP y que no presentaban enfermedad 24 meses después del tratamiento, la tasa de recaída del linfoma de crecimiento lento a los 5 años fue más alta con un diagnóstico de linfoma folicular simultáneo (7,4 vs. 2,1 % a los 5 años, P < 0,01) y con un fenotipo de células B de centro germinal (3,9 vs. 0,0 % a los 5 años, P = 0,02).[15]
Linfoma difuso de células B grandes gástrico en estadio IE o IIE
En cuatro series de casos con más de 100 pacientes de enfermedad en estadio IE o IIE (con tejido linfático asociado a mucosa o sin este), y con infección por Helicobacter pylori se notificó que más del 50 % de los pacientes lograron una remisión completa duradera después de un tratamiento antibiótico apropiado para erradicar el H. pylori.[16-19][Nivel de evidencia C3]
Factores pronósticos
En el International Prognostic Index (IPI) del National Comprehensive Cancer Network para el LNH de crecimiento rápido (linfoma difuso de células grades) se incluyen los siguientes 5 factores de riesgo significativos para el pronóstico de la SG y los puntajes de riesgo relacionado:[20]
- Edad.
- <40 años: 0.
- 41–60 años: 1.
- 61–75 años: 2.
- >75 años: 3.
- Estadio III/IV: 1.
- Estado funcional 2, 3 o 4: 1.
- Concentración sérica de LDH.
- Normalizada: 0.
- >1x–3x: 1.
- >3x: 2.
- Número de sitios extraganglionares ≥2: 1.
Puntaje de riesgo:
- Bajo (0 o 1): SG a 5 años de 96 %; supervivencia sin progresión (SSP) de 91 %.
- Intermedio bajo (2 o 3): SG a 5 años de 82 %; SSP de 74 %.
- Intermedio alto (4 o 5): SG a 5 años de 64 %; SSP de 51 %.
- Alto (>6): SG a 5 años de 33 %; SSP de 30 %.
Se utilizan modificaciones del IPI ajustadas por edad y estadio para los pacientes más jóvenes con enfermedad localizada.[21] Según parece, los intervalos de tiempo más cortos entre el diagnóstico y el tratamiento son marcadores indirectos de factores biológicos de pronóstico precario.[22]
La identificación de reordenamientos de los genes BCL2 y MYC, una sobreexpresión dual del gen MYC, o ambos, confieren un pronóstico particularmente desfavorable.[23-26] Los pacientes en riesgo alto de recaída se consideran aptos para participar en ensayos clínicos.[27] La obtención de perfiles moleculares de expresión génica mediante micromatrices de ADN quizás sirva en el futuro para ayudar a estratificar a los pacientes en grupos de tratamiento dirigido a dianas específicas y para mejorar la predicción de la supervivencia después de la quimioterapia estándar.[28]
Tratamiento del síndrome de lisis tumoral
Los pacientes con linfadenopatía extensa, gran masa tumoral, elevación del ácido úrico sérico y la LDH tienen un riesgo alto de síndrome de lisis tumoral que da lugar a trastornos metabólicos como hiperuricemia, hiperpotasemia, hiperfosfatemia, hipocalcemia e insuficiencia renal aguda subsiguiente.[29] Las opciones de tratamiento incluyen hidratación alcalina, alopurinol y rasburicasa, una oxidasa de urato recombinante.[30]
Profilaxis del sistema nervioso central
El CNS-IPI es un instrumento usado para predecir qué pacientes tienen un riesgo mayor del 10 % de recidiva en el sistema nervioso central (SNC). El German Lymphoma Study Group formuló este instrumento y se validó en la base de datos de la British Columbia Cancer Agency. Se usó la presencia de 4 a 6 de los factores de riesgo del CNS-IPI (edad >60 años, estado funcional ≥2, concentración elevada de LDH, enfermedad en estadio III o IV, >1 sitio extraganglionar o compromiso renal o suprarrenal) para definir el grupo de riesgo alto para la recaída en el SNC (un riesgo del 12 % de compromiso en el SNC al cabo de 2 años).[31]
Por lo general, se recomienda la profilaxis del SNC (a menudo con 4 a 6 dosis de metotrexato intratecal) para los pacientes con compromiso testicular.[32-34][Nivel de evidencia C3] En un análisis retrospectivo de los estudios alemanes RICOVER, se comparó el metotrexato intratecal con la ausencia de profilaxis en los pacientes con LDCBG. Este estudio se llevó a cabo durante la era del tratamiento con R-CHOP. Con la posible excepción de los pacientes con compromiso testicular, el análisis mostró que el metotrexato intratecal no disminuyó el riesgo de enfermedad en el SNC.[35][Nivel de evidencia C3] Algunos médicos emplean dosis altas intravenosas (IV) (a menudo 4 dosis) de metotrexato en lugar del tratamiento intratecal porque esto mejora la administración del fármaco y reduce la morbilidad del paciente.[36] En 5 estudios retrospectivos y un metanálisis de red en los que se evaluaron las dosis altas de metotrexato solo en pacientes con riesgo alto de LDCBG, tampoco se indicó una mejora de la tasa de recidiva en el SNC.[37-42][Nivel de evidencia C3] Los pacientes que se consideran de riesgo alto para la recidiva en el SNC (por ejemplo, pacientes con 4 a 6 factores de riesgo del CNS-IPI) es posible que reciban metotrexato intratecal o dosis altas IV de metotrexato, pero la falta de estudios aleatorizados confirmatorios pone en entredicho este estándar y refleja una necesidad importante de tratamientos mejor verificados en los ensayos clínicos. Aunque los pacientes con compromiso testicular o renal/ adrenal se consideran una excepción, ya que solo hay un beneficio anecdótico con el metotrexato intratecal o las dosis altas IV de metotrexato en la reducción de la recidiva en el SNC.[32-34][Nivel de evidencia C3].
En análisis retrospectivos, la adición de rituximab a los regímenes a base de CHOP redujo de modo significativo el riesgo de recaída en el SNC.[35,43][Nivel de evidencia C3] Los pacientes con diseminación al SNC en el momento del diagnóstico o de una recaída, a menudo reciben rituximab y dosis altas de metotrexato solo o con citarabina, seguidas por TCM autógeno, pero este abordaje no se ha evaluado en ensayos aleatorizados.[44,45][Nivel de evidencia C3]
Trasplante de médula ósea o trasplante de células madre
En varios ensayos prospectivos aleatorizados se evaluó la función de la consolidación con trasplante de médula ósea (TMO) autógeno o trasplante de células madre (TCM) versus quimioterapia sola para pacientes con linfoma difuso de células grandes en primera remisión.[46-53]; [54-56][Nivel de evidencia A1] Aunque en algunos de estos ensayos se observaron aumentos significativos de la SSC (10 al 20 %) en los pacientes que recibieron tratamiento de dosis altas, no se pudo demostrar de modo prospectivo una diferencia significativa en la SG en ninguna de las series.
En análisis retrospectivos con pacientes de riesgo intermedio (2 factores de riesgo) o riesgo alto (más de 3 factores de riesgo) a partir del puntaje de IPI, se indicó una mejora para la supervivencia con el TMO en 2 ensayos.[47,53] En estos estudios no se establece que la consolidación con dosis altas tiene valor para los pacientes de linfoma de crecimiento rápido que en realidad tienen un riesgo alto de recaída; además, se demuestra que la SSC quizás es un sustituto inadecuado de la SG en estos pacientes.[57]
Consolidación con radioterapia dirigida a los sitios de enfermedad con gran masa tumoral
Después de la quimioterapia de inducción con R-CHOP (o un régimen similar), la adición de radioterapia dirigida al campo comprometido para los sitios de enfermedad con gran masa tumoral inicial (≥5–10 cm) o a sitios extralinfáticos aún es polémica.[58-60] Se debe considerar el aumento de los riesgos, como la aparición de efectos tóxicos a largo plazo (por ejemplo, neoplasias malignas secundarias).
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Shankland KR, Armitage JO, Hancock BW: Non-Hodgkin lymphoma. Lancet 380 (9844): 848-57, 2012. [PUBMED Abstract]
- Coiffier B: State-of-the-art therapeutics: diffuse large B-cell lymphoma. J Clin Oncol 23 (26): 6387-93, 2005. [PUBMED Abstract]
- Cunningham D, Hawkes EA, Jack A, et al.: Rituximab plus cyclophosphamide, doxorubicin, vincristine, and prednisolone in patients with newly diagnosed diffuse large B-cell non-Hodgkin lymphoma: a phase 3 comparison of dose intensification with 14-day versus 21-day cycles. Lancet 381 (9880): 1817-26, 2013. [PUBMED Abstract]
- Coiffier B, Lepage E, Briere J, et al.: CHOP chemotherapy plus rituximab compared with CHOP alone in elderly patients with diffuse large-B-cell lymphoma. N Engl J Med 346 (4): 235-42, 2002. [PUBMED Abstract]
- Coiffier B, Thieblemont C, Van Den Neste E, et al.: Long-term outcome of patients in the LNH-98.5 trial, the first randomized study comparing rituximab-CHOP to standard CHOP chemotherapy in DLBCL patients: a study by the Groupe d'Etudes des Lymphomes de l'Adulte. Blood 116 (12): 2040-5, 2010. [PUBMED Abstract]
- Pfreundschuh M, Trümper L, Osterborg A, et al.: CHOP-like chemotherapy plus rituximab versus CHOP-like chemotherapy alone in young patients with good-prognosis diffuse large-B-cell lymphoma: a randomised controlled trial by the MabThera International Trial (MInT) Group. Lancet Oncol 7 (5): 379-91, 2006. [PUBMED Abstract]
- Pfreundschuh M, Kuhnt E, Trümper L, et al.: CHOP-like chemotherapy with or without rituximab in young patients with good-prognosis diffuse large-B-cell lymphoma: 6-year results of an open-label randomised study of the MabThera International Trial (MInT) Group. Lancet Oncol 12 (11): 1013-22, 2011. [PUBMED Abstract]
- Récher C, Coiffier B, Haioun C, et al.: Intensified chemotherapy with ACVBP plus rituximab versus standard CHOP plus rituximab for the treatment of diffuse large B-cell lymphoma (LNH03-2B): an open-label randomised phase 3 trial. Lancet 378 (9806): 1858-67, 2011. [PUBMED Abstract]
- Casasnovas RO, Ysebaert L, Thieblemont C, et al.: FDG-PET-driven consolidation strategy in diffuse large B-cell lymphoma: final results of a randomized phase 2 study. Blood 130 (11): 1315-1326, 2017. [PUBMED Abstract]
- Nowakowski GS, Hong F, Scott DW, et al.: Addition of Lenalidomide to R-CHOP Improves Outcomes in Newly Diagnosed Diffuse Large B-Cell Lymphoma in a Randomized Phase II US Intergroup Study ECOG-ACRIN E1412. J Clin Oncol 39 (12): 1329-1338, 2021. [PUBMED Abstract]
- Tilly H, Morschhauser F, Sehn LH, et al.: Polatuzumab Vedotin in Previously Untreated Diffuse Large B-Cell Lymphoma. N Engl J Med 386 (4): 351-363, 2022. [PUBMED Abstract]
- Dührsen U, Müller S, Hertenstein B, et al.: Positron Emission Tomography-Guided Therapy of Aggressive Non-Hodgkin Lymphomas (PETAL): A Multicenter, Randomized Phase III Trial. J Clin Oncol 36 (20): 2024-2034, 2018. [PUBMED Abstract]
- Gobba S, Moccia AA, Gulden-Sala W, et al.: Outcome of patients older than 80 years with diffuse large B-cell lymphoma (DLBCL) treated with "standard" immunochemotherapy: A large retrospective study from 4 institutions. Hematol Oncol 36 (1): 84-92, 2018. [PUBMED Abstract]
- Wang Y, Link BK, Witzig TE, et al.: Impact of concurrent indolent lymphoma on the clinical outcome of newly diagnosed diffuse large B-cell lymphoma. Blood 134 (16): 1289-1297, 2019. [PUBMED Abstract]
- Wang Y, Farooq U, Link BK, et al.: Late Relapses in Patients With Diffuse Large B-Cell Lymphoma Treated With Immunochemotherapy. J Clin Oncol 37 (21): 1819-1827, 2019. [PUBMED Abstract]
- Morgner A, Miehlke S, Fischbach W, et al.: Complete remission of primary high-grade B-cell gastric lymphoma after cure of Helicobacter pylori infection. J Clin Oncol 19 (7): 2041-8, 2001. [PUBMED Abstract]
- Chen LT, Lin JT, Shyu RY, et al.: Prospective study of Helicobacter pylori eradication therapy in stage I(E) high-grade mucosa-associated lymphoid tissue lymphoma of the stomach. J Clin Oncol 19 (22): 4245-51, 2001. [PUBMED Abstract]
- Chen LT, Lin JT, Tai JJ, et al.: Long-term results of anti-Helicobacter pylori therapy in early-stage gastric high-grade transformed MALT lymphoma. J Natl Cancer Inst 97 (18): 1345-53, 2005. [PUBMED Abstract]
- Kuo SH, Yeh KH, Wu MS, et al.: Helicobacter pylori eradication therapy is effective in the treatment of early-stage H pylori-positive gastric diffuse large B-cell lymphomas. Blood 119 (21): 4838-44; quiz 5057, 2012. [PUBMED Abstract]
- Zhou Z, Sehn LH, Rademaker AW, et al.: An enhanced International Prognostic Index (NCCN-IPI) for patients with diffuse large B-cell lymphoma treated in the rituximab era. Blood 123 (6): 837-42, 2014. [PUBMED Abstract]
- Møller MB, Christensen BE, Pedersen NT: Prognosis of localized diffuse large B-cell lymphoma in younger patients. Cancer 98 (3): 516-21, 2003. [PUBMED Abstract]
- Maurer MJ, Ghesquières H, Link BK, et al.: Diagnosis-to-Treatment Interval Is an Important Clinical Factor in Newly Diagnosed Diffuse Large B-Cell Lymphoma and Has Implication for Bias in Clinical Trials. J Clin Oncol 36 (16): 1603-1610, 2018. [PUBMED Abstract]
- Cuccuini W, Briere J, Mounier N, et al.: MYC+ diffuse large B-cell lymphoma is not salvaged by classical R-ICE or R-DHAP followed by BEAM plus autologous stem cell transplantation. Blood 119 (20): 4619-24, 2012. [PUBMED Abstract]
- Johnson NA, Slack GW, Savage KJ, et al.: Concurrent expression of MYC and BCL2 in diffuse large B-cell lymphoma treated with rituximab plus cyclophosphamide, doxorubicin, vincristine, and prednisone. J Clin Oncol 30 (28): 3452-9, 2012. [PUBMED Abstract]
- Green TM, Young KH, Visco C, et al.: Immunohistochemical double-hit score is a strong predictor of outcome in patients with diffuse large B-cell lymphoma treated with rituximab plus cyclophosphamide, doxorubicin, vincristine, and prednisone. J Clin Oncol 30 (28): 3460-7, 2012. [PUBMED Abstract]
- Horn H, Ziepert M, Becher C, et al.: MYC status in concert with BCL2 and BCL6 expression predicts outcome in diffuse large B-cell lymphoma. Blood 121 (12): 2253-63, 2013. [PUBMED Abstract]
- Canellos GP: CHOP may have been part of the beginning but certainly not the end: issues in risk-related therapy of large-cell lymphoma. J Clin Oncol 15 (5): 1713-6, 1997. [PUBMED Abstract]
- Sha C, Barrans S, Cucco F, et al.: Molecular High-Grade B-Cell Lymphoma: Defining a Poor-Risk Group That Requires Different Approaches to Therapy. J Clin Oncol 37 (3): 202-212, 2019. [PUBMED Abstract]
- Coiffier B, Altman A, Pui CH, et al.: Guidelines for the management of pediatric and adult tumor lysis syndrome: an evidence-based review. J Clin Oncol 26 (16): 2767-78, 2008. [PUBMED Abstract]
- Cortes J, Moore JO, Maziarz RT, et al.: Control of plasma uric acid in adults at risk for tumor Lysis syndrome: efficacy and safety of rasburicase alone and rasburicase followed by allopurinol compared with allopurinol alone--results of a multicenter phase III study. J Clin Oncol 28 (27): 4207-13, 2010. [PUBMED Abstract]
- Schmitz N, Zeynalova S, Nickelsen M, et al.: CNS International Prognostic Index: A Risk Model for CNS Relapse in Patients With Diffuse Large B-Cell Lymphoma Treated With R-CHOP. J Clin Oncol 34 (26): 3150-6, 2016. [PUBMED Abstract]
- Zucca E, Conconi A, Mughal TI, et al.: Patterns of outcome and prognostic factors in primary large-cell lymphoma of the testis in a survey by the International Extranodal Lymphoma Study Group. J Clin Oncol 21 (1): 20-7, 2003. [PUBMED Abstract]
- Vitolo U, Chiappella A, Ferreri AJ, et al.: First-line treatment for primary testicular diffuse large B-cell lymphoma with rituximab-CHOP, CNS prophylaxis, and contralateral testis irradiation: final results of an international phase II trial. J Clin Oncol 29 (20): 2766-72, 2011. [PUBMED Abstract]
- Cheah CY, Wirth A, Seymour JF: Primary testicular lymphoma. Blood 123 (4): 486-93, 2014. [PUBMED Abstract]
- Boehme V, Schmitz N, Zeynalova S, et al.: CNS events in elderly patients with aggressive lymphoma treated with modern chemotherapy (CHOP-14) with or without rituximab: an analysis of patients treated in the RICOVER-60 trial of the German High-Grade Non-Hodgkin Lymphoma Study Group (DSHNHL). Blood 113 (17): 3896-902, 2009. [PUBMED Abstract]
- Glantz MJ, Cole BF, Recht L, et al.: High-dose intravenous methotrexate for patients with nonleukemic leptomeningeal cancer: is intrathecal chemotherapy necessary? J Clin Oncol 16 (4): 1561-7, 1998. [PUBMED Abstract]
- Puckrin R, El Darsa H, Ghosh S, et al.: Ineffectiveness of high-dose methotrexate for prevention of CNS relapse in diffuse large B-cell lymphoma. Am J Hematol 96 (7): 764-771, 2021. [PUBMED Abstract]
- Jeong H, Cho H, Kim H, et al.: Efficacy and safety of prophylactic high-dose MTX in high-risk DLBCL: a treatment intent-based analysis. Blood Adv 5 (8): 2142-2152, 2021. [PUBMED Abstract]
- Orellana-Noia VM, Reed DR, McCook AA, et al.: Single-route CNS prophylaxis for aggressive non-Hodgkin lymphomas: real-world outcomes from 21 US academic institutions. Blood 139 (3): 413-423, 2022. [PUBMED Abstract]
- Lewis KL, Jakobsen LH, Villa D, et al.: High-dose methotrexate is not associated with reduction in CNS relapse in patients with aggressive B-cell lymphoma: an international retrospective study of 2300 high-risk patients. [Abstract] Blood 138 (Suppl 1): A-181, 2021.
- Wilson MR, Eyre TA, Kirkwood AA, et al.: Timing of high-dose methotrexate CNS prophylaxis in DLBCL: a multicenter international analysis of 1384 patients. Blood 139 (16): 2499-2511, 2022. [PUBMED Abstract]
- Haddad PA, Hammoud D, Gallagher KM: Effective central nervous system (CNS) prophylaxis chemotherapy approach in high risk diffuse large B-cell lymphoma (DLBCL): a network meta-analysis. [Abstract] Blood 138 (Suppl 1): A-1461, 2021.
- Villa D, Connors JM, Shenkier TN, et al.: Incidence and risk factors for central nervous system relapse in patients with diffuse large B-cell lymphoma: the impact of the addition of rituximab to CHOP chemotherapy. Ann Oncol 21 (5): 1046-52, 2010. [PUBMED Abstract]
- Ferreri AJ, Donadoni G, Cabras MG, et al.: High Doses of Antimetabolites Followed by High-Dose Sequential Chemoimmunotherapy and Autologous Stem-Cell Transplantation in Patients With Systemic B-Cell Lymphoma and Secondary CNS Involvement: Final Results of a Multicenter Phase II Trial. J Clin Oncol 33 (33): 3903-10, 2015. [PUBMED Abstract]
- Schmitz N, Wu HS: Advances in the Treatment of Secondary CNS Lymphoma. J Clin Oncol 33 (33): 3851-3, 2015. [PUBMED Abstract]
- Haioun C, Lepage E, Gisselbrecht C, et al.: Survival benefit of high-dose therapy in poor-risk aggressive non-Hodgkin's lymphoma: final analysis of the prospective LNH87-2 protocol--a groupe d'Etude des lymphomes de l'Adulte study. J Clin Oncol 18 (16): 3025-30, 2000. [PUBMED Abstract]
- Haioun C, Lepage E, Gisselbrecht C, et al.: Benefit of autologous bone marrow transplantation over sequential chemotherapy in poor-risk aggressive non-Hodgkin's lymphoma: updated results of the prospective study LNH87-2. Groupe d'Etude des Lymphomes de l'Adulte. J Clin Oncol 15 (3): 1131-7, 1997. [PUBMED Abstract]
- Santini G, Salvagno L, Leoni P, et al.: VACOP-B versus VACOP-B plus autologous bone marrow transplantation for advanced diffuse non-Hodgkin's lymphoma: results of a prospective randomized trial by the non-Hodgkin's Lymphoma Cooperative Study Group. J Clin Oncol 16 (8): 2796-802, 1998. [PUBMED Abstract]
- Gianni AM, Bregni M, Siena S, et al.: High-dose chemotherapy and autologous bone marrow transplantation compared with MACOP-B in aggressive B-cell lymphoma. N Engl J Med 336 (18): 1290-7, 1997. [PUBMED Abstract]
- Kluin-Nelemans HC, Zagonel V, Anastasopoulou A, et al.: Standard chemotherapy with or without high-dose chemotherapy for aggressive non-Hodgkin's lymphoma: randomized phase III EORTC study. J Natl Cancer Inst 93 (1): 22-30, 2001. [PUBMED Abstract]
- Gisselbrecht C, Lepage E, Molina T, et al.: Shortened first-line high-dose chemotherapy for patients with poor-prognosis aggressive lymphoma. J Clin Oncol 20 (10): 2472-9, 2002. [PUBMED Abstract]
- Martelli M, Gherlinzoni F, De Renzo A, et al.: Early autologous stem-cell transplantation versus conventional chemotherapy as front-line therapy in high-risk, aggressive non-Hodgkin's lymphoma: an Italian multicenter randomized trial. J Clin Oncol 21 (7): 1255-62, 2003. [PUBMED Abstract]
- Milpied N, Deconinck E, Gaillard F, et al.: Initial treatment of aggressive lymphoma with high-dose chemotherapy and autologous stem-cell support. N Engl J Med 350 (13): 1287-95, 2004. [PUBMED Abstract]
- Betticher DC, Martinelli G, Radford JA, et al.: Sequential high dose chemotherapy as initial treatment for aggressive sub-types of non-Hodgkin lymphoma: results of the international randomized phase III trial (MISTRAL). Ann Oncol 17 (10): 1546-52, 2006. [PUBMED Abstract]
- Stiff PJ, Unger JM, Cook JR, et al.: Autologous transplantation as consolidation for aggressive non-Hodgkin's lymphoma. N Engl J Med 369 (18): 1681-90, 2013. [PUBMED Abstract]
- Chiappella A, Martelli M, Angelucci E, et al.: Rituximab-dose-dense chemotherapy with or without high-dose chemotherapy plus autologous stem-cell transplantation in high-risk diffuse large B-cell lymphoma (DLCL04): final results of a multicentre, open-label, randomised, controlled, phase 3 study. Lancet Oncol 18 (8): 1076-1088, 2017. [PUBMED Abstract]
- Shipp MA, Abeloff MD, Antman KH, et al.: International Consensus Conference on high-dose therapy with hematopoietic stem-cell transplantation in aggressive non-Hodgkin's lymphomas: report of the jury. Ann Oncol 10 (1): 13-9, 1999. [PUBMED Abstract]
- Held G, Murawski N, Ziepert M, et al.: Role of radiotherapy to bulky disease in elderly patients with aggressive B-cell lymphoma. J Clin Oncol 32 (11): 1112-8, 2014. [PUBMED Abstract]
- Kahl BS: Bulky aggressive B-cell lymphoma: to radiate or not to radiate--that is the question. J Clin Oncol 32 (11): 1097-8, 2014. [PUBMED Abstract]
- Phan J, Mazloom A, Medeiros LJ, et al.: Benefit of consolidative radiation therapy in patients with diffuse large B-cell lymphoma treated with R-CHOP chemotherapy. J Clin Oncol 28 (27): 4170-6, 2010. [PUBMED Abstract]
Tratamiento del linfoma no Hodgkin de crecimiento rápido recidivante
Opciones de tratamiento para el linfoma no Hodgkin de crecimiento rápido recidivante
En una revisión retrospectiva de múltiples ensayos internacionales, se identificaron 636 con linfoma de células B grandes difuso (LDCBG) resistente al tratamiento que se define como la progresión o estabilización de la enfermedad, durante o justo en el momento de la finalización de un ciclo de quimioterapia completo o la recaída durante el primer año posterior a un trasplante de células madre (TCM) autógeno.[1] Cuando se usó terapia subsiguiente se observó una tasa de respuesta objetiva de 26 %, una tasa de respuesta completa (RC) de 7 %, una mediana de supervivencia general (SG) de 6,3 meses y solo un 20 % de los pacientes estaban vivos al cabo de 2 años. Incluso con quimioterapia de reinducción con un TCM autógeno planificado, los resultados siguen siendo precarios.[2]
Las opciones de tratamiento para el linfoma no Hodgkin de crecimiento rápido recidivante son las siguientes:
- Terapia de células T con CAR para la enfermedad primaria resistente al tratamiento o que presenta recaída en el primer año.
- Consolidación con trasplante de médula ósea o de células madre.
- Terapia de células T con CAR para la recaída tras un trasplante de células madre autógeno.
- Tafasitamab con lenalidomida.
- Rituximab con lenalidomida.
- Polatuzumab vedotina con rituximab y bendamustina.
- Loncastuximab tesirina.
- Activadores biespecíficos de células T.
- Radioterapia paliativa.
Terapia de células T con CAR para la enfermedad primaria resistente al tratamiento o que presenta recaída en el primer año
Los pacientes con LDCB que presentan recaída durante el tratamiento o dentro de los 2 meses siguientes a recibir la quimioterapia R-CHOP (rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona) tienen enfermedad resistente al tratamiento primaria. Cualquier paciente con recaída de la enfermedad en el plazo de 1 año después de la quimioterapia R-CHOP o con enfermedad primaria resistente al tratamiento tiene un pronóstico precario incluso con la reinducción mediante quimioinmunoterapia seguida de un TCM autógeno.[1,2] Los pacientes que recibieron terapia de células T con CAR tuvieron una tasa de supervivencia sin progresión (SSP) a 3 años del 40 % al 50 % al cabo de un seguimiento de 40 meses, un resultado equivalente de manera retrospectiva al TCM autógeno en los registros de médula ósea.[3-6]
En 3 ensayos aleatorizados se comparó la quimioinmunoterapia seguida de TCM autógeno con la terapia de células T con CAR con quimioinmunoterapia puente o sin esta para pacientes con enfermedad recidivante de riesgo alto definida como enfermedad primaria resistente al tratamiento o en recaída dentro de los 12 meses del tratamiento inicial con R-CHOP.
Evidencia (terapia de células T con CAR):
- En un ensayo prospectivo aleatorizado se incluyeron 359 pacientes con enfermedad primaria resistente al tratamiento o en recaída en los 12 meses siguientes a la quimioterapia inicial R-CHOP. Los pacientes recibieron la terapia de células T con CAR axicabtagén ciloleucel con solo corticoesteroides como terapia puente o quimioinmunoterapia de segunda línea (por lo general R-ICE [rituximab, ifosfamida, etopósido y carboplatino] o R-DHAP [rituximab, dexametasona, altas dosis de citarabina y cisplatino]) seguida de un TCM autógeno.[7]
- Al cabo de una mediana de seguimiento de 24,9 meses, la tasa de supervivencia sin complicaciones (SSC) a los 2 años fue del 40,5 % en los pacientes que recibieron axicabtagén ciloleucel y del 16,3 % en los pacientes que recibieron quimioinmunoterapia seguida de TCM autógeno (cociente de riesgos instantáneos [CRI], 0,398; intervalo de confianza [IC] 95 %, 0,308−0,514; P < 0,0001).[7][Nivel de evidencia B1]
- La SG no fue significativamente mejor a los 2 años, con un CRI de 0,73 (IC 95%, 0,53−1,01; P = 0,027).
- En el grupo de quimioinmunoterapia del estudio, el 64 % de los pacientes nunca recibió un TCM autógeno debido a una respuesta inadecuada, progresión o muerte.
- Se obtuvieron diferencias importantes desde el punto de vista clínico y estadísticamente significativas en la calidad de vida en el grupo de células T con CAR en los días 100 y 150, en comparación con el tratamiento estándar.[8][Nivel de evidencia A2]
- El síndrome de liberación de citoquinas de grado 3 o 4 se produjo en el 6 % de los pacientes y el 21 % de los pacientes presentó neurotoxicidad de grado 3 o 4.
- En un ensayo prospectivo aleatorizado se incluyó a 184 pacientes con enfermedad primaria resistente al tratamiento o en recaída en los 12 meses siguientes a la quimioterapia R-CHOP inicial. Los pacientes recibieron terapia de células T con CAR lisocabtagén maraleucel, y el 63 % de los pacientes recibieron terapia puente o quimioinmunoterapia de segunda línea seguida de TCM autógeno.[9]
- Al cabo de una mediana de seguimiento de 6,2 meses, la mediana de SSP fue de 14,8 meses para los pacientes que recibieron lisocabtagén maraleucel y de 5,7 meses para los pacientes que recibieron quimioinmunoterapia seguida de TCM autógeno (CRI, 0,41; P = 0,001).[9][Nivel de evidencia B1]
- En el grupo de quimioinmunoterapia del estudio, el 53 % de los pacientes nunca recibió TCM autógeno debido a respuesta inadecuada, progresión o muerte.[9]
- El síndrome de liberación de citoquinas de grado 3 se produjo en el 1 % de los pacientes, y la neurotoxicidad de grado 3 se produjo en el 4 % de los pacientes. No se produjeron casos de grado 4 ni 5.
- Un ensayo prospectivo aleatorizado incluyó a 322 pacientes con enfermedad primaria resistente al tratamiento o en recaída en los 12 meses siguientes a la quimioterapia R-CHOP inicial. Los pacientes recibieron terapia de células T con CAR tisagenlecleucel, y la mayoría de los pacientes recibieron terapia puente para lograr una respuesta, o quimioinmunoterapia de segunda línea seguida de TCM autógeno.[10]
- No hubo diferencias en la SSC para los pacientes de cualquiera de los 2 grupos (CRI, 1,07; IC 95 %, 0,82–1,40; P = 0,69).[10][Nivel de evidencia B1]
- En el grupo de la terapia de células T con CAR, el 48 % de los pacientes recibió 2 o más ciclos de quimioinmunoterapia como parte de la terapia puente. Es posible que este abordaje de la terapia puente haya producido un número inaceptable de casos de enfermedad progresiva.
En resumen:
- Para los pacientes con LDCBG recidivante de riesgo alto con enfermedad primaria resistente al tratamiento o en recaída en los 12 meses siguientes a la quimioterapia R-CHOP, axicabtagén ciloleucel y lisocabtagén maraleucel son regímenes de inducción superiores en comparación con la quimioinmunoterapia con regímenes como R-ICE, R-DHAP y R-GDP (rituximab, gemcitabina, dexametasona y cisplatino).
- El intervalo hasta que los pacientes reciban las células T CAR debe reducirse al mínimo, idealmente utilizando solo corticoesteroides, eliminando la quimioinmunoterapia puente y administrando la infusión del producto de células T CAR lo más rápido posible.
- La preferencia por la terapia de células T con CAR sobre la quimioinmunoterapia seguida de TCM autógeno no es aplicable a los pacientes que recaen más de 12 meses después de la terapia R-CHOP.
- La American Society of Clinical Oncology (ASCO) ha elaborado unas directrices para el abordaje de los eventos adversos en pacientes tratados con terapia con células T CAR.[11]
Consolidación con trasplante de médula ósea o de células madre
La consolidación con el trasplante de médula ósea (TMO) es un tratamiento para los pacientes de linfoma que recaen.[12] En estudios preliminares se indica que entre el 20 % y el 40 % de los pacientes permanecerán libres de enfermedad a largo plazo, pero el porcentaje preciso depende de la selección de los pacientes y del tratamiento específico que se use. Los regímenes farmacológicos de preparación varían; algunos investigadores también usan la irradiación corporal total. Se logró un éxito similar con médula autógena, con purga de la médula o sin ella, y con uso de médula alogénica.[13-17]
Evidencia (trasplante de médula ósea):
- En un ensayo prospectivo aleatorizado (EORTC-PARMA) con 215 pacientes menores de 60 años en la primera o segunda recaída de un linfoma de crecimiento rápido y sin compromiso de la médula ósea o del sistema nervioso central, los pacientes recibieron 2 ciclos de quimioterapia combinada intensiva. Respondieron 109 pacientes que se asignaron al azar a recibir 4 ciclos adicionales de quimioterapia y radioterapia dirigida al campo comprometido (RTCC) o recibir un TMO autógeno seguido de RTCC. Al cabo de una mediana de seguimiento de 5 años, la tasa SSC mejoró de manera significativa con el trasplante (46 vs. 12 %). La tasa de SG también mejoró de manera significativa con el trasplante (53 vs. 32 %).[18][Nivel de evidencia A1] El rescate con TMO fue ineficaz en los pacientes con recaída de la enfermedad del grupo no asignado a trasplante.
En general, los pacientes que respondieron al tratamiento inicial y al tratamiento convencional para la recaída antes del TMO obtuvieron los mejores resultados.[19]
- En un ensayo prospectivo, los pacientes con recaída tardía (>12 meses después del diagnóstico) tuvieron una SG superior a los pacientes que recayeron más temprano (la tasa de supervivencia a 8 años fue de 29 vs. 13 %, P = 0,001).[20][Nivel de evidencia C1]
El TCM periféricas produce resultados equivalentes al trasplante de células madre autógeno estándar.[21,22] Incluso aquellos pacientes que nunca tuvieron una remisión completa con la quimioterapia convencional a veces logran una prolongada SSP (31 % a los 5 años) después del tratamiento con dosis altas de quimioterapia y TCM hematopoyéticas, si conservan la quimiosensibilidad al tratamiento de reinducción.[23][Nivel de evidencia C2] Algunos pacientes que recaen después de un TCM autógeno previo tienen remisiones duraderas después de un TMO autógeno, mielosupresor o no mielosupresor.[24,25]; [26][Nivel de evidencia C3] El acondicionamiento de intensidad reducida para el TCM alógeno por lo general incluye fludarabina con busulfano o fludarabina con ciclofosfamida, con 2 Gy de irradiación corporal total.[27]
Evidencia (trasplante de células madre periféricas):
- En un ensayo prospectivo aleatorizado, 396 pacientes con LDCBG en primera recaída o resistentes al tratamiento de primera línea recibieron R-ICE o R-DHAP seguidos de TCM autógeno.[28]
- No hubo diferencia en la SSC o la SG a 3 años.[28][Nivel de evidencia A1]
- En un ensayo prospectivo aleatorizado, 619 pacientes de linfoma de crecimiento rápido en recaída o resistente al tratamiento recibieron R-DHAP o R-GDP, seguidos de TCM autógeno.[29]
- Al cabo de una mediana de seguimiento de 53 meses, no hubo diferencias en la SSC o la SG, pero los pacientes que recibieron R-GDP notificaron menos efectos tóxicos.[29][Nivel de evidencia A3]
Terapia de células T con CAR para la recaída tras un trasplante de células madre autógeno
En el caso de recaída de la enfermedad después de un TCM autógeno, muchos pacientes reciben consolidación con terapia de células T con CAR.
En múltiples ensayos se describen a pacientes con linfoma de células B resistente al tratamiento sometidos a infusión de células T modificadas para que expresen un CAR dirigido al antígeno CD19 que se expresa en las células B malignas mediante el uso de tres compuestos: axicabtagén ciloleucel, tisagenlecleucel y lisocabtagén maraleucel.[30-34] En cada estudio se notificó una tasa de RC del 50 % al 60 % y una tasa de SG a 2 años del 40 % al 50 %, pero la duración de la respuesta a largo plazo aún no se ha determinado en estos pacientes muy específicos.[30-32][Nivel de evidencia C3] Esta terapia es una opción para los pacientes con enfermedad resistente al tratamiento. Estos resultados se verificaron fuera del estudio en 2 informes que incluyeron 397 pacientes que recibieron tratamiento después de la aprobación de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA).[35,36][Nivel de evidencia C3] Es posible que los pacientes con riesgo más alto que responden bien reciban consolidación con un TCM alogénico subsecuente, en algunos casos si son aptos.
ASCO ha elaborado directrices para el abordaje de los eventos adversos en pacientes que reciben terapia con células T con CAR.[11]
Tafasitamab con lenalidomida
Evidencia (tafasitamab con lenalidomida):
- En un estudio de fase II, se trataron 80 pacientes de LDCBG en recaída o resistente al tratamiento con tafasitamab, un anticuerpo monoclonal humanizado dirigido a CD19 combinado con lenalidomida.[37]
- La tasa de RC fue del 43 % y la tasa de respuesta objetiva fue del 60 %.
La FDA aprobó la combinación de tafasitamab con lenalidomida para los pacientes con LDCBG en recaída o resistente al tratamiento.[37][Nivel de evidencia C3] No está claro si el uso de esta terapia dirigida a CD19 interferiría con la consolidación mediante células T con CAR CD19.
Rituximab con lenalidomida
Evidencia (rituximab con lenalidomida):
- En 2 ensayos de fase II, 49 pacientes demostraron una tasa de respuesta objetiva para la lenalidomida con rituximab del 19 % al 35 %.[38,39][Nivel de evidencia C3]
Polatuzumab vedotina con rituximab y bendamustina
Polatuzumab vedotina es un anticuerpo monoclonal dirigido a CD79b conjugado con el citotóxico vedotina (un conjugado anticuerpo-fármaco).
Evidencia (polatuzumab vedotina con rituximab y bendamustina):
- En un ensayo aleatorizado y prospectivo, se trataron 80 pacientes de LDCBG en recaída o resistente al tratamiento con polatuzumab vedotina, combinado con bendamustina y rituximab (BR) o BR solo; el criterio principal de valoración fue la respuesta completa.[40]
- La tasa de RC determinada mediante tomografía por emisión de positrones y tomografía computarizada fue del 40 % para la combinación de polatuzumab vedotina y BR, en comparación con una tasa del 18 % para BR solo (P = 0,026).[40]
- De manera similar, la mediana de la SSP fue más alta para los pacientes que recibieron la combinación de polatuzumab vedotina (9,5 meses) que para los pacientes que recibieron BR solo (3,7 meses) (CRI, 0,36; IC 95 %, 0,21−0,63; P < 0,001); la SG fue de 12,4 meses para los pacientes que recibieron la combinación de polatuzumab vedotina versus 4,7 meses para los pacientes que recibieron BR solo (CRI, 0,42; IC 95 %, 0,24−0,75; P = 0,002).[40][Nivel de evidencia C1]
La FDA aprobó la combinación de polatuzumab vedotina y BR para pacientes de LDCBG en recaída o resistente al tratamiento.
Loncastuximab tesirina
Loncastuximab tesirina es un anticuerpo dirigido a CD19 conjugado con una citotoxina del dímero pirrolobenzodiazepina (un conjugado anticuerpo-fármaco).[41]
Evidencia (loncastuximab tesirina):
- En un ensayo de fase I y subsiguiente de fase II se incluyó a 184 pacientes con enfermedad en recaída o resistente al tratamiento.
- La tasa de respuesta objetiva fue del 48,3 % (IC 95 %, 39,9–56,7%) y la tasa de RC fue del 24 %.[42,43][Nivel de evidencia C3]
Activadores biespecíficos de células T
Los activadores biespecíficos de células T se unen a CD20 (o CD19) y a CD3 para dirigir a las células T a eliminar los linfocitos B malignos.[44] De forma similar a la terapia con células T con CAR, casi la mitad de los pacientes que reciben esta terapia presentan síndrome de liberación de citoquinas.
Radioterapia paliativa
En general, los pacientes con linfoma de crecimiento rápido que recaen con un tipo histológico de crecimiento lento se benefician de la terapia paliativa.[45] Es posible obtener paliación con dosis muy bajas (4 Gy) de RTCC en los pacientes con recaída de crecimiento rápido y lento.[46]
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Crump M, Neelapu SS, Farooq U, et al.: Outcomes in refractory diffuse large B-cell lymphoma: results from the international SCHOLAR-1 study. Blood 130 (16): 1800-1808, 2017. [PUBMED Abstract]
- Ayers EC, Li S, Medeiros LJ, et al.: Outcomes in patients with aggressive B-cell non-Hodgkin lymphoma after intensive frontline treatment failure. Cancer 126 (2): 293-303, 2020. [PUBMED Abstract]
- Schuster SJ, Tam CS, Borchmann P, et al.: Long-term clinical outcomes of tisagenlecleucel in patients with relapsed or refractory aggressive B-cell lymphomas (JULIET): a multicentre, open-label, single-arm, phase 2 study. Lancet Oncol 22 (10): 1403-1415, 2021. [PUBMED Abstract]
- Shah NN, Ahn KW, Litovich C, et al.: Is autologous transplant in relapsed DLBCL patients achieving only a PET+ PR appropriate in the CAR T-cell era? Blood 137 (10): 1416-1423, 2021. [PUBMED Abstract]
- Shadman M, Pasquini M, Ahn KW, et al.: Autologous transplant vs chimeric antigen receptor T-cell therapy for relapsed DLBCL in partial remission. Blood 139 (9): 1330-1339, 2022. [PUBMED Abstract]
- Cappell KM, Sherry RM, Yang JC, et al.: Long-Term Follow-Up of Anti-CD19 Chimeric Antigen Receptor T-Cell Therapy. J Clin Oncol 38 (32): 3805-3815, 2020. [PUBMED Abstract]
- Locke FL, Miklos DB, Jacobson CA, et al.: Axicabtagene Ciloleucel as Second-Line Therapy for Large B-Cell Lymphoma. N Engl J Med 386 (7): 640-654, 2022. [PUBMED Abstract]
- Elsawy M, Chavez JC, Avivi I, et al.: Patient-reported outcomes in ZUMA-7, a phase 3 study of axicabtagene ciloleucel in second-line large B-cell lymphoma. Blood 140 (21): 2248-2260, 2022. [PUBMED Abstract]
- Kamdar M, Solomon SR, Arnason J, et al.: Lisocabtagene maraleucel versus standard of care with salvage chemotherapy followed by autologous stem cell transplantation as second-line treatment in patients with relapsed or refractory large B-cell lymphoma (TRANSFORM): results from an interim analysis of an open-label, randomised, phase 3 trial. Lancet 399 (10343): 2294-2308, 2022. [PUBMED Abstract]
- Bishop MR, Dickinson M, Purtill D, et al.: Second-Line Tisagenlecleucel or Standard Care in Aggressive B-Cell Lymphoma. N Engl J Med 386 (7): 629-639, 2022. [PUBMED Abstract]
- Santomasso BD, Nastoupil LJ, Adkins S, et al.: Management of Immune-Related Adverse Events in Patients Treated With Chimeric Antigen Receptor T-Cell Therapy: ASCO Guideline. J Clin Oncol 39 (35): 3978-3992, 2021. [PUBMED Abstract]
- Shipp MA, Abeloff MD, Antman KH, et al.: International Consensus Conference on high-dose therapy with hematopoietic stem-cell transplantation in aggressive non-Hodgkin's lymphomas: report of the jury. Ann Oncol 10 (1): 13-9, 1999. [PUBMED Abstract]
- Freedman AS, Takvorian T, Anderson KC, et al.: Autologous bone marrow transplantation in B-cell non-Hodgkin's lymphoma: very low treatment-related mortality in 100 patients in sensitive relapse. J Clin Oncol 8 (5): 784-91, 1990. [PUBMED Abstract]
- Phillips GL, Fay JW, Herzig RH, et al.: The treatment of progressive non-Hodgkin's lymphoma with intensive chemoradiotherapy and autologous marrow transplantation. Blood 75 (4): 831-8, 1990. [PUBMED Abstract]
- Chopra R, Goldstone AH, Pearce R, et al.: Autologous versus allogeneic bone marrow transplantation for non-Hodgkin's lymphoma: a case-controlled analysis of the European Bone Marrow Transplant Group Registry data. J Clin Oncol 10 (11): 1690-5, 1992. [PUBMED Abstract]
- Ratanatharathorn V, Uberti J, Karanes C, et al.: Prospective comparative trial of autologous versus allogeneic bone marrow transplantation in patients with non-Hodgkin's lymphoma. Blood 84 (4): 1050-5, 1994. [PUBMED Abstract]
- Mills W, Chopra R, McMillan A, et al.: BEAM chemotherapy and autologous bone marrow transplantation for patients with relapsed or refractory non-Hodgkin's lymphoma. J Clin Oncol 13 (3): 588-95, 1995. [PUBMED Abstract]
- Philip T, Guglielmi C, Hagenbeek A, et al.: Autologous bone marrow transplantation as compared with salvage chemotherapy in relapses of chemotherapy-sensitive non-Hodgkin's lymphoma. N Engl J Med 333 (23): 1540-5, 1995. [PUBMED Abstract]
- Vellenga E, van Putten WL, van 't Veer MB, et al.: Rituximab improves the treatment results of DHAP-VIM-DHAP and ASCT in relapsed/progressive aggressive CD20+ NHL: a prospective randomized HOVON trial. Blood 111 (2): 537-43, 2008. [PUBMED Abstract]
- Guglielmi C, Gomez F, Philip T, et al.: Time to relapse has prognostic value in patients with aggressive lymphoma enrolled onto the Parma trial. J Clin Oncol 16 (10): 3264-9, 1998. [PUBMED Abstract]
- Vose JM, Anderson JR, Kessinger A, et al.: High-dose chemotherapy and autologous hematopoietic stem-cell transplantation for aggressive non-Hodgkin's lymphoma. J Clin Oncol 11 (10): 1846-51, 1993. [PUBMED Abstract]
- Liberti G, Pearce R, Taghipour G, et al.: Comparison of peripheral blood stem-cell and autologous bone marrow transplantation for lymphoma patients: a case-controlled analysis of the EBMT Registry data. Lymphoma Working Party of the EBMT. Ann Oncol 5 (Suppl 2): 151-3, 1994. [PUBMED Abstract]
- Vose JM, Zhang MJ, Rowlings PA, et al.: Autologous transplantation for diffuse aggressive non-Hodgkin's lymphoma in patients never achieving remission: a report from the Autologous Blood and Marrow Transplant Registry. J Clin Oncol 19 (2): 406-13, 2001. [PUBMED Abstract]
- van Kampen RJ, Canals C, Schouten HC, et al.: Allogeneic stem-cell transplantation as salvage therapy for patients with diffuse large B-cell non-Hodgkin's lymphoma relapsing after an autologous stem-cell transplantation: an analysis of the European Group for Blood and Marrow Transplantation Registry. J Clin Oncol 29 (10): 1342-8, 2011. [PUBMED Abstract]
- Freytes CO, Loberiza FR, Rizzo JD, et al.: Myeloablative allogeneic hematopoietic stem cell transplantation in patients who experience relapse after autologous stem cell transplantation for lymphoma: a report of the International Bone Marrow Transplant Registry. Blood 104 (12): 3797-803, 2004. [PUBMED Abstract]
- Rezvani AR, Norasetthada L, Gooley T, et al.: Non-myeloablative allogeneic haematopoietic cell transplantation for relapsed diffuse large B-cell lymphoma: a multicentre experience. Br J Haematol 143 (3): 395-403, 2008. [PUBMED Abstract]
- Ghosh N, Ahmed S, Ahn KW, et al.: Association of Reduced-Intensity Conditioning Regimens With Overall Survival Among Patients With Non-Hodgkin Lymphoma Undergoing Allogeneic Transplant. JAMA Oncol 6 (7): 1011-1018, 2020. [PUBMED Abstract]
- Gisselbrecht C, Glass B, Mounier N, et al.: Salvage regimens with autologous transplantation for relapsed large B-cell lymphoma in the rituximab era. J Clin Oncol 28 (27): 4184-90, 2010. [PUBMED Abstract]
- Crump M, Kuruvilla J, Couban S, et al.: Randomized comparison of gemcitabine, dexamethasone, and cisplatin versus dexamethasone, cytarabine, and cisplatin chemotherapy before autologous stem-cell transplantation for relapsed and refractory aggressive lymphomas: NCIC-CTG LY.12. J Clin Oncol 32 (31): 3490-6, 2014. [PUBMED Abstract]
- Neelapu SS, Locke FL, Bartlett NL, et al.: Axicabtagene Ciloleucel CAR T-Cell Therapy in Refractory Large B-Cell Lymphoma. N Engl J Med 377 (26): 2531-2544, 2017. [PUBMED Abstract]
- Schuster SJ, Bishop MR, Tam CS, et al.: Tisagenlecleucel in Adult Relapsed or Refractory Diffuse Large B-Cell Lymphoma. N Engl J Med 380 (1): 45-56, 2019. [PUBMED Abstract]
- Locke FL, Ghobadi A, Jacobson CA, et al.: Long-term safety and activity of axicabtagene ciloleucel in refractory large B-cell lymphoma (ZUMA-1): a single-arm, multicentre, phase 1-2 trial. Lancet Oncol 20 (1): 31-42, 2019. [PUBMED Abstract]
- Abramson JS, Palomba ML, Gordon LI, et al.: Lisocabtagene maraleucel for patients with relapsed or refractory large B-cell lymphomas (TRANSCEND NHL 001): a multicentre seamless design study. Lancet 396 (10254): 839-852, 2020. [PUBMED Abstract]
- Lin JK, Muffly LS, Spinner MA, et al.: Cost Effectiveness of Chimeric Antigen Receptor T-Cell Therapy in Multiply Relapsed or Refractory Adult Large B-Cell Lymphoma. J Clin Oncol 37 (24): 2105-2119, 2019. [PUBMED Abstract]
- Jacobson CA, Hunter BD, Redd R, et al.: Axicabtagene Ciloleucel in the Non-Trial Setting: Outcomes and Correlates of Response, Resistance, and Toxicity. J Clin Oncol 38 (27): 3095-3106, 2020. [PUBMED Abstract]
- Nastoupil LJ, Jain MD, Feng L, et al.: Standard-of-Care Axicabtagene Ciloleucel for Relapsed or Refractory Large B-Cell Lymphoma: Results From the US Lymphoma CAR T Consortium. J Clin Oncol 38 (27): 3119-3128, 2020. [PUBMED Abstract]
- Salles G, Duell J, González Barca E, et al.: Tafasitamab plus lenalidomide in relapsed or refractory diffuse large B-cell lymphoma (L-MIND): a multicentre, prospective, single-arm, phase 2 study. Lancet Oncol 21 (7): 978-988, 2020. [PUBMED Abstract]
- Zinzani PL, Pellegrini C, Gandolfi L, et al.: Combination of lenalidomide and rituximab in elderly patients with relapsed or refractory diffuse large B-cell lymphoma: a phase 2 trial. Clin Lymphoma Myeloma Leuk 11 (6): 462-6, 2011. [PUBMED Abstract]
- Wiernik PH, Lossos IS, Tuscano JM, et al.: Lenalidomide monotherapy in relapsed or refractory aggressive non-Hodgkin's lymphoma. J Clin Oncol 26 (30): 4952-7, 2008. [PUBMED Abstract]
- Sehn LH, Herrera AF, Flowers CR, et al.: Polatuzumab Vedotin in Relapsed or Refractory Diffuse Large B-Cell Lymphoma. J Clin Oncol 38 (2): 155-165, 2020. [PUBMED Abstract]
- Calabretta E, Hamadani M, Zinzani PL, et al.: The antibody-drug conjugate loncastuximab tesirine for the treatment of diffuse large B-cell lymphoma. Blood 140 (4): 303-308, 2022. [PUBMED Abstract]
- Caimi PF, Ai W, Alderuccio JP, et al.: Loncastuximab tesirine in relapsed or refractory diffuse large B-cell lymphoma (LOTIS-2): a multicentre, open-label, single-arm, phase 2 trial. Lancet Oncol 22 (6): 790-800, 2021. [PUBMED Abstract]
- Hamadani M, Radford J, Carlo-Stella C, et al.: Final results of a phase 1 study of loncastuximab tesirine in relapsed/refractory B-cell non-Hodgkin lymphoma. Blood 137 (19): 2634-2645, 2021. [PUBMED Abstract]
- Dickinson MJ, Carlo-Stella C, Morschhauser F, et al.: Glofitamab for Relapsed or Refractory Diffuse Large B-Cell Lymphoma. N Engl J Med 387 (24): 2220-2231, 2022. [PUBMED Abstract]
- Lee AY, Connors JM, Klimo P, et al.: Late relapse in patients with diffuse large-cell lymphoma treated with MACOP-B. J Clin Oncol 15 (5): 1745-53, 1997. [PUBMED Abstract]
- Haas RL, Poortmans P, de Jong D, et al.: Effective palliation by low dose local radiotherapy for recurrent and/or chemotherapy refractory non-follicular lymphoma patients. Eur J Cancer 41 (12): 1724-30, 2005. [PUBMED Abstract]
Tratamiento del linfoma linfoblástico y la leucemia linfoblástica aguda
El linfoma linfoblástico (LBL) es una forma muy maligna del linfoma no Hodgkin (LNH), que a menudo se presenta en pacientes jóvenes, pero no es exclusiva de este grupo de edad. El LBL es la manifestación linfomatosa de la leucemia linfoblástica aguda (LLA). Los paradigmas de tratamiento se basan en ensayos clínicos para la LLA, porque el LBL y la LLA se consideran diferentes manifestaciones de la misma enfermedad biológica. El LBL a menudo produce masas mediastínicas grandes y tiene una predilección fuerte por diseminarse a la médula ósea y el sistema nervioso central (SNC). La quimioterapia combinada intensiva con profilaxis del SNC es el tratamiento estándar para este tipo histológico de crecimiento rápido de LNH. A veces, se administra radioterapia dirigida a las masas tumorales voluminosas. Debido a que estas formas de LNH tienden a progresar rápido, la quimioterapia combinada se administra de inmediato una vez que se confirma el diagnóstico. Para obtener más información, consultar Tratamiento de la leucemia linfoblástica aguda en adultos.
Los aspectos más importantes de los exámenes para la estadificación pretratamiento incluyen una revisión cuidadosa de las siguientes muestras para análisis patológicos:
- Aspirado de médula ósea.
- Pieza de biopsia.
- Muestra para citología del líquido cefalorraquídeo.
- Marcadores de linfocitos.
Opciones de tratamiento para el linfoma linfoblástico y la leucemia linfoblástica aguda
Las opciones de tratamiento para el linfoma linfoblástico son las siguientes:
Los grupos cooperativos nacionales están formulando abordajes nuevos de tratamiento. Otros abordajes incluyen el uso de trasplante de médula ósea para la consolidación.
Para obtener más información, consultar Tratamiento de la leucemia linfoblástica aguda en adultos.
Tratamiento intensivo
El tratamiento estándar es quimioterapia combinada intensiva con profilaxis del SNC.
Radioterapia
A veces, se administra radioterapia dirigida a las masas tumorales voluminosas.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Tratamiento del linfoma difuso de células pequeñas no hendidas o linfoma de Burkitt
El linfoma difuso de células pequeñas no hendidas o linfoma de Burkitt, en general, afecta a pacientes más jóvenes y constituyen el tipo más común de linfoma no Hodgkin (LNH) infantil.[1,2] El linfoma de células B de grado alto, sin especificar, incluye linfomas con características morfológicas tipo Burkitt o blastoide sin características citogenéticas de mutación doble, y con fenotipo de células B de centro germinal.[3] Hasta la mitad de los pacientes presentan un único reordenamiento de MYC. El tratamiento óptimo no está bien definido porque el diagnóstico es poco frecuente. Suelen elegirse regímenes para el linfoma de Burkitt con profilaxis del sistema nervioso central (SNC).[3]
Opciones de tratamiento para el linfoma difuso de células pequeñas no hendidas o linfoma de Burkitt
Las opciones de tratamiento para el linfoma difuso de células pequeñas no hendidas o linfoma de Burkitt son las siguientes:
Regímenes multifarmacológicos intensivos
El tratamiento del linfoma difuso de células pequeñas no hendidas o el linfoma de Burkitt habitualmente se realiza con regímenes multifarmacológicos intensivos similares a los usados para los linfomas de crecimiento rápido en estadio avanzado (como el difuso de células grandes).[4-6] Los factores de pronóstico adversos incluyen la edad mayor a 40 años, una enfermedad abdominal voluminosa y una elevación de las concentraciones séricas de lactato–deshidrogenasa (>3 veces de lo normal), estado funcional 2 o superior del Eastern Cooperative Oncology Group y afectación del SNC.[2] En una revisión retrospectiva de 641 pacientes adultos con linfoma de Burkitt procedentes de 30 centros oncológicos estadounidenses se reveló una tasa de supervivencia sin progresión (SSP) a 3 años del 64 %. El 19 % de los pacientes presentaba afectación del SNC, el 14 % tenía enfermedad primaria resistente al tratamiento y la tasa de mortalidad relacionada con el tratamiento era del 10 %.[2]
Evidencia (regímenes multifarmacológicos intensivos):
- La quimioterapia combinada intensiva estructurada de la misma forma que para el linfoma de Burkitt infantil resultó muy eficaz en pacientes adultos. Más del 60 % de los pacientes en estadio avanzado permanecieron libres enfermedad a los 5 años.[6-9]
- El rituximab se ha incorporado a esos regímenes de quimioterapia combinada intensiva. En un ensayo multicéntrico prospectivo no aleatorizado de un solo grupo con 363 pacientes de 16 a 85 años, se observó una tasa de SSP a 5 años del 71 % y una tasa de supervivencia general a 5 años del 80 %.[5][Nivel de evidencia C1]
Profilaxis del sistema nervioso central
Los pacientes de linfoma difuso de células pequeñas no hendidas o linfoma de Burkitt tienen un riesgo de por vida del 20 % al 30 % de compromiso del SNC. Se recomienda la profilaxis del SNC para todos los pacientes, por lo general se administran 4 a 6 inyecciones intratecales.[10] Para obtener más información, consultar Tratamiento de la leucemia linfoblástica aguda en adultos.
Evidencia (profilaxis del sistema nervioso central):
- En una serie de 41 pacientes tratados con quimioterapia sistémica e intratecal, el 44 % de aquellos que presentaron enfermedad en el SNC y el 13 % de aquellos que recayeron con compromiso del SNC sobrevivieron a largo plazo sin enfermedad.[11] Los modelos de recaída del SNC fueron similares independientemente de que los pacientes recibieran o no radioterapia, pero se notó un aumento de déficits neurológicos en aquellos que recibieron radioterapia.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Blum KA, Lozanski G, Byrd JC: Adult Burkitt leukemia and lymphoma. Blood 104 (10): 3009-20, 2004. [PUBMED Abstract]
- Evens AM, Danilov A, Jagadeesh D, et al.: Burkitt lymphoma in the modern era: real-world outcomes and prognostication across 30 US cancer centers. Blood 137 (3): 374-386, 2021. [PUBMED Abstract]
- Olszewski AJ, Kurt H, Evens AM: Defining and treating high-grade B-cell lymphoma, NOS. Blood 140 (9): 943-954, 2022. [PUBMED Abstract]
- Thomas DA, Faderl S, O'Brien S, et al.: Chemoimmunotherapy with hyper-CVAD plus rituximab for the treatment of adult Burkitt and Burkitt-type lymphoma or acute lymphoblastic leukemia. Cancer 106 (7): 1569-80, 2006. [PUBMED Abstract]
- Hoelzer D, Walewski J, Döhner H, et al.: Improved outcome of adult Burkitt lymphoma/leukemia with rituximab and chemotherapy: report of a large prospective multicenter trial. Blood 124 (26): 3870-9, 2014. [PUBMED Abstract]
- Roschewski M, Dunleavy K, Abramson JS, et al.: Multicenter Study of Risk-Adapted Therapy With Dose-Adjusted EPOCH-R in Adults With Untreated Burkitt Lymphoma. J Clin Oncol 38 (22): 2519-2529, 2020. [PUBMED Abstract]
- Magrath I, Adde M, Shad A, et al.: Adults and children with small non-cleaved-cell lymphoma have a similar excellent outcome when treated with the same chemotherapy regimen. J Clin Oncol 14 (3): 925-34, 1996. [PUBMED Abstract]
- Hoelzer D, Ludwig WD, Thiel E, et al.: Improved outcome in adult B-cell acute lymphoblastic leukemia. Blood 87 (2): 495-508, 1996. [PUBMED Abstract]
- Mead GM, Sydes MR, Walewski J, et al.: An international evaluation of CODOX-M and CODOX-M alternating with IVAC in adult Burkitt's lymphoma: results of United Kingdom Lymphoma Group LY06 study. Ann Oncol 13 (8): 1264-74, 2002. [PUBMED Abstract]
- Rizzieri DA, Johnson JL, Niedzwiecki D, et al.: Intensive chemotherapy with and without cranial radiation for Burkitt leukemia and lymphoma: final results of Cancer and Leukemia Group B Study 9251. Cancer 100 (7): 1438-48, 2004. [PUBMED Abstract]
- Magrath IT, Haddy TB, Adde MA: Treatment of patients with high grade non-Hodgkin's lymphomas and central nervous system involvement: is radiation an essential component of therapy? Leuk Lymphoma 21 (1-2): 99-105, 1996. [PUBMED Abstract]
Tratamiento del linfoma no Hodgkin durante el embarazo
Información general sobre el linfoma no Hodgkin durante el embarazo
Los linfomas no Hodgkin (LNH) se presentan con más frecuencia que el linfoma de Hodgkin en poblaciones de edad más avanzada. Esta diferencia de edad quizás explique la escasez de casos notificados de LNH en pacientes embarazadas.[1]
Información sobre los estadios del linfoma no Hodgkin durante el embarazo
Con el fin de evitar la exposición a la radiación ionizante, las imágenes por resonancia magnética son el método preferido durante la evaluación para la estadificación.[2] Para obtener más información, consultar la sección Información sobre los estadios del linfoma no Hodgkin.
Aspectos generales de las opciones de tratamiento del linfoma no Hodgkin durante el embarazo
| Estadio | Opciones de tratamiento |
|---|---|
| Linfoma no Hodgkin de crecimiento lento durante el embarazo | Diferir el tratamiento hasta después del parto |
| Linfoma no Hodgkin de crecimiento rápido durante el embarazo | Tratamiento inmediato |
| Adelanto del parto, cuando sea posible | |
| Interrupción del embarazo |
Linfoma no Hodgkin de crecimiento lento durante el embarazo
El tratamiento se puede diferir en las mujeres con linfoma no Hodgkin (LNH) de crecimiento lento.
Linfoma no Hodgkin de crecimiento rápido durante el embarazo
Tratamiento inmediato
De acuerdo con informes anecdóticos de series de casos, la mayoría de los linfomas no Hodgkin (LNH) en embarazadas son de crecimiento rápido, y se obtienen desenlaces desfavorables cuando se difiere la terapia hasta después del parto.[1,3-5] Por lo tanto, algunos investigadores están a favor de administrar tratamiento inmediato, incluso durante el embarazo.[5] En una revisión de informes de casos de 121 pacientes de 74 publicaciones, la mitad de las pacientes tenían linfomas de crecimiento rápido, como linfoma de Burkitt, y la otra mitad tenía compromiso de mama, ovario, útero o placenta.[6] La mitad de las pacientes recibió tratamiento durante el embarazo, la tasa de supervivencia a 6 meses fue del 53 % y la tasa de nacidos vivos fue del 83 %.[6][Nivel de evidencia C3]
En un análisis retrospectivo multicéntrico con 50 pacientes, se describió la interrupción del embarazo en 3 pacientes, aplazamiento de la terapia hasta el posparto en 15 pacientes (mediana de 30 semanas de gestación) y tratamiento durante el embarazo en las 32 pacientes restantes (mediana de 21 semanas de gestación, todo el tratamiento se hizo después del primer trimestre).[7] Después de una mediana de seguimiento de 41 meses, la tasa de supervivencia sin progresión a 3 años fue del 53 % y la tasa de supervivencia general fue del 82 % cuando se usó rituximab, ciclofosfamida, clorhidrato de doxorrubicina, sulfato de vincristina y prednisona (R-CHOP) o modificaciones de este régimen.[7][Nivel de evidencia C3]
Adelanto del parto, cuando sea posible
Para algunas mujeres, adelantar el parto cuando es posible, reduce al mínimo o evita la exposición de su hijo a la quimioterapia y la radioterapia.
Interrupción del embarazo
La interrupción del embarazo durante el primer trimestre es una opción que permite el tratamiento inmediato de las mujeres con un LNH de crecimiento rápido.
Evidencia (efecto del tratamiento en los niños expuestos en el útero):
- Después de un seguimiento que osciló entre varios meses y 11 años, se encontró que los niños expuestos en el útero a dosis altas de quimioterapia combinada de doxorrubicina (en especial, durante el segundo y tercer trimestre) crecen de forma normal y no presentan indicios de malformaciones congénitas..[5,8-10] La mayoría de los fármacos quimioterapéuticos que se usan para el tratamiento del LNH no cuentan con datos sobre los efectos a largo plazo en los niños expuestos en el útero.
- En un informe anecdótico, un recién nacido expuesto en el útero a un régimen con rituximab nació sin linfocitos B circulantes. Por lo demás, el recién nacido estaba sano y recuperó los linfocitos B circulantes a los 6 meses, sin infecciones intercurrentes inusuales o persistentes.[11]
Bibliografía
- Ward FT, Weiss RB: Lymphoma and pregnancy. Semin Oncol 16 (5): 397-409, 1989. [PUBMED Abstract]
- Nicklas AH, Baker ME: Imaging strategies in the pregnant cancer patient. Semin Oncol 27 (6): 623-32, 2000. [PUBMED Abstract]
- Steiner-Salz D, Yahalom J, Samuelov A, et al.: Non-Hodgkin's lymphoma associated with pregnancy. A report of six cases, with a review of the literature. Cancer 56 (8): 2087-91, 1985. [PUBMED Abstract]
- Spitzer M, Citron M, Ilardi CF, et al.: Non-Hodgkin's lymphoma during pregnancy. Gynecol Oncol 43 (3): 309-12, 1991. [PUBMED Abstract]
- Gelb AB, van de Rijn M, Warnke RA, et al.: Pregnancy-associated lymphomas. A clinicopathologic study. Cancer 78 (2): 304-10, 1996. [PUBMED Abstract]
- Horowitz NA, Benyamini N, Wohlfart K, et al.: Reproductive organ involvement in non-Hodgkin lymphoma during pregnancy: a systematic review. Lancet Oncol 14 (7): e275-82, 2013. [PUBMED Abstract]
- Evens AM, Advani R, Press OW, et al.: Lymphoma occurring during pregnancy: antenatal therapy, complications, and maternal survival in a multicenter analysis. J Clin Oncol 31 (32): 4132-9, 2013. [PUBMED Abstract]
- Avilés A, Díaz-Maqueo JC, Torras V, et al.: Non-Hodgkin's lymphomas and pregnancy: presentation of 16 cases. Gynecol Oncol 37 (3): 335-7, 1990. [PUBMED Abstract]
- Moore DT, Taslimi MM: Multi-agent chemotherapy in a case of non-Hodgkin's lymphoma in second trimester of pregnancy. J Tenn Med Assoc 84 (9): 435-6, 1991. [PUBMED Abstract]
- Nantel S, Parboosingh J, Poon MC: Treatment of an aggressive non-Hodgkin's lymphoma during pregnancy with MACOP-B chemotherapy. Med Pediatr Oncol 18 (2): 143-5, 1990. [PUBMED Abstract]
- Mandal PK, Dolai TK, Bagchi B, et al.: B cell suppression in newborn following treatment of pregnant diffuse large B-cell lymphoma patient with rituximab containing regimen. Indian J Pediatr 81 (10): 1092-4, 2014. [PUBMED Abstract]
Actualizaciones más recientes a este resumen (06/30/2023)
Los resúmenes del PDQ con información sobre el cáncer se revisan con regularidad y se actualizan a medida que se obtiene nueva información. Esta sección describe los cambios más recientes incorporados en este resumen a partir de la fecha arriba indicada.
Linfoma no Hodgkin de crecimiento lento
Se añadió texto para indicar que las células T con receptor de antígeno quimérico (CAR) dirigido a CD19 pueden utilizarse en pacientes con progresión de la enfermedad tras dos o más líneas de tratamiento previas (se citó a Jacobson et al. como referencia 30). También se añadió texto para indicar que también es posible usar mosunetuzumab en este entorno (se citó a Bartlett et al. como referencia 31).
Se añadió a Gertz como referencia 48. También se revisó el texto para indicar que, por lo general, la quimioterapia o las terapias dirigidas de tipo biológico se inician de manera directa para los pacientes sintomáticos con viscosidad sérica de 4 o menos. Es posible que se necesite tratamiento para corregir una anemia hemolítica en los pacientes con enfermedad por crioaglutininas crónica; a menudo se usan rituximab, bendamustina y corticoesteroides. Es posible que sutimlimab reduzca la hemólisis cuando las terapias dirigidas al linfoma linfoplasmocítico resultan ineficaces (se citó a Röth et al. como referencia 49).
Se añadió texto para indicar que el linfoma esplénico de zona marginal es una entidad clínica distinta que suele presentarse con esplenomegalia masiva. Una variante del linfomas de tejido linfoide asociado a mucosa se conoce como enfermedad inmunoproliferativa del intestino delgado (se citó a Rossi et al. como referencia 80).
Se revisó el texto para indicar que los pacientes con infección simultánea por el virus de la hepatitis C (VHC), entre un 40 % y un 60 % logran una remisión completa o parcial cuando ya no se detecta el ARN del VHC, mediante tratamiento antivírico (se citó a Merli et al. como referencia 119).
Linfoma no Hodgkin de crecimiento rápido
Se revisó el texto para indicar que, entre los pacientes con enfermedad en estadio avanzado, el 50 % se curan con quimioterapia combinada a base de doxorrubicina y rituximab, por lo general, R-CHOP (rituximab, ciclofosfamida, doxorrubicina, vincristina y prednisona).
Se añadió texto para indicar que los linfomas de células B grandes positivos para la cinasa del linfoma anaplásico (ALK) son extremadamente raros y no responden bien al tratamiento convencional con R-CHOP. Se han descrito respuestas anecdóticas a inhibidores de ALK como lorlatinib o alectinib (se citó a Soumerai et al. como referencia 22 y nivel de evidencia C3).
Se añadió Savage como referencia 37.
Se añadió texto para indicar que, entre los pacientes que habían recibido dos líneas de tratamiento previas, más de la mitad de los que recibieron terapia de células T con CAR con lisocabtagén maraleucel presentaron respuesta de la enfermedad (se citó a Abramson et al. como referencia 53 y nivel de evidencia C3).
Se añadió texto para indicar que, entre los pacientes que habían recibido dos líneas de tratamiento previas, más de la mitad de los que recibieron terapia de células T con CAR con lisocabtagén maraleucel presentaron respuesta de la enfermedad.
Se añadió texto para indicar que, en una revisión retrospectiva de 84 pacientes con ALCL ALK negativo se indicó un beneficio en la supervivencia con el TCM autógeno. Esta hipótesis requiere confirmación en un ensayo prospectivo aleatorizado (se citó a Brink et al. como referencia 72).
Se añadió texto para indicar que el LACG cutáneo primario es una entidad distinta que es, por lo general, negativa para ALK y tiene un curso clínico de crecimiento lento y de grado bajo.
Se añadió texto sobre un ensayo de fase II de 131 pacientes de 65 años o menos con LCM sin tratamiento previo, 1 año de ibrutinib más 4 semanas de rituximab dieron lugar a una tasa de RC del 89 % antes de cualquier consolidación con quimioterapia (se citó a 2022 Wang et al. como referencia 210 y nivel de evidencia C3). En otro ensayo de fase II con ibrutinib y rituximab se incluyó a pacientes asintomáticos con LCM sin tratamiento previo; la tasa de RC fue del 87 % (se citó a Giné et al. como referencia 211 y nivel de evidencia C3).
Se añadió Hermine et al. como referencia 220.
Se revisó el texto sobre los resultados de un ensayo de fase II de brexucabtagén autoleucel para pacientes con LCM en recaída o resistente al tratamiento cuya enfermedad no respondió al ibrutinib o al acalabrutinib (se citó a 2023 Wang et al. como referencia 232).
Información sobre los estadios del linfoma no Hodgkin
Se añadió texto para indicar que una revisión retrospectiva de más de 32 000 casos de linfoma en Francia, hasta el 40 % de los diagnósticos se realizaron mediante biopsia con aguja gruesa, y el 60 % mediante biopsia por escisión (se citó a Syrykh et al. como referencia 1). La biopsia con aguja gruesa proporcionó un diagnóstico definitivo en el 92,3 % de los casos, pero fue menos concluyente que la biopsia por escisión, que proporcionó un diagnóstico definitivo en el 98,1 % de los casos.
Se añadió texto sobre un estudio retrospectivo de 580 pacientes con linfoma folicular en los que no se observó ninguna mejora en la evaluación de la respuesta al tratamiento cuando se añadió la biopsia de médula ósea a las imágenes radiológicas (se citó a Rutherford et al. como referencia 10).
Tratamiento del linfoma no Hodgkin de crecimiento lento no contiguo en estadios II, III y IV
Se añadió Morschhauser et al. como referencia 59.
Se revisó el texto sobre los resultados del ensayo (RELEVANCE) con 1030 pacientes de linfoma folicular sin tratamiento previo, en el que se comparó el uso de rituximab y lenalidomida durante 18 meses con el uso de rituximab y quimioterapia (por lo general, R-CHOP).
Tratamiento del linfoma no Hodgkin de crecimiento lento recidivante
Se revisó la lista de las opciones de tratamiento del linfoma no Hodgkin de crecimiento lento recidivante para incluir los activadores biespecíficos de células T.
Se revisó el texto para indicar que La terapia de células T con receptor de antígeno quimérico (CAR), con la terapia autógena anti-CD19 axicabtagén ciloleucel, lisocabtagén maraleucel o tisagenlecleucel, ha sido aprobada para pacientes con linfoma folicular recidivante tras dos o más líneas de tratamiento previo.
Se revisaron los resultados de un ensayo de fase II con axicabtagén ciloleucel.
Se añadió texto sobre un ensayo de fase II, 98 pacientes con linfoma folicular en recaída o resistente al tratamiento tras dos o más líneas de tratamiento previo recibieron terapia de células T con CAR anti-CD19 con tisagenlecleucel (se citó a Fowler et al. como referencia 33 y nivel de evidencia C3).
Se añadió Activadores biespecíficos de células T como subsección nueva.
Se añadió texto sobre un análisis retrospectivo de 341 pacientes que recibieron R-CHOP (o un régimen similar), con o sin radioterapia (se citó a Bobillo et al. como referencia 7 y nivel de evidencia C3).
Se añadió texto para indicar que en un estudio retrospectivo se indicó que es posible que los pacientes con enfermedad extraganglionar en estadio I y una TEP positiva al final del tratamiento se beneficien de la radioterapia, esta hipótesis debe confirmarse en un ensayo prospectivo aleatorizado.
Tratamiento del linfoma no Hodgkin de crecimiento rápido no contiguo en estadios II, III y IV
Se añadió a Nowakowski et al. como referencia 10.
Tratamiento del linfoma no Hodgkin de crecimiento rápido recidivante
Se revisó la lista de opciones de tratamiento del linfoma no Hodgkin de crecimiento rápido recidivante para incluir los activadores biespecíficos de células T y radioterapia paliativa.
Se revisó el texto sobre los resultados de un ensayo prospectivo aleatorizado de una terapia de células T con CAR para indicar diferencias importantes desde el punto de vista clínico y estadísticamente significativas en la calidad de vida en el grupo de células T con CAR en los días 100 y 150, en comparación con el tratamiento estándar (se citó a Elsawy et al. como referencia 8 y nivel de evidencia A2).
Se revisó el texto sobre los resultados de otro ensayo prospectivo aleatorizado de una terapia de células T con CAR para indicar que el síndrome de liberación de citoquinas de grado 3 se produjo en el 1 % de los pacientes, y la neurotoxicidad de grado 3 se produjo en el 4 % de los pacientes.
Se añadió Calabretta et al. como referencia 41.
Se añadió Activadores biespecíficos de células T como subsección nueva.
Tratamiento del linfoma difuso de células pequeñas no hendidas o linfoma de Burkitt
Se añadió texto para describir el linfoma de células B de grado alto, sin especificar (se citó a Evens et al como referencia 2 y Olszewski et al. como referencia 3).
Se añadió texto sobre los factores de pronóstico adverso del linfoma difuso de células pequeñas no hendidas o linfoma de Burkitt y sobre los resultados de una revisión retrospectiva de 641 pacientes adultos con linfoma de Burkitt procedentes.
El Consejo editorial del PDQ sobre el tratamiento para adultos es responsable de la redacción y actualización de este resumen y mantiene independencia editorial respecto del NCI. El resumen refleja una revisión independiente de la bibliografía médica y no representa las políticas del NCI ni de los NIH. Para obtener más información sobre las políticas relativas a los resúmenes y la función de los consejos editoriales del PDQ responsables de su actualización, consultar Información sobre este resumen del PDQ e Información del PDQ® sobre el cáncer dirigida a profesionales de la salud.
Información sobre este resumen del PDQ
Propósito de este resumen
Este resumen de información del PDQ sobre el cáncer dirigido a profesionales de la salud proporciona información integral revisada por expertos y basada en la evidencia sobre el tratamiento del linfoma no Hodgkin en adultos. El objetivo es servir como fuente de información y ayuda para los profesionales clínicos durante la atención de pacientes. No ofrece pautas ni recomendaciones formales para tomar decisiones relacionadas con la atención sanitaria.
Revisores y actualizaciones
El Consejo editorial del PDQ sobre el tratamiento para adultos, que mantiene independencia editorial respecto del Instituto Nacional del Cáncer (NCI), revisa este resumen de manera periódica y, en caso necesario, lo actualiza. Este resumen es el resultado de una revisión bibliográfica independiente y no constituye una declaración de política del NCI ni de los Institutos Nacionales de la Salud (NIH).
Cada mes, los integrantes de este consejo revisan los artículos publicados recientemente para determinar lo siguiente:
- Si el artículo se debe analizar en una reunión del consejo.
- Si conviene añadir texto acerca del artículo.
- Si se debe reemplazar o actualizar un artículo que ya se citó.
Los cambios en los resúmenes se deciden mediante consenso de los integrantes del consejo después de evaluar la solidez de la evidencia de los artículos publicados y determinar la forma de incorporar el artículo en el resumen.
Los revisores principales del sumario sobre Tratamiento del linfoma no Hodgkin son:
- Eric J. Seifter, MD (Johns Hopkins University)
- Cole H. Sterling, MD (Johns Hopkins University)
Cualquier comentario o pregunta sobre el contenido de este resumen se debe enviar al Servicio de Información de Cáncer del Instituto Nacional del Cáncer. Por favor, no enviar preguntas o comentarios directamente a los integrantes del consejo, ya que no responderán consultas de manera individual.
Niveles de evidencia
Algunas de las referencias bibliográficas de este resumen se acompañan del nivel de evidencia. El propósito de esto es ayudar al lector a evaluar la solidez de la evidencia que respalda el uso de ciertas intervenciones o abordajes. El Consejo editorial del PDQ sobre el tratamiento para adultos emplea un sistema de jerarquización formal para asignar los niveles de evidencia científica.
Permisos para el uso de este resumen
PDQ (Physician Data Query) es una marca registrada. Se autoriza el uso del texto de los documentos del PDQ; sin embargo, no se podrá identificar como un resumen de información sobre cáncer del PDQ del NCI, salvo que el resumen se reproduzca en su totalidad y se actualice de manera periódica. Por otra parte, se permitirá que un autor escriba una oración como “En el resumen del PDQ del NCI de información sobre la prevención del cáncer de mama se describen, de manera concisa, los siguientes riesgos: [incluir fragmento del resumen]”.
Se sugiere citar la referencia bibliográfica de este resumen del PDQ de la siguiente forma:
PDQ® sobre el tratamiento para adultos. PDQ Tratamiento del linfoma no Hodgkin. Bethesda, MD: National Cancer Institute. Actualización: <MM/DD/YYYY>. Disponible en: https://www.cancer.gov/espanol/tipos/linfoma/pro/tratamiento-lnh-adultos-pdq. Fecha de acceso: <MM/DD/YYYY>.
Las imágenes en este resumen se reproducen con autorización del autor, el artista o la editorial para uso exclusivo en los resúmenes del PDQ. La utilización de las imágenes fuera del PDQ requiere la autorización del propietario, que el Instituto Nacional del Cáncer no puede otorgar. Para obtener más información sobre el uso de las ilustraciones de este resumen o de otras imágenes relacionadas con el cáncer, consultar Visuals Online, una colección de más de 2000 imágenes científicas.
Cláusula sobre el descargo de responsabilidad
Según la solidez de la evidencia, las opciones de tratamiento se clasifican como “estándar” o “en evaluación clínica”. Estas clasificaciones no se deben utilizar para justificar decisiones sobre reembolsos de seguros. Para obtener más información sobre la cobertura de seguros, consultar la página Manejo de la atención del cáncer en Cancer.gov/espanol.
Comuníquese con el Instituto Nacional del Cáncer
Para obtener más información sobre las opciones para comunicarse con el NCI, incluso la dirección de correo electrónico, el número telefónico o el chat, consultar la página del Servicio de Información de Cáncer del Instituto Nacional del Cáncer.