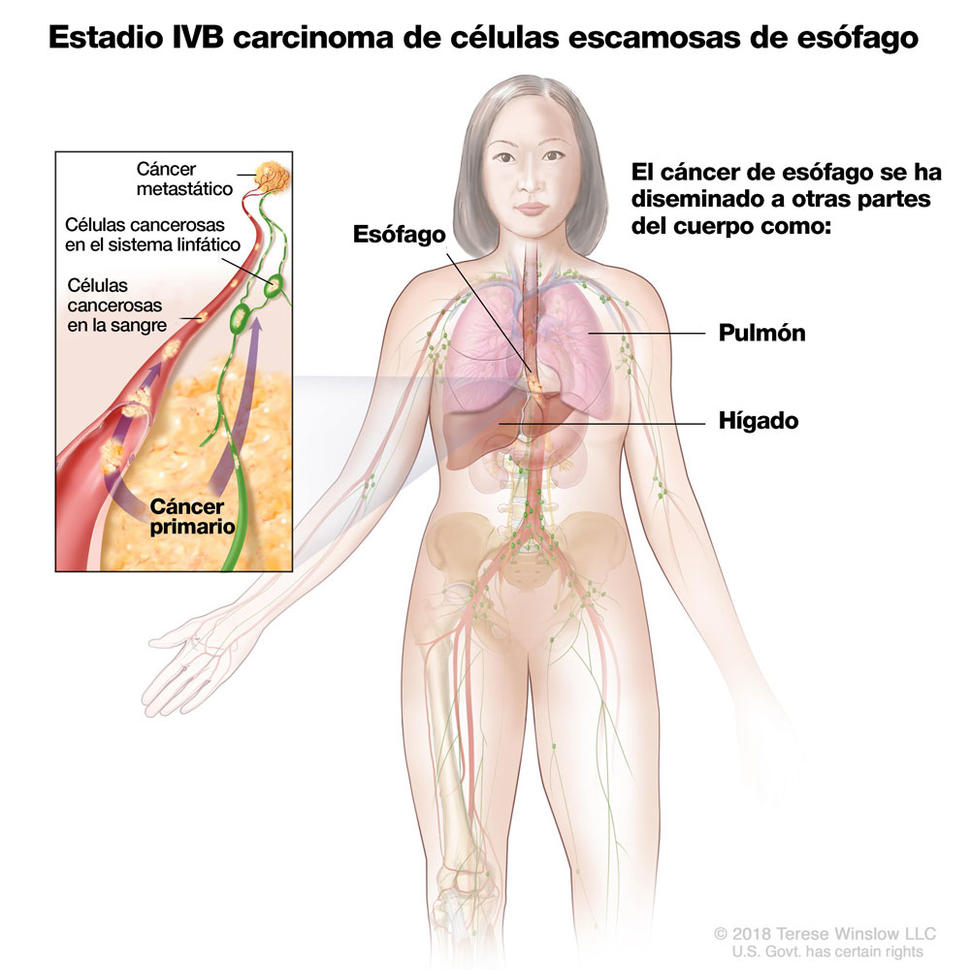
El medicamento pembrolizumab fue aprobado para algunos pacientes con cáncer avanzado de esófago
, por Equipo del NCI
La Administración de Alimentos y Medicamentos (FDA) aprobó el fármaco de inmunoterapia pembrolizumab (Keytruda) para tratar a algunos pacientes con cáncer avanzado de esófago.
El tratamiento se aprobó para pacientes con carcinoma de células escamosas de esófago (ESCC) localmente avanzado o metastásico que empeoró después de una o más líneas de tratamiento estándar. Para recibir el tratamiento, los pacientes deben tener ciertas concentraciones de la proteína PD-L1 en los tumores, las cuales se determinan con una prueba aprobada por la FDA. La FDA también aprobó el uso de PD-L1 IHC 22C3 pharmDx como prueba diagnóstica con fines terapéuticos para esta indicación.
La FDA aprobó anteriormente el pembrolizumab para pacientes con cáncer avanzado gástrico o de la unión gastroesofágica que haya empeorado a pesar de dos o más líneas de tratamiento estándar, y esa aprobación se hizo junto con la misma prueba de PD-L1. En esa aprobación, a los pacientes se les requería tener tumores que expresaran concentraciones relativamente moderadas de PD-L1 (una puntuación positiva combinada de por lo menos 1). En el caso de la aprobación para el cáncer de esófago, los pacientes deberán tener tumores con una expresión de PD-L1 mucho mayor (una puntuación de por lo menos 10).
Aunque se esperaba esta nueva aprobación, “es un avance importante”, dijo el doctor Carmen Allegra, director de tratamientos para el cáncer gastrointestinal en la División de Tratamiento y Diagnóstico del Cáncer del NCI. “La aprobación proporciona otro fármaco para pacientes que tienen una enfermedad con malos desenlaces clínicos, y presenta un beneficio clínico considerable en algunos pacientes”.
El doctor Sarbajit Mukherjee, un especialista en el tratamiento del cáncer de esófago en el Roswell Park Comprehensive Center, estuvo de acuerdo.
“Pienso que, contar con el pembrolizumab como una nueva opción, amplía el horizonte”, comentó. “Significa que podremos ofrecer más tratamientos a pacientes por fuera de un estudio clínico”.
Ampliación de las opciones de tratamiento para el cáncer avanzado de esófago
La quimioterapia, el tratamiento de segunda línea estándar para personas con cáncer avanzado de esófago, tiene beneficios limitados para muchos pacientes y puede presentar efectos secundarios importantes, explicó el doctor Mukherjee.
Además, hay pocas opciones de tratamiento para pacientes con cáncer avanzado de esófago que haya empeorado después del tratamiento estándar, dijo. Añadió que, uno de los motivos de esto puede ser que ha habido un progreso limitado en la identificación de alteraciones moleculares en tumores que podrían convertirse en buenos objetivos para el tratamiento.
En un esfuerzo por ampliar las opciones de tratamiento, los investigadores han estado estudiando la posibilidad de que la inmunoterapia ofrezca una opción para las personas con cáncer avanzado de esófago. El pembrolizumab, un inhibidor de puntos de control inmunitario que inhibe la actividad de la proteína PD-L1 en las células tumorales, ya se ha aprobado para muchos tipos de cáncer.
En un estudio clínico en fase inicial, algunos pacientes con cáncer avanzado de esófago cuyos tumores presentaban concentraciones altas de PD-L1 respondieron al pembrolizumab por períodos prolongados. Por lo tanto, los investigadores iniciaron estudios clínicos más grandes para entender mejor si el pembrolizumab puede beneficiar a personas con cáncer avanzado de esófago, lo cual incluye una mejora en la duración de vida.
La aprobación se basó en los resultados de dos estudios clínicos
La nueva aprobación se basó en dos estudios clínicos, los cuales fueron patrocinados por Merck, el fabricante del fármaco. En un estudio clínico en fase 3, llamado KEYNOTE-181, a 628 pacientes cuyo cáncer avanzado de esófago había empeorado durante una línea de tratamiento o después de esta, se les asignó al azar a recibir el pembrolizumab o 1 de 3 esquemas terapéuticos distintos de quimioterapia elegido por el médico responsable.
En el caso de los pacientes en el estudio clínico que tenían ESCC y tumores con expresión de PD-L1 de por lo menos 10, la mediana de la supervivencia general fue de 10.3 meses para quienes recibieron el pembrolizumab, en comparación con 6.3 meses para los pacientes que recibieron quimioterapia. El índice de respuesta general fue de 22 % en los pacientes que recibieron el pembrolizumab, en comparación con 7 % en los pacientes que recibieron la quimioterapia.
El KEYNOTE-180 fue un estudio clínico en fase dos en el que se inscribieron 121 pacientes con cáncer avanzado y metastásico de esófago que había empeorado después de dos o más líneas de tratamiento estándar. Todos los pacientes en el estudio clínico recibieron el pembrolizumab.
En los 35 pacientes con ESCC en el estudio KEYNOTE-180 cuyos tumores tenían una expresión de PD-L1 de por lo menos 10, el índice de respuesta general fue de 20 %, con respuestas que variaron aproximadamente de 4 meses a más de 25 meses. Entre los pacientes que tuvieron una respuesta, cinco tuvieron respuestas que duraron 6 meses o más y tres tuvieron respuestas que duraron 12 meses o más.
Los efectos secundarios frecuentes en ambos estudios clínicos para los pacientes que tomaron el pembrolizumab incluyeron cansancio, sarpullido, náuseas y diarrea. Cuando se publicaron los resultados del estudio KEYNOTE-180 en diciembre de 2018, los investigadores informaron que 15 pacientes tuvieron eventos adversos de grado 3 a 5 relacionados con el tratamiento, cinco pacientes suspendieron el tratamiento y hubo una muerte relacionada con el tratamiento a causa de neumonitis.
El doctor Allegra señaló que, a pesar de que el porcentaje de pacientes en ambos estudios clínicos que respondieron al tratamiento fue de aproximadamente el 20 %, la respuesta fue, a menudo, relativamente duradera en los pacientes cuyo cáncer reaccionó al tratamiento.
“Esto es lo que distingue a los fármacos de inmunoterapia de los de la quimioterapia”, dijo. “Es la perdurabilidad del fármaco lo que es verdaderamente increíble”.
El doctor Mukherjee enfatizó la importancia de validar la puntuación límite de PD-L1 en el estudio clínico KEYNOTE-181. “Así que, ahora podemos ver la puntuación [de PD-L1] y decirle a nuestros pacientes si tienen probabilidad de beneficiarse más del pembrolizumab que de la quimioterapia”, dijo.
Tratamiento del cáncer de esófago en estadios iniciales y de nuevas maneras
El hecho de que la nueva aprobación sea para uso como tratamiento de segunda línea será beneficioso para los pacientes, explicó el doctor Allegra.
“Esto mueve al fármaco a una fase anterior en la evolución de la enfermedad, algo que es siempre muy bueno para el paciente”, dijo, “porque si el paciente se va a beneficiar, lo mejor es que eso suceda tan pronto como sea posible”.
La evaluación de la inmunoterapia en pacientes que no tienen una enfermedad avanzada continúa siendo un campo activo de investigación.
Por ejemplo, en un estudio clínico patrocinado por el NCI, los investigadores están estudiando al nivolumab (Opdivo) y al ipilimumab (Yervoy), una combinación de fármacos de inmunoterapia, con radiación y quimioterapia estándar en pacientes con cáncer de esófago que se someten a cirugía.
Se está evaluando si la administración de los tratamientos tanto antes como después de la cirugía, cuando el cáncer todavía esté localizado en el esófago, puede prevenir mejor el regreso de la enfermedad, dijo el doctor Allegra.
Además, en otro estudio clínico patrocinado por el NCI se está comparando el tratamiento convencional con radiación fotónica frente a la radioterapia con haz de protones en pacientes con cáncer de esófago en cualquier estadio.
Los resultados de otro estudio clínico, llamado KEYNOTE-062, que se presentaron en el congreso anual de este año de la Sociedad Americana de Oncología Clínica, demostraron que el pembrolizumab benefició a pacientes con cáncer gástrico o de la unión gastroesofágica con una expresión más alta de PD-L1, como tratamiento inicial o de primera línea, dijo el doctor Mukherjee.
Aunque estos son resultados iniciales, agregó, “este estudio clínico nos dio algunos indicios en general para decir que hay pacientes que se pueden beneficiar más de la inmunoterapia, incluso en el entorno del tratamiento de primera línea”.
Los estudios clínicos reflejan una tendencia a continuar evaluando la inmunoterapia como tratamiento para el cáncer de esófago, dijo el doctor Allegra. “Son fármacos claramente activos”, añadió, “así que, si los pudiéramos usar más pronto en los pacientes que posiblemente sean curables, tal vez podríamos curar a más de ellos”.