Tratamiento del cáncer de seno (mama) masculino (PDQ®)–Versión para profesionales de salud
Información general sobre el cáncer de mama masculino
Incidencia y mortalidad
Número estimado de casos nuevos y defunciones por cáncer de mama (seno) en hombres de los Estados Unidos para 2025:[1]
- Casos nuevos: 2800.
- Defunciones: 510.
El cáncer de mama masculino es infrecuente.[2] Representa menos del 1 % de todos los carcinomas de mama.[3,4] La media de edad en el momento del diagnóstico es de 60 a 70 años; sin embargo, la enfermedad se puede presentar en hombres de todas las edades.
Características anatómicas
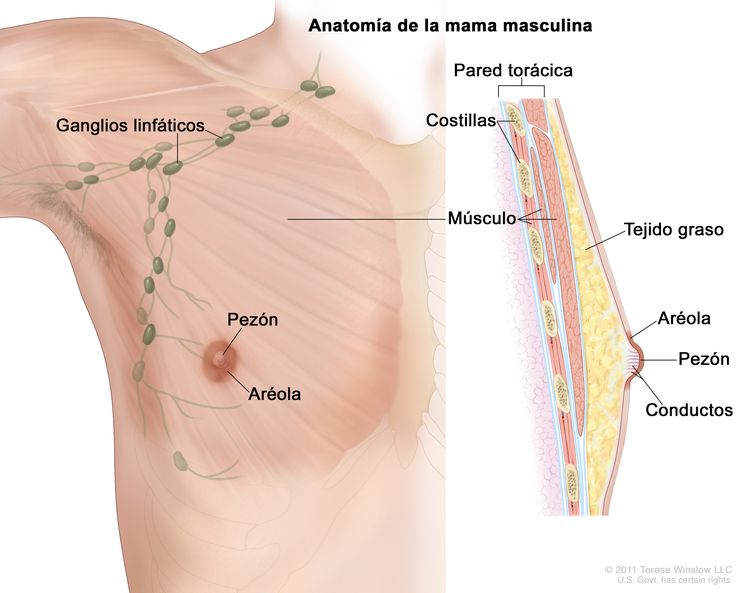
Factores de riesgo
Los factores de riesgo que predisponen al cáncer de mama masculino son los siguientes:[5,6]
- Exposición a la radiación dirigida a la mama o el tórax.
- Uso de estrógeno.
- Enfermedades relacionadas con hiperestrogenismo, como la cirrosis o el síndrome de Klinefelter.
- Antecedentes médicos familiares. Es evidente que hay tendencias familiares definidas; la incidencia es más alta en hombres que tienen varias familiares mujeres con antecedentes de cáncer de mama.
- Mayor susceptibilidad hereditaria. Se notificó un aumento de riesgo de cáncer de mama masculino en familias con variantes patogénicas de BRCA, aunque, el riesgo es más alto cuando se heredan variantes de BRCA2 que cuando se heredan variantes de BRCA1.[7,8] A los 70 años, los hombres tienen un riesgo acumulado estimado de cáncer de mama del 1,2 % si tienen variantes patogénicas de BRCA1 y del 6,8 % si tienen variantes patogénicas de BRCA2.[9] Es posible que la presencia de variantes patogénicas de otros genes, además de BRCA, participen en la predisposición al cáncer de mama masculino; por ejemplo, variantes patogénicas del antioncogén PTEN, del gen TP53 (síndrome de Li-Fraumeni), del gen PALB2 y de los genes de reparación de errores de emparejamiento relacionados con el síndrome de Lynch (también conocido como cáncer colorrectal hereditario sin poliposis).[10-12] Para obtener más información en inglés, consultar las secciones High-Penetrance Breast and/or Gynecologic Cancer Susceptibility Genes en Genetics of Breast and Gynecologic Cancers y Male Breast Cancer Screening and Surveillance for BRCA1/2 Carriers en BRCA1 and BRCA2: Cancer Risks and Management.
Características clínicas
La mayoría de los cánceres de mama en hombres se presentan con una masa tumoral retroareolar. Otros signos son los siguientes:
- Retracción del pezón.
- Sangrado del pezón.
- Ulceración cutánea.
- Piel de naranja.
- Adenopatía axilar palpable.
Debido a que se suele demorar el diagnóstico, es más probable que el cáncer de mama masculino se detecte en un estadio avanzado.[2,5,13]
Evaluación diagnóstica
Cuando se sospecha cáncer se deben hacer exámenes de la mama mediante técnicas de imagen. La American College of Radiology recomienda el uso de la ultrasonografía como la modalidad principal de obtención de imágenes en hombres menores de 25 años ya que a esa edad es menos probable que se forme cáncer de mama. Cuando los hallazgos de la ultrasonografía despiertan sospechas, se realiza una mamografía.
Se recomienda la mamografía como prueba inicial en los hombres de 25 años o más, o quienes tuvieron resultados preocupantes en el examen físico. La ultrasonografía es útil si los resultados de la mamografía son inconcluyentes o dudosos.[14] Los hallazgos sospechosos se deben confirmar mediante una biopsia con aguja gruesa. Si se confirma la presencia de tumores, se debe evaluar el estado del receptor de estrógeno y el receptor de progesterona, así como la expresión o amplificación del factor de crecimiento epidérmico humano de tipo 2 (HER2).[15]
Para obtener más información, consultar la sección Diagnóstico en Tratamiento del cáncer de seno (mama).
Clasificación histopatológica
El cáncer ductal infiltrante es el tipo de cáncer de mama más común en hombres mientras que el carcinoma lobulillar invasivo casi nunca se observa en esta población.[16] El cáncer de mama masculino casi siempre es positivo para receptor hormonal. En una serie de casos de hombres con cáncer de mama, el 99 % de los tumores fueron positivos para el receptor de estrógeno, el 82 % fueron positivos para el receptor de progesterona, el 9 % fueron positivos para HER2 y el 0,3 % fueron triple negativos.[16]
Factores pronósticos y predictivos
Los factores pronósticos anatómicos son el tamaño del tumor, el compromiso ganglionar y el grado del cáncer, mientras que los factores predictivos de la respuesta al tratamiento son los estados del receptor de estrógeno, receptor de progesterona y HER2.
Un estadio más avanzado del cáncer de mama masculino en el momento del diagnóstico confiere un pronóstico más precario.[2,5,13] En un estudio, se encontró que la mortalidad después del diagnóstico de cáncer de mama fue más alta en hombres que en mujeres. Esta diferencia persistió después de considerar las características clínicas, los factores del tratamiento y el acceso a la atención médica, lo que sugiere la posibilidad de que los factores biológicos y la eficacia del tratamiento desempeñen una función.[17]
Bibliografía
- American Cancer Society: Cancer Facts and Figures 2025. American Cancer Society, 2025. Available online. Last accessed January 16, 2025.
- Giordano SH, Cohen DS, Buzdar AU, et al.: Breast carcinoma in men: a population-based study. Cancer 101 (1): 51-7, 2004. [PUBMED Abstract]
- Borgen PI, Wong GY, Vlamis V, et al.: Current management of male breast cancer. A review of 104 cases. Ann Surg 215 (5): 451-7; discussion 457-9, 1992. [PUBMED Abstract]
- Fentiman IS, Fourquet A, Hortobagyi GN: Male breast cancer. Lancet 367 (9510): 595-604, 2006. [PUBMED Abstract]
- Giordano SH, Buzdar AU, Hortobagyi GN: Breast cancer in men. Ann Intern Med 137 (8): 678-87, 2002. [PUBMED Abstract]
- Hultborn R, Hanson C, Köpf I, et al.: Prevalence of Klinefelter's syndrome in male breast cancer patients. Anticancer Res 17 (6D): 4293-7, 1997 Nov-Dec. [PUBMED Abstract]
- Wooster R, Bignell G, Lancaster J, et al.: Identification of the breast cancer susceptibility gene BRCA2. Nature 378 (6559): 789-92, 1995 Dec 21-28. [PUBMED Abstract]
- Thorlacius S, Tryggvadottir L, Olafsdottir GH, et al.: Linkage to BRCA2 region in hereditary male breast cancer. Lancet 346 (8974): 544-5, 1995. [PUBMED Abstract]
- Tai YC, Domchek S, Parmigiani G, et al.: Breast cancer risk among male BRCA1 and BRCA2 mutation carriers. J Natl Cancer Inst 99 (23): 1811-4, 2007. [PUBMED Abstract]
- Ding YC, Steele L, Kuan CJ, et al.: Mutations in BRCA2 and PALB2 in male breast cancer cases from the United States. Breast Cancer Res Treat 126 (3): 771-8, 2011. [PUBMED Abstract]
- Silvestri V, Rizzolo P, Zanna I, et al.: PALB2 mutations in male breast cancer: a population-based study in Central Italy. Breast Cancer Res Treat 122 (1): 299-301, 2010. [PUBMED Abstract]
- Boyd J, Rhei E, Federici MG, et al.: Male breast cancer in the hereditary nonpolyposis colorectal cancer syndrome. Breast Cancer Res Treat 53 (1): 87-91, 1999. [PUBMED Abstract]
- Ravandi-Kashani F, Hayes TG: Male breast cancer: a review of the literature. Eur J Cancer 34 (9): 1341-7, 1998. [PUBMED Abstract]
- Mainiero MB, Lourenco AP, Barke LD, et al.: ACR Appropriateness Criteria Evaluation of the Symptomatic Male Breast. J Am Coll Radiol 12 (7): 678-82, 2015. [PUBMED Abstract]
- Giordano SH: A review of the diagnosis and management of male breast cancer. Oncologist 10 (7): 471-9, 2005. [PUBMED Abstract]
- Cardoso F, Paluch-Shimon S, Senkus E, et al.: 5th ESO-ESMO international consensus guidelines for advanced breast cancer (ABC 5). Ann Oncol 31 (12): 1623-1649, 2020. [PUBMED Abstract]
- Wang F, Shu X, Meszoely I, et al.: Overall Mortality After Diagnosis of Breast Cancer in Men vs Women. JAMA Oncol 5 (11): 1589-1596, 2019. [PUBMED Abstract]
Información sobre los estadios del cáncer de mama masculino
La estadificación del cáncer de mama masculino es igual a la del cáncer de mama femenino. Para obtener más información, consultar la sección Definiciones TNM en Tratamiento del cáncer de seno (mama).
Aspectos generales de las opciones de tratamiento para el cáncer de mama masculino
El abordaje de tratamiento de los hombres con cáncer de mama es similar al de las mujeres. Dado que el cáncer de mama masculino es infrecuente, no hay datos de ensayos aleatorizados que sustenten modalidades específicas de tratamiento. Las opciones de tratamiento para los hombres con cáncer de mama se describen en el Cuadro 1.
| Estadio (Definiciones TNM) | Opciones de tratamiento |
|---|---|
| T = tumor primario; N = ganglio linfático regional; M = metástasis a distancia; GnRH = hormona liberadora de gonadotropina. | |
| Cáncer de mama masculino en estadio temprano, localizado y operable | Cirugía con radioterapia o sin esta |
| Terapia adyuvante | |
| Cáncer de mama masculino localmente avanzado | Quimioterapia neoadyuvante |
| Escisión quirúrgica | |
| Radioterapia y terapia endocrina | |
| Cáncer de mama masculino metastásico | Terapia con un inhibidor de la aromatasa y un agonista de GnRH |
Tratamiento para el cáncer de mama masculino en estadio temprano, localizado y operable
Al igual que para las mujeres, las opciones de tratamiento estándar para los hombres con cáncer de mama en estadio temprano son las siguientes:
- Cirugía con radioterapia o sin esta (terapia locorregional).
- Terapia adyuvante (terapia sistémica).
- Quimioterapia.
- Terapia endocrina.
- Terapia dirigida al receptor 2 del factor de crecimiento epidérmico humano (HER2).
Cirugía con radioterapia o sin esta
La terapia de primera línea es la mastectomía con disección de ganglios linfáticos axilares.[1-3] Por lo general, las respuestas en los hombres son similares a las observadas en las mujeres con cáncer de mama.[2] También se ha usado la cirugía para conservar la mama, es decir la lumpectomía con radioterapia; esta es una opción a considerar si se cumplen los criterios estándar para el tratamiento de conservación de la mama. Los resultados en los hombres han sido similares a los observados en las mujeres con cáncer de mama.[4]
Para obtener más información, consultar la sección Tratamiento quirúrgico del cáncer de mama en Tratamiento del cáncer de seno (mama).
Terapia adyuvante
El tratamiento sistémico óptimo para los hombres con cáncer de mama no se ha estudiado en ensayos clínicos aleatorizados. La terapia adyuvante debe administrarse de acuerdo con los mismos criterios que se utilizan para las mujeres. Las terapias adyuvantes utilizadas para tratar el cáncer de mama masculino en estadio temprano, localizado y operable se describen en el Cuadro 2. Para obtener más información, consultar la sección Terapia sistémica para el cáncer de mama en estadios I, II y III en Tratamiento del cáncer de seno (mama).
| Tipo de terapia adyuvante | Fármacos utilizados |
|---|---|
| HER2 = receptor 2 del factor de crecimiento epidérmico humano; HLHL = hormona liberadora de hormona luteinizante. | |
| Quimioterapia | Docetaxel y ciclofosfamida |
| Doxorrubicina y ciclofosfamida, con paclitaxel o sin este | |
| Terapia endocrina | Tamoxifeno [5] |
| Inhibidores de la aromatasa con un agonista de HLHL [5-9] | |
| Terapia dirigida a HER2 | Trastuzumab [1,5] |
| Pertuzumab | |
Tamoxifeno
Evidencia (tamoxifeno):
- En un análisis retrospectivo de 257 hombres con cáncer de mama en estadios I a III, se incluyeron 50 hombres tratados con un inhibidor de la aromatasa (IA) y 207 hombres tratados con tamoxifeno.[10]
- Al cabo de una mediana de seguimiento de 42 meses, el tratamiento con un IA se relacionó con un riesgo más alto de muerte en comparación con el tamoxifeno (32 % con IA vs. 18 % con tamoxifeno; cociente de riesgos instantáneos, 1,55; intervalo de confianza 95 %, 1,13–2,13).
No se recomienda la administración de un IA en monoterapia para los hombres que tienen contraindicaciones para el tratamiento con tamoxifeno. Los IA deben combinarse con análogos de la hormona liberadora de gonadotropina (GnRH).[6]
En los pacientes con cáncer de mama masculino, el uso de tamoxifeno se vincula con una tasa alta de síntomas que limitan el tratamiento, como sofocos e impotencia.[11]
El German Breast Group llevó a cabo un ensayo clínico aleatorizado de fase II (NCT01638247) de tamoxifeno con un análogo de la HLGn o sin este versus IA con un análogo de GnRH en hombres con cáncer de mama en estadio temprano, positivo para receptor hormonal. Están pendientes los resultados de este ensayo.
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Borgen PI, Wong GY, Vlamis V, et al.: Current management of male breast cancer. A review of 104 cases. Ann Surg 215 (5): 451-7; discussion 457-9, 1992. [PUBMED Abstract]
- Giordano SH, Buzdar AU, Hortobagyi GN: Breast cancer in men. Ann Intern Med 137 (8): 678-87, 2002. [PUBMED Abstract]
- Kinne DW: Management of male breast cancer. Oncology (Huntingt) 5 (3): 45-7; discussion 47-8, 1991. [PUBMED Abstract]
- Golshan M, Rusby J, Dominguez F, et al.: Breast conservation for male breast carcinoma. Breast 16 (6): 653-6, 2007. [PUBMED Abstract]
- Giordano SH: A review of the diagnosis and management of male breast cancer. Oncologist 10 (7): 471-9, 2005. [PUBMED Abstract]
- Giordano SH, Hortobagyi GN: Leuprolide acetate plus aromatase inhibition for male breast cancer. J Clin Oncol 24 (21): e42-3, 2006. [PUBMED Abstract]
- Cocconi G, Bisagni G, Ceci G, et al.: Low-dose aminoglutethimide with and without hydrocortisone replacement as a first-line endocrine treatment in advanced breast cancer: a prospective randomized trial of the Italian Oncology Group for Clinical Research. J Clin Oncol 10 (6): 984-9, 1992. [PUBMED Abstract]
- Gale KE, Andersen JW, Tormey DC, et al.: Hormonal treatment for metastatic breast cancer. An Eastern Cooperative Oncology Group Phase III trial comparing aminoglutethimide to tamoxifen. Cancer 73 (2): 354-61, 1994. [PUBMED Abstract]
- Zagouri F, Sergentanis TN, Koutoulidis V, et al.: Aromatase inhibitors with or without gonadotropin-releasing hormone analogue in metastatic male breast cancer: a case series. Br J Cancer 108 (11): 2259-63, 2013. [PUBMED Abstract]
- Eggemann H, Ignatov A, Smith BJ, et al.: Adjuvant therapy with tamoxifen compared to aromatase inhibitors for 257 male breast cancer patients. Breast Cancer Res Treat 137 (2): 465-70, 2013. [PUBMED Abstract]
- Anelli TF, Anelli A, Tran KN, et al.: Tamoxifen administration is associated with a high rate of treatment-limiting symptoms in male breast cancer patients. Cancer 74 (1): 74-7, 1994. [PUBMED Abstract]
Tratamiento del cáncer de mama masculino localmente avanzado
Las opciones de tratamiento para los hombres con cáncer de mama localmente avanzado son las siguientes:[1]
- Quimioterapia neoadyuvante.
- Escisión quirúrgica.
- Radioterapia y terapia endocrina.
Las decisiones relacionadas con el orden y la elección de los tratamientos para los hombres y las mujeres con cáncer de mama se fundamentan en los mismos principios (sobre todo, en la evaluación de la respuesta patológica).[1,2]
Para obtener más información, consultar la sección Tratamiento del cáncer de mama con recidiva locorregional en Tratamiento del cáncer de seno (mama).
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Giordano SH, Buzdar AU, Hortobagyi GN: Breast cancer in men. Ann Intern Med 137 (8): 678-87, 2002. [PUBMED Abstract]
- Kamila C, Jenny B, Per H, et al.: How to treat male breast cancer. Breast 16 (Suppl 2): S147-54, 2007. [PUBMED Abstract]
Tratamiento del cáncer de mama masculino metastásico
La opción de tratamiento para los hombres con cáncer de mama metastásico es la siguiente:
- Terapia con un inhibidor de la aromatasa (IA) y un agonista de la hormona liberadora de gonadotropina (GnRH).
Las opciones de tratamiento para los hombres con cáncer de mama metastásico positivo para receptor hormonal son las mismas que para las mujeres. Sin embargo, los datos sobre la actividad de los IA con agonistas de GnRH y fulvestrant en hombres se limitan a series de casos.[1-4] Según los datos adyuvantes, se recomienda la administración de un IA con un agonista de GnRH. No hay datos en los que se compare la actividad de fulvestrant en monoterapia con la actividad del fulvestrant combinado con un análogo de GnRH.
A partir de datos de la vida real y estudios limitados, es razonable extrapolar el uso de opciones de tratamiento adicionales para los hombres. Estas opciones incluyen los inhibidores de cinasas dependientes de ciclinas (CDK) 4/6, los inhibidores del blanco de la rapamicina en los mamíferos (mTOR) y los inhibidores de fosfatidilinositol-3–cinasa (PI3K) que se administran en combinación con terapia endocrina.
La administración de quimioterapia, terapia dirigida al receptor 2 del factor de crecimiento epidérmico humano (HER2), inmunoterapia e inhibidores de la poli-adenosina-difosfato-ribosa–polimerasa (PARP) en los hombres con cáncer de mama metastásico se lleva a cabo bajo principios de tratamiento similares a los usados en las mujeres.[5,6]
Para obtener más información, consultar la sección Tratamiento del cáncer de mama metastásico en Tratamiento del cáncer de seno (mama).
Ensayos clínicos en curso
Realizar una búsqueda avanzada en inglés de los ensayos clínicos sobre cáncer auspiciados por el NCI que ahora aceptan pacientes. La búsqueda se puede simplificar por ubicación del ensayo, tipo de tratamiento, nombre del fármaco y otros criterios. También se dispone de información general sobre los ensayos clínicos.
Bibliografía
- Di Lauro L, Vici P, Barba M, et al.: Antiandrogen therapy in metastatic male breast cancer: results from an updated analysis in an expanded case series. Breast Cancer Res Treat 148 (1): 73-80, 2014. [PUBMED Abstract]
- Zagouri F, Sergentanis TN, Chrysikos D, et al.: Fulvestrant and male breast cancer: a pooled analysis. Breast Cancer Res Treat 149 (1): 269-75, 2015. [PUBMED Abstract]
- Zagouri F, Sergentanis TN, Koutoulidis V, et al.: Aromatase inhibitors with or without gonadotropin-releasing hormone analogue in metastatic male breast cancer: a case series. Br J Cancer 108 (11): 2259-63, 2013. [PUBMED Abstract]
- Di Lauro L, Vici P, Del Medico P, et al.: Letrozole combined with gonadotropin-releasing hormone analog for metastatic male breast cancer. Breast Cancer Res Treat 141 (1): 119-23, 2013. [PUBMED Abstract]
- Giordano SH, Buzdar AU, Hortobagyi GN: Breast cancer in men. Ann Intern Med 137 (8): 678-87, 2002. [PUBMED Abstract]
- Kamila C, Jenny B, Per H, et al.: How to treat male breast cancer. Breast 16 (Suppl 2): S147-54, 2007. [PUBMED Abstract]
Actualizaciones más recientes a este resumen (05/13/2025)
Los resúmenes del PDQ con información sobre el cáncer se revisan con regularidad y se actualizan a medida que se obtiene nueva información. Esta sección describe los cambios más recientes introducidos en este resumen a partir de la fecha arriba indicada.
Información general sobre el cáncer de mama masculino
Se actualizaron las estadísticas con el número estimado de casos nuevos y defunciones para 2025 (se citó a la American Cancer Society como referencia 1).
El Consejo editorial del PDQ sobre el tratamiento para adultos es responsable de la redacción y actualización de este resumen y mantiene independencia editorial respecto del NCI. El resumen refleja una revisión independiente de la bibliografía médica y no representa las políticas del NCI ni de los NIH. Para obtener más información sobre las políticas relativas a los resúmenes y la función de los consejos editoriales del PDQ responsables de su actualización, consultar Información sobre este resumen del PDQ e Información del PDQ® sobre el cáncer dirigida a profesionales de la salud.
Información sobre este resumen del PDQ
Propósito de este resumen
Este resumen de información del PDQ sobre el cáncer dirigido a profesionales de la salud proporciona información integral revisada por expertos y basada en la evidencia sobre el tratamiento del cáncer de seno (mama) masculino. El objetivo es servir como fuente de información y ayuda para los profesionales clínicos durante la atención de pacientes. No ofrece pautas ni recomendaciones formales para tomar decisiones relacionadas con la atención sanitaria.
Revisores y actualizaciones
El consejo editorial del PDQ sobre el tratamiento para adultos, que mantiene independencia editorial respecto del Instituto Nacional del Cáncer (NCI), revisa este resumen de manera periódica y, en caso necesario, lo actualiza. Este resumen es el resultado de una revisión bibliográfica independiente y no constituye una declaración de política del NCI ni de los Institutos Nacionales de la Salud (NIH).
Cada mes, los integrantes de este consejo revisan los artículos publicados recientemente para determinar lo siguiente:
- Si el artículo se debe analizar en una reunión del consejo.
- Si conviene añadir texto acerca del artículo.
- Si se debe reemplazar o actualizar un artículo que ya se citó.
Los cambios en los resúmenes se deciden mediante consenso de los integrantes del consejo después de evaluar la solidez de la evidencia de los artículos publicados y determinar la forma de incorporar el artículo en el resumen.
Los revisores principales del sumario sobre Tratamiento del cáncer de seno (mama) masculino son:
- Fumiko Chino, MD (MD Anderson Cancer Center)
- Tarek Hijal, MD (McGill University Health Centre)
- Joseph L. Pater, MD (NCIC-Clinical Trials Group)
- Carol Tweed, MD (Maryland Oncology Hematology)
Cualquier comentario o pregunta sobre el contenido de este resumen se debe enviar al Servicio de Información de Cáncer del Instituto Nacional del Cáncer. Por favor, no enviar preguntas o comentarios directamente a los integrantes del consejo, ya que no responderán consultas de manera individual.
Niveles de evidencia
Algunas de las referencias bibliográficas de este resumen se acompañan del nivel de evidencia. El propósito de esto es ayudar al lector a evaluar la solidez de la evidencia que respalda el uso de ciertas intervenciones o abordajes. El consejo editorial del PDQ sobre el tratamiento para adultos emplea un sistema de jerarquización formal para asignar los niveles de evidencia científica.
Permisos para el uso de este resumen
PDQ (Physician Data Query) es una marca registrada. Se autoriza el uso del texto de los documentos del PDQ; sin embargo, no se podrá identificar como un resumen de información sobre cáncer del PDQ del NCI, salvo que el resumen se reproduzca en su totalidad y se actualice de manera periódica. Por otra parte, se permitirá que un autor escriba una oración como “En el resumen del PDQ del NCI de información sobre la prevención del cáncer de mama se describen, de manera concisa, los siguientes riesgos: [incluir fragmento del resumen]”.
Se sugiere citar la referencia bibliográfica de este resumen del PDQ de la siguiente forma:
PDQ® sobre el tratamiento para adultos. PDQ Tratamiento del cáncer de seno (mama) masculino. Bethesda, MD: National Cancer Institute. Actualización: <MM/DD/YYYY>. Disponible en: https://www.cancer.gov/espanol/tipos/seno/pro/tratamiento-seno-masculino-pdq. Fecha de acceso: <MM/DD/YYYY>.
Las imágenes en este resumen se reproducen con autorización del autor, el artista o la editorial para uso exclusivo en los resúmenes del PDQ. La utilización de las imágenes fuera del PDQ requiere la autorización del propietario, que el Instituto Nacional del Cáncer no puede otorgar. Para obtener más información sobre el uso de las ilustraciones de este resumen o de otras imágenes relacionadas con el cáncer, consultar Visuals Online, una colección de más de 2000 imágenes científicas.
Cláusula sobre el descargo de responsabilidad
Según la solidez de la evidencia, las opciones de tratamiento se clasifican como “estándar” o “en evaluación clínica”. Estas clasificaciones no se deben utilizar para justificar decisiones sobre reembolsos de seguros. Para obtener más información sobre la cobertura de seguros, consultar la página Manejo de la atención del cáncer en Cancer.gov/espanol.
Comuníquese con el Instituto Nacional del Cáncer
Para obtener más información sobre las opciones para comunicarse con el NCI, incluso la dirección de correo electrónico, el número telefónico o el chat, consultar la página del Servicio de Información de Cáncer del Instituto Nacional del Cáncer.