Planificar la transición para la atención del cáncer avanzado en la etapa final de la vida (PDQ®)–Versión para profesionales de salud
Aspectos generales
La American Cancer Society estima que 618 120 personas morirán por cáncer en los Estados Unidos en 2025.[1] La anticipación de la etapa final de la vida (EFV) y la toma de decisiones sobre el tratamiento o la atención, o los cuidados adecuados o preferidos cerca de esta etapa presentan retos intelectuales y emocionales para los pacientes con cáncer avanzado, sus familias y amigos, los oncólogos, y otros profesionales de la atención de la salud. Sin embargo, las siguientes son las consecuencias adversas de la falta de planificación para hacer una transición adecuada al tratamiento durante la EFV:
- Aumento del malestar psicológico.
- Tratamientos médicos que contradicen las preferencias personales.
- Uso de recursos sanitarios engorrosos y costosos con escasos beneficios terapéuticos.
- Un duelo más difícil.
A menudo, los oncólogos y sus pacientes evitan o aplazan la planificación de la atención en la EFV hasta el último momento por muchos factores posibles, que pueden ser individuales, familiares o sociales. Sin embargo, hay pruebas que indican que muchos de estos factores no son en realidad obstáculos y que se pueden superar.
El objetivo de este resumen es revisar las pruebas provenientes de conversaciones sobre la atención en la EFV de los pacientes de cáncer avanzado, a fin de informar a los proveedores de atención de la salud, los pacientes y sus familias acerca de la transición a una atención compasiva y eficaz en la EFV.
Bibliografía
- American Cancer Society: Cancer Facts and Figures 2025. American Cancer Society, 2025. Available online. Last accessed January 16, 2025.
Calidad de la atención en la etapa final de la vida de los pacientes con cáncer en estadio avanzado
Con frecuencia, el paciente con cáncer en estadio avanzado, su familia y amigos, así como los oncólogos, enfrentan decisiones terapéuticas que afectan de forma profunda la calidad de vida (CV) del paciente. Los oncólogos tienen la obligación de considerar, junto con el paciente y su familia, los posibles efectos de los tratamientos continuados dirigidos a la enfermedad o la atención enfocada en los síntomas y la CV.
En esta sección, se resume la información que permitirá a los oncólogos y los pacientes con cáncer en estadio avanzado planificar la atención a fin de mejorar su CV en la etapa final de la vida (EFV), al tomar decisiones fundamentadas con respecto a los posibles perjuicios de la continuación del tratamiento intensivo y los posibles beneficios de los cuidados paliativos o de los programas en los que se administran dichos cuidados. En esta sección:
- Se revisa el concepto de calidad de la atención en la EFV.
- Se resumen y evalúan los indicadores de calidad de la atención en la EFV que se citan con mayor frecuencia.
- Se analiza el concepto del bien morir.
Además, la información sobre los desenlaces relacionados con la reanimación cardiopulmonar (RCP) y el ingreso en una unidad de cuidados intensivos (UCI) facilitará a los oncólogos presentar las opciones a los pacientes de cáncer en estadio avanzado en la EFV.
Calidad de la atención en la etapa final de la vida
Las siguientes son preguntas pertinentes a la medición de la calidad de la atención en la EFV de los pacientes con cáncer en estadio avanzado:[1]
- ¿En qué directrices respaldadas por pruebas se basan las evaluaciones de calidad?
- ¿Qué período comprende la EFV?
- ¿Se puede acceder de forma sencilla a los indicadores de calidad de interés precisos y guardan estos una relación plausible con los resultados esperados?
- ¿Qué constituye alta calidad?
- Más importante aún, ¿se da prioridad a la perspectiva del paciente?
Perspectiva del paciente
Las encuestas y las entrevistas a pacientes con enfermedades que tal vez provoquen la muerte, las cuales no se limitan al cáncer, quizás ayuden a comprender lo que constituye la atención de alta calidad en la EFV. Un grupo de investigadores propuso que los pacientes evaluaran 5 áreas principales de la atención cerca de la EFV:[2]
- Recibir tratamiento adecuado para el dolor y los síntomas.
- Evitar la prolongación innecesaria de la agonía.
- Lograr una sensación de control.
- Alivianar la carga del agobio.
- Reforzar las relaciones con los seres queridos.
Un estudio prospectivo sobre CV realizado en 2011 con una cohorte de pacientes con cáncer avanzado en clínicas oncológicas ambulatorias proporcionó más información sobre la perspectiva de los pacientes sobre lo que constituye una buena CV.[3] La mediana de supervivencia de la cohorte fue de 10 meses; por lo tanto, es posible que los resultados no reflejen la situación de los pacientes más cercanos a la muerte. No obstante, los factores pronósticos más firmes de la CV fueron los siguientes:
- Edad avanzada.
- Buen estado funcional.
- Período de supervivencia mayor de 6 meses.
Los pacientes que esperaban un tratamiento nuevo tuvieron peor bienestar emocional. Esta experiencia indica que la CV se relaciona con factores como la progresión de la enfermedad y sus complicaciones, así como con los objetivos del paciente relacionados con cualquier tratamiento que reciba.[3] Además, otros investigadores notificaron que los familiares a cargo del cuidado de los pacientes con cáncer avanzado, a menudo asignan puntajes más bajos que los mismos pacientes en las autoevaluaciones de la CV.[4]
Indicadores de la calidad de la atención en la etapa final de la vida
Se han propuesto varios indicadores para medir la calidad de la atención en la EFV de los pacientes con cáncer avanzado. Las siguientes son algunas de las críticas más destacadas de los indicadores propuestos:
- Los indicadores se suelen medir en un período previo a la muerte, que se define de forma retrospectiva a partir de esta. Los médicos no pueden pronosticar si una intervención será inútil para prevenir la muerte; en consecuencia, se pueden exagerar las preocupaciones por la calidad si el indicador depende del tiempo hasta la muerte.
- Es posible que los indicadores de calidad no se ajusten a las preferencias del paciente. Por ejemplo, un paciente puede preferir recibir quimioterapia en el período cercano a la muerte y renunciar a los cuidados paliativos. Por el contrario, dejar de administrar tratamiento según las directrices puede reflejar la negativa del paciente o las contraindicaciones médicas a la terapia recomendada. En un estudio,[5] se demostró que la adherencia al cumplimiento de 6 indicadores de calidad en pacientes con cáncer de pulmón al cuidado de la Administración de la Salud de Veteranos (VHA) se vio comprometida por la negativa (entre el 0 % y el 14 % de las veces) o las contraindicaciones médicas (entre el 1 % y el 30 % de las veces), según el indicador.
- En las bases de datos administrativas, no se registra la información de todos los pacientes. Por ejemplo, en las bases de datos de los Centros de Servicios de Medicare y Medicaid solo se registra la población asegurada por Medicare.
- Muchos de los indicadores no se definieron de forma deliberada como medidas de calidad y pueden pasar por alto resultados importantes.
Sin embargo, es posible que el estudio de los indicadores, ya sea con el tiempo o entre subespecialidades o sistemas de salud en regiones geográficas importantes, proporcione percepciones importantes sobre la calidad de la atención en la EFV.
Tendencias en el tiempo de los indicadores de calidad de la atención en la etapa final de la vida
Se dispone de múltiples informes de interés para comprender las tendencias de calidad de vida en el tiempo durante la atención en la EFV para varios tipos de cáncer. Un análisis de 2004 respaldó las siguientes observaciones,[6] con sustento bibliográfico adicional que se indica cuando sea pertinente:
- Un creciente número de pacientes comienza un nuevo régimen quimioterapéutico en los 30 días previos a la muerte o continúa recibiendo quimioterapia en los 14 días previos a esta.
- Un creciente número de pacientes se deriva a programas de cuidados paliativos; sin embargo, su estancia en estos programas continúa siendo relativamente corta; lo que respalda la preocupación de que estas derivaciones se pueden hacer demasiado tarde. Por ejemplo, en un estudio de 2011 con hombres en la etapa final por cáncer de próstata, se demostró una mayor utilización de los cuidados paliativos (alrededor del 32—60 %), pero hubo un aumento en la proporción de estancias menores de 7 días.[7]
- Las tasas de ocupación de la UCI también aumentaron. Por ejemplo, en un estudio,[8] se notificó que por todos los pacientes de cáncer de próstata en la EFV debido a cáncer de páncreas, los ingresos en la UCI aumentaron en 2 períodos diferentes: de 1992 a 1994, del 15,5 % al 19,6 %, y de 2004 a 2006, del 8,1 % al 16,4 %.
- Las tasas de órdenes de no reanimar (ONR) han aumentado, pero permanecen cercanas al momento de la muerte: en un estudio de 2008 sobre la tasa y la frecuencia de las ONR en un importante centro oncológico entre 2000 y 2005, se demostró que las tasas de órdenes de ONR en el momento de la muerte aumentaron del 83 % al 86 % para las muertes en el hospital y del 28 al 52 % para las muertes fuera de este.[9] No obstante, para las muertes en el hospital, la mediana de tiempo entre la firma de la ONR y la muerte fue de 0 días; para las muertes fuera del hospital, fue de 30 días. Este hallazgo indica que se difiere la comunicación sobre la decisión de reanimar. Este atraso puede tener un efecto negativo en la preparación del paciente para la EFV.
Variaciones regionales de los indicadores de la calidad de la atención en la etapa final de la vida
Las variaciones regionales en términos de tasas de utilización de los recursos sanitarios cerca de la EFV despiertan interés porque, en escasas ocasiones, las diferencias se relacionan con mejores resultados. Si bien las conclusiones iniciales se enfocaron en las diferencias entre regiones geográficas de Estados Unidos, en estudios posteriores se demostraron diferencias, quizás significativas, entre los sistemas de salud y en el interior de estos.[10] A continuación, se incluye un resumen de algunas de las variaciones más notables.
- En comparación con los hombres que se inscribieron en un servicio de Medicare con pago por servicio, los hombres mayores con cáncer avanzado a quienes se les administró tratamiento en el entorno de la VHA tuvieron menores probabilidades de recibir quimioterapia en los 14 días previos a la muerte (4,6 vs. 7,5 %), de estar en una UCI en los 30 días previos a la muerte (12,5 vs. 19,7 %) y de acudir al servicio de urgencias más de una vez (13,1 vs. 14,7 %).[11]
- En un análisis de datos realizado por parte del Dartmouth Institute for Health Policy & Clinical Practice sobre la atención de los pacientes de Medicare con pronósticos adversos, se demostraron variaciones regionales importantes de la atención en la EFV.[12] Las siguientes son las principales conclusiones:
- Variaciones en la tasa de hospitalización, estancias en UCI e intervenciones radicales, como RCP y respiración mecánica.
- Variaciones en la administración de quimioterapia en los últimos 14 días de vida.
- Variaciones en el uso de programas de cuidados paliativos que se miden como tasas de derivación o períodos de estancia hospitalaria.
Según los autores, las variaciones regionales que se observaron fueron demasiado grandes como para representar preferencias raciales o étnicas, ni grados de enfermedad. Los factores que se correlacionan con la intensidad de la atención en la EFV son la disponibilidad de recursos, como el número de camas en la UCI o los equipos de imaginología, el número de médicos que participan en la atención de cada paciente y el entorno mismo del tratamiento.[12]
Factores relacionados con las variaciones de la atención en la etapa final de la vida
La disponibilidad de médicos especialistas, el número de camas en los hospitales, y las características de los médicos y del sistema de salud son factores establecidos de forma clara que se relacionan con mayores gastos en los últimos 6 meses de vida. En un estudio de 2011,[13] se usaron datos de descendientes inscritos en Health and Retirement Study, Medicare, y Dartmouth Atlas para identificar los factores relativos al paciente que podían contribuir a las variaciones regionales. Los siguientes factores se relacionaron con mayores gastos, incluso después de un ajuste con respecto a las características regionales:
- Deterioro del estado funcional.
- Etnia hispana.
- Raza negra.
- Enfermedades crónicas, como la diabetes.
Los factores relativos al paciente representaron solo el 10 % de las variaciones. Los modelos de práctica en la EFV y el número de camas per cápita en los hospitales también se relacionaron con mayores gastos. La planificación anticipada de la atención no influyó en los gastos.[13]
Una posible explicación para las variaciones regionales de la atención en la EFV son las diferencias regionales de las preferencias de los pacientes. Sin embargo, las pruebas son contradictorias.
- En un estudio, se encuestó a 2515 beneficiarios de Medicare sobre sus preferencias generales relacionadas con la atención médica en caso de una enfermedad grave que acorte la vida, con una esperanza de vida menor de 1 año.[14] Las preferencias se correlacionaron con los gastos de la atención en la EFV por región hospitalaria de derivación. No se observaron diferencias entre las preferencias de paliación o prolongación de la vida por región. Por consiguiente, es poco probable que las variaciones regionales en las preferencias representen las variaciones observadas en los gastos por la atención en la EFV.
- Por el contrario, en un análisis secundario de la posible influencia del sitio del tratamiento en las conclusiones del estudio Coping with Cancer, se demostró que el efecto del sitio del tratamiento, en parte, se produjo por las diferencias en las preferencias de los pacientes.[15]
El buen morir
Perspectiva del profesional de la salud
El concepto de buen morir es polémico, pero tal vez sea un constructo útil para los oncólogos a fin de formular de manera más clara los objetivos de la atención oportuna, compasiva y eficaz en la EFV. En un artículo del BMJ de 2003 sobre la atención del paciente moribundo, los autores propusieron que había suficientes pautas respaldadas por pruebas para facilitar el bien morir; en un comentario que acompañó el artículo se lee: "La educación profesional no puede expresar, de modo adecuado, tanto en el momento como después, como hacer frente a la muerte de un ser querido sabiendo que tuvo un ‘buen morir’".[16] Se presentaron varios argumentos destacados en posteriores cartas al editor:
- La salud mental del paciente y su familia es una preocupación básica para garantizar un bien morir.
- Las creencias y las actitudes del proveedor de la atención de la salud pueden disminuir las probabilidades de un bien morir si interfieren con el control adecuado del dolor o los síntomas.
- Los proveedores de la atención de la salud corren el riesgo de caer en paternalismo médico si no respetan el punto de vista del paciente e insisten en proporcionar atención en la EFV, o se niegan a ofrecer medidas de alivio que pueden acortar la vida.
- La fe religiosa y las creencias espirituales son importantes para muchas personas que se acercan al final de sus vidas.
- El buen morir requiere dejar de concentrarse en prolongar la vida.
Perspectiva del paciente
En un estudio de referencia de pacientes, familiares y proveedores de atención de la salud,[17] se encuestó a pacientes con enfermedad grave, dolientes que estuvieron a cargo del paciente, médicos y otros proveedores de atención de la salud sobre los aspectos importantes de la EFV. Los encuestados calificaron la importancia de 44 atributos que se identificaron en entrevistas previas y sesiones de grupo en las que se les pidió a los participantes que definieran el bien morir. Hubo un amplio consenso en relación con el control del dolor y de otros síntomas, la comunicación y la preparación para la muerte. Sin embargo, ciertos atributos como no sentirse una carga para su familia o la sociedad, o estar en paz con Dios, tuvieron igual importancia para los pacientes, pero no para los médicos. En un estudio con base en la población, realizado en los Países Bajos, se mostró una correlación entre las actitudes positivas de los encuestados hacia el concepto del bien morir y las preferencias que podrían influir en la toma de decisiones en la EFV.[18]
Los pacientes de cáncer en estadio avanzado quizás quieran tener oportunidades para prepararse para la EFV. En una encuesta de 469 pacientes que participaron en un ensayo aleatorizado grupal de cuidados paliativos tempranos,[19,20] se informó que cuanto mejor preparado estuviera el paciente, obtendría puntajes más altos con respecto a la calidad de la comunicación con los médicos, la edad avanzada, el vivir solos, menos síntomas y bienestar espiritual. Curiosamente, el 31 % de los encuestados estaban preocupados por el modo en que su familia enfrentaría las dificultades futuras. Los resultados destacan la importancia de ofrecer a los pacientes la oportunidad de hablar con anticipación sobre la EFV y el hecho de que los pacientes que califican de forma favorable la calidad de la comunicación con sus médicos se sienten más preparados.
Perspectiva de quien cuida del paciente
En un estudio,[21] se entrevistó a las personas a cargo formal e informal de 396 pacientes que murieron de cáncer avanzado sobre la CV del difunto en su última semana de vida. La CV se correlacionó con una variedad de factores obtenidos por medio de entrevistas de referencia sobre difuntos en el momento de la inscripción al estudio y medidas encuestales de los estilos de hacer frente a la situación, formas religiosas para sobrellevar las dificultades, religiosidad o espiritualidad, y preferencias en la EFV. No se pudieron explicar la mayoría de las varianzas de CV en la EFV. Sin embargo, los siguientes son los factores que tienen una correlación negativa con la CV:
- Cuidados intensivos en la última semana.
- Muerte en el hospital.
- Sonda de alimentación en la última semana.
- Quimioterapia en la última semana de vida.
Por el contrario, los siguientes son los factores que tienen una correlación con una mejor CV:
- Oración y meditación.
- Visitas de capellanes.
- Percepción de que el médico fue respetuoso, confiable y estuvo dispuesto a responder preguntas.
Resultados posteriores a las intervenciones para una posible prolongación de la vida
Reanimación cardiopulmonar
En un principio, la reanimación cardiopulmonar (RCP) se diseñó, en mayor medida, para restaurar la circulación de los pacientes con ataques cardíacos. Los resultados posteriores a la RCP en adultos de edad avanzada hospitalizados no mejoraron de manera significativa, en parte, por la práctica de RCP en los pacientes con enfermedades concurrentes y con potencial de provocar la muerte. Se dificulta el abordaje del beneficio limitado de la RCP durante la transición a la EFV porque, en Estados Unidos, los pacientes se someten a RCP, a menos que haya una ONR en la historia clínica que impida el procedimiento. La evidencia que sigue a continuación demuestra la utilidad limitada de la RCP en los pacientes con cáncer avanzado.
- En una revisión retrospectiva de la historia clínica de 41 pacientes que se sometieron a RCP debido a un paro cardiaco provocado por fuera del hospital, se encontró que solo 18 (43 %) sobrevivieron para ingresar en una UCI y solo 9 pacientes lo hicieron para ser dados de alta (2 a sus hogares, 7 a un establecimiento).[22] Los autores notaron que la documentación del estadio avanzado de la enfermedad y el pronóstico adverso se mencionaban con frecuencia en los registros médicos.
- En un metanálisis de estudios de supervivencia después de una RCP hospitalaria, se encontró que la supervivencia para dar de alta fue del 6,2 % en general.[23] Los pacientes con enfermedad avanzada y neoplasias malignas hematológicas sometidos a RCP en la UCI fueron menos propensos a sobrevivir.
- Los investigadores describieron resultados muy adversos en los pacientes reanimados en la UCI.[24,25] Solo 7 de 406 pacientes reanimados (2 %) sobrevivieron para ser dados de alta. El resto murió en el momento del paro provocado (63 %) o en un promedio de 4 días (26 %).
Ingreso en la unidad de cuidados intensivos
Además de la RCP, es posible que los pacientes necesiten respiración mecánica o ingreso en una unidad de cuidados intensivos (UCI). Los resultados son precarios en los pacientes con cáncer avanzado. En un estudio, se notificó que la mediana de supervivencia de 212 pacientes con cáncer avanzado (que se derivaron a un ensayo de fase I) fue de 3,2 semanas.[26] Los pacientes que necesitaron RCP tuvieron una mediana de supervivencia de un día.
No obstante, el diagnóstico subyacente puede ser una variable fundamental para pronosticar el desenlace del paciente. Los pacientes con neoplasias malignas hematológicas pueden tener un mejor pronóstico que aquellos con tumores sólidos. Por ejemplo, en un estudio, se informó que los pacientes con neoplasias malignas hematológicas recién diagnosticadas tenían un 60,7 % de probabilidades de sobrevivir para ser dados de alta y una tasa de supervivencia a 1 año del 43,3 %.[27] En análisis multivariantes, se demostró que el estado de remisión y el ingreso temprano en la UCI fueron factores de riesgo favorables.
Bibliografía
- Kendall M, Harris F, Boyd K, et al.: Key challenges and ways forward in researching the "good death": qualitative in-depth interview and focus group study. BMJ 334 (7592): 521, 2007. [PUBMED Abstract]
- Singer PA, Martin DK, Kelner M: Quality end-of-life care: patients' perspectives. JAMA 281 (2): 163-8, 1999. [PUBMED Abstract]
- Zimmermann C, Burman D, Swami N, et al.: Determinants of quality of life in patients with advanced cancer. Support Care Cancer 19 (5): 621-9, 2011. [PUBMED Abstract]
- Jones JM, McPherson CJ, Zimmermann C, et al.: Assessing agreement between terminally ill cancer patients' reports of their quality of life and family caregiver and palliative care physician proxy ratings. J Pain Symptom Manage 42 (3): 354-65, 2011. [PUBMED Abstract]
- Ryoo JJ, Ordin DL, Antonio AL, et al.: Patient preference and contraindications in measuring quality of care: what do administrative data miss? J Clin Oncol 31 (21): 2716-23, 2013. [PUBMED Abstract]
- Earle CC, Neville BA, Landrum MB, et al.: Trends in the aggressiveness of cancer care near the end of life. J Clin Oncol 22 (2): 315-21, 2004. [PUBMED Abstract]
- Bergman J, Saigal CS, Lorenz KA, et al.: Hospice use and high-intensity care in men dying of prostate cancer. Arch Intern Med 171 (3): 204-10, 2011. [PUBMED Abstract]
- Sheffield KM, Boyd CA, Benarroch-Gampel J, et al.: End-of-life care in Medicare beneficiaries dying with pancreatic cancer. Cancer 117 (21): 5003-12, 2011. [PUBMED Abstract]
- Levin TT, Li Y, Weiner JS, et al.: How do-not-resuscitate orders are utilized in cancer patients: timing relative to death and communication-training implications. Palliat Support Care 6 (4): 341-8, 2008. [PUBMED Abstract]
- Newhouse JP, Garber AM: Geographic variation in health care spending in the United States: insights from an Institute of Medicine report. JAMA 310 (12): 1227-8, 2013. [PUBMED Abstract]
- Keating NL, Landrum MB, Lamont EB, et al.: End-of-life care for older cancer patients in the Veterans Health Administration versus the private sector. Cancer 116 (15): 3732-9, 2010. [PUBMED Abstract]
- Goodman DC, Morden NE, Chang CH, et al.: Trends in Cancer Care Near the End of Life: A Dartmouth Atlas of Health Care Brief. Lebanon, NH: Dartmouth Institute for Health Policy & Clinical Practice, 2013. Available online. Last accessed Jan. 23, 2025.
- Kelley AS, Ettner SL, Morrison RS, et al.: Determinants of medical expenditures in the last 6 months of life. Ann Intern Med 154 (4): 235-42, 2011. [PUBMED Abstract]
- Barnato AE, Herndon MB, Anthony DL, et al.: Are regional variations in end-of-life care intensity explained by patient preferences?: A Study of the US Medicare Population. Med Care 45 (5): 386-93, 2007. [PUBMED Abstract]
- Wright AA, Mack JW, Kritek PA, et al.: Influence of patients' preferences and treatment site on cancer patients' end-of-life care. Cancer 116 (19): 4656-63, 2010. [PUBMED Abstract]
- Ellershaw J, Ward C: Care of the dying patient: the last hours or days of life. BMJ 326 (7379): 30-4, 2003. [PUBMED Abstract]
- Steinhauser KE, Christakis NA, Clipp EC, et al.: Factors considered important at the end of life by patients, family, physicians, and other care providers. JAMA 284 (19): 2476-82, 2000. [PUBMED Abstract]
- Rietjens JA, van der Heide A, Onwuteaka-Philipsen BD, et al.: Preferences of the Dutch general public for a good death and associations with attitudes towards end-of-life decision-making. Palliat Med 20 (7): 685-92, 2006. [PUBMED Abstract]
- Zimmermann C, Swami N, Krzyzanowska M, et al.: Early palliative care for patients with advanced cancer: a cluster-randomised controlled trial. Lancet 383 (9930): 1721-30, 2014. [PUBMED Abstract]
- Wentlandt K, Burman D, Swami N, et al.: Preparation for the end of life in patients with advanced cancer and association with communication with professional caregivers. Psychooncology 21 (8): 868-76, 2012. [PUBMED Abstract]
- Zhang B, Nilsson ME, Prigerson HG: Factors important to patients' quality of life at the end of life. Arch Intern Med 172 (15): 1133-42, 2012. [PUBMED Abstract]
- Hwang JP, Patlan J, de Achaval S, et al.: Survival in cancer patients after out-of-hospital cardiac arrest. Support Care Cancer 18 (1): 51-5, 2010. [PUBMED Abstract]
- Reisfield GM, Wallace SK, Munsell MF, et al.: Survival in cancer patients undergoing in-hospital cardiopulmonary resuscitation: a meta-analysis. Resuscitation 71 (2): 152-60, 2006. [PUBMED Abstract]
- Ewer MS, Kish SK, Martin CG, et al.: Characteristics of cardiac arrest in cancer patients as a predictor of survival after cardiopulmonary resuscitation. Cancer 92 (7): 1905-12, 2001. [PUBMED Abstract]
- Wallace S, Ewer MS, Price KJ, et al.: Outcome and cost implications of cardiopulmonary resuscitation in the medical intensive care unit of a comprehensive cancer center. Support Care Cancer 10 (5): 425-9, 2002. [PUBMED Abstract]
- Fu S, Hong DS, Naing A, et al.: Outcome analyses after the first admission to an intensive care unit in patients with advanced cancer referred to a phase I clinical trials program. J Clin Oncol 29 (26): 3547-52, 2011. [PUBMED Abstract]
- Azoulay E, Mokart D, Pène F, et al.: Outcomes of critically ill patients with hematologic malignancies: prospective multicenter data from France and Belgium--a groupe de recherche respiratoire en réanimation onco-hématologique study. J Clin Oncol 31 (22): 2810-8, 2013. [PUBMED Abstract]
Factores que influyen en las decisiones y los desenlaces en la etapa final de la vida
Aspectos generales
Una interpretación de las pruebas resumidas en la sección Calidad de la atención en la etapa terminal de los pacientes con cáncer avanzado es que a estos pacientes se les suelen administrar, con bastante frecuencia, tratamientos incómodos y tal vez nocivos sin muchas probabilidades de beneficio, y en detrimento de recibir una atención significativa en la EFV. En los estudios de pacientes con cáncer avanzado, se identificaron factores que pueden influir en las decisiones y los resultados relacionados con la atención médica en la etapa terminal.
En esta sección, se le ofrecen al oncólogo percepciones sobre los posibles factores determinantes y que pueden llevar a interacciones más eficaces con el paciente para la planificación de la transición a la atención en la etapa terminal. Sin embargo, a continuación, se destacan varias advertencias sobre los estudios citados:
- El diseño trasversal de la mayoría de los estudios impide llegar a conclusiones sobre la causalidad. Por ejemplo, se pueden frustrar los estudios en los que se demuestra una correlación entre los pronósticos optimistas de un paciente y las decisiones de tratamiento debido la tendencia del paciente que escoge un tratamiento específico a ser optimista sobre del resultado, en lugar de que su optimismo sea la razón fundamental del tratamiento.
- Es posible que las definiciones de cáncer avanzado, las medianas de tiempo de supervivencia de los sujetos inscritos y las metodologías del estudio tengan diferencias importantes en todos los estudios y sesguen las correlaciones notificadas debido a factores de confusión que no se controlan o no se reconocen.
- En análisis multivariantes, muchos de los posibles factores pertinentes se trataron como resultados primarios o secundarios, o solo como una variable. En consecuencia, no siempre se consolidan las relaciones entre la comunicación del paciente con el oncólogo, la toma de decisiones de la atención de la salud cerca de la EFV y los resultados. Sin embargo, las pruebas de múltiples fuentes demuestran nexos plausibles y convincentes.
- Los factores que no guardan relación con la comunicación o la toma de decisiones pueden influir en las decisiones de atención de la salud de los pacientes con cáncer avanzado cercanos a la EFV.
Estudios citados
Tres estudios muy grandes e integrales ofrecen información para caracterizar las relaciones entre los marcadores de comunicación de calidad, toma de decisiones, decisiones sobre la atención de la salud y los resultados en los pacientes con cáncer avanzado. Estos estudios se explican a continuación y sus resultados hacen parte de las secciones posteriores.
- The Study to Understand Prognoses and Preferences for Outcomes and Risks of Treatments (SUPPORT): en este estudio bifásico que se realizó en varios lugares (Ohio, Carolina del Norte, Massachusetts, Wisconsin y California), se evaluó una intervención para mejorar la comprensión por parte del médico de las preferencias del paciente, la documentación y el momento oportuno de las órdenes de no reanimar (ONR), el dolor, el tiempo en cuidados intensivos, el estado de coma o la respiración mecánica antes de la muerte, y el uso de los recursos hospitalarios.[1] La primera fase fue un estudio descriptivo y prospectivo para confirmar los obstáculos y las brechas en la comunicación entre los pacientes y los médicos; la segunda fase fue un ensayo aleatorizado por grupos para probar una intervención que se enfocó en identificar los obstáculos. En la fase I, se inscribió un total de 4301 pacientes y a 4804 en la fase II. La intervención se concentró en proporcionar información confiable sobre el pronóstico, la documentación de las preferencias del paciente y su familia, y los servicios de un enfermero especializado para capacitar a los pacientes y sus familias, facilitando así la comunicación.
En la fase I del SUPPORT, se confirmaron fallas considerables en la comunicación entre los pacientes y los médicos.[2,3] En la fase II, se demostró que la intervención de enfermeros no aumentó las conversaciones sobre las preferencias de RCP ni la concordancia entre los pacientes y sus médicos sobre las preferencias de RCP de los primeros. Tampoco logró disminuir el número de días en la unidad de cuidados intensivos (UCI), la frecuencia de la respiración mecánica ni la intensidad del dolor.
- Estudio sobre cómo lidiar con el cáncer (CwC): en este estudio prospectivo, longitudinal, realizado en varios lugares con pacientes de cáncer terminales y las personas a su cuidado informal, se analizó la influencia de los factores psicosociales en la atención del paciente y el duelo de la persona a su cargo.[4] En el CwC, se inscribieron 718 pacientes y las personas a su cargo entre septiembre de 2002 y agosto de 2008. Los principales criterios de inclusión fueron un diagnóstico de cáncer avanzado (metástasis a distancia y enfermedad resistente a la quimioterapia de primera línea), y la presencia de una persona al cuidado informal del paciente. La mediana de supervivencia general de los pacientes inscritos fue de 4,5 meses.
- The Cancer Care Outcomes Research and Surveillance (CanCORS) Consortium: en este estudio, se inscribieron más de 5000 personas con diagnóstico de cáncer pulmonar o colorrectal entre 2003 y 2005, que se identificaron a las semanas de recibir el diagnóstico mediante un método de comprobación rápida.[5,6] Los pacientes residían en 1 de 5 áreas geográficas (norte de California; Condado de Los Ángeles, en California; Carolina del Norte; Iowa; o Alabama), o recibían atención mediante una organización de mantenimiento de la salud o un hospital de la Administración de la Salud de Veteranos. Se encuestó a los pacientes (o a sus representantes legales, en caso de que el paciente hubiera muerto o no estuviera disponible) mediante formularios computarizados de 4 a 7 meses después del diagnóstico. También se extrajeron las historias clínicas de los adultos que dieron su consentimiento.
Características demográficas de los pacientes
El objetivo de planificar la transición a la atención en la EFV de una forma prudente y considerada es aumentar las probabilidades de que una persona con cáncer avanzado reciba atención de alta calidad en la EFV, acorde con sus preferencias informadas. Hay una variedad de características del paciente que influyen en su interacción con el oncólogo, y en las decisiones o resultados del paciente. En la siguiente sección, se destacan los resultados representativos de los estudios de las características demográficas de los pacientes y otros factores.
Edad
El cáncer es una enfermedad de adultos de edad avanzada.[7] Sin embargo, es importante recordar que es probable que haya diferencias entre las distintas cohortes de adultos de edad avanzada.
- En el ensayo SUPPORT, se mostró la correlación entre una edad mayor y una menor disposición a someterse a tratamientos para prolongar la vida. Fue menos probable que los pacientes de edad avanzada se sometieran a tratamientos intensivos.[1]
- Se entrevistó a 73 pacientes de 70 a 89 años con cáncer de colon metastásico acerca de la toma de decisiones sobre el tratamiento. Menos de la mitad (44 %) de los pacientes deseaba recibir información sobre la supervivencia prevista al tomar decisiones sobre su tratamiento.[8]
- Las mujeres de edad avanzada tienen más probabilidades de someterse a cuidados paliativos cuando se acerca la EFV que las mujeres más jóvenes. En un estudio, se notificó que el 69,6 % de las mujeres que murieron de cáncer de mama metastásico entre 1992 y 1998 en la provincia de Quebec, Canadá, lo hicieron en un hospital para enfermedades agudas.[9] Si bien la mayoría de las mujeres (75 %) tuvieron algunos indicadores de un modelo enfocado en los cuidados paliativos (como se extrajo de la información de dos bases de datos administrativas), fue menos probable que las mujeres menores de 50 años se sometieran a cuidados paliativos que aquellas mayores de 70 años (oportunidad relativa [OR], 1,85).
- En un estudio, se analizaron las relaciones entre la edad, las preferencias del tratamiento y las terapias administradas de una cohorte de 396 pacientes muertos que estaban inscritos en el CwC.[10] Los pacientes mayores de 65 años y aquellos entre 45 y 64 años fueron más propensos que los más jóvenes a preferir y recibir tratamientos para prolongar la vida. No obstante, los pacientes mayores que prefirieron tratamientos para prolongar la vida tuvieron menos probabilidades de recibirlas que los más jóvenes.
Sexo
- En un estudio,[8] los hombres de edad avanzada con cáncer colorrectal metastásico fueron más propensos que las mujeres a desear recibir información sobre su pronóstico (56 vs. 29 %; P < 0,05).
- En otro estudio, se entrevistó a los pacientes con cáncer avanzado antes y después de visitar al oncólogo para hablar sobre los resultados de la exploración. Las mujeres fueron más propensas que los hombres a reconocer que el cáncer era incurable y a identificar su estadio de modo preciso. También fueron más propensas a decir que tuvieron conversaciones sobre su expectativa de vida.[11]
Raza
- En un análisis secundario del CwC, se mostró que los pacientes negros tuvieron mayores probabilidades de recibir tratamientos intensivos que los pacientes blancos cuando se acercaba la EFV. La frecuencia de administración de los tratamientos de intensidad alta cerca de la EFV no se correlaciona con las preferencias expresadas y, a diferencia de los pacientes blancos, las conversaciones sobre la EFV no disminuyeron la probabilidad de administración de tratamientos intensivos.[12] Este efecto relacionado con la raza persistió incluso con la presencia de una ONR en vigor en el momento de la muerte.[13]
- En otro estudio, se analizaron entrevistas con pacientes terminales blancos y afroamericanos a fin de determinar si la calidad de las relaciones con los médicos notificada por los pacientes se correlacionaba con la planificación anticipada de la atención (PAA) y las preferencias por tratamientos para mantener a los pacientes con vida (TPV).[14] Los pacientes afroamericanos notificaron relaciones de menor calidad, pero estas calificaciones más bajas no explicaron las tasas menores de PAA ni las tasas mayores de preferencia por los TPV.
- Es menos probable que los pacientes afroamericanos o de ascendencia asiática se registren en un centro de cuidados paliativos y es más probable que se sometan a tratamientos intensivos, como hospitalizaciones e ingresos en UCI, que los pacientes blancos.[15-17]
Estado socioeconómico
- Es menos probable que los pacientes con Medicaid se sometan a cuidados paliativos que aquellos con Medicare. También es más probable que se les de el alta médica y mueran en centros para enfermedades agudas que en el hogar con un programa de cuidados paliativos.[18][Nivel de evidencia: II];[19] Por el contrario, en una población de Medicaid, es más probable que los pacientes negros muestren pruebas de conversaciones sobre la EFV que los pacientes blancos.[20]
- Los beneficiarios de Medicare inscritos en un programa de atención con contención de los gastos tuvieron una mayor probabilidad de participar en un centro de cuidados paliativos y por períodos más prolongados.[21]
Comprensión del diagnóstico por parte del paciente
En varios estudios, se mostró que hay correlaciones entre la comprensión del diagnóstico por parte del paciente y las decisiones de atención de la salud, los resultados médicos o la adaptación psicológica cuando este se acerca a la etapa terminal. Sin embargo, las diferencias de las metodologías del estudio, las poblaciones de pacientes, las medidas de comprensión del pronóstico y el criterio de valoración estudiado como el criterio primario, descartan conclusiones definitivas sobre la importancia de las correlaciones. Además, solo se puede inferir causalidad, dada la naturaleza trasversal de la mayoría de los estudios. No obstante, un resumen de los datos publicados, organizados según la medición de la comprensión del pronóstico, puede arrojar luz sobre los procesos de toma de decisiones de los pacientes con cáncer avanzado.
- A menudo, los pacientes hacen cálculos demasiado optimistas de sus probabilidades de supervivencia más allá de los 6 meses. Un grupo de investigadores analizó la comprensión del pronóstico (medida como el estimado de supervivencia más allá de los 6 meses) de 917 adultos con cáncer colorrectal o pulmonar metastásico registrados en el SUPPORT.[3] Fue más probable que los pacientes que estimaron una probabilidad del 90 % o más de sobrevivir seis meses prefirieran tratamientos para prolongar la vida y que regresaran al hospital, de que se les intentara practicar RCP o de morir mientras se les administraba respiración mecánica.
- En un análisis secundario de un ensayo controlado aleatorizado de intervenciones de cuidados paliativos en el que participaron 350 pacientes con cáncer de pulmón incurable, metastásico o cáncer digestivo diferente al colorrectal, se evaluaron los desenlaces durante la EFV y la percepción del pronóstico por parte de los pacientes. Estos se incluyeron en un plazo de 8 semanas desde el diagnóstico inicial y se les pidió que notificaran en las semanas 12 y 24, desde la inclusión en el estudio, su estado de salud autopercibido y hasta qué punto sentían que su cáncer era curable. En el análisis se encontró que el 59 % de los pacientes notificaron que su estado de salud era “de enfermedad terminal” en el momento de evaluación más cercano a la muerte, en comparación con el 58 % al inicio (un 59 % permaneció o se volvió exacto, mientras que un 41% permaneció o se volvió inexacto). Un total del 66 % de los participante notificaron que su cáncer era “probablemente curable” en el momento de la evaluación más cercana a la muerte, en comparación con el 71 % en la semana 12 (un 35 % permaneció o se volvió exacto y un 65 % permaneció o se volvió inexacto). Los pacientes que clasificaron el cáncer como probablemente curable fueron menos propensos a ingresar en un programa de cuidados paliativos (OR, 0,25; P = 0,002) o morir en sus hogares (OR, 0,56; P = 0,043), y más propensos a ser hospitalizados en los últimos 30 días de vida (OR, 2,28; P = 0,011).[22][Nivel de evidencia: II]
- Con frecuencia, los pacientes no logran informar de manera correcta el objetivo del tratamiento anticanceroso. Un grupo de investigadores informó que, en el inicio, el 30,4 % de una cohorte de 181 pacientes con cáncer avanzado pensó que el tratamiento era curativo; el 20 % manifestó que no sabía.[23] Fue más probable que quienes no estaban casados, vivían en áreas rurales, murieron en un término de 6 meses o recibían quimioterapia informaran que el objetivo del tratamiento era curativo. A las 12 semanas de la evaluación, menos pacientes informaron que el objetivo fuera la curación, pero la diferencia no fue significativa. Otro estudio descubrió que proporcionar a los pacientes que comenzaban a recibir quimioterapia de segunda línea información escrita y audiovisual, concebida de manera especial, en la que se analiza la finalidad paliativa de su tratamiento, no mejoró la comprensión exacta de los pacientes en cuanto al objetivo del tratamiento.[24]
- Con frecuencia, los pacientes no son conscientes del carácter terminal del diagnóstico del cáncer avanzado. Sin embargo, los pacientes que son conscientes de que su diagnóstico es terminal tienen una calidad de vida (CV) más alta [25] y más probabilidades de recibir atención acorde con sus preferencias.[26,27]
Preferencias del paciente
El respeto a las preferencias de los pacientes es fundamental para una atención del cáncer de alta calidad y para proteger su autonomía. Fue más probable que los pacientes con cáncer avanzado que tuvieron la oportunidad de expresar sus preferencias para la EFV recibieran una atención acorde con sus deseos.[26]
En la actualidad, la evidencia indica que los oncólogos no suelen preguntarles a los pacientes sobre sus preferencias o aclararlas y, en última instancia, no logran proporcionarles una atención que coincida con dichas preferencias. Por ejemplo, en un estudio de 2011 [28] de 128 pacientes de cáncer de pulmón avanzado y recién diagnosticado, se observó lo siguiente:
- El 88,2 % deseaba información sobre la esperanza de vida (52,7 % manifestó que estaba informado).
- El 63,5 % deseaba información sobre los cuidados paliativos (25 % manifestó que estaba informado).
- El 56,8 % deseaba información sobre las decisiones en la EFV (31 % manifestó que estaba informado).
- Ninguno de los pacientes recordó que se le preguntara sobre la información que deseaba recibir.
La observación final destaca la cuestión fundamental sobre la forma en que los oncólogos deben deducir las preferencias del paciente. Si bien la preguntas directas parecen ser el abordaje más sincero, en un estudio con 2 medidas de preferencia concretas, se observó que las preferencias de los pacientes a la hora de decidir parecen diferir con base en la medida que se utilizó.[29]
Aunque no está clara la forma óptima de preguntar sobre las preferencias, algunos estudios han arrojado luz sobre este tema. Los pacientes de cáncer avanzado tienen varias preferencias con posible utilidad para la planificación de la atención en la EFV, como las siguientes:
- Momento y forma en que se les comunica el pronóstico.
- Función de la toma de decisiones.
- Quimioterapia paliativa en lugar de atención paliativa sin quimioterapia.
- CV o duración de la vida.
Las conversaciones sobre las preferencias son complicadas. Es posible que las preferencias se interpreten de manera estricta o reflejen valores fundamentales de la persona. En un estudio sobre la disposición de 337 pacientes de edad avanzada a proporcionar instrucciones anticipadas para la atención en la EFV,[30] el 85 % de los encuestados pensó que era definitivamente necesario (55 %) o moderadamente necesario (30 %) registrar sus deseos en instrucciones por adelantado. Sin embargo, la mayoría (80 %) prefirió el valor general y una declaración de sus objetivos, o instrucciones precisas y generales. Hubo una gran preferencia por las conversaciones entre los representantes legales que decidían en nombre de las personas incapacitadas.[30]
En un estudio de encuesta de 2020, realizado en el Johns Hopkins Hospital, los investigadores entrevistaron a 200 pacientes de oncología quirúrgica y médica acerca de sus preferencias en cuanto a las conversaciones sobre las instrucciones por adelantado, que la encuesta definió como “un documento o escrito que informa a los proveedores de atención acerca del tipo de tratamiento médico que usted desearía si estuviera muy enfermo y no pudiera tomar esas decisiones por sí mismo”.[31] Se observó que:
- El 43,5 % de los pacientes prefería conversar sobre la planificación de la atención avanzada con sus proveedores de atención primaria, en comparación con el 7 %, que prefería conversar con sus cirujanos, y el 5,5 %, que prefería hacerlo con sus oncólogos médicos. Como motivos de estas preferencias, los pacientes mencionaron relaciones de larga duración con sus proveedores de atención primaria y las “fuertes habilidades interpersonales” de dichos proveedores.
- Por lo general, los pacientes preferían que dichas conversaciones tuvieran lugar en una etapa temprana del curso de la enfermedad. Un 48,5 % dijo que pensaba que el momento oportuno era antes del diagnóstico de cáncer, y el 32 % manifestó que era con ocasión del diagnóstico.
- El 82,5 % de los pacientes opinaban que las conversaciones sobre las instrucciones por adelantado deberían iniciarse por el médico, en lugar del paciente.
Preferencia por recibir información sobre el pronóstico
Los pacientes con enfermedades terminales desean más información sobre el pronóstico,[32] creen que dicha información se puede suministrar sin que les haga perder las esperanzas [33] y prefieren que los oncólogos les pregunten sobre sus preferencias en relación con dicha información.[34] El que el paciente sea más joven, sea mujer o tenga una percepción de esperanza de vida más corta se correlaciona con una mayor necesidad de información.[8]
Preferencias por la función de toma de decisiones
Diversas medidas evalúan las preferencias del paciente en relación con la función de tomar decisiones. En la Control Preference Scale,[35] se les pide a los pacientes que seleccionen 1 de 5 afirmaciones que mejor refleje su punto de vista; los resultados se codifican como activo ("prefiero tomar la decisión final"), cooperativo ("prefiero compartir la responsabilidad con mi médico") o pasivo ("prefiero que sea mi médico quien tome la decisión"). La información disponible indica que las preferencias varían ampliamente. No está claro hasta qué punto esta variación en las preferencias se debe a las diferencias entre la enfermedad, los distintos tipos de pacientes o las diferencias metodológicas.
- Se entrevistó a pacientes de entre 70 y 89 años con cáncer colorrectal metastásico sobre su preferencia de función en la toma de decisiones;[8] el 52 % prefirió una función pasiva. La preferencia por una función pasiva fue más frecuente en los pacientes de edad avanzada, las mujeres, o en aquellos con un estado funcional más deficiente o con enfermedad metastásica recién diagnosticada.
- En un estudio separado, un porcentaje similar (47 %) de mujeres entre 31 y 83 años con cáncer de mama metastásico informó sobre su función pasiva en la toma de decisiones relacionadas con la administración de la quimioterapia paliativa. Las mujeres que enfrentaban la decisión sobre la quimioterapia de segunda línea notificaron una tasa mucho más alta de participación activa (43 vs. 33 %; P = 0,06).[36]
- En otro estudio, el 63 % de los pacientes con cáncer avanzado en una clínica de cuidados paliativos prefirió tener una función activa en la toma de decisiones.[37]
Preferencia por la quimioterapia paliativa
En varios estudios, se ha demostrado que la mayoría de los pacientes prefiere la quimioterapia antes de consultar con un oncólogo.[38] Por ejemplo, un grupo de investigadores neerlandeses evaluó el proceso de toma de decisiones de 140 pacientes con cáncer metastásico que consideraban como opciones razonables la quimioterapia paliativa o los mejores cuidados de apoyo disponibles.[39] Antes de la consulta, el 68 % de los pacientes expresó una preferencia por la quimioterapia y, en último término, la eligió el 78 % de los mismos. La única característica del paciente relacionada con la preferencia por el tratamiento fue una menor edad. El factor pronóstico más significativo de la opción de tratamiento fue la preferencia por la preconsulta.
La preferencia por la quimioterapia se puede relacionar, en parte, con las observaciones de que los pacientes no están informados del todo, rechazan la información o la reinterpretan para acomodar sus puntos de vista. Además, es posible que los pacientes valoren más la supervivencia y menos la calidad de vida de lo que los oncólogos anticipan.[40]
Preferencias relacionadas con la duración o calidad de vida
Como se mencionó en la sección Preferencias del paciente, estas se pueden interpretar de manera estricta o amplia. Las preferencias fundamentales para otras más específicas se pueden considerar mejor como valores del paciente.[41] Además de medir la preferencia, los métodos de medición varían de forma considerable. El lector interesado puede consultar una revisión de 2012 [42] para un análisis de los diferentes instrumentos. Se destacan algunas de las observaciones más importantes:
- En análisis multivariantes de un estudio,[43] se observó que la preferencia de los pacientes con cáncer avanzado por la quimioterapia se explicaba debido a los mayores puntajes que asignaron a la duración de la vida y los mejores puntajes para la CV. La última variable se midió mediante el Quality-Quantity Questionnaire (QQQ), en el cual se categoriza a los pacientes como que prefieren la CV, la duración de la vida o ninguna de estas.[44] Las preferencias de los pacientes en la preconsulta se explicaron en mayor medida por preferir la duración antes que la calidad de vida. Dada la carencia de beneficio de supervivencia demostrable de la quimioterapia en el cáncer avanzado, los autores especularon que es posible que los pacientes no reciban información precisa en la consulta que defina de forma clara el objetivo de la quimioterapia.
- En otro estudio,[45] se entrevistó a 125 pacientes ambulatorios con cáncer (en todos los estadios) sobre su disposición al tratamiento. Los pacientes también diligenciaron el cuestionario QQQ. Los investigadores encontraron que los pacientes de edad más avanzada, que estaban cansados o eran más negativos, valoraban menos la CV que los otros. Los pacientes que se encontraban en los 6 meses de diagnóstico consideraron que la duración de la vida era más importante. Sin embargo, se debe tener en cuenta que, en este estudio, los pacientes no calificaron la importancia de la duración en relación con la calidad. Hubo una correlación entre esforzarse para alcanzar la CV y valorar la planificación anticipada de la atención (PAA).
- En un tercer estudio, se inscribieron solo pacientes con cáncer avanzado (459 encuestados) y se les pidió que calificaran el valor relativo de la CV o la duración de la vida.[46] Al 55 % de ellos le dio igual valor a la CV y la duración de la vida, el 27 % prefirió la CV y el 18 %, la duración de la vida. La preferencia por la CV se correlacionó con los pacientes de edad más avanzada, los hombres y los grados más altos de escolaridad. Los pacientes que se inclinaron por la duración de la vida también prefirieron una comunicación menos pesimista por parte de los oncólogos.
Objetivos de atención del paciente
Se consideran que las conversaciones sobre los objetivos de la atención de los pacientes con cáncer avanzado son un componente fundamental de la planificación de la transición a la atención en la EFV. Sin embargo, las definiciones de los objetivos de la atención varían de manera considerable en la bibliografía pertinente. Antes de analizar las observaciones en relación con los objetivos de la atención de los pacientes con cáncer avanzado (y otras enfermedades que acortan la vida), es importante considerar si se debe distinguir entre los objetivos del tratamiento y los objetivos de la atención.
- Algunos investigadores han usado la frase objetivos de la atención para identificar los objetivos de los tratamientos dirigidos a la enfermedad. Quizá sería más claro si dichos objetivos se denominaran objetivos del tratamiento.
- Visto de otra forma, los objetivos de la atención son diferentes de los objetivos relacionados con el tratamiento de la enfermedad con intento de remisión o cura; estos objetivos reflejan el interés de los pacientes y sus familiares después de haber aceptado que las terapias dirigidas a la enfermedad no lograrán los objetivos planteados y buscan "la profunda necesidad humana de sentido, bienestar y rumbo".[47] Desde ese punto de vista, los objetivos de la atención son similares a los atributos que definen el buen morir, según lo que se analizó antes.
Otro punto de vista es que hay una serie continua de objetivos y que la intención de las conversaciones sobre objetivos de atención es ayudar a los pacientes a identificar las alternativas para alcanzarlos. Este punto de vista está respaldado por una revisión estructurada de la bibliografía y un análisis cualitativo de las consultas de cuidados paliativos sobre los objetivos de la atención, como se resume a continuación:
- En un estudio, se analizaron las publicaciones pertinentes para categorizar los objetivos de la atención para los pacientes con enfermedades que acortan la vida.[47] Los autores propusieron seis objetivos integrales: curarse, vivir por más tiempo, mejorar o mantener el funcionamiento, tener CV e independencia, sentir bienestar, lograr los objetivos de vida, y dar apoyo a la familia o a las personas a cargo del cuidado.
- En otro estudio, se notificó un análisis cuantitativo de la comunicación del pronóstico en las consultas de cuidados paliativos.[48] Los investigadores observaron que los médicos especializados en cuidados paliativos empleaban la táctica de excluir ciertos objetivos de atención con el fin de alentar a los pacientes a pensar en otros objetivos. Esta táctica indica que los objetivos relacionados con el tratamiento, a menudo, se remplazan por objetivos más personales, una vez que ya no se recomiende el tratamiento dirigido a la enfermedad.
Hasta el momento, no se dispone de información sobre la influencia positiva o negativa de las conversaciones sobre los objetivos de la atención en los resultados de la atención en la EFV de los pacientes con cáncer avanzado.
Creencias religiosas y valores espirituales de los pacientes
El grado de religiosidad del paciente y el brindarle una atención espiritual que sea acorde con sus preferencias se han correlacionado con los resultados en la EFV. En una serie de informes del CwC,[49-51] se encontró que alrededor de la mitad de los pacientes con enfermedades graves o con potencial de causar la muerte indicó que las creencias religiosas o espirituales eran importantes para ellos, como lo mostraron puntajes más altos en las subescalas Positive Religious Coping Scales de la RCOPE, una medición de las estrategias religiosas para sobrellevar las situaciones difíciles.[52] Los puntajes de la RCOPE fueron significativamente más altos en los pacientes afroamericanos e hispanos.
En los análisis ajustados por diferencias demográficas, los grados más altos de estrategias religiosas positivas para sobrellevar las situaciones difíciles tenían una relación significativa con la administración de respiración mecánica, en comparación con los grados bajos de esas estrategias (11,3 vs. 3,6 %) y los cuidados intensivos para prolongar la vida en la última semana (13,6 vs. 4,2 %).[49] El grado en que el establecimiento de atención médica atiende las preocupaciones religiosas y espirituales puede, en gran medida, afectar la relación. Los pacientes que manifestaron que el equipo médico respondía, en gran medida, a sus necesidades espirituales (26,3 %) tuvieron muchas más probabilidades de recibir cuidados paliativos y menos probabilidades de que se les administrara una atención intensiva; también notificaron una mejor CV. La atención pastoral, recibida por cerca del 46 % de los pacientes, no afectó el hecho de recibir dichos servicios, pero sí la CV justo antes de la muerte.[50]
Conversaciones entre los pacientes y los oncólogos sobre la etapa final de la vida
Recuerdo de las conversaciones sobre la etapa final de la vida
El recuerdo de las conversaciones sobre la atención médica en la EFV influye en las decisiones y los resultados de los pacientes con cáncer avanzado. De 332 pacientes que se inscribieron en el CwC, 123 (37 %) contestaron de forma afirmativa cuando se les preguntó "¿ha hablado con su médico sobre sus deseos particulares relativos a la atención que le gustaría recibir si estuviera muriendo?".[4] El recuerdo de las conversaciones sobre la EFV se relacionó con menores tasas de respiración mecánica, reanimación o ingreso en la UCI, y derivación temprana a programas de cuidados paliativos.
En un análisis posterior, se informó sobre las preferencias de tratamiento de 325 pacientes que murieron al estar inscritos en el CwC.[26] De los pacientes de cáncer avanzado, el 72 % prefirió el tratamiento concentrado en el bienestar, al contestar de manera afirmativa la pregunta: "¿si pudiera escoger, preferiría un plan de atención que se concentre en el alivio del dolor y la incomodidad, incluso si esto significara no vivir por tanto tiempo?"; el 28 % prefirió el tratamiento para prolongar la vida. De los pacientes, el 68 % recibió atención en la EFV acorde con sus preferencias iniciales. Las probabilidades de recibir atención compatible con las preferencias aumentaron si el paciente notificaba una conversación con su médico sobre la EFV (OR = 2,26; P < 0,0001) o sabía que su enfermedad era terminal (OR = 3,94; P = 0,0005).
Carácter de la decisión
Decisión de recibir terapia dirigida al cáncer
Con frecuencia, a los pacientes de cáncer avanzado se les administran varios regímenes quimioterapéuticos en el curso del tratamiento. El hecho de que la decisión comprenda terapia de primera o segunda línea para la enfermedad avanzada puede influir en el proceso de toma de decisiones. Un grupo de investigadores llevó a cabo 117 entrevistas semiestructuradas con 102 mujeres con cáncer de mama avanzado, sometidas a quimioterapia paliativa de primera línea (n = 70) o de segunda línea (n = 47).[36] Fue más probable que las mujeres de la cohorte de segunda línea explicaran su decisión de someterse a quimioterapia porque les daba esperanzas que aquellas de la cohorte de primera línea (43 vs. 19 %; P = 0,006) y que notificaran haber adoptado una función activa en el proceso de toma de decisiones. Otro grupo de investigación mostró que los médicos ejercieron un mayor control sobre las decisiones cuando las pruebas a favor o en contra de un determinado tratamiento eran menos convincentes o si el cáncer estaba avanzado.[53] Por consiguiente, la justificación del paciente para el tratamiento y la pertinencia del punto de vista del oncólogo cambian con el carácter de la decisión.
Decisión de limitar el tratamiento
La mayoría de las muertes por cáncer avanzado están precedidas por decisiones de limitar el tratamiento. Sin embargo, dada la prevalencia, la importancia y la dificultad de estas decisiones, se dispone de información un tanto escasa sobre la forma en que se consideran las preferencias del paciente en el proceso de toma de decisiones.
Con la colaboración de investigadores que hacían parte de equipos de atención de la salud, un grupo de investigadores describió las deliberaciones sobre la posibilidad de limitar los tratamientos con potencial de prolongar la vida de 76 pacientes hospitalizados con un cáncer incurable.[54] Dos tercios de los pacientes prefirieron recibir atención que les proporcionara bienestar y un tercio prefirió la terapia para prolongar la vida. La preferencia de los pacientes por el bienestar coincidió, más a menudo, con la de los oncólogos que la de prolongar la vida (91,4 vs. 46,7 %; P = 0,001). Solo en la mitad de los casos, los pacientes estuvieron involucrados en la decisión de limitar el tratamiento. La edad, el estado funcional o la capacidad de tomar decisiones no afectaron la tasa de participación del paciente; el factor pronóstico más importante fue la coincidencia con las preferencias del oncólogo. Por lo tanto, la decisión de limitar el tratamiento puede reflejar una percepción compartida, en lugar de un proceso conjunto de toma de decisiones.
Bibliografía
- A controlled trial to improve care for seriously ill hospitalized patients. The study to understand prognoses and preferences for outcomes and risks of treatments (SUPPORT). The SUPPORT Principal Investigators. JAMA 274 (20): 1591-8, 1995 Nov 22-29. [PUBMED Abstract]
- Haidet P, Hamel MB, Davis RB, et al.: Outcomes, preferences for resuscitation, and physician-patient communication among patients with metastatic colorectal cancer. SUPPORT Investigators. Study to Understand Prognoses and Preferences for Outcomes and Risks of Treatments. Am J Med 105 (3): 222-9, 1998. [PUBMED Abstract]
- Weeks JC, Cook EF, O'Day SJ, et al.: Relationship between cancer patients' predictions of prognosis and their treatment preferences. JAMA 279 (21): 1709-14, 1998. [PUBMED Abstract]
- Wright AA, Zhang B, Ray A, et al.: Associations between end-of-life discussions, patient mental health, medical care near death, and caregiver bereavement adjustment. JAMA 300 (14): 1665-73, 2008. [PUBMED Abstract]
- Chen AB, Cronin A, Weeks JC, et al.: Palliative radiation therapy practice in patients with metastatic non-small-cell lung cancer: a Cancer Care Outcomes Research and Surveillance Consortium (CanCORS) Study. J Clin Oncol 31 (5): 558-64, 2013. [PUBMED Abstract]
- Ayanian JZ, Chrischilles EA, Fletcher RH, et al.: Understanding cancer treatment and outcomes: the Cancer Care Outcomes Research and Surveillance Consortium. J Clin Oncol 22 (15): 2992-6, 2004. [PUBMED Abstract]
- American Cancer Society: Cancer Facts and Figures 2025. American Cancer Society, 2025. Available online. Last accessed January 16, 2025.
- Elkin EB, Kim SH, Casper ES, et al.: Desire for information and involvement in treatment decisions: elderly cancer patients' preferences and their physicians' perceptions. J Clin Oncol 25 (33): 5275-80, 2007. [PUBMED Abstract]
- Gagnon B, Mayo NE, Hanley J, et al.: Pattern of care at the end of life: does age make a difference in what happens to women with breast cancer? J Clin Oncol 22 (17): 3458-65, 2004. [PUBMED Abstract]
- Parr JD, Zhang B, Nilsson ME, et al.: The influence of age on the likelihood of receiving end-of-life care consistent with patient treatment preferences. J Palliat Med 13 (6): 719-26, 2010. [PUBMED Abstract]
- Fletcher K, Prigerson HG, Paulk E, et al.: Gender differences in the evolution of illness understanding among patients with advanced cancer. J Support Oncol 11 (3): 126-32, 2013. [PUBMED Abstract]
- Loggers ET, Maciejewski PK, Paulk E, et al.: Racial differences in predictors of intensive end-of-life care in patients with advanced cancer. J Clin Oncol 27 (33): 5559-64, 2009. [PUBMED Abstract]
- Mack JW, Paulk ME, Viswanath K, et al.: Racial disparities in the outcomes of communication on medical care received near death. Arch Intern Med 170 (17): 1533-40, 2010. [PUBMED Abstract]
- Smith AK, Davis RB, Krakauer EL: Differences in the quality of the patient-physician relationship among terminally ill African-American and white patients: impact on advance care planning and treatment preferences. J Gen Intern Med 22 (11): 1579-82, 2007. [PUBMED Abstract]
- Smith AK, Earle CC, McCarthy EP: Racial and ethnic differences in end-of-life care in fee-for-service Medicare beneficiaries with advanced cancer. J Am Geriatr Soc 57 (1): 153-8, 2009. [PUBMED Abstract]
- Haas JS, Earle CC, Orav JE, et al.: Lower use of hospice by cancer patients who live in minority versus white areas. J Gen Intern Med 22 (3): 396-9, 2007. [PUBMED Abstract]
- Mullins MA, Ruterbusch JJ, Clarke P, et al.: Trends and racial disparities in aggressive end-of-life care for a national sample of women with ovarian cancer. Cancer 127 (13): 2229-2237, 2021. [PUBMED Abstract]
- Singh S, Molina E, Perraillon M, et al.: Post-Acute Care Outcomes of Cancer Patients <65 Reveal Disparities in Care Near the End of Life. J Palliat Med 26 (8): 1081-1089, 2023. [PUBMED Abstract]
- Mack JW, Chen K, Boscoe FP, et al.: Underuse of hospice care by Medicaid-insured patients with stage IV lung cancer in New York and California. J Clin Oncol 31 (20): 2569-79, 2013. [PUBMED Abstract]
- Sharma RK, Dy SM: Documentation of information and care planning for patients with advanced cancer: associations with patient characteristics and utilization of hospital care. Am J Hosp Palliat Care 28 (8): 543-9, 2011. [PUBMED Abstract]
- McCarthy EP, Burns RB, Ngo-Metzger Q, et al.: Hospice use among Medicare managed care and fee-for-service patients dying with cancer. JAMA 289 (17): 2238-45, 2003. [PUBMED Abstract]
- Gray TF, Plotke R, Heuer L, et al.: Perceptions of prognosis and end-of-life care outcomes in patients with advanced lung and gastrointestinal cancer. Palliat Med 37 (5): 740-748, 2023. [PUBMED Abstract]
- Craft PS, Burns CM, Smith WT, et al.: Knowledge of treatment intent among patients with advanced cancer: a longitudinal study. Eur J Cancer Care (Engl) 14 (5): 417-25, 2005. [PUBMED Abstract]
- Enzinger AC, Uno H, McCleary N, et al.: Effectiveness of a Multimedia Educational Intervention to Improve Understanding of the Risks and Benefits of Palliative Chemotherapy in Patients With Advanced Cancer: A Randomized Clinical Trial. JAMA Oncol 6 (8): 1265-1270, 2020. [PUBMED Abstract]
- Yun YH, Kwon YC, Lee MK, et al.: Experiences and attitudes of patients with terminal cancer and their family caregivers toward the disclosure of terminal illness. J Clin Oncol 28 (11): 1950-7, 2010. [PUBMED Abstract]
- Mack JW, Weeks JC, Wright AA, et al.: End-of-life discussions, goal attainment, and distress at the end of life: predictors and outcomes of receipt of care consistent with preferences. J Clin Oncol 28 (7): 1203-8, 2010. [PUBMED Abstract]
- Loh KP, Seplaki CL, Sanapala C, et al.: Association of Prognostic Understanding With Health Care Use Among Older Adults With Advanced Cancer: A Secondary Analysis of a Cluster Randomized Clinical Trial. JAMA Netw Open 5 (2): e220018, 2022. [PUBMED Abstract]
- Pardon K, Deschepper R, Vander Stichele R, et al.: Are patients' preferences for information and participation in medical decision-making being met? Interview study with lung cancer patients. Palliat Med 25 (1): 62-70, 2011. [PUBMED Abstract]
- Gattellari M, Ward JE: Measuring men's preferences for involvement in medical care: getting the question right. J Eval Clin Pract 11 (3): 237-46, 2005. [PUBMED Abstract]
- Hawkins NA, Ditto PH, Danks JH, et al.: Micromanaging death: process preferences, values, and goals in end-of-life medical decision making. Gerontologist 45 (1): 107-17, 2005. [PUBMED Abstract]
- Kubi B, Istl AC, Lee KT, et al.: Advance Care Planning in Cancer: Patient Preferences for Personnel and Timing. JCO Oncol Pract 16 (9): e875-e883, 2020. [PUBMED Abstract]
- Fried TR, Bradley EH, O'Leary J: Prognosis communication in serious illness: perceptions of older patients, caregivers, and clinicians. J Am Geriatr Soc 51 (10): 1398-403, 2003. [PUBMED Abstract]
- Hagerty RG, Butow PN, Ellis PM, et al.: Communicating with realism and hope: incurable cancer patients' views on the disclosure of prognosis. J Clin Oncol 23 (6): 1278-88, 2005. [PUBMED Abstract]
- Hagerty RG, Butow PN, Ellis PM, et al.: Communicating prognosis in cancer care: a systematic review of the literature. Ann Oncol 16 (7): 1005-53, 2005. [PUBMED Abstract]
- Degner LF, Sloan JA: Decision making during serious illness: what role do patients really want to play? J Clin Epidemiol 45 (9): 941-50, 1992. [PUBMED Abstract]
- Grunfeld EA, Maher EJ, Browne S, et al.: Advanced breast cancer patients' perceptions of decision making for palliative chemotherapy. J Clin Oncol 24 (7): 1090-8, 2006. [PUBMED Abstract]
- Bruera E, Sweeney C, Calder K, et al.: Patient preferences versus physician perceptions of treatment decisions in cancer care. J Clin Oncol 19 (11): 2883-5, 2001. [PUBMED Abstract]
- Kiely BE, Stockler MR, Tattersall MH: Thinking and talking about life expectancy in incurable cancer. Semin Oncol 38 (3): 380-5, 2011. [PUBMED Abstract]
- Koedoot CG, de Haan RJ, Stiggelbout AM, et al.: Palliative chemotherapy or best supportive care? A prospective study explaining patients' treatment preference and choice. Br J Cancer 89 (12): 2219-26, 2003. [PUBMED Abstract]
- Harrington SE, Smith TJ: The role of chemotherapy at the end of life: "when is enough, enough?". JAMA 299 (22): 2667-78, 2008. [PUBMED Abstract]
- Epstein RM, Peters E: Beyond information: exploring patients' preferences. JAMA 302 (2): 195-7, 2009. [PUBMED Abstract]
- Blinman P, King M, Norman R, et al.: Preferences for cancer treatments: an overview of methods and applications in oncology. Ann Oncol 23 (5): 1104-10, 2012. [PUBMED Abstract]
- Koedoot CG, Oort FJ, de Haan RJ, et al.: The content and amount of information given by medical oncologists when telling patients with advanced cancer what their treatment options are. palliative chemotherapy and watchful-waiting. Eur J Cancer 40 (2): 225-35, 2004. [PUBMED Abstract]
- Stiggelbout AM, de Haes JC, Kiebert GM, et al.: Tradeoffs between quality and quantity of life: development of the QQ Questionnaire for Cancer Patient Attitudes. Med Decis Making 16 (2): 184-92, 1996 Apr-Jun. [PUBMED Abstract]
- Voogt E, van der Heide A, Rietjens JA, et al.: Attitudes of patients with incurable cancer toward medical treatment in the last phase of life. J Clin Oncol 23 (9): 2012-9, 2005. [PUBMED Abstract]
- Meropol NJ, Egleston BL, Buzaglo JS, et al.: Cancer patient preferences for quality and length of life. Cancer 113 (12): 3459-66, 2008. [PUBMED Abstract]
- Kaldjian LC, Curtis AE, Shinkunas LA, et al.: Goals of care toward the end of life: a structured literature review. Am J Hosp Palliat Care 25 (6): 501-11, 2008 Dec-2009 Jan. [PUBMED Abstract]
- Norton SA, Metzger M, DeLuca J, et al.: Palliative care communication: linking patients' prognoses, values, and goals of care. Res Nurs Health 36 (6): 582-90, 2013. [PUBMED Abstract]
- Phelps AC, Maciejewski PK, Nilsson M, et al.: Religious coping and use of intensive life-prolonging care near death in patients with advanced cancer. JAMA 301 (11): 1140-7, 2009. [PUBMED Abstract]
- Balboni TA, Paulk ME, Balboni MJ, et al.: Provision of spiritual care to patients with advanced cancer: associations with medical care and quality of life near death. J Clin Oncol 28 (3): 445-52, 2010. [PUBMED Abstract]
- Maciejewski PK, Phelps AC, Kacel EL, et al.: Religious coping and behavioral disengagement: opposing influences on advance care planning and receipt of intensive care near death. Psychooncology 21 (7): 714-23, 2012. [PUBMED Abstract]
- Pargament KI, Smith BW, Koenig HG, et al.: Patterns of positive and negative religious coping with major life stressors. J Sci Study Relig 37 (4): 710-24, 1998.
- Keating NL, Beth Landrum M, Arora NK, et al.: Cancer patients' roles in treatment decisions: do characteristics of the decision influence roles? J Clin Oncol 28 (28): 4364-70, 2010. [PUBMED Abstract]
- Winkler EC, Reiter-Theil S, Lange-Riess D, et al.: Patient involvement in decisions to limit treatment: the crucial role of agreement between physician and patient. J Clin Oncol 27 (13): 2225-30, 2009. [PUBMED Abstract]
Posibles obstáculos para planificar la transición a la atención en la etapa final de la vida
Las preferencias de los pacientes con cáncer avanzado deben, en gran medida, determinar la atención que reciben. Sin embargo, la evidencia indica que los pacientes no tienen suficientes oportunidades para determinar sus preferencias de una manera informada y, como resultado, pueden buscar atención que no sea acorde con sus valores u objetivos personales. Para obtener más información, consultar la sección Factores que influyen en las decisiones y los desenlaces en la etapa final de la vida.
En esta sección, se identifican los posibles obstáculos que pueden impedir que un paciente de cáncer avanzado y su oncólogo tengan una conversación sobre el pronóstico, los objetivos, las opciones y las preferencias.[1] La información permitirá al oncólogo diseñar estrategias necesarias para abordar estas conversaciones difíciles de una manera más cautelosa.
Los siguientes son los posibles obstáculos:
- Interpretación del pronóstico por parte del paciente.
- Falta de acuerdo entre el paciente y el oncólogo.
- Conductas comunicativas del oncólogo.
- Ideas erróneas de los oncólogos sobre el perjuicio de tocar el tema sobre la etapa final de la vida (EFV).
- Actitudes y preferencias del oncólogo.
- Rembolso del costo de la quimioterapia y aspectos económicos del tratamiento.
- Incertidumbre sobre opciones diferentes de los tratamientos dirigidos a la enfermedad.
Interpretación del pronóstico por parte del paciente
Un hallazgo constante de las dos últimas décadas es que los pacientes de cáncer en estadio avanzado suelen ser demasiado optimistas en cuanto a su esperanza de vida o la posibilidad de curación mediante el uso de terapias dirigidas a la enfermedad.
- En un estudio de 1193 pacientes del Cancer Care Outcomes Research and Surveillance (CanCORS) Consortium, se observó que la gran mayoría de pacientes de cáncer de pulmón o colorrectal en estadio avanzado no comprendió que el tratamiento no era curativo. El 69 % de los pacientes no entendió que era improbable que la quimioterapia curara el cáncer.[2] Fue más probable que los pacientes que no eran blancos, que recibieron un diagnóstico de cáncer colorrectal o que declararon estar satisfechos con la comunicación del médico notificaran una comprensión inexacta del propósito del tratamiento.
- De modo similar, el 64 % de los pacientes con cáncer de pulmón incurable que se sometieron a radioterapia no entendió que existía la probabilidad de que no se curara el cáncer. Fue más probable que los pacientes de mayor edad y los que no eran blancos no lo entendieran; en cambio, era más probable que los representantes legales de los pacientes sí lo entendieran.[3]
Hay muchos posibles obstáculos para lograr un entendimiento más exacto del pronóstico, como una comunicación precaria por parte de los oncólogos. No obstante, los pacientes también interpretan la información de acuerdo con razones que no están relacionadas con la calidad de la comunicación. Los puntos de vista de los pacientes con cáncer en estadio avanzado que se inscriben en ensayos clínicos de fase I, o de los representantes legales que deben tomar las decisiones por los pacientes en la unidad de cuidados intensivos (UCI), ayudan a comprender mejor la razón por la que es posible que estos pacientes malinterpreten la información pronóstica.
- Las expectativas optimistas de los pacientes en cuanto al beneficio de los ensayos de fase I se relacionaron con mejor calidad de vida, fe religiosa más profunda, optimismo, menores conocimientos matemáticos básicos (capacidad de entender cálculos estadísticos o resultados del tratamiento) y aversión al riesgo financiero. No tuvieron relación con edad, sexo, nivel educativo ni estado funcional.[4]
- En un estudio de 163 pacientes inscritos en un ensayo de fase I, la mayoría conocía los programas de cuidados paliativos (81 %) o la asistencia paliativa (84 %), pero solo unos pocos consideraron de manera seria una de las 2 opciones (programa de cuidados paliativos, 10 %; asistencia paliativa, 7 %). El 75 % los pacientes informó que la influencia más importante fue enterarse de que el cáncer se estaba diseminando; el 63 % afirmó que saber que el fármaco administrado en la fase I eliminaba las células cancerosas fue el factor principal para tomar la decisión de inscribirse en el ensayo.[5]
- En un estudio de 80 representantes legales encargados de la toma de decisiones, provenientes de familias con pacientes en la UCI, la mayoría interpretó la información cuantitativa de forma muy exacta y los cálculos cualitativos que proporcionaron los médicos de la UCI de un modo menos ambiguo. No obstante, la necesidad de expresar optimismo, la creencia de que la fortaleza del paciente prevalece por encima del pronóstico y la desconfianza en que el médico realice un diagnóstico exacto son varias posibles fuentes importantes de malentendidos relacionados con el pronóstico.[6]
Falta de un acuerdo entre el paciente y el oncólogo
Varias conversaciones entre los pacientes de cáncer avanzado y sus médicos deben llevar a la comprensión del pronóstico, los objetivos, las preferencias, las opciones y el proceso de toma de decisiones. Sin embargo, las pruebas indican que los pacientes y los oncólogos, a menudo, no llegan a las mismas conclusiones sobre estos aspectos. No está clara la forma en que este desacuerdo afecta la transición a la atención en la EFV. No obstante, es poco probable que el desacuerdo o las percepciones equivocadas sobre los objetivos del tratamiento, por ejemplo, puedan contribuir de forma positiva a la planificación oportuna de la transición a la atención en la EFV.
Comprensión del pronóstico
Un grupo de investigadores analizó los cálculos del pronóstico de 917 adultos con cáncer pulmonar o colorrectal metastásico que estaban inscritos en el Study to Understand Prognoses and Preferences for Outcomes and Risks of Treatments (SUPPORT) y de sus médicos.[7] Se destacaron tres conclusiones:
- Los pacientes fueron más optimistas que los médicos.
- Los cálculos de los médicos estaban más ajustados a la supervivencia observada que los de los pacientes.
- Los pacientes, más optimistas que los oncólogos, fueron más propensos a elegir tratamientos para prolongar la vida.
La escasa concordancia entre los pacientes y los oncólogos se ha observado en una amplia gama de pacientes, como en aquellos con leucemia mieloide aguda [8] o quienes consideran trasplantes de células madre alogénicos.[9] Para obtener más información, consultar la sección Interpretación del pronóstico por parte del paciente.
La discordancia sobre la expectativa de vida de los pacientes con cáncer en estadio avanzado y los oncólogos tal vez se deba a la mala comunicación o a factores independientes de los pronósticos que calculan los oncólogos. Un grupo de investigadores intentó aclarar la fuente de esta discordancia pronóstica mediante una encuesta a 236 pacientes de cáncer avanzado que participaron en un ensayo clínico aleatorizado de una intervención sobre comunicación.[10] Se solicitó a los pacientes y sus 38 oncólogos que proporcionaran un cálculo de la probabilidad de que los pacientes estuvieran vivos en 2 años. Las respuestas posibles se fijaron en el 100 %, alrededor del 90 %, alrededor del 75 %, alrededor del 50 %, alrededor del 25 %, alrededor del 10 % y el 0 %. La discordancia se definió por la presencia de más de una categoría de respuesta divergente.
Como se esperaba, la mayoría de las díadas de paciente y oncólogo fueron discordantes (161 de 236 calificaciones [68 %]; intervalo de confianza [IC], 95 %; 62–75 %), y casi todos los pacientes discordantes expresaron un pronóstico más optimista (155 de 161 pacientes [96 %]).[10] Los investigadores también pidieron a los pacientes que trataran de predecir el cálculo que proporcionarían sus oncólogos. Las categorías de las respuestas y la definición de la discordancia fueron idénticas. De los 161 pacientes que disintieron con sus oncólogos, 144 (89 %) no estaban al tanto de la discrepancia. Se observó una mayor probabilidad de expectativas de pronóstico discordantes en los pacientes que no eran blancos. El ingreso de los pacientes, el nivel de educación, el sexo o el nivel de recuerdo de la comunicación sobre el pronóstico no se correlacionó con la discordancia. Estos resultados respaldan la creencia de que la discordancia pronóstica refleja una comunicación inadecuada de los cálculos pronósticos. Sin embargo, es posible que las expresiones del paciente sobre la expectativa de vida también reflejen la necesidad de optimismo o la creencia de que tienen características personales únicas.[6]
Objetivos del tratamiento
Con frecuencia, los pacientes y los oncólogos no coinciden en la interpretación de los objetivos del tratamiento del cáncer. Un grupo de investigadores notificó que de las díadas de pacientes de cáncer avanzado y los médicos entrevistados, en el 25 % de los casos el paciente pensó que el objetivo del tratamiento era curar la enfermedad, cuando este no era el caso.[11] Fue más probable que los pacientes más jóvenes, aquellos que eran hablantes nativos de inglés y quienes recibieron información escrita coincidieran con sus oncólogos en la intención de la quimioterapia. Otro grupo de investigadores notificó que el 64 % de los pacientes con cáncer de pulmón avanzado no comprendía que la radioterapia que se les prescribió no era curativa.[3]
En un estudio de 206 pacientes con cáncer y sus 11 oncólogos, se intentó identificar qué tanto comprendían estos oncólogos los objetivos de la atención proporcionada a sus pacientes, definidos como la preferencia por la calidad de vida versus la preferencia por una mayor expectativa de vida.[12] Los investigadores entrevistaron a los oncólogos y pacientes al inicio, y luego repitieron la entrevista cada 3 meses por 15 meses (hasta que el paciente falleciera o ingresara a un programa de cuidados paliativos). Se les mostró a los participantes una escala visual analógica con una puntuación que llegaba hasta 100, esta escala tenía en un extremo la frase "la calidad de vida es lo más importante" (puntuación 0) y en el extremo opuesto la frase "la expectativa de vida es lo más importante" (puntuación 100). Se le pidió a los pacientes y oncólogos que asignaran una puntuación de la escala para cada respuesta a las siguientes dos preguntas: "teniendo en cuenta la atención que recibe, ¿qué es lo más importante para usted en este momento?" (pacientes) y "teniendo en cuenta la atención que le proporciona a este paciente ¿qué cree que es lo más importante para el paciente en este momento?" (oncólogos). Los participantes que obtuvieron una puntuación de 0 a 30 se clasificaron como aquellos cuyo objetivo principal era el bienestar, mientras que los que obtuvieron puntuaciones de 70 a 100 tenían como objetivo principal la supervivencia. Se cree que la díada de paciente y oncólogo coinciden más cuando ambos asignan puntuaciones dentro del mismo intervalo de 30 puntos para un objetivo importante ya sea el bienestar (puntaje 0–30) o la supervivencia (puntaje 70–100). Sin embargo, en la última entrevista previa al fallecimiento del paciente, el 76,7 % de las díadas de paciente y oncólogo no coincidieron.[12]
Temas de la consulta que se recuerdan
Los investigadores informaron que los pacientes y los oncólogos, con frecuencia, recordaban varios aspectos de la comunicación y de la toma de decisiones a partir de conversaciones en los ensayos de fase I.[13] Por ejemplo, 13 de 17 oncólogos que participaron mencionaron el pronóstico en menos del 50 % de las consultas. Si bien los oncólogos notificaron con frecuencia las conversaciones sobre el pronóstico, solo estuvieron de acuerdo el 12 % de los pacientes y el 20 % de los investigadores independientes que codificaron y registraron los resultados. Hubo mayor coincidencia sobre los efectos adversos desconocidos y el carácter voluntario de la inscripción en el ensayo.
Preferencia del paciente por adoptar la función de toma de decisiones
Con frecuencia, los oncólogos no identifican de manera correcta las preferencias de los pacientes por adoptar funciones de toma de decisiones. A continuación, se resumen los resultados de unos pocos estudios ilustrativos.
- En un estudio de pacientes de edad avanzada con cáncer colorrectal metastásico, el 52 % prefirió una función pasiva. Sin embargo, los oncólogos solo identificaron de forma correcta las preferencias de los pacientes en el 41 % de los casos.[14]
- Los médicos especializados en cuidados paliativos solo identificaron de manera correcta las preferencias relacionadas con la toma de decisiones de los pacientes con cáncer avanzado de clínicas de cuidados paliativos en el 38 % de los casos.[15]
Evaluación del estado funcional del paciente
Los médicos evalúan el estado funcional (EF) del paciente al hacer el pronóstico y tomar las decisiones sobre el tratamiento. Los investigadores del Eastern Cooperative Oncology Group compararon el ECOG notificado por los médicos y 1.636 pacientes de cáncer pulmonar o colorrectal avanzado,[16] y demostraron un desacuerdo entre los pacientes y los médicos con respecto al EF en 56,6% de los casos; un mayor optimismo por parte del médico por el EF (media, 0,91 vs. 1,30) y una relación de desacuerdo con un aumento del riesgo más alto de muerte.
Preferencia del paciente por la reanimación cardiopulmonar
En la fase inicial del SUPPORT, se observó que solo el 47 % de los médicos sabía cuándo sus pacientes querían evitar la reanimación cardiopulmonar (RCP).[17] En un análisis posterior, los investigadores estudiaron a 520 pacientes con cáncer colorrectal metastásico.[18] Aunque se disponía de información sobre las preferencias de RCP de 339 pacientes, 223 (63 %) deseaba RCP, los médicos no lograron identificar de forma correcta la preferencia del paciente en el 30 % de los casos. La preferencia por RCP fue más marcada en los pacientes con una actitud más optimista en relación con la supervivencia a dos meses. Otros investigadores observaron resultados similares en un grupo de pacientes con neumopatía.[19] A menudo, los médicos interpretaron de forma errónea las preferencias de los pacientes (25–40 % de las díadas). La falta de acuerdo fue mayor si los pacientes no deseaban recibir reanimación. En ningún estudio se informó sobre el efecto del desacuerdo en los resultados del paciente.
Conducta del oncólogo en la comunicación
En esta sección, se incluye un resumen de la evidencia que identifica la carencia de comunicación por parte de los oncólogos que tratan a pacientes con cáncer avanzado. Las pruebas indica de forma clara que, con frecuencia, la comunicación entre el paciente y el médico no se basa del todo en la toma de decisiones informadas y conjuntas. Esta información permitirá a los oncólogos reflexionar sobre sus hábitos comunicativos y considerar la modificación de los impedimentos, a fin de planificar de manera oportuna la transición a la atención en la EFV.
Estudios de observación sobre la comunicación entre el paciente y el oncólogo
Los investigadores informaron sobre un estudio de consultas grabadas entre 1 de 9 oncólogos y 118 pacientes de cáncer avanzado.[20] Idearon un sistema de codificación para evaluar la frecuencia con que se revelaba información importante (por ejemplo, objetivo del tratamiento, imposibilidad de curar el cáncer, riesgos del tratamiento, información sobre la esperanza de vida y otras opciones de tratamiento) y el grado en que el médico facilitaba la participación del paciente en la toma de decisiones. A continuación, se incluye un resumen de los resultados con observaciones independientes que se citan según corresponda.
- La mayoría de los oncólogos reveló la intención no curativa de la quimioterapia en los casos de cáncer avanzado, pero pocos hablaron sobre las alternativas a la quimioterapia. En el 74,6 % de los encuentros, se les informó a los pacientes que el cáncer no se podía curar. No obstante, en solo el 57,6 % de los encuentros, se les informó a los pacientes sobre la esperanza de vida y en el 44,6 % de estos, se les ofrecieron opciones de tratamiento.
- En escasas ocasiones, los oncólogos comprobaron si los pacientes habían comprendido de forma correcta. Solo en el 10 % de los encuentros, les preguntaron si comprendían la información revelada y el proceso de toma de decisiones que se les comunicaba.
- Con frecuencia, se carecía de los elementos fundamentales para la toma conjunta de decisiones. Los oncólogos participantes, a menudo, reconocieron la incertidumbre del beneficio del tratamiento (72,9 %), hablaron sobre soluciones intermedias para recibir tratamiento (60,2 %) y le preguntaron al paciente sobre sus puntos de vista con respecto a este (69,5 %). Sin embargo, solo al 29,7 % de los pacientes se les ofreció una alternativa y en solo el 10,2 % de los encuentros los oncólogos evaluaron la comprensión del paciente.
Las siguientes son otras fallas comunicativas de los oncólogos:
- A menudo, los oncólogos usan un lenguaje ambiguo o falsamente tranquilizante, como afirmaciones optimistas inadecuadas. Un grupo de investigadores analizó las grabaciones de los encuentros entre los oncólogos y los pacientes, en los que los primeros proporcionaron una probabilidad de cura con los tratamientos actuales.[21] Las grabaciones se seleccionaron según el grado de coincidencia con el pronóstico y, luego, se codificaron para determinar los factores que determinaron dicha coincidencia. Los oncólogos fueron más propensos a hacer afirmaciones optimistas, pero fue más probable que las afirmaciones pesimistas aumentaran el grado de coincidencia con el pronóstico. Los autores concluyeron que la mejor estrategia de comunicación puede incluir ser consciente de que es posible que la tendencia al optimismo interfiera en la comprensión del pronóstico por parte del paciente y esforzarse por hablar sinceramente, según lo justifique el pronóstico.
- Con frecuencia, los oncólogos no hablan sobre el beneficio de supervivencia anticipado de la quimioterapia en los casos de cáncer avanzado. Un grupo de investigadores mostró que en 26 de 37 consultas analizadas, los oncólogos no informaron al paciente sobre los posibles beneficios de supervivencia de la quimioterapia paliativa (es decir, sin intención curativa).[22]
Formas de comunicar el pronóstico notificadas por los oncólogos
Existe evidencia que indica que la actitud de los médicos al comunicar el pronóstico influye en el conocimiento que tienen los pacientes sobre el mismo. En un análisis de encuestas a médicos del Cancer Care Outcomes Research and Surveillance (CanCORS) Consortium,[23] los investigadores notificaron que los pacientes con cáncer de pulmón o colorrectal metastásico tenían más probabilidad de conocer de forma exacta el pronóstico si su médico principal había notificado que hablaron sobre este antes, en lugar de esperar hasta que se presentara el deterioro del paciente (18,5 vs. 7,6 %; oportunidad relativa, 3,23; intervalo de confianza 95 %, 1,39–7,52; P = 0,006). Por lo tanto, resulta apropiado entender los factores que influyen en las actitudes de los oncólogos con el fin de mejorar la comunicación del pronóstico. Se publicaron 2 encuestas adicionales de oncólogos estadounidenses y la comunicación del pronóstico. En un estudio, se analizaron las respuestas a la encuesta de 729 oncólogos (tasa de respuesta del 64 %).[24] Casi todos (98 %) indicaron que revelarían un pronóstico de cáncer terminal, pero el 48 % indicó que solo lo haría cuando se conociera la preferencia del paciente en cuanto a la divulgación del diagnóstico. Menos de la mitad (43 %) de los oncólogos proporcionó siempre un cálculo estimado del tiempo restante hasta la muerte. Tres cuartas partes indicaron que no recibieron capacitación formal para comunicar pronósticos de tipos de cáncer terminal, y el 96 % opinó que este tipo de capacitación debería ser obligatoria.
En otro estudio, se notificó que el 65 % de los médicos encuestados hablaron de inmediato sobre el pronóstico con los pacientes asintomáticos que presentaron cáncer en estadio avanzado y cuya esperanza de vida prevista era de 4 a 6 meses.[25] No obstante, menos médicos hablarían de inmediato sobre la preferencia por la reanimación (44 %), los programas de cuidados paliativos (26 %) o el lugar preferido para morir (21 %); la mayoría de ellos preferiría esperar hasta que los pacientes presentaran síntomas o hasta que no hubiera más tratamientos que ofrecer. Fue más probable que los médicos, los cirujanos y los oncólogos más jóvenes hablaran sobre el pronóstico que aquellos que no eran especialistas en cáncer.
Ideas erróneas de los oncólogos sobre el perjuicio de las conversaciones sobre la etapa final de la vida
Los oncólogos citan varias razones para su negativa a iniciar conversaciones sobre la EFV. No obstante, varios estudios han proporcionado pruebas de que muchas de sus preocupaciones (por ejemplo, causar perjuicios psicológicos o disipar las esperanzas) no son válidas.[26][Nivel de evidencia: II] Por el contrario, las conversaciones sobre la EFV no causan perjuicios y pueden mejorar la adaptación psicológica, ya que la información explícita sobre el pronóstico no afecta necesariamente las esperanzas del paciente.
- En un estudio de cohortes longitudinal, prospectivo y realizado en varios lugares, se notificó que las conversaciones sobre la atención en la EFV no causaron perjuicios psicológicos. Los pacientes con cáncer avanzado que contestaron de forma afirmativa a la pregunta: "¿ha hablado con sus médicos sobre el tipo de atención que le gustaría recibir si estuviera muriendo?" no tuvieron una tasa más alta de trastorno por ansiedad generalizada ni de trastorno depresivo grave que los pacientes que no recordaban haber tenido esas conversaciones (3,3 vs. 1,4 % y 8,3 vs. 5,8 %, respectivamente).[27] Además, el hecho de recordar dichas conversaciones no tuvo relación con los grados de preocupación.
- En otro estudio, se encontró que la ansiedad del paciente por haber conocido la información y por la toma de decisiones fue pasajera o pudo haber facilitado la adaptación psicológica. La cantidad de información revelada por los oncólogos no anticipó los grados de ansiedad del paciente.[20] Sin embargo, un mayor grado de estímulo del paciente para participar en la toma de decisiones tuvo una relación independiente con grados más elevados de ansiedad, justo después de la consulta y en las 2 semanas posteriores.
En otro estudio, los hombres con cáncer avanzado, en quienes se calcularon menores probabilidades de supervivencia a los 6 meses, presentaron un mayor grado de ansiedad y depresión.[28] No obstante, los hombres que manifestaron haber tenido una conversación completa sobre el pronóstico con sus oncólogos tuvieron un menor grado de depresión y grados similares de ansiedad. Por consiguiente, las conversaciones sobre el pronóstico moderaron las relaciones con la ansiedad y la depresión, y pueden haber facilitado la adaptación psicológica a largo plazo.
- En un estudio, se encontró que una revelación explícita del pronóstico y la reconfirmación de que no se les iba a abandonar fueron útiles para los pacientes. Los investigadores estudiaron la forma en que reaccionaron algunas pacientes de cáncer de mama y mujeres sanas a 2 grados de revelación pronóstica y reconfirmación que se representaron en 4 secuencias de video diferentes.[29] La explicitud y la reconfirmación disminuyeron la incertidumbre y la ansiedad. Los autores advirtieron que los hallazgos son de carácter experimental.
Actitudes y preferencias del oncólogo
Los estudios indican con claridad que las actitudes y las preferencias de los oncólogos afectan sus conductas de comunicación y toma de decisiones, de tal forma, que pueden cambiar las decisiones de los pacientes sobre la EFV.
En un estudio, se observó que el personal hospitalario atribuyó las variaciones en el grado de intensidad de los cuidados hacia la etapa terminal a las características del médico, incluidas sus creencias, actitudes y socialización en la práctica de su profesión.[30] Como resultado, hubo una variación significativa entre los médicos en relación con la comunicación sobre las instrucciones anticipadas, el pronóstico, la limitación del tratamiento hacia la EFV y el reconocimiento de que el paciente estaba muriendo. En un estudio de 2011, se observó que los médicos pueden recomendar a los pacientes tratamientos diferentes de los que elegirían para ellos mismos.[31] En esta sección, se anima a los oncólogos a reflexionar sobre estos sesgos y sobre cómo reducir al mínimo sus efectos en la comunicación.
Preferencias de los oncólogos por los tratamientos que no son curativos
Los oncólogos influencian la forma en que los pacientes comprenden las preferencias de tratamiento. Un grupo de investigadores neerlandeses encuestó a algunos oncólogos sobre sus preferencias por la quimioterapia paliativa (que no son curativos) o la observación mediante el uso de casos prácticos.[32] Ni el sexo, ni la edad, ni la situación laboral del oncólogo, ni el tipo de hospital influyeron en las preferencias por la quimioterapia. No obstante, los pacientes de edad avanzada o aquellos que no manifestaron sus preferencias tuvieron menos probabilidades de recibir quimioterapia. Hubo una mayor preferencia por la quimioterapia si el aumento previsto de supervivencia era de al menos 3 meses, si el grado de toxicidad del tratamiento era bajo o si se habían identificado los síntomas de progresión de la enfermedad. Estas conclusiones son compatibles con un estudio de oncólogos estadounidenses en el que se mostró una preferencia por el tratamiento para mantener a los pacientes con vida en lugar de la atención para brindarles bienestar.[33]
Los oncólogos y la toma conjunta de decisiones
En las encuestas, los oncólogos respaldan de forma amplia el concepto de toma conjunta de decisiones. Sin embargo, la investigación empírica demuestra que, con frecuencia, los hábitos comunicativos no reflejan la toma conjunta de decisiones.
Un grupo de investigadores entrevistó a especialistas en cáncer australianos sobre la práctica de incluir a los pacientes en la toma de decisiones e identificó varios factores que influyen en la participación de los pacientes.[34] Los factores relacionados con la enfermedad fueron los siguientes:
- Estadio de la enfermedad.
- Disponibilidad de opciones de tratamiento.
- Riesgos para el paciente.
Además, fue importante tanto la percepción pública de la enfermedad como la posibilidad de que hubiera una mejor opción de tratamiento. Fue más probable que los especialistas en cáncer incluyeran a los pacientes en la toma de decisiones cuando el estadio de la enfermedad era avanzado y las opciones de tratamiento no eran tan claras. Las siguientes son las características de los pacientes que disminuyeron los esfuerzos de los médicos para involucrarlos:
- Mayor ansiedad.
- Edad más avanzada.
- Sexo femenino.
- Origen mediterráneo o de Europa del Este.
- Vida profesional ocupada.
Los médicos conocían las preferencias de los pacientes en relación con su participación, pero tuvieron la impresión de que la mayoría defería la decisión a su pericia. Es más, pocos médicos tenían una estrategia válida para determinar las preferencias de los pacientes.
Actitudes de los oncólogos hacia los cuidados terminales
Las actitudes hacia la atención en la etapa terminal también pueden afectar la comunicación y la toma de decisiones de los oncólogos. En un estudio cualitativo de 18 oncólogos académicos a los que se les pidió que reflexionaran sobre las muertes recientes de pacientes, un grupo de investigadores notificó que aquellos que consideraban la atención en la EFV como parte importante de su trabajo, sentían mayor satisfacción profesional.[35] Otros investigadores determinaron, mediante una encuesta a oncólogos japoneses, la carga que sienten los oncólogos sobre sus hombros al recomendar suspender el tratamiento del cáncer;[36] el 47 % notificó sentir una carga agobiante. En análisis multivariantes sobre los determinantes del sentido de carga, se identificaron los siguientes cofactores:
- Sensación de que se priva de esperanza al paciente.
- Preocupación por que la familia culpe al médico.
- Preocupación por que el paciente pierda el control.
- Preocupación por que no hubo tiempo suficiente para hablar sobre la recomendación.
Rembolso del costo de la quimioterapia y aspectos económicos del tratamiento
Antes de 2003, el rembolso por la quimioterapia excedía, en gran medida, el costo de adquisición para los oncólogos. Aunque el margen de ganancia ha disminuido, el tratamiento continúa siendo una fuente considerable de ingresos para los oncólogos. Un grupo de investigadores mostró que las tasas de rembolso no afectaron la decisión de los médicos de prescribir quimioterapia a los pacientes de cáncer avanzado, pero fue más probable que prescribieran regímenes más costosos cuando estos tenían tasas más altas de rembolso.[37] A continuación, se resumen otros resultados:
- Los urólogos que adquirieron equipos para administrar radioterapia de intensidad modulada (RIM) aumentaron su administración (del 13,1 al 32,3 %) en comparación con quienes no prestaban este servicio (del 14,3 al 15,6 %).[38] La tasa de los programas de cáncer de la National Comprehensive Cancer Network permaneció en el 8 %.
- Es más probable que los oncólogos que trabajan en un esquema de pago por servicio o quienes reciben un salario con incentivos por productividad informen que sus ingresos aumentan con la prescripción de órdenes altas de quimioterapia o de factores de crecimiento.[39]
Incertidumbre sobre las opciones diferentes de los tratamientos dirigidos a la enfermedad
Un obstáculo final a la planificación de la transición a la atención en la EFV puede ser el lenguaje confuso con el que se enfrentan los pacientes al ponderar si deben someterse a la reanimación u otras intervenciones para prolongar la vida. Con base en su experiencia y comprensión, los oncólogos, los pacientes y sus familias asignan valores diferentes (y a menudo, válidos) a términos, como de apoyo o paliativo. En una revisión sistemática de la bibliografía en 2013, se encontraron grandes contradicciones entre las definiciones de cuidados médicos de apoyo, cuidados paliativos y programas de cuidados paliativos.[40]
Para obtener información sobre las definiciones de los términos y un análisis sobre la comunicación clara del propósito de cada grado de cuidado para los pacientes con cáncer avanzado, consultar la sección Factores que influyen en las decisiones y los desenlaces en la etapa final de la vida.
Bibliografía
- Quill TE, Holloway RG: Evidence, preferences, recommendations--finding the right balance in patient care. N Engl J Med 366 (18): 1653-5, 2012. [PUBMED Abstract]
- Weeks JC, Catalano PJ, Cronin A, et al.: Patients' expectations about effects of chemotherapy for advanced cancer. N Engl J Med 367 (17): 1616-25, 2012. [PUBMED Abstract]
- Chen AB, Cronin A, Weeks JC, et al.: Expectations about the effectiveness of radiation therapy among patients with incurable lung cancer. J Clin Oncol 31 (21): 2730-5, 2013. [PUBMED Abstract]
- Weinfurt KP, Castel LD, Li Y, et al.: The correlation between patient characteristics and expectations of benefit from Phase I clinical trials. Cancer 98 (1): 166-75, 2003. [PUBMED Abstract]
- Agrawal M, Grady C, Fairclough DL, et al.: Patients' decision-making process regarding participation in phase I oncology research. J Clin Oncol 24 (27): 4479-84, 2006. [PUBMED Abstract]
- Zier LS, Sottile PD, Hong SY, et al.: Surrogate decision makers' interpretation of prognostic information: a mixed-methods study. Ann Intern Med 156 (5): 360-6, 2012. [PUBMED Abstract]
- Weeks JC, Cook EF, O'Day SJ, et al.: Relationship between cancer patients' predictions of prognosis and their treatment preferences. JAMA 279 (21): 1709-14, 1998. [PUBMED Abstract]
- Sekeres MA, Stone RM, Zahrieh D, et al.: Decision-making and quality of life in older adults with acute myeloid leukemia or advanced myelodysplastic syndrome. Leukemia 18 (4): 809-16, 2004. [PUBMED Abstract]
- Lee SJ, Fairclough D, Antin JH, et al.: Discrepancies between patient and physician estimates for the success of stem cell transplantation. JAMA 285 (8): 1034-8, 2001. [PUBMED Abstract]
- Gramling R, Fiscella K, Xing G, et al.: Determinants of Patient-Oncologist Prognostic Discordance in Advanced Cancer. JAMA Oncol 2 (11): 1421-1426, 2016. [PUBMED Abstract]
- Lennes IT, Temel JS, Hoedt C, et al.: Predictors of newly diagnosed cancer patients' understanding of the goals of their care at initiation of chemotherapy. Cancer 119 (3): 691-9, 2013. [PUBMED Abstract]
- Douglas SL, Daly BJ, Lipson AR, et al.: Association between strong patient-oncologist agreement regarding goals of care and aggressive care at end-of-life for patients with advanced cancer. Support Care Cancer 28 (11): 5139-5146, 2020. [PUBMED Abstract]
- Jenkins V, Solis-Trapala I, Langridge C, et al.: What oncologists believe they said and what patients believe they heard: an analysis of phase I trial discussions. J Clin Oncol 29 (1): 61-8, 2011. [PUBMED Abstract]
- Elkin EB, Kim SH, Casper ES, et al.: Desire for information and involvement in treatment decisions: elderly cancer patients' preferences and their physicians' perceptions. J Clin Oncol 25 (33): 5275-80, 2007. [PUBMED Abstract]
- Bruera E, Sweeney C, Calder K, et al.: Patient preferences versus physician perceptions of treatment decisions in cancer care. J Clin Oncol 19 (11): 2883-5, 2001. [PUBMED Abstract]
- Schnadig ID, Fromme EK, Loprinzi CL, et al.: Patient-physician disagreement regarding performance status is associated with worse survivorship in patients with advanced cancer. Cancer 113 (8): 2205-14, 2008. [PUBMED Abstract]
- A controlled trial to improve care for seriously ill hospitalized patients. The study to understand prognoses and preferences for outcomes and risks of treatments (SUPPORT). The SUPPORT Principal Investigators. JAMA 274 (20): 1591-8, 1995 Nov 22-29. [PUBMED Abstract]
- Haidet P, Hamel MB, Davis RB, et al.: Outcomes, preferences for resuscitation, and physician-patient communication among patients with metastatic colorectal cancer. SUPPORT Investigators. Study to Understand Prognoses and Preferences for Outcomes and Risks of Treatments. Am J Med 105 (3): 222-9, 1998. [PUBMED Abstract]
- Downey L, Au DH, Curtis JR, et al.: Life-sustaining treatment preferences: matches and mismatches between patients' preferences and clinicians' perceptions. J Pain Symptom Manage 46 (1): 9-19, 2013. [PUBMED Abstract]
- Gattellari M, Voigt KJ, Butow PN, et al.: When the treatment goal is not cure: are cancer patients equipped to make informed decisions? J Clin Oncol 20 (2): 503-13, 2002. [PUBMED Abstract]
- Robinson TM, Alexander SC, Hays M, et al.: Patient-oncologist communication in advanced cancer: predictors of patient perception of prognosis. Support Care Cancer 16 (9): 1049-57, 2008. [PUBMED Abstract]
- Audrey S, Abel J, Blazeby JM, et al.: What oncologists tell patients about survival benefits of palliative chemotherapy and implications for informed consent: qualitative study. BMJ 337: a752, 2008. [PUBMED Abstract]
- Liu PH, Landrum MB, Weeks JC, et al.: Physicians' propensity to discuss prognosis is associated with patients' awareness of prognosis for metastatic cancers. J Palliat Med 17 (6): 673-82, 2014. [PUBMED Abstract]
- Daugherty CK, Hlubocky FJ: What are terminally ill cancer patients told about their expected deaths? A study of cancer physicians' self-reports of prognosis disclosure. J Clin Oncol 26 (36): 5988-93, 2008. [PUBMED Abstract]
- Keating NL, Landrum MB, Rogers SO, et al.: Physician factors associated with discussions about end-of-life care. Cancer 116 (4): 998-1006, 2010. [PUBMED Abstract]
- Cohen MG, Althouse AD, Arnold RM, et al.: Is Advance Care Planning Associated With Decreased Hope in Advanced Cancer? JCO Oncol Pract 17 (2): e248-e256, 2021. [PUBMED Abstract]
- Wright AA, Zhang B, Ray A, et al.: Associations between end-of-life discussions, patient mental health, medical care near death, and caregiver bereavement adjustment. JAMA 300 (14): 1665-73, 2008. [PUBMED Abstract]
- Cripe LD, Rawl SM, Schmidt KK, et al.: Discussions of life expectancy moderate relationships between prognosis and anxiety or depression in men with advanced cancer. J Palliat Med 15 (1): 99-105, 2012. [PUBMED Abstract]
- van Vliet LM, van der Wall E, Plum NM, et al.: Explicit prognostic information and reassurance about nonabandonment when entering palliative breast cancer care: findings from a scripted video-vignette study. J Clin Oncol 31 (26): 3242-9, 2013. [PUBMED Abstract]
- Larochelle MR, Rodriguez KL, Arnold RM, et al.: Hospital staff attributions of the causes of physician variation in end-of-life treatment intensity. Palliat Med 23 (5): 460-70, 2009. [PUBMED Abstract]
- Ubel PA, Angott AM, Zikmund-Fisher BJ: Physicians recommend different treatments for patients than they would choose for themselves. Arch Intern Med 171 (7): 630-4, 2011. [PUBMED Abstract]
- Koedoot CG, De Haes JC, Heisterkamp SH, et al.: Palliative chemotherapy or watchful waiting? A vignettes study among oncologists. J Clin Oncol 20 (17): 3658-64, 2002. [PUBMED Abstract]
- Kozminski MA, Neumann PJ, Nadler ES, et al.: How long and how well: oncologists' attitudes toward the relative value of life-prolonging v. quality of life-enhancing treatments. Med Decis Making 31 (3): 380-5, 2011 May-Jun. [PUBMED Abstract]
- Shepherd HL, Butow PN, Tattersall MH: Factors which motivate cancer doctors to involve their patients in reaching treatment decisions. Patient Educ Couns 84 (2): 229-35, 2011. [PUBMED Abstract]
- Jackson VA, Mack J, Matsuyama R, et al.: A qualitative study of oncologists' approaches to end-of-life care. J Palliat Med 11 (6): 893-906, 2008. [PUBMED Abstract]
- Otani H, Morita T, Esaki T, et al.: Burden on oncologists when communicating the discontinuation of anticancer treatment. Jpn J Clin Oncol 41 (8): 999-1006, 2011. [PUBMED Abstract]
- Jacobson M, O'Malley AJ, Earle CC, et al.: Does reimbursement influence chemotherapy treatment for cancer patients? Health Aff (Millwood) 25 (2): 437-43, 2006 Mar-Apr. [PUBMED Abstract]
- Mitchell JM: Urologists' use of intensity-modulated radiation therapy for prostate cancer. N Engl J Med 369 (17): 1629-37, 2013. [PUBMED Abstract]
- Malin JL, Weeks JC, Potosky AL, et al.: Medical oncologists' perceptions of financial incentives in cancer care. J Clin Oncol 31 (5): 530-5, 2013. [PUBMED Abstract]
- Hui D, De La Cruz M, Mori M, et al.: Concepts and definitions for "supportive care," "best supportive care," "palliative care," and "hospice care" in the published literature, dictionaries, and textbooks. Support Care Cancer 21 (3): 659-85, 2013. [PUBMED Abstract]
Cuidados médicos de apoyo, cuidados paliativos y programas de cuidados paliativos para el cáncer avanzado
Importancia del nombre
Las encuestas han identificado el término cuidados paliativos como un posible impedimento para la derivación a clínicas que prestan este tipo de atención.[1] En un informe de 2013 de una sola institución en la que se cambió el nombre de su servicio de cuidados paliativos por servicio de cuidados médicos de apoyo, se demostró que los pacientes ambulatorios se derivaban más pronto después del primer ingreso en el hospital (mediana, 9,2 vs. 13,2 meses; P < 0,001) y más pronto después del primer diagnóstico de cáncer avanzado (mediana, 5,2 vs. 6,9 meses; P < 0,001).[2] A pesar de que no está claro cómo interpretan los pacientes estos términos diversos, los investigadores de un estudio de 2018 que ofreció a pacientes de cáncer de mama información por escrito sobre cuidados médicos de apoyo, cuidados paliativos y cuidados paliativos para enfermos terminales, encontraron que los pacientes notificaron más interés y se mostraban más abiertos a aceptar artículos sobre cuidados médicos de apoyo, versus cuidados paliativos para enfermos terminales o atención paliativa.[3][Nivel de evidencia: II]
Actitudes de los oncólogos hacia los cuidados paliativos
La European Society of Medical Oncology encuestó a sus miembros sobre las actitudes hacia los cuidados paliativos y su participación en estos por parte de los pacientes con cáncer avanzado.[4] De los encuestados, un 88 % respaldó la creencia de que los oncólogos deben coordinar la atención en la EFV, pero el 42 % pensó que no tenía la capacitación suficiente para hacerlo. Relativamente pocos encuestados colaboraron con un especialista en cuidados paliativos (35 %) o con los servicios prestados en programas de cuidados paliativos (26 %).
Actitudes públicas hacia los cuidados paliativos
Las actitudes públicas hacia los cuidados paliativos dependen de la descripción del servicio. En 2011, en una encuesta de opinión pública a más de 100 consumidores, se encontró una falta de conocimiento sobre los cuidados paliativos de más del 75 % de los encuestados.[5] Después de la encuesta, se revisó la definición de cuidados paliativos para el público. En la nueva definición, los cuidados paliativos se describen como "cuidados médicos especializados para las personas con enfermedades graves". El objetivo principal de la atención se define como el alivio del dolor y de otros síntomas, con independencia del diagnóstico. La definición incorpora la calidad de vida (CV) del paciente y su familia, el grupo interdisciplinario de especialistas y la afirmación de que los cuidados paliativos son adecuados en todas las edades, en cualquier estadio de la enfermedad y en conjunto con el tratamiento curativo.[5]
Mejores cuidados médicos de apoyo
La capacidad de administrar varios ciclos de quimioterapia de forma inocua depende de una serie de intervenciones para reducir al mínimo los efectos adversos. La mayoría de oncólogos aceptan que anticipar, reconocer y responder a los efectos adversos frecuentes con antieméticos, factores de crecimiento hematopoyéticos para reducir las transfusiones de eritrocitos o el riesgo de infecciones relacionadas con neutrocitopenia, transfusiones, ansiolíticos o antidepresivos, y analgésicos para el dolor son un conjunto de habilidades en el ámbito de la oncología. En este ámbito, los cuidados médicos de apoyo son auxiliares al objetivo de potenciar los beneficios del tratamiento dirigido a la enfermedad, al reducir al mínimo el posible deterioro de la CV relacionada con la salud del paciente.
Hay tres aspectos del término cuidados médicos de apoyo que son pertinentes para esta sección:
- No se presta suficiente atención a los síntomas o a la CV relacionada con la salud en las evaluaciones oncológicas de rutina. Aunque los oncólogos pueden sobrestimar su habilidad, es prudente derivar a los pacientes con síntomas molestos a médicos con interés particular en la CV relacionada con la salud y especializados en el tratamiento de los síntomas. El objetivo es siempre ofrecer cuidados médicos de apoyo óptimos; en ocasiones, es posible que se necesite un especialista en cuidados paliativos.
- El término mejores cuidados médicos de apoyo se ha usado para describir la atención que reciben los pacientes cuando ya no reciben tratamiento dirigido a la enfermedad. Es poco probable que los mejores cuidados médicos de apoyo (incluso cuando se especifican en los protocolos) se confundan con la atención paliativa especializada que se provee a los pacientes de cáncer avanzado.
- Es posible que los médicos que derivan y sus pacientes prefieran el término cuidados médicos de apoyo, ya que evita la connotación negativa del término cuidados paliativos.
Cuidados paliativos
Los cuidados paliativos constituyen un modelo interdisciplinario de atención que se centra en los pacientes con enfermedades graves, o que ponen en peligro la vida, y en sus familias. Los siguientes son los objetivos de los cuidados paliativos:
- Reducir la carga agobiante de la enfermedad, aliviar el sufrimiento y mantener la CV por medio de intervenciones para conservar el bienestar físico, psicológico, social y espiritual.
- Mejorar la comunicación y la coordinación de la atención.
- Garantizar que la atención sea acorde con los valores y las preferencias del paciente.
- Asegurar que la muerte trascurra con el menor sufrimiento y las mayores oportunidades para su conclusión.
En general, son los médicos, los profesionales clínicos de práctica avanzada, los enfermeros, los trabajadores sociales o los capellanes quienes proveen los cuidados paliativos. Los equipos de cuidados paliativos se suelen concentrar en los siguientes aspectos:
- Alivio de los síntomas que no están controlados.
- Objetivos de la atención.
- Sufrimiento relacionado con el proceso de la muerte.
- Carga para la familia.
Los cuidados paliativos constituyen tanto una filosofía de atención como un sistema organizado y muy estructurado. Además, van más allá del modelo tradicional de la enfermedad para incluir los objetivos de la atención, como los siguientes:
- Mejor CV.
- Optimización del funcionamiento.
- Toma activa e informada de decisiones.
- Oportunidades de cierre y crecimiento personal.
Los cuidados paliativos se pueden proveer de forma simultánea a aquellos para prolongar la vida o como el objetivo principal de la atención. Para obtener más información, consultar la sección Integración de los cuidados paliativos y la atención convencional del cáncer.
El término cuidados paliativos se ha usado, con frecuencia, para comunicar la intención no curativa de la quimioterapia en los pacientes de cáncer avanzado o para designar, sin aclarar el objetivo, la transición a partir de la quimioterapia. Este uso puede contribuir a la sensación persistente y generalizada de que los cuidados paliativos equivalen a la atención en la EFV. Sin embargo, los cuidados paliativos son una estrategia especializada para atender a los pacientes con enfermedades graves o que ponen en peligro la vida; guiados por criterios y logrados (aunque no de forma exclusiva) mediante un conjunto de capacidades diferentes de aquellas necesarias para prescribir y administrar la quimioterapia.
Cuidados paliativos para enfermos terminales
Los cuidados paliativos para enfermos terminales son una estrategia de equipo para proveer atención médica especializada, control del dolor y apoyo emocional o espiritual a los pacientes cuya esperanza de vida es, como máximo, de 6 meses. Para obtener más información en inglés, consulte Hospice.
Bibliografía
- Fadul N, Elsayem A, Palmer JL, et al.: Supportive versus palliative care: what's in a name?: a survey of medical oncologists and midlevel providers at a comprehensive cancer center. Cancer 115 (9): 2013-21, 2009. [PUBMED Abstract]
- Dalal S, Palla S, Hui D, et al.: Association between a name change from palliative to supportive care and the timing of patient referrals at a comprehensive cancer center. Oncologist 16 (1): 105-11, 2011. [PUBMED Abstract]
- Fishman JM, Greenberg P, Bagga MB, et al.: Increasing Information Dissemination in Cancer Communication: Effects of Using "Palliative," "Supportive," or "Hospice" Care Terminology. J Palliat Med 21 (6): 820-824, 2018. [PUBMED Abstract]
- Cherny NI, Catane R; European Society of Medical Oncology Taskforce on Palliative and Supportive Care: Attitudes of medical oncologists toward palliative care for patients with advanced and incurable cancer: report on a survery by the European Society of Medical Oncology Taskforce on Palliative and Supportive Care. Cancer 98 (11): 2502-10, 2003. [PUBMED Abstract]
- Center to Advance Palliative Care: 2011 Public Opinion Research on Palliative Care: A Report Based on Research by Public Opinion Strategies. New York, NY: The Center to Advance Palliative Care, 2011. Available online. Last accessed Jan. 23, 2025.
Estrategias para mejorar la comunicación y la toma de decisiones entre el paciente de cáncer avanzado y el oncólogo
Hay varias estrategias que pueden mejorar la calidad de la comunicación y la toma de decisiones entre el paciente y el oncólogo, y facilitar la transición a la atención en la EFV para los pacientes de cáncer avanzado. Para obtener más información, consultar la sección Educación y capacitación en comunicación en el ámbito del cáncer en Comunicación en la atención del cáncer.
En esta sección se resume la información pertinente a las siguientes estrategias:
- Mejorar la determinación del pronóstico o la comunicación de este.
- Fomentar la planificación anticipada de la atención.
- Proporcionar materiales a los pacientes para preparar su consulta con el oncólogo.
- Usar ayudas para la toma de decisiones.
- Integrar los servicios de cuidados paliativos especializados a la atención convencional del cáncer.
Mejorar la realización del pronóstico
Una revisión integral de las diferentes estrategias para mejorar la realización del pronóstico está más allá del alcance de este resumen. Recientemente se publicó un estudio con un resumen conciso.[1] Se dispone de varias fuentes de información pronóstica:
- Pronóstico clínico de la supervivencia.
- Estado funcional del paciente.
- La calidad de vida (CV) relacionada con la salud y autonotificada por el paciente, es un factor pronóstico en los pacientes de cáncer avanzado. En un estudio de pacientes con cáncer de pulmón de células no pequeñas (CPCNP) localmente avanzado, se remplazaron los factores pronósticos clásicos, incluso la escala de Karnofsky (KPS) por los puntajes del European Organization for Research and Treatment of Cancer Quality of Life Questionnaire C30 (EORTC QLQ-C30) (KPS) en análisis multivariantes.[2] Los pacientes con puntajes del EORTC QLQ-C30 de 66,7 o más tuvieron una mediana de supervivencia general (SG) de 27,1 meses en comparación con 15,4 meses de los pacientes con puntajes más bajos. Sin embargo, puede ser suficiente una sola medición de la CV.
Otros investigadores informaron sobre el efecto pronóstico de un solo ítem de CV autonotificado en una cohorte de al menos 2500 pacientes con cáncer de pulmón recién diagnosticado.[3] Los pacientes con un deterioro clínico considerable de la CV tuvieron una mediana de supervivencia de 1,6 años en comparación con 5,6 años para aquellos sin deterioro. Otros factores pronósticos importantes fueron la edad más avanzada, el estado funcional más precario y el estadio avanzado de la enfermedad; la medición de la CV mantuvo un efecto independiente en los análisis multivariantes.
- Sistemas pronósticos formales en los que se usan variables múltiples.
Nuevas estrategias para mejorar la comunicación del pronóstico
En un estudio australiano, se mostró que la mayoría de pacientes con cáncer metastásico deseaba tener información sobre la esperanza de vida o el pronóstico; algunos pacientes opinaron que sería aceptable recibir estimaciones del desenlace en los peores y mejores casos, así como en los casos típicos.[4] Otros investigadores propusieron que los percentiles derivados de varias curvas de SG publicadas de cáncer metastásico servirían como base para estimar los mejores y peores casos.[5] Su trabajo posterior estableció lo siguiente:
- El método es confiable y preciso. En el caso de la quimioterapia de primera línea para el cáncer de mama metastásico o el CPCNP, los investigadores podrían estimar los desenlaces de forma precisa al usar varios múltiplos de la mediana derivada de una curva de SG.[6] Por ejemplo, para los pacientes con cáncer de mama metastásico, la estimación de la supervivencia en el peor de los casos fue de 6,3 meses y, en el mejor de los casos, de 55,8 meses. La precisión fue menor en la estimación del peor de los casos. Se han demostrado resultados similares para el cáncer de pulmón avanzado.[7]
- Los cálculos de supervivencia de los oncólogos pueden servir como medios razonables para determinar los desenlaces en el peor y mejor de los casos, así como en los casos típicos. Los investigadores usaron las respuestas de los oncólogos, a quienes se les pidió que estimaran el tiempo de supervivencia de cada paciente con cáncer avanzado inscrito en un ensayo aleatorizado, con enmascaramiento doble y controlado con placebo de sertralina.[8] Se pidió a los oncólogos que registraran sus estimaciones como una mediana de tiempo para un grupo de pacientes idénticos. La precisión de los cálculos de los oncólogos se definió por la proporción de pacientes con un tiempo de supervivencia observado limitado por múltiplos prestablecidos del cálculo de tiempo de supervivencia. La mediana de SG de la cohorte de 114 pacientes fue de 11 meses. De los pacientes, 63 % tuvo una supervivencia observada que osciló entre la mitad y el doble de las estimaciones de los oncólogos. A pesar de que los autores concluyeron que las estimaciones de los oncólogos pueden servir como base para determinar la supervivencia, hubo otros factores, como la el KPS que tuvieron mayor valor pronóstico del desenlace en análisis multivariantes.
- Esta estrategia es una forma razonable de comunicar la esperanza de vida, según lo consideran las personas con cáncer. Un grupo de pacientes de cáncer respondió a una encuesta después de analizar dos formatos en los que se explicaba la esperanza de vida de un paciente hipotético: en cada uno de los casos (típico, el mejor o el peor) o la mediana de supervivencia. La mayoría de los encuestados estuvieron de acuerdo con que la explicación de los tres casos tendría sentido, sería útil, y les daría esperanzas y tranquilidad.[9] En relación con la información sobre su propia esperanza de vida, 88 % de los encuestados prefirió que se les presentara información de los tres casos.
Planificación anticipada de la atención
La Ley de Autodeterminación del Paciente de 1990 garantiza al paciente el derecho de aceptar o rechazar el tratamiento, y de preparar instrucciones médicas anticipadas, a fin de documentar sus preferencias en la EFV o de asignar a alguien para tomar las decisiones en su lugar, en caso de que se viera afectada su capacidad de hacerlo. Sin embargo, los estudios indican que muchos pacientes no han participado en la planificación anticipada de la atención (PAA). Hay varias posibles razones que explican la escasa PAA:[10-12]
- En estudios iniciales de PAA, no se mostró una mejora anticipada de los resultados.
- Tanto los médicos como los pacientes son ambivalentes con respecto a la PAA.
- La preferencia del paciente puede cambiar con el tiempo.
- Hubo una falla al trasferir información sobre las preferencias entre los entornos de los pacientes hospitalizados y ambulatorios u otros establecimientos de atención médica.
En esta sección, se incluye un glosario de términos de PAA y se destaca la ambivalencia que la rodea. También se incluye un análisis de pruebas posteriores que demuestran el beneficio de la PAA y se indica que un enfoque flexible de la PAA mejorará la atención hacia la EFV en los pacientes con cáncer avanzado.
Términos de la planificación anticipada de la atención
Un glosario breve de términos de la planificación anticipada de la atención (PAA) puede reducir al mínimo la confusión.
- Instrucciones por adelantado: documento jurídico formal que entra en vigor cuando un paciente está incapacitado o no es capaz de hablar por sí mismo. Este documento, está autorizado por las leyes estatales, permite a los pacientes mantener su autonomía personal al formular instrucciones en caso de incapacidad para tomar decisiones. Los dos elementos principales de las instrucciones anticipadas son un testamento vital y un poder notarial duradero para la atención médica.
- Testamento vital: documento escrito en el que se informa al oncólogo la forma en que el paciente desea ser tratado en caso de que esté muriendo o en estado permanente de inconsciencia, y sea incapaz de tomar decisiones sobre su tratamiento. En un testamento vital, los pacientes pueden especificar los procedimientos para prolongar la vida que deseen y que no deseen, y las condiciones en las que se debe realizar cada elección. Es posible que los pacientes también preparen documentos separados para expresar sus deseos específicos sobre otros tratamientos médicos, como las trasfusiones sanguíneas, la donación de órganos y tejidos, y la diálisis renal.
- Poder notarial duradero para la atención médica: también se conoce como poder para cuidados de la salud. Documento jurídico en el que se autoriza a otra persona (apoderado para la atención médica, representante legal o agente para la atención de la salud) para tomar decisiones médicas cuando el paciente esté incapacitado para hacerlo. Es importante que el apoderado esté familiarizado con los valores y los deseos del paciente a fin de poderlos comunicar correctamente en su lugar y de tomar las decisiones adecuadas. En una situación ideal, el paciente y su apoderado conversarán sobre estos asuntos durante el trascurso de la enfermedad en lugar de hacerlo durante una crisis médica.
Se puede escoger un poder además del testamento vital o en lugar de este. Un poder notarial duradero para la atención médica permite al paciente ser más específico sobre el tratamiento médico que un testamento vital.
Documentación de las decisiones sobre la planificación anticipada de la atención
Los siguientes son otros documentos para comunicar las preferencias del paciente:
- Orden de no reanimar (ONR): le indica al personal médico en un hospital o establecimiento de cuidados médicos no realizar reanimación cardiopulmonar (RCP) si el corazón del paciente deja de latir.
- Orden de no reanimar (ONR) fuera del hospital: alerta al personal médico de emergencia de los deseos del paciente que no está hospitalizado sobre la RCP y otras medidas de reanimación. Los requisitos legales de una ONR por fuera del hospital pueden ser diferentes en cada estado, pero suelen incluir un documento firmado por el paciente, un testigo y el médico. Se recomienda a los pacientes y las personas a cargo de su cuidado informal que tengan varias copias a fin de que el documento esté disponible de inmediato para el personal médico de emergencia.
- Orden de no intubar (ONI): le indica al personal médico del hospital o establecimiento de cuidados médicos que el paciente no desea que se le conecte a un respirador.
- Orden del médico sobre tratamientos para prologar la vida (OMTPV): permite a los pacientes especificar el tipo de tratamiento médico que desean cerca de la EFV. El documento OPTB, impreso diligenciado y firmado por el médico y el paciente, ayuda a los pacientes con enfermedades graves a tener mayor control sobre su atención en la EFV.
- Orden del paciente sobre tratamientos para prologar la vida (OPTPV): pretende asegurarse de que los pacientes reciban atención en la EFV que sea acorde con sus deseos y por su bien. El documento OPTB permite que los pacientes indiquen el tipo de atención que les gustaría recibir en situaciones en las que no se puedan comunicar, como durante la reanimación, la intubación y otros tratamientos de soporte para prolongar la vida. La ley actual dispone que todo el personal médico, incluso el del servicio de emergencias, se adhiera a las instrucciones del documento OPTB tanto en el hogar como en el hospital, se sigan, tanto en el hogar como en el hospital, por parte de todo el personal médico, incluido el del servicio de emergencias.
Ambivalencia del paciente y el médico con respecto a la planificación anticipada de la atención
Uno de los mayores impedimentos para la PAA eficaz es la ambivalencia de los pacientes y los médicos. Los pacientes de cáncer avanzado pueden ser ambivalentes con sus oncólogos en relación con la PAA porque perciben que estos últimos son reacios a participar en esta conversación.[11,13] Por ejemplo, un grupo de investigadores notificó que 87 % de las mujeres con cáncer de mama metastásico tuvo una conversación sobre las decisiones relativas a la EFV con sus familiares y amigos, 75 % recopiló información sobre las instrucciones anticipadas y 66 % tenía un documento escrito con estas instrucciones.[14] No obstante, solo 19 % de estas mujeres había hablado sobre las decisiones de la EFV con sus proveedores de atención médica; solo 24 % informó a los proveedores sobre las instrucciones y solo 14 % de estos estaban informados sobre las instrucciones anticipadas. Del mismo modo, en un estudio de pacientes de edad avanzada hospitalizados, se observó que muchos habían reflexionado sobre sus preferencias en la EFV (76,3 %) o tenían un plan anticipado de atención (47,9 %), pero relativamente pocos (30,3 %) se lo habían mencionado a sus médicos.[15]
Estos resultados indican que los pacientes participan en la PAA, pero son reacios a comunicar sus opiniones a los oncólogos. Sin embargo, el oncólogo está en la mejor posición para saber cuándo introducir el tema de la atención en la EFV, a fin de poder iniciar y guiar una conversación sobre la PAA de una forma considerada.[16]
Reconsideración de la planificación anticipada de la atención
Las pruebas equívocas son una fuente de ambivalencia para los médicos sobre la planificación anticipada de la atención (PAA). Sin embargo, a pesar de las preocupaciones iniciales, hay cada vez más pruebas de que la PAA mejora los cuidados en la EFV para los pacientes de cáncer avanzado.
Preocupaciones iniciales sobre los límites de la planificación anticipada de la atención
Las pruebas iniciales sobre la planificación anticipada de la atención (PAA) no fueron favorables. Por ejemplo, en varios estudios se encontró lo siguiente:
- Menos del 50 % de los pacientes con enfermedad terminal tenía instrucciones anticipadas en sus historias clínicas.[17-19]
- Más del 65 % de los médicos no sabía que sus pacientes tenían documentos con instrucciones anticipadas.[20]
- Las instrucciones anticipadas no se documentaron, fueron difíciles de interpretar, o complicadas de seguir para los médicos o los representantes legales.[17,21]
Posibles beneficios de la planificación anticipada de la atención
Desde la década de 1990, se ha demostrado el beneficio de la planificación anticipada de la atención (PAA) mediante ensayos aleatorizados. Por ejemplo, en un estudio aleatorizado, se comparó la atención usual con una estrategia estructurada que consistía en un folleto y una conversación con un trabajador social para motivar la PAA, así como un folleto que la describía y solicitaba obtener información sobre los valores y los estados de salud deseados por los pacientes.[22] Los criterios de valoración primarios fueron las comparaciones del grado de coincidencia sobre los siguientes aspectos:
- Preferencias del paciente por renunciar a someterse a tratamientos para prolongar la vida en estados de salud hipotéticos.
- Valores.
- Creencias personales sobre estados de salud hipotéticos.
La intervención se relacionó con una mayor frecuencia de conversaciones sobre la PAA entre el médico y el paciente (64 vs. 38 %; P < 0,001) y el grupo de intervención mostró grados más altos de coincidencia en los tres criterios.[22] No se estudió el efecto de la PAA en los resultados de atención de la salud.
En un estudio realizado en 2010, se observó a 309 pacientes mayores de 80 años y a las personas a su cuidado por seis meses hasta la muerte de los primeros.[23] Los investigadores encontraron que los pacientes que participaron en la PAA tenían una mayor tendencia a comunicar sus preferencias y a recibir atención acorde con estas. Además, comparados con los de los pacientes del grupo de control, los familiares de los pacientes del grupo de intervención (con PAA) que murieron tuvieron mucha menos tensión (5 en el grupo de intervención, 15 en el grupo de control; P < 0,001), ansiedad (0 en el grupo de intervención, 3 en el grupo de control; P = 0,02) y depresión (0 en el grupo de intervención, 5 en el grupo de control; P = 0,002). Asimismo, el grado de satisfacción del paciente y su familia fue más alto en el grupo de intervención.[23]
En los estudios financiados por la Agency for Healthcare Research and Quality, se muestra que el grado de satisfacción de los pacientes de 65 años o más aumentó cuando estos participaron en la PAA con sus médicos. En particular, los pacientes que hablaron sobre sus preferencias relacionadas con la atención en la etapa terminal indicaron lo siguiente:[24]
- Menor ansiedad y temor.
- Mayor sensación de control sobre su atención médica.
- Percepción de que los médicos comprendían mejor sus deseos.
Los representantes legales experimentaron beneficios parecidos.[24]
En un informe de 2011, también se indica que la PAA contribuye, en gran medida, a una atención de mayor calidad en la EFV. Los investigadores demostraron que la relación entre las pruebas de PAA y la reducción de los gastos de Medicare en la EFV varió según el grado de gasto en tratamientos intensivos durante esta etapa.[25] Las instrucciones anticipadas de limitar el tratamiento se relacionaron con grados más bajos de gastos de Medicare, menores probabilidades de muerte en el hospital y un mayor uso de los servicios de cuidados paliativos para enfermos terminales en regiones con gastos altos, pero no en aquellas con gastos bajos o medios. Como mínimo, el estudio indica que la PAA puede ser una explicación para las regiones con gastos bajos.
Un enfoque más matizado de la planificación anticipada de la atención
Los defensores sostienen que se ha hecho una interpretación muy limitada de la planificación anticipada de la atención (PAA) como el diligenciamiento de un documento en el que se expresan las preferencias de un paciente en la etapa final de su vida o se designa a un representante legal para tomar las decisiones en caso de que el paciente ya no pueda hacerlo. En términos generales, la mayoría de pacientes de los países occidentales manifiesta una mayor necesidad de información relacionada con la enfermedad, las opciones de tratamiento, el pronóstico, los futuros síntomas, las posibles trayectorias de la enfermedad y el proceso de muerte. Los pacientes más jóvenes y con un grado de educación más alto suelen buscar información más detallada, mientras que los pacientes mayores y aquellos de culturas que no son occidentales suelen preferir que no se les informe. Desde ese punto de vista, las limitaciones de la PAA se pueden abordar al revisar este concepto.
Una propuesta consiste en considerar la PAA como una conversación continua con la que se pretende preparar a los pacientes y sus familias o amigos a participar, de un modo más significativo, en las futuras decisiones médicas que sean necesarias.[26] En un estudio de sesiones de grupo con pacientes y representantes legales encargados de tomar decisiones, se identificaron 4 temas prominentes al hablar de las decisiones futuras de la atención de la salud.[27]
- Identificar los valores con base en las experiencias y la CV.
- Escoger bien a los representantes legales y asegurarse de que comprendan sus funciones.
- Determinar el grado de discreción de los representantes legales para tomar decisiones.
- Informar a otros para evitar conflictos.
Antes de hablar sobre la PAA, es fundamental que el oncólogo determine las necesidades de información del paciente para poder adaptar la comunicación y la PAA de modo correspondiente.[28]
Intervenciones para mejorar la comunicación entre el paciente y el oncólogo
Se han estudiado varias intervenciones para mejorar la comunicación entre el paciente y el oncólogo. Hay pocos ensayos comparativos y los resultados de interés han variado, por lo que no es posible evaluar las intervenciones. Sin embargo, la variedad de intervenciones permitirá que el oncólogo encuentre alguna que le interese.
Información por escrito
Se dispone de un sinnúmero de folletos para consulta de los pacientes; algunos incluyen información sobre el pronóstico. Un grupo de investigadores realizó un estudio de métodos mixtos sobre los puntos de vista de los pacientes de cáncer con respecto a los materiales impresos proporcionados por sus oncólogos.[29] Los pacientes manifestaron su preocupación sobre el hecho de que la información contradictoria podía socavar su confianza en el oncólogo y esta preocupación fue la que los llevó a consultar materiales impresos.
Se generó otra advertencia a partir de un ensayo aleatorizado en el que se comparó la CV y la insatisfacción en los pacientes de cáncer de pulmón programados para cirugía que solo recibieron información verbal y aquellos que recibieron información tanto verbal como escrita.[30] No se observaron diferencias en el grado de satisfacción de los pacientes con la información; sin embargo, quienes recibieron la información verbal y escrita estuvieron menos satisfechos con su estancia hospitalaria. De esta forma, la presentación de la información escrita pudo haber tenido consecuencias involuntarias y los oncólogos pueden considerar distribuir solo información que refleje sus prácticas reales.
Consultas grabadas
El efecto de solo grabar las consultas en una cinta de audio es significativo, en particular, dada su facilidad para hacerlo. En un ensayo aleatorizado de consultas iniciales por cáncer en todos los estadios, 105 pacientes recibieron grabaciones y 96 no lo hicieron.[31] Los pacientes que recibieron las grabaciones estuvieron más satisfechos y recordaron mejor la información que aquellos que no lo hicieron. Además, los pacientes más jóvenes estuvieron más satisfechos y los de edad más avanzada la recordaron mejor. En otro estudio, se notificaron resultados similares.[32]
Información grabada en video
El uso de videos para facilitar las conversaciones entre los proveedores de atención de la salud, los pacientes y sus familiares, y para ayudar a la tomar de decisiones informadas, ha sido eficaz en ensayos controlados aleatorizados.[33,34] En estos estudios, los pacientes y sus cuidadores (cuando correspondía) determinaron que los videos eran aceptables y se sintieron cómodos con su contenido. En otro estudio, se asignó al azar a 50 pacientes con glioma maligno a escuchar el audio o a escuchar el mismo audio y ver un video en el que describían 3 tipos de atención del cáncer:[33]
- Atención para prolongar la vida (extensión de la vida a cualquier costo).
- Atención médica básica (que incluye la mayoría de cuidados, pero excluye RCP, intubación, respiración mecánica e ingreso en una unidad de cuidados intensivos).
- Grado de bienestar paliativo (alivio de los síntomas, aumento al máximo del bienestar y, en general, evitación de la hospitalización).
Los participantes de la muestra tenían una media de edad de 54 años; el 44 % eran mujeres, el 50 % no deseaban RCP al inicio y el 76 % habían proporcionado instrucciones anticipadas. Al preguntarles después de la intervención sobre el tipo de atención que preferían, el 26 % de los participantes del grupo de control verbal prefirieron atención para prolongar la vida, en comparación con ninguno en el grupo de intervención con video. Más pacientes en el grupo de intervención con video prefirieron cuidados paliativos que los del grupo de control verbal (91 vs. 22 %, respectivamente).[33]
En el segundo estudio, se asignó al azar a 150 pacientes con cáncer avanzado de 4 programas oncológicos a que escucharan una descripción verbal de la RCP o a que escucharan la misma descripción verbal y vieran un video de 3 minutos de RCP simulada, realizada en un paciente conectado a un respirador.[34] El resultado primario fue la preferencia de los participantes por la RCP o no, medida justo después de la exposición a cualquiera de las modalidades. Como en el primer estudio, hubo más pacientes que se sometieron a la intervención con video y la narración que decidieron no realizarse la RCP que quienes solo escucharon la narración (79 vs. 51 %, respectivamente). Los puntajes de conocimiento fueron significativamente más altos en el grupo al que se le mostró el video (P < 0,001). Los resultados del seguimiento de 6 a 8 semanas después demostraron decisiones bastante estables.
En un tercer ensayo controlado aleatorizado de un solo centro, los investigadores asignaron 150 pacientes hospitalizados con cáncer avanzado y 44 de sus cuidadores a uno de 2 grupos. Un grupo vio un video de 6 minutos sobre los programas de cuidados paliativos, mientras que al otro se le leyó una descripción verbal idéntica de los programas de cuidados paliativos. El resultado primario, la preferencia del paciente por los programas de cuidados paliativos, no cambio de manera significativa y no fue diferente entre los 2 grupos después de la intervención (aunque ambos grupos expresaron altos niveles de preferencia por programa de cuidados paliativos al inicio). Sin embargo, los pacientes que vieron el video habían mejorado su conocimiento sobre los programas de cuidados paliativos y era menos probable que estuvieran de acuerdo con la siguiente declaración: “Creo que la atención de los programas de cuidados paliativos solo tiene que ver con la muerte”. Sin embargo, el efecto más interesante de la intervención fue sobre el uso y la duración de la estadía en los programas de cuidados paliativos. Entre los pacientes que murieron durante el estudio, era más probable que aquellos que habían sido parte del grupo del video usaran la atención de los programas de cuidados paliativos (85,2 vs. 63,6 %; P = 0,01) y que la duración de la estadía en los programas de cuidados paliativos fuera mayor (mediana, 12 días vs. 3 días; P = 0,01). Era más probable que los cuidadores del grupo de video prefirieran los programas de cuidados paliativos y que hubieran mejorado su conocimiento sobre los mismos, aunque los hallazgos estuvieron limitados por el pequeño número de cuidadores en el estudio.[35]
Estos estudios indican que es posible que los videos sean útiles para mejorar el conocimiento del paciente en relación con la PAA y que, incluso, afectan la toma de decisiones sobre la misma de los pacientes. Los resultados son alentadores en relación con el valor de los videos como forma de complementar la comunicación y educación entre el oncólogo y el paciente.
Listas de temas que generan preguntas
Los pacientes pueden tener dificultades para hacer preguntas sobre temas delicados y complicados, como el pronóstico y la atención en la EFV. Es posible que las listas de temas ayuden a guiar a los pacientes a resolver esas inquietudes. Unos investigadores diseñaron y probaron un lista de temas que generan preguntas para que los pacientes de cáncer avanzado las usaran en la consulta con un médico experto en cuidados paliativos.[36] Los pacientes que se asignaron al azar al grupo de intervención hicieron, con mayor frecuencia, más preguntas sobre el pronóstico y temas relacionados con la EFV que los del grupo de control (30 vs. 10 %; P = 0,001). No se presentaron efectos negativos en el grado de satisfacción o de ansiedad de los pacientes. En otro estudio, se evaluó una estrategia un poco diferente (presentar la lista a personas al cuidado del paciente con cáncer avanzado) y pareció prometedora.[37]
Paquete de preparación para la consulta del cáncer
Un paquete de preparación para la consulta del cáncer (PPCC) diseñado por un grupo de investigadores tiene 4 componentes:[38]
- Un folleto en el que se describen los procedimientos y la estructura del centro oncológico.
- Un folleto en el que se introduce el concepto de toma de decisiones con base en pruebas y otros factores que influyen en las decisiones.
- Un folleto en el que se describen los derechos y las responsabilidades del paciente.
- Una lista de temas que generan preguntas.
En un ensayo aleatorizado de PPCC versus un folleto de control en 164 consultas iniciales de pacientes con varios tipos de cáncer en diferentes estadios, se mostró que quienes recibieron PPCC hicieron muchas más preguntas (11 vs. 7 preguntas; P = 0,005) sin que aumentara su grado de ansiedad. No obstante, los pacientes que se asignaron a PPCC no participaron con mayor frecuencia o de modo más activo en la toma de decisiones que aquellos del grupo de control.[38]
Folletos y conversaciones facilitadas por psicólogos
En un ensayo aleatorizado, se comparó un folleto sobre la PAA complementado con una conversación con un psicólogo con la atención usual.[39] Los pacientes de ambas cohortes tenían tasas de ONR equivalentes (68 vs. 76 %) pero, en el grupo de intervención, estas se realizaron en el momento de una mediana de 27 días, en comparación con 12,5 días en el grupo de control (P = 0,03). Los pacientes del grupo de intervención fueron menos propensos a morir en el hospital (19 vs. 50 %) y no se aumentó el grado de ansiedad. La interpretación de los resultados del estudio se dificulta por la tasa alta de pérdida para hacer seguimiento y el análisis de la intención de tratar no fue de carácter significativo.
Ayudas para la toma de decisiones
Las ayudas para la toma de decisiones son intervenciones más complicadas que se diseñan para proporcionar a los pacientes un resumen equilibrado de información acerca de las posibles opciones de tratamiento y los posibles resultados, a fin de permitir que los pacientes tomen decisiones informadas acordes con sus preferencias. Las ayudas para la toma de decisiones complementan la relación entre el oncólogo y el paciente, y se han estudiado en dos situaciones relacionadas con el cuidado de pacientes de cáncer avanzado: la decisión de someterse a quimioterapia en un estadio avanzado de la enfermedad y la de prepararse para la EFV.
La decisión de someterse a quimioterapia
En un estudio de 2011 de pacientes con cáncer colorrectal metastásico que estaban en proceso de decidir si iniciaban la quimioterapia sistémica de primera línea, se asignó al azar a 207 pacientes a recibir una consulta oncológica estándar o una consulta estándar complementada con un folleto para llevar a casa y una grabación de la consulta.[40] Los pacientes asignados a la ayuda para la toma de decisiones demostraron una mayor comprensión del pronóstico, las opciones y los objetivos del tratamiento. No hubo diferencias en relación con el conflicto de toma de decisiones, los grados de ansiedad, el logro del paciente o el grado preferido de compromiso en la toma de decisiones, o el tratamiento seleccionado.
Decisión de involucrarse en la planificación anticipada de la atención
En un ensayo piloto semialeatorizado, fue más probable que los pacientes de cáncer avanzado que se reunieron con un mediador capacitado en la planificación de la atención hablarán sobre preferencias futuras con sus familiares y amigos (pero no con sus oncólogos).[41] Un poco más de la mitad de los pacientes con cáncer avanzado estaban dispuestos a reunirse con un orientador independiente capacitado en la planificación anticipada de la atención (PAA). Los pacientes que se asignaron a reunirse con el mediador tuvieron la tendencia a estar menos satisfechos con su comunicación con los profesionales de la atención de la salud y menos satisfechos con la atención futura. De este modo, si bien la PAA es viable con un mediador capacitado, los costos de personal adicional pueden ser inasequibles y crear expectativas en los pacientes que no se satisfacen.
En un ensayo controlado aleatorizado llevado a cabo en Corea, se examinó el efecto de las ayudas para la toma de decisiones en la preferencia del paciente en cuanto a recibir tratamiento activo, tratamiento para prolongar la vida o participar en un programa de cuidados paliativos. Además, se evaluó el conocimiento de los pacientes sobre la PAA y la reanimación cardiopulmonar (RCP): se asignaron 204 pacientes con cáncer avanzado a uno de los siguientes 2 grupos, uno que recibió capacitación mediante una grabación y un folleto sobre la PAA (grupo de intervención) y otro que recibió capacitación mediante una grabación y un folleto sobre el control del dolor del cáncer (grupo de control).[42] Al cabo de 7 semanas de la intervención, los pacientes en el grupo de intervención, en quienes se dio por sentado un pronóstico de expectativa de muerte dentro de varias semanas o meses, expresaron una mayor preferencia por participar en un programa de cuidados paliativos en comparación con los pacientes del grupo de control. Asimismo, los pacientes en el grupo de intervención tenían un mayor conocimiento sobre la RCP después de la intervención. No hubo diferencias estadísticamente significativas entre los 2 grupos con respecto a la documentación de los pacientes sobre las preferencias de la planificación anticipada de la atención o las conversaciones con los familiares, amigos o médicos sobre la atención durante la EFV.
Decisiones relacionadas con el estado de reanimación
Se han estudiado varios abordajes para facilitar la conversación sobre las preferencias y el estado de reanimación de un paciente. Estos abordajes son los siguientes:
- Uso de avisos por computadora que le recuerden al médico iniciar la conversación.[43]
- DVD y folletos con información para que los familiares a cargo del paciente entiendan mejor la opción de reanimación.[34]
- Viñetas audiovisuales para ilustrar el proceso y los resultados de la reanimación.[44]
- Conversación estructurada con un psicólogo clínico.[39]
En varios estudios, fueron más frecuentes las ONR en el grupo de intervención o se presentaron más temprano. Los resultados secundarios son tasas más tempranas y más altas de conversaciones con pacientes y familiares sobre la reanimación, menor grado de contradicción e incertidumbre en la toma de decisiones, y más claridad de los valores. En por lo menos 2 estudios no aumentaron los síntomas de ansiedad ni depresión. El uso de estas ayudas para la toma de decisiones está limitado a los pacientes adultos.
Actitudes de los médicos en relación con las ayudas para la toma de decisiones
Un grupo de investigadores realizó una encuesta trasversal a médicos, radiólogos y cirujanos canadienses especializados en oncología para determinar su grado de sensibilización y el uso de las ayudas para la toma de decisiones de los pacientes.[45] Un poco menos de la mitad (46 %) conocía las ayudas para la toma de decisiones pertinentes a sus prácticas y solo un 24 % las usó. La mayoría de encuestados reconoció la importancia de los resultados clínicos relacionados con las ayudas para la toma de decisiones; es decir, mayor conocimiento, menor ansiedad y mayor grado de satisfacción del paciente. La falta de sensibilización fue el obstáculo para el uso que se mencionó con mayor frecuencia (69 %), seguido de carencia de recursos (24 %) y escasez de tiempo para aprender sobre las ayudas para la toma de decisiones (24 %). Solo el 3 % de los encuestados mencionó la escasez de tiempo como un obstáculo para el uso de ayudas para la toma de decisiones. Está claro que son necesarias estrategias a fin de introducir las ayudas para la toma de decisiones en la práctica clínica y una posibilidad sería comenzar por la capacitación de los oncólogos sobre aquellas ayudas que están disponibles.
Integración de los cuidados paliativos y la atención convencional del cáncer
En 2016, la American Society of Clinical Oncology publicó una guía actualizada aconsejándole a sus miembros que "los pacientes hospitalizados y los pacientes ambulatorios con cáncer avanzado deben recibir servicios de cuidados paliativos específicos, al principio de la enfermedad, junto con el tratamiento activo".[46] Los autores basaron sus recomendaciones de manera principal en 2 ensayos clínicos aleatorizados de intervenciones de cuidados paliativos en el marco de la atención convencional del cáncer en personas con cáncer metastásico, los cuales respaldaron los resultados de varios ensayos clínicos aleatorizados inconclusos más antiguos.[47] Posteriormente, se notificaron 2 ensayos aleatorizados adicionales en los que se compararon los desenlaces entre cohortes de pacientes sometidos a atención oncológica convencional y una intervención de atención paliativa de modo simultáneo, o atención oncológica convencional en diferentes momentos.[48,49] Los 4 estudios se resumen a continuación:
ENABLE II: ensayo aleatorizado sobre una intervención psicoeducacional realizada por personal de enfermería especializado
Este grupo de investigadores notificó sobre los resultados del Project ENABLE (Educate, Nurture, Advise, Before Life Ends).[50] Se asignó al azar a 322 pacientes con cáncer avanzado a recibir atención usual o a someterse a una intervención psicoeducacional de varios componentes, realizada por enfermeros especializados, simultánea a la atención usual. Los criterios de valoración fueron la CV, medida mediante la Functional Assessment of Chronic Illness Therapy for Palliative Care; la intensidad de los síntomas, medida mediante la Edmonton Symptom Assessment Scale, y el estado de ánimo, medido mediante la Center for Epidemiological Studies Depression Scale.
La intervención se basó en el modelo de atención crónica; el objetivo fue fomentar la participación de los pacientes en la planificación de su atención, autocuidado y empoderamiento. La intervención consistió en 4 sesiones pedagógicas semanales y un seguimiento mensual. Los 4 módulos incluyeron lo siguiente:
- Solución de problemas.
- Comunicación y apoyo social.
- Control de síntomas.
- PAA y asuntos pendientes.
La media de puntajes de los participantes en el grupo de intervención fue 4,6 más alta para la CV (P = 0,02); 27,8 más baja para la intensidad de los síntomas (P = 0,06) y 1,8 más baja para el estado de ánimo depresivo (P = 0,02). Los pacientes que murieron durante el estudio tuvieron efectos menos marcados por el tratamiento. No hubo diferencia en la SG ni en la administración de quimioterapia o atención médica intensiva cerca de la EFV. Además, no hubo diferencia entre los grupos en relación con las tasas de derivación a cuidados paliativos o a los programas que prestan estos cuidados.[50]
Ensayo aleatorizado de cuidados paliativos simultáneos y atención oncológica estándar en pacientes con cáncer de pulmón metastásico
En el segundo estudio, se asignó al azar a 151 pacientes con CPCNP metastásico recién diagnosticado a recibir atención oncológica estándar o atención oncológica estándar con incorporación temprana de cuidados paliativos. Los pacientes que se asignaron a someterse a cuidados paliativos se reunieron con un miembro del equipo que administraba este tipo de atención a las 3 semanas a partir del diagnóstico. Las pautas generales indicaban a los médicos especializados en cuidados paliativos que prestaran atención particular a los siguientes aspectos:
- Evaluación de los síntomas físicos y psicológicos.
- Determinación de los objetivos de la atención.
- Ayuda con la toma de decisiones sobre el tratamiento.
- Coordinación de la atención con base en las necesidades individuales del paciente.
Se informó sobre los análisis primario y secundario del estudio en una publicación original y, más tarde, en varias publicaciones secundarias,[51-53] que se enumeran a continuación.
- Los criterios de valoración primarios de este ensayo fueron la CV (medida mediante la Functional Assessment of Cancer Therapy—Lung) y el estado de ánimo (medido mediante la Hospital Anxiety and Depression Scale). Los criterios se evaluaron al inicio y, de nuevo, a las 12 semanas. Los criterios de valoración secundarios fueron la supervivencia y las mediciones de la atención en la EFV extraídas de historias clínicas. Los pacientes que se asignaron a recibir cuidados paliativos simultáneos notificaron mejor CV (98,0 vs. 91,5; P = 0,01). Menos pacientes del grupo de cuidados paliativos presentaron síntomas depresivos (16 vs. 38 %; P = 0,05). Además, la mediana de SG de los pacientes de la cohorte de cuidados paliativos fue más larga (11,6 vs. 8,9 meses; P = 0,02). Por último, menos pacientes de la cohorte de cuidados paliativos recibieron tratamiento intensivo (quimioterapia en los 14 días previos a la muerte, ningún cuidado paliativo ni estancia hospitalaria en los tres días previos a la muerte) que aquellos del grupo de atención usual (33 vs. 54 %; P = 0,05).[51]
- Dada la importancia de la comprensión del diagnóstico por parte del paciente para establecer las preferencias de tratamiento y tomar decisiones, se llevó a cabo un segundo análisis para evaluar el efecto de los cuidados paliativos en la precisión de la percepción del pronóstico y el tratamiento contra el cáncer por parte del paciente.[52] Al inicio, el 31,7 % de los pacientes con CPCNP metastásico manifestaron que su cáncer era curable. Fue más probable que los pacientes que recibieron cuidados paliativos tempranos manifestaran que conocían el objetivo del tratamiento a las 12 y 18 semanas que aquellos de la cohorte de atención estándar (por ejemplo, a las 12 semanas, el 39,5 % de los pacientes en la cohorte de atención estándar informaron que su cáncer era curable, en comparación con el 22,2 % de la cohorte de cuidados paliativos; P = 0,08). La mayoría de pacientes de los dos grupos mantuvieron la creencia de que el objetivo del tratamiento era "librarse del cáncer". No obstante, el 82,5 % de los pacientes del grupo de cuidados paliativos mantuvo y creó la percepción acertada de su pronóstico, en comparación con el 59,6 % del grupo de atención estándar.
Fue más probable que los pacientes de la cohorte de cuidados paliativos con una comprensión acertada del pronóstico recibieran quimioterapia que aquellos que no comprendían bien su pronóstico (9,4 vs. 50 %; P = 0,02). No se observó un efecto similar en los pacientes del grupo de atención estándar; el porcentaje de pacientes de este grupo a los que se les administró quimioterapia no difirió en la percepción del pronóstico.
- En otro análisis secundario, se buscó determinar si los cuidados paliativos tempranos afectaban la administración de la quimioterapia o el uso de cuidados paliativos.[53] Un grupo de investigadores notificó que el número general de regímenes no cambió con base en la asignación a la atención estándar o a la cohorte de cuidados paliativos. Sin embargo, fue menos probable que los pacientes asignados a cuidados paliativos recibieran quimioterapia en los 60 días previos a la muerte (52,5 vs. 70,1 %; P = 0,05). Con respecto a la inscripción en los cuidados paliativos, a pesar de que no hubo diferencias significativas en las tasas de derivación, cerca del doble de participantes del grupo de cuidados paliativos tempranos, comparados con los del grupo de atención usual, recibió cuidados paliativos por más de una semana (60 vs. 33,3 %; P = 0,004).
- Los investigadores también probaron la hipótesis de que la mejora observada en la supervivencia se podía atribuir a la mejora en la tasa de depresión.[54] La depresión fue un factor pronóstico de supervivencia más corta y los pacientes que se asignaron a la cohorte de cuidados paliativos tuvieron tasas más altas de mejoría. Sin embargo, no hubo una correlación significativa con la mejora en la supervivencia.
- Un grupo de investigadores notificó un estudio sobre el resumen de la consulta inicial de las historias clínicas electrónicas a fin de determinar la frecuencia del tratamiento de los síntomas, la comprensión de la enfermedad, la toma de decisiones sobre el tratamiento, las estrategias del paciente y su familiar a cargo para hacer frente y la planificación de la atención.[55] La mediana de tiempo de la consulta inicial fue de 55 minutos (intervalo, 20–120 minutos) y la mayoría del tiempo se usó para tratar los síntomas de la enfermedad, hacerle frente y comprenderla. Fue más probable que los pacientes con menor CV solicitaran más tiempo.
- Se llevaron a cabo otros análisis cualitativos de notas clínicas para identificar elementos clave de las consultas de cuidados paliativos y su coordinación, y para comparar el contenido de los cuidados paliativos versus las visitas a oncología.[56] Fue más probable que las consultas de cuidados paliativos se concentraran en los síntomas, los asuntos psicológicos y la mejor comprensión de la enfermedad. Los oncólogos se concentraron más en el tratamiento del cáncer y sus complicaciones. No se conoce la contribución de estas diferencias a los resultados observados.
Ensayo aleatorizado grupal de cuidados paliativos tempranos para pacientes de cáncer en estadio avanzado
Se notificaron los resultados de este estudio con enmascaramiento simple de pacientes asignados a recibir cuidados paliativos y atención convencional del cáncer, o solo tratamiento convencional del cáncer.[57] La intervención de cuidados paliativos incluyó una visita inicial seguida de visitas mensuales a la clínica de atención paliativa, con seguimiento telefónico y acceso directo a la unidad de cuidados paliativos para pacientes hospitalizados, según fuera necesario. El resultado principal fue el cambio de puntaje en la Functional Assessment of Chronic Illness Therapy—Spiritual Well-Being (FACIT-Sp) a los tres meses. Los resultados secundarios fueron los puntajes en la FACIT-Sp a los 4 meses y otras mediciones validadas de CV, la carga agobiante que constituyen los síntomas, satisfacción con la atención y calidad de las interacciones con los médicos a los 3 y 4 meses.
No hubo diferencias estadísticamente significativas en el cambio de puntajes de FACIT-Sp a los 3 meses, pero las diferencias sí aparecieron a los 4 meses; además, hubo diferencias significativas en los resultados secundarios a los 3 y 4 meses. Estos resultados confirman el beneficio de la administración simultánea de cuidados paliativos e indican que los beneficios de los cuidados paliativos se incrementarán con el tiempo. La coordinación de la atención entre el Princess Margaret Cancer Centre y los Community Care Access Centres pueden dificultar la reproducción de resultados.[57]
ENABLE III: inicio temprano versus inicio tardío de la atención de cuidados paliativos oncológicos simultáneos
En este estudio se compararon los desenlaces de 207 pacientes asignados al azar para comenzar a recibir las intervenciones de cuidados paliativos dentro de los 30 a 60 días de diagnóstico versus a los 3 meses a partir del diagnóstico de cáncer avanzado.[49] Las sesiones semanales de orientación telefónica descritas en el resumen de ENABLE II incluyeron un componente de 3 sesiones de recapitulación de la vida que se diseñó para intervenir de forma específica en las personas a cargo del paciente. Los resultados de interés fueron la CV, el efecto de los síntomas, el estado de ánimo, el uso de recursos, y la mejora de la supervivencia a 1 año. La atención oncológica paliativa precoz se relacionó con una mejora de la supervivencia (63 vs. 48 %, P = 0,038). Sin embargo, no hubo diferencias estadísticamente significativas en los resultados informados por los pacientes o el uso de los recursos. Por otra parte, la prueba del orden logarítmico para la SG no reveló una diferencia significativa, lo que indica que las curvas de supervivencia convergen después del punto de 1 año.
Algunas limitaciones del estudio pueden complicar una interpretación. En primer lugar, el estudio no cumplió con su objetivo de inscribir a 360 pacientes, en parte debido a las altas tasas de inelegibilidad después de los exámenes de detección y la negativa del paciente. En segundo lugar, el análisis con intención de tratar puede haber perdido diferencias debidas a variaciones en la "cantidad" de intervención completada. En tercer lugar, los múltiples resultados pueden haber limitado el poder estadístico para detectar diferencias significativas, en especial teniendo en cuenta el tamaño de muestra menor que la deseada. Por lo tanto, una interpretación más precisa de los resultados puede ser que la duración óptima de las intervenciones de cuidados paliativos permanece indeterminada.
En contraste con los resultados para los pacientes, con la intervención ENABLE III mejoraron los resultados para los cuidadores.[58] Se asignó al azar a 122 cuidadores para recibir, ya sea temprano o más tarde en el estudio, 3 sesiones semanales de entrenamiento telefónico, seguimiento mensual y una llamada relacionada con el duelo. Para todos los cuidadores, la intervención temprana se relacionó con puntajes más bajos de depresión a los 3 meses. Los cuidadores de las personas que fallecieron y que recibieron cuidados paliativos temprano presentaron menor carga de depresión y agobio en la fase terminal. Estos resultados son importantes pues establecen un beneficio para los cuidadores.
Dificultades para la integración temprana de los cuidados paliativos
A continuación, se enumeran varias de las dificultades más pertinentes de la integración de los cuidados paliativos en la atención oncológica estándar y se incluye un resumen de la información disponible.
- Disponibilidad de los servicios de cuidados paliativos especiales: en una encuesta publicada en 2010, solo el 59 % de los centros oncológicos del Instituto Nacional del Cáncer (NCI) y el 33 % de los centros por fuera de este notificaron disponer de programas de cuidados paliativos, con niveles de recursos ampliamente variados.[59] Sin embargo, al menos la mitad de los directivos encuestados manifestaron un interés en ampliar los servicios en los años siguientes, aunque hubo diferencias con base en la designación del NCI. Como dato interesante, los impedimentos que se identificaron para expandir los servicios tuvieron más relación con tasas más bajas de rembolso o limitaciones del presupuesto institucional que con las preocupaciones sobre las pruebas que respaldan estos servicios.
Una posible solución para la escasez de personal es la formación de los oncólogos en las destrezas necesarias para la llamada atención primaria de cuidados paliativos.[60] Las destrezas necesarias para los cuidados paliativos primarios incluyen discusiones básicas sobre el pronóstico, objetivos del tratamiento, el sufrimiento, o la identificación del estado y el control de los síntomas, reservando así derivaciones especiales para obtener ayuda con la resolución de conflictos relacionados con los objetivos o métodos de tratamiento.
- Derivación de los pacientes a los servicios de cuidados paliativos especializados por parte de los oncólogos: en una encuesta a especialistas en cáncer canadienses, se mostró que el 94 % tenía acceso a por lo menos un componente de los servicios de cuidados paliativos, pero solo el 36 % de los encuestados tenía acceso a servicios de cuidados paliativos integrales.[61] Además, el 80 % de los médicos indicó que siempre o algunas veces derivaba a los enfermos terminales; el tiempo de derivación distribuido de forma equitativa entre el momento del diagnóstico, durante la quimioterapia paliativa, o después de que se suspendieran la quimioterapia o las transfusiones.
- Actitudes de los oncólogos hacia los cuidados paliativos.
- Aceptación del paciente.
- Preguntas sin respuesta: los resultados de 4 ensayos aleatorizados resumidos más arriba proporcionan una justificación convincente para facilitar el acceso a los servicios de cuidados paliativos de forma simultánea con la atención convencional del cáncer.[62,63] Sin embargo, hay preguntas que permanecen sin respuesta que podrían disminuir el entusiasmo por la integración sistemática de la atención de cuidados paliativos con la atención convencional del cáncer.
- ¿Quiénes son los pacientes que serán atendidos? Una revisión de los criterios de elegibilidad muestra que los pacientes se seleccionaron con base en características tales como la supervivencia del paciente calculada por el médico, además del estadio de la enfermedad. Como se indica en el Cuadro 1, muchos pacientes potencialmente aptos se negaron a participar en los ensayos. Los diversos motivos para no participar necesitan aclararse a fin de identificar posibles factores de confusión que pueden afectar a la probabilidad de beneficiarse de los servicios.
- ¿Cuándo es el momento óptimo para presentar la especialidad de cuidados paliativos?
- ¿Qué componentes de los cuidados paliativos son fundamentales para obtener resultados positivos? Las intervenciones de ENABLE incluyeron varias sesiones educativas a lo largo de un mes dirigidas por personal de enfermería con práctica avanzada. Además, solo hubo una única consulta de cuidados paliativos programada al inicio del estudio. Esto indica que las alternativas para los equipos de cuidados paliativos multidisciplinarios descritos por otros investigadores [48,52] pueden tener efectos importantes.
- ¿Cuál es el mecanismo de acción del beneficio supuesto? Esta pregunta parece especialmente importante porque los centros de cáncer luchan con la disminución de reembolsos, de modo que hay una necesidad legítima para aumentar al máximo el valor de los servicios de apoyo prestados.
- ¿Cuáles son los mecanismos que explican la mejora observada en la supervivencia?[50,64,65]
- Financiamiento: en una encuesta a 20 pacientes ambulatorios de clínicas de cuidados paliativos, se indicó que las principales fuentes de financiamiento eran los cobros por servicio y el apoyo institucional, pero la mayoría identificó el financiamiento para cubrir los gastos de personal como el principal problema.[66]
| Autor/Referencia | Inscripción (No.) | Criterios seleccionados de elegibilidad | ||||
|---|---|---|---|---|---|---|
| Aleatorizado | Posiblemente apto | Sometido a detección | Tipo de cáncer | Tiempo desde el diagnóstico | Supervivencia calculada por el oncólogo | |
| GI = gastrointestinal; GU = genitourinario. | ||||||
| Bakitas et al., 2009 [50] | 322 | 681 | 1222 | GI; pulmón; GU; mama | Entre 8–12 semanas | ~1 año |
| Temel et al., 2010 [51] | 151 | Pulmón | ≤8 semanas | Sin especificar | ||
| Zimmermann et al., 2014 [48] | 461 | 892 | 3293 | GI; pulmón; GU; mama; ginecológico | Sin especificar | 6–24 meses |
| Bakitas et al., 2015 [49] | 207 | 545 | 1468 | GI; pulmón; GU; mama; otros; neoplasia hematológica maligna | Temprano: 30–60 días; demorado: >90 días | 6–24 meses |
| Criterio de valoración | Variable medida | |||
|---|---|---|---|---|
| CARES-MIS = Cancer Rehabilitation Evaluation System Medical Interaction Subscale; CES-D = Center for Epidemiologic Studies Depression Scale; ED = servicio de urgencias; ENABLE = Educate, Nurture, Advise Before Life Ends; ESAS = Edmonton Symptom Assessment System; FACIT-Pal = Functional Assessment of Chronic Illness Therapy - Palliative Care; FACIT-Sp = Functional Assessment of Chronic Illness Therapy - Spiritual Well-Being; FACT-L = Functional Assessment of Cancer Therapy - Lung; FAMCARE-P16 = medición de 16 aspectos de la satisfacción del paciente con la atención del cáncer; HADS = Hospital Anxiety and Depression Scale; ICU = unidad de cuidados intensivos; NR = desenlace medido, pero no notificado; QUAL-E = calidad de vida en la etapa final de la vida; — = desenlace no medido. | ||||
| Bakitas et al., 2009 (ENABLE II) [50] | Temel et al., 2010 [51] | Zimmermann et al., 2014 [48] | Bakitas et al., 2015 (ENABLE III) [49] | |
| Calidad de vida | FACIT-Pal | FACT-L | FACIT-Sp; QUAL-E | FACIT-Pal; QUAL-E |
| Estado de ánimo | CES-D | HADS | — | — |
| Síntomas | ESAS | — | QUAL-E | ESAS |
| Satisfacción con la atención | — | — | FAMCARE-P16 | — |
| Interacciones con los médicos | — | — | CARES-MIS | — |
| Administración de quimioterapia | NR | NR | NR | NR |
| Uso de recursos para la etapa final de la vida | Hospital/días en la ICU; visitas al ED | Días en el hospital o la ICU; visitas al ED; quimioterapia administrada en los 14 días anteriores a la muerte; uso de programas de cuidados paliativos terminales; lugar de la muerte | Sin especificar | Días en el hospital o la ICU; visitas al ED; quimioterapia administrada en los 14 días anteriores a la muerte; lugar de la muerte |
| Mediana de supervivencia general | Si | Si | — | Si |
| Desenlace | Autor/Referencia | |||
|---|---|---|---|---|
| ENABLE = Educate, Nurture, Advise Before Life Ends; NR = desenlace medido, pero no notificado; NS = sin diferencia significativa en los desenlaces notificados; PC = favorece la intervención de cuidados paliativos; — = desenlace no medido. | ||||
| Bakitas et al., 2009 (ENABLE II) [50] | Temel et al., 2010 [51] | Zimmermann et al., 2014 [48] | Bakitas et al., 2015 (ENABLE III) [49] | |
| Calidad de vida | PC | PC | NS a los 3 meses; PC a los 4 meses | NS |
| Estado de ánimo | PC | PC | NS a los 3 meses; PC a los 4 meses | NS |
| Síntomas | NS | — | NS a los 3 meses; PC a los 4 meses | NS |
| Satisfacción con la atención | — | — | PC a los 3 meses; PC a los 4 meses | — |
| Interacciones con los médicos | — | — | NS a los 3 meses; NS a los 4 meses | — |
| Uso de recursos para la etapa final de la vida | NS | NR | NR | NS |
| Supervivencia general | NS | PC | NR | Temprano |
Bibliografía
- Krishnan M, Temel JS, Wright AA, et al.: Predicting life expectancy in patients with advanced incurable cancer: a review. J Support Oncol 11 (2): 68-74, 2013. [PUBMED Abstract]
- Movsas B, Moughan J, Sarna L, et al.: Quality of life supersedes the classic prognosticators for long-term survival in locally advanced non-small-cell lung cancer: an analysis of RTOG 9801. J Clin Oncol 27 (34): 5816-22, 2009. [PUBMED Abstract]
- Sloan JA, Zhao X, Novotny PJ, et al.: Relationship between deficits in overall quality of life and non-small-cell lung cancer survival. J Clin Oncol 30 (13): 1498-504, 2012. [PUBMED Abstract]
- Hagerty RG, Butow PN, Ellis PA, et al.: Cancer patient preferences for communication of prognosis in the metastatic setting. J Clin Oncol 22 (9): 1721-30, 2004. [PUBMED Abstract]
- Stockler MR, Tattersall MH, Boyer MJ, et al.: Disarming the guarded prognosis: predicting survival in newly referred patients with incurable cancer. Br J Cancer 94 (2): 208-12, 2006. [PUBMED Abstract]
- Kiely BE, Soon YY, Tattersall MH, et al.: How long have I got? Estimating typical, best-case, and worst-case scenarios for patients starting first-line chemotherapy for metastatic breast cancer: a systematic review of recent randomized trials. J Clin Oncol 29 (4): 456-63, 2011. [PUBMED Abstract]
- Kiely BE, Alam M, Blinman P, et al.: Estimating typical, best-case and worst-case life expectancy scenarios for patients starting chemotherapy for advanced non-small-cell lung cancer: a systematic review of contemporary randomized trials. Lung Cancer 77 (3): 537-44, 2012. [PUBMED Abstract]
- Kiely BE, Martin AJ, Tattersall MH, et al.: The median informs the message: accuracy of individualized scenarios for survival time based on oncologists' estimates. J Clin Oncol 31 (28): 3565-71, 2013. [PUBMED Abstract]
- Kiely BE, McCaughan G, Christodoulou S, et al.: Using scenarios to explain life expectancy in advanced cancer: attitudes of people with a cancer experience. Support Care Cancer 21 (2): 369-76, 2013. [PUBMED Abstract]
- Teno JM: Advance directives: time to move on. Ann Intern Med 141 (2): 159-60, 2004. [PUBMED Abstract]
- Barnes KA, Barlow CA, Harrington J, et al.: Advance care planning discussions in advanced cancer: analysis of dialogues between patients and care planning mediators. Palliat Support Care 9 (1): 73-9, 2011. [PUBMED Abstract]
- Hawkins NA, Ditto PH, Danks JH, et al.: Micromanaging death: process preferences, values, and goals in end-of-life medical decision making. Gerontologist 45 (1): 107-17, 2005. [PUBMED Abstract]
- Dow LA, Matsuyama RK, Ramakrishnan V, et al.: Paradoxes in advance care planning: the complex relationship of oncology patients, their physicians, and advance medical directives. J Clin Oncol 28 (2): 299-304, 2010. [PUBMED Abstract]
- Ozanne EM, Partridge A, Moy B, et al.: Doctor-patient communication about advance directives in metastatic breast cancer. J Palliat Med 12 (6): 547-53, 2009. [PUBMED Abstract]
- Heyland DK, Barwich D, Pichora D, et al.: Failure to engage hospitalized elderly patients and their families in advance care planning. JAMA Intern Med 173 (9): 778-87, 2013. [PUBMED Abstract]
- Emanuel LL, Danis M, Pearlman RA, et al.: Advance care planning as a process: structuring the discussions in practice. J Am Geriatr Soc 43 (4): 440-6, 1995. [PUBMED Abstract]
- Teno JM, Licks S, Lynn J, et al.: Do advance directives provide instructions that direct care? SUPPORT Investigators. Study to Understand Prognoses and Preferences for Outcomes and Risks of Treatment. J Am Geriatr Soc 45 (4): 508-12, 1997. [PUBMED Abstract]
- Teno J, Lynn J, Wenger N, et al.: Advance directives for seriously ill hospitalized patients: effectiveness with the patient self-determination act and the SUPPORT intervention. SUPPORT Investigators. Study to Understand Prognoses and Preferences for Outcomes and Risks of Treatment. J Am Geriatr Soc 45 (4): 500-7, 1997. [PUBMED Abstract]
- Bradley EH, Rizzo JA: Public information and private search: evaluating the Patient Self-Determination Act. J Health Polit Policy Law 24 (2): 239-73, 1999. [PUBMED Abstract]
- Virmani J, Schneiderman LJ, Kaplan RM: Relationship of advance directives to physician-patient communication. Arch Intern Med 154 (8): 909-13, 1994. [PUBMED Abstract]
- Teno JM, Lynn J, Phillips RS, et al.: Do formal advance directives affect resuscitation decisions and the use of resources for seriously ill patients? SUPPORT Investigators. Study to Understand Prognoses and Preferences for Outcomes and Risks of Treatments. J Clin Ethics 5 (1): 23-30, 1994. [PUBMED Abstract]
- Pearlman RA, Starks H, Cain KC, et al.: Improvements in advance care planning in the Veterans Affairs System: results of a multifaceted intervention. Arch Intern Med 165 (6): 667-74, 2005. [PUBMED Abstract]
- Detering KM, Hancock AD, Reade MC, et al.: The impact of advance care planning on end of life care in elderly patients: randomised controlled trial. BMJ 340: c1345, 2010. [PUBMED Abstract]
- Kass-Bartelmes BL, Hughes R: Advance Care Planning, Preferences for Care at the End of Life: Research in Action, Issue 12. Rockville, Md: Agency for Healthcare Research and Quality, 2003. Available online. Last accessed Jan. 23, 2025.
- Nicholas LH, Langa KM, Iwashyna TJ, et al.: Regional variation in the association between advance directives and end-of-life Medicare expenditures. JAMA 306 (13): 1447-53, 2011. [PUBMED Abstract]
- Sudore RL, Fried TR: Redefining the "planning" in advance care planning: preparing for end-of-life decision making. Ann Intern Med 153 (4): 256-61, 2010. [PUBMED Abstract]
- McMahan RD, Knight SJ, Fried TR, et al.: Advance care planning beyond advance directives: perspectives from patients and surrogates. J Pain Symptom Manage 46 (3): 355-65, 2013. [PUBMED Abstract]
- Johnston G, Abraham C: Managing awareness: negotiating and coping with a terminal prognosis. Int J Palliat Nurs 6 (10): 485-94, 2000 Nov-Dec. [PUBMED Abstract]
- Davey HM, Armstrong BK, Butow PN: An exploratory study of cancer patients' views on doctor-provided and independent written prognostic information. Patient Educ Couns 56 (3): 349-55, 2005. [PUBMED Abstract]
- Barlési F, Barrau K, Loundou A, et al.: Impact of information on quality of life and satisfaction of non-small cell lung cancer patients: a randomized study of standardized versus individualized information before thoracic surgery. J Thorac Oncol 3 (10): 1146-52, 2008. [PUBMED Abstract]
- Ong LM, Visser MR, Lammes FB, et al.: Effect of providing cancer patients with the audiotaped initial consultation on satisfaction, recall, and quality of life: a randomized, double-blind study. J Clin Oncol 18 (16): 3052-60, 2000. [PUBMED Abstract]
- Bruera E, Pituskin E, Calder K, et al.: The addition of an audiocassette recording of a consultation to written recommendations for patients with advanced cancer: A randomized, controlled trial. Cancer 86 (11): 2420-5, 1999. [PUBMED Abstract]
- El-Jawahri A, Podgurski LM, Eichler AF, et al.: Use of video to facilitate end-of-life discussions with patients with cancer: a randomized controlled trial. J Clin Oncol 28 (2): 305-10, 2010. [PUBMED Abstract]
- Volandes AE, Paasche-Orlow MK, Mitchell SL, et al.: Randomized controlled trial of a video decision support tool for cardiopulmonary resuscitation decision making in advanced cancer. J Clin Oncol 31 (3): 380-6, 2013. [PUBMED Abstract]
- El-Jawahri A, Traeger L, Greer JA, et al.: Randomized trial of a hospice video educational tool for patients with advanced cancer and their caregivers. Cancer 126 (15): 3569-3578, 2020. [PUBMED Abstract]
- Clayton JM, Butow PN, Tattersall MH, et al.: Randomized controlled trial of a prompt list to help advanced cancer patients and their caregivers to ask questions about prognosis and end-of-life care. J Clin Oncol 25 (6): 715-23, 2007. [PUBMED Abstract]
- Hebert RS, Schulz R, Copeland VC, et al.: Pilot testing of a question prompt sheet to encourage family caregivers of cancer patients and physicians to discuss end-of-life issues. Am J Hosp Palliat Care 26 (1): 24-32, 2009 Feb-Mar. [PUBMED Abstract]
- Butow P, Devine R, Boyer M, et al.: Cancer consultation preparation package: changing patients but not physicians is not enough. J Clin Oncol 22 (21): 4401-9, 2004. [PUBMED Abstract]
- Stein RA, Sharpe L, Bell ML, et al.: Randomized controlled trial of a structured intervention to facilitate end-of-life decision making in patients with advanced cancer. J Clin Oncol 31 (27): 3403-10, 2013. [PUBMED Abstract]
- Leighl NB, Shepherd HL, Butow PN, et al.: Supporting treatment decision making in advanced cancer: a randomized trial of a decision aid for patients with advanced colorectal cancer considering chemotherapy. J Clin Oncol 29 (15): 2077-84, 2011. [PUBMED Abstract]
- Jones L, Harrington J, Barlow CA, et al.: Advance care planning in advanced cancer: can it be achieved? An exploratory randomized patient preference trial of a care planning discussion. Palliat Support Care 9 (1): 3-13, 2011. [PUBMED Abstract]
- Yun YH, Kang E, Park S, et al.: Efficacy of a Decision Aid Consisting of a Video and Booklet on Advance Care Planning for Advanced Cancer Patients: Randomized Controlled Trial. J Pain Symptom Manage 58 (6): 940-948.e2, 2019. [PUBMED Abstract]
- Temel JS, Greer JA, Gallagher ER, et al.: Electronic prompt to improve outpatient code status documentation for patients with advanced lung cancer. J Clin Oncol 31 (6): 710-5, 2013. [PUBMED Abstract]
- Yun YH, Lee MK, Park S, et al.: Use of a decision aid to help caregivers discuss terminal disease status with a family member with cancer: a randomized controlled trial. J Clin Oncol 29 (36): 4811-9, 2011. [PUBMED Abstract]
- Brace C, Schmocker S, Huang H, et al.: Physicians' awareness and attitudes toward decision aids for patients with cancer. J Clin Oncol 28 (13): 2286-92, 2010. [PUBMED Abstract]
- Ferrell BR, Temel JS, Temin S, et al.: Integration of Palliative Care Into Standard Oncology Care: American Society of Clinical Oncology Clinical Practice Guideline Update. J Clin Oncol 35 (1): 96-112, 2017. [PUBMED Abstract]
- Lorenz KA, Lynn J, Dy SM, et al.: Evidence for improving palliative care at the end of life: a systematic review. Ann Intern Med 148 (2): 147-59, 2008. [PUBMED Abstract]
- Zimmermann C, Swami N, Krzyzanowska M, et al.: Early palliative care for patients with advanced cancer: a cluster-randomised controlled trial. Lancet 383 (9930): 1721-30, 2014. [PUBMED Abstract]
- Bakitas MA, Tosteson TD, Li Z, et al.: Early Versus Delayed Initiation of Concurrent Palliative Oncology Care: Patient Outcomes in the ENABLE III Randomized Controlled Trial. J Clin Oncol 33 (13): 1438-45, 2015. [PUBMED Abstract]
- Bakitas M, Lyons KD, Hegel MT, et al.: Effects of a palliative care intervention on clinical outcomes in patients with advanced cancer: the Project ENABLE II randomized controlled trial. JAMA 302 (7): 741-9, 2009. [PUBMED Abstract]
- Temel JS, Greer JA, Muzikansky A, et al.: Early palliative care for patients with metastatic non-small-cell lung cancer. N Engl J Med 363 (8): 733-42, 2010. [PUBMED Abstract]
- Temel JS, Greer JA, Admane S, et al.: Longitudinal perceptions of prognosis and goals of therapy in patients with metastatic non-small-cell lung cancer: results of a randomized study of early palliative care. J Clin Oncol 29 (17): 2319-26, 2011. [PUBMED Abstract]
- Greer JA, Pirl WF, Jackson VA, et al.: Effect of early palliative care on chemotherapy use and end-of-life care in patients with metastatic non-small-cell lung cancer. J Clin Oncol 30 (4): 394-400, 2012. [PUBMED Abstract]
- Pirl WF, Greer JA, Traeger L, et al.: Depression and survival in metastatic non-small-cell lung cancer: effects of early palliative care. J Clin Oncol 30 (12): 1310-5, 2012. [PUBMED Abstract]
- Jacobsen J, Jackson V, Dahlin C, et al.: Components of early outpatient palliative care consultation in patients with metastatic nonsmall cell lung cancer. J Palliat Med 14 (4): 459-64, 2011. [PUBMED Abstract]
- Yoong J, Park ER, Greer JA, et al.: Early palliative care in advanced lung cancer: a qualitative study. JAMA Intern Med 173 (4): 283-90, 2013. [PUBMED Abstract]
- Hannon B, Swami N, Pope A, et al.: The oncology palliative care clinic at the Princess Margaret Cancer Centre: an early intervention model for patients with advanced cancer. Support Care Cancer 23 (4): 1073-80, 2015. [PUBMED Abstract]
- Dionne-Odom JN, Azuero A, Lyons KD, et al.: Benefits of Early Versus Delayed Palliative Care to Informal Family Caregivers of Patients With Advanced Cancer: Outcomes From the ENABLE III Randomized Controlled Trial. J Clin Oncol 33 (13): 1446-52, 2015. [PUBMED Abstract]
- Hui D, Elsayem A, De la Cruz M, et al.: Availability and integration of palliative care at US cancer centers. JAMA 303 (11): 1054-61, 2010. [PUBMED Abstract]
- Quill TE, Abernethy AP: Generalist plus specialist palliative care--creating a more sustainable model. N Engl J Med 368 (13): 1173-5, 2013. [PUBMED Abstract]
- Wentlandt K, Krzyzanowska MK, Swami N, et al.: Referral practices of oncologists to specialized palliative care. J Clin Oncol 30 (35): 4380-6, 2012. [PUBMED Abstract]
- Parikh RB, Kirch RA, Smith TJ, et al.: Early specialty palliative care--translating data in oncology into practice. N Engl J Med 369 (24): 2347-51, 2013. [PUBMED Abstract]
- Gomes B: Palliative care: if it makes a difference, why wait? J Clin Oncol 33 (13): 1420-1, 2015. [PUBMED Abstract]
- Temel JS, Jackson VA, Billings JA, et al.: Phase II study: integrated palliative care in newly diagnosed advanced non-small-cell lung cancer patients. J Clin Oncol 25 (17): 2377-82, 2007. [PUBMED Abstract]
- Gaertner J, Wolf J, Hallek M, et al.: Standardizing integration of palliative care into comprehensive cancer therapy--a disease specific approach. Support Care Cancer 19 (7): 1037-43, 2011. [PUBMED Abstract]
- Smith AK, Thai JN, Bakitas MA, et al.: The diverse landscape of palliative care clinics. J Palliat Med 16 (6): 661-8, 2013. [PUBMED Abstract]
Función del oncólogo en la planificación del estado de transición a los cuidados paliativos terminales
Panorama
En 1961, se publicó una encuesta a 219 médicos, donde el 88 % de los encuestados indicaron que su política regular de decirle "la verdad" al paciente sobre su cáncer era "no decir nada”; sin embargo, el 34 % de ese grupo indicó que ellos hacían excepciones ocasionales y revelaban el diagnóstico, por lo general a miembros de la familia.[1] En 1977 se repitió una encuesta idéntica con un grupo diferente de 264 médicos; en ese momento, el 98 % de los encuestados indicaron que informarle al paciente su diagnóstico de cáncer era su política inicial, aunque el 28 % dijeron que hacían una excepción en ocasiones.[2]
A pesar del progreso, la comunicación eficaz del pronóstico sigue siendo un reto, de acuerdo con la medida de los cálculos que hacen los pacientes de la esperanza de vida o metas del tratamiento. Por ejemplo, un estudio de 1984 reveló que el 37 % de los pacientes con cáncer metastásico incurable sentían que el tratamiento les curaría la enfermedad.[3] De forma similar, en 2012 otro estudio informaba que el 69 % de los pacientes con cáncer avanzado de pulmón y el 81 % de los pacientes con cáncer colorrectal avanzado que ingresaron al estudio Cancer Care Outcomes Research and Surveillance (CanCORS) no tenían conocimiento que, con probabilidad, la terapia no les curaría la enfermedad.[4] De hecho, casi el 40 % de los pacientes de cáncer colorrectal respondieron que era muy probable que la quimioterapia les curara la enfermedad. En un análisis relacionado del conjunto de datos de CanCORS se reveló que solo el 16,5 % de los pacientes dijeron estar conscientes de su pronóstico de forma plena.[5] Resultados similares dan cuenta de un estudio con pacientes de cáncer avanzado que evaluaron su comprensión del pronóstico al momento de su ingreso y después de 12 semanas.[6]
En la sección Posibles obstáculos para planificar la transición a la atención en la etapa final de la vida, se resumen las explicaciones factibles para el déficit de comunicación con relación al pronóstico. Sin embargo, con independencia de la explicación, los malentendidos del paciente sobre el pronóstico perjudican la capacidad del paciente de tomar decisiones bien fundamentadas sobre el cuidado de su salud que sean congruentes con sus valores, metas y preferencias. En última instancia, cada oncólogo clínico, escoge, de cierta forma, cuándo y cómo explicarle al paciente de cáncer avanzado que es poco probable que el tratamiento directo de la enfermedad sea eficaz y que un enfoque continuo en el tratamiento puede perjudicar al paciente.
El propósito de esta sección del resumen es proveer a los médicos un marco de trabajo para sopesar su función en la planificación de la transición a la etapa terminal (ET) y dialogar con los pacientes y sus seres queridos sobre el concepto de transición.
La relación médico paciente y la planificación de la transición a los cuidados paliativos terminales
Es importante que los oncólogos clínicos tomen en consideración como su relación con el paciente ayudará a este a expresar sus preferencias en congruencia con sus valores y metas de recibir un cuidado terminal de excelente calidad. Un estudio propuso los siguientes 4 modelos de la relación médico paciente, con base en las metas de interacción, las obligaciones del médico, la importancia de los valores del paciente y cómo la autonomía del paciente influye en la relación:[7]
- Paternalista: el foco está en la evaluación y juicio del médico sobre el mejor tratamiento, con muy poca o ninguna participación del paciente que no sea dar su autorización.
- Informativa: el foco está en el médico que le provee al paciente una información lo más completa posible sobre la enfermedad y tratamiento, dejando que sea el paciente quien tome sus decisiones.
- Interpretativa: el médico actúa como consejero a fin de ayudar al paciente a discernir sus valores y preferencias, provee información médica y luego aconseja al paciente sobre cuáles pruebas y tratamientos apropiados reflejan mejor los valores del paciente.
- Deliberativa: la función del médico es ayudar al paciente a determinar y escoger la mejor meta en cuanto a sus opciones de salud, con una actitud de amigo o maestro. El médico desempeña una parte activa al sugerir cuales valores y opciones valen más la pena.
En un razonamiento argumentado con cuidado, los autores concluyeron que el modelo predilecto es el deliberativo, el cual se puede resumir como la creencia de que las metas y preferencias del paciente están abiertas al cambio. La meta de esta relación es ayudar al paciente a escoger las mejores metas y opciones relacionadas con la salud que pueden obtenerse, dada la situación clínica. La obligación del médico es explicarle al paciente las metas y preferencias más imperativas e informarle de otras opciones. En este sentido, el médico es un maestro.[7]
Los estudios cualitativos sobre la percepción de la toma de decisiones indica que el modelo deliberativo en la relación médico paciente es de suma importancia en cáncer avanzado. Por ejemplo, un grupo de investigadores entrevistó a 36 pacientes de cáncer esofágico con posibilidad de curación sobre su decisión de someterse a una esofagectomía. Los investigadores anticipaban que los temas relacionados con la autonomía, las decisiones compartidas y revelación de la información serían obvios; sin embargo, surgieron los siguientes temas:[8]
- Creencias culturales sobre la cura mediante cirugía.
- Aumento de la confianza a través del proceso de derivación.
- Idealización del cirujano especializado.
- Creencia en la práctica en vez de la información médica.
- Resignación al riesgo del tratamiento.
- Aceptación de las recomendaciones de un experto como autorización para el tratamiento.
Otro grupo de investigadores entrevistaron a pacientes de carcinoma pancreático e identificaron, durante el transcurso del tiempo, un cambio de actitudes en sus decisiones sobre el tratamiento.[9] En un principio, los pacientes mostraron poco interés en los detalles sobre los tratamientos médicos o quirúrgicos y enfatizaron su confianza en el médico. Luego, en la medida en que los pacientes mostraron más experiencia con la progresión de la enfermedad y los tratamientos, estos mostraron la búsqueda de una actitud más proactiva en las decisiones sobre el tratamiento. Todos los pacientes dijeron haber tenido conversaciones sobre lo precario de su pronóstico, pero un tema común era la dificultad en reconocer cuándo era el momento de suspender el tratamiento y hacer la transición a los cuidados paliativos terminales.
Planificación de la transición desde el diagnóstico a los cuidados paliativos terminales.
La palabra transición implica el paso de un lugar a otro. Por tanto, la planificación de la transición a los cuidados paliativos requiere una comprensión compartida del punto en el cual se encuentra el paciente de cáncer avanzado en la trayectoria de la enfermedad y por qué es necesaria o aconsejable la transición.
El momento más oportuno de transición a los cuidados paliativos terminales es cuando el cambio es más congruente con los objetivos del paciente en cuanto a su cuidado. Al determinar cuándo dar el paso hacia la transición para cuidados terminales, el oncólogo clínico se esforzará por ser un maestro y amigo de confianza. El médico debe presentar su opinión sobre la eficacia del tratamiento continuo directo al cáncer y ayudar al paciente a comprender sus propios valores, perspectivas, metas de tratamiento y preferencias. De esta forma el médico ayuda al paciente a elaborar sus preferencias en cuanto al tratamiento y cuidados en la etapa terminal.[10]
El concepto de transición por lo general se invoca desde una perspectiva sanitaria.[11,12] Por ejemplo, se habla con frecuencia sobre los pacientes que recibieron quimioterapia adyuvante con intenciones curativas y se dice que realizan la transición desde la fase curativa a la fase paliativa del tratamiento.
La imagen a continuación describe un modelo sobre las fases de la planificación para la etapa terminal de los pacientes de cáncer avanzado.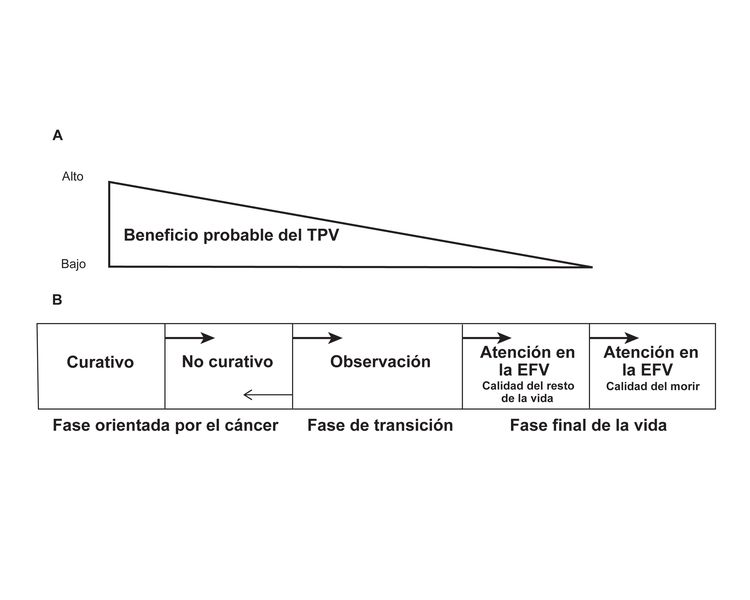
El Panel A de la imagen muestra, con el transcurso del tiempo, un aumento del riesgo en relación con el beneficio de los tratamientos contra la enfermedad. Esta conceptualización, lo es también desde la perspectiva del oncólogo clínico. El oncólogo clínico puede escoger dos tácticas para compartir la comprensión de la disminución en la proporción riesgo beneficio:
- Distinguir entre eficacia y beneficio: las decisiones sobre el cuidado de la salud que toman los pacientes de cáncer avanzado hacia los cuidados paliativos terminales podrían, algunas veces parecer contrarios a su mejor interés desde el punto de vista médico.[13] Tal vez una explicación relevante de esta diferencia es que el paciente piensa en términos de beneficio, lo cual incluye los resultados posibles y que tan deseados sean estos; mientras que los médicos piensan sobre las pruebas de eficacia, lo cual se evalúa con las probabilidades.[14]
- Explore la comprensión del paciente sobre el pronóstico y sus objetivos en las eventualidades importantes: hay unos puntos relativamente discontinuos en la trayectoria de la enfermedad, llamados eventualidades, cuando el oncólogo tienen le oportunidad de clarificar el pronóstico y discernir los objetivos y preferencias del paciente.[15] Entre las eventualidades están las evaluaciones periódicas del estado de la enfermedad (es decir, repetición de las dimensiones tumorales luego de la prescripción de un número de ciclos quimioterapéuticos), los efectos de la quimioterapia en la calidad de vida en general relativa a la salud y los efectos secundarios o complicaciones de la progresión de la enfermedad o su tratamiento (es decir, disminución del estado funcional).
El panel B de la imagen representa el concepto de transición. La trayectoria de la enfermedad se divide en cinco fases relativamente discontinuas, desde el diagnóstico de cáncer avanzado a la muerte. Las primeras dos fases están dominadas por las estrategias dirigidas a la enfermedad, lo que incluye una fase en la que la intención del tratamiento dirigido a la enfermedad es la cura y una segunda fase en la que la intención del tratamiento es el alivio de los síntomas, el control de la enfermedad y, quizás, una mejoría en la esperanza de vida. La fase terminal se subdivide en el tiempo en que el paciente no recibe tratamiento pero que quizás lo espera en el futuro, y la fase en que la meta de tratamiento es asegurar que la etapa terminal esté libre de sufrimientos y cargas innecesarias. Con frecuencia se modifican imágenes similares a fin de incluir una línea diagonal que describe un aumento gradual del enfoque en cuidados paliativos a medida que el cáncer progresa y la vida llega a su término.
La imagen representa la trayectoria del cáncer avanzado con el fin de ayudar a los oncólogos a formular y articular las diferencias, con potencial de destacarse, entre las fases, desde la perspectiva del oncólogo y en términos de lo siguiente:
- Opciones, intenciones, amplitud de los resultados posibles y probabilidades de desenlace del tratamiento.
- Probabilidades de que se presenten, entre otros, los riesgos y el agobio que conlleva cada opción en términos de efectos secundarios y requisitos prácticos de tratamiento.
- Actividades clave (es decir, quimioterapia) evaluaciones periódicas sobre el estado de la enfermedad, y los resultados del tratamiento en relación con cada opción o fase.
El oncólogo clínico debe empeñarse en comunicar la información de una manera compasiva y comprensible para el paciente y sus familiares. Para obtener más información, consultar la sección Estrategias para mejorar la comunicación y la toma de decisiones entre el paciente de cáncer avanzado y el oncólogo.
Sin embargo, el describir de forma clara cada fase, no le comunica de manera necesaria al paciente cuándo es el momento de transición. Un estudio con un grupo focal compuesto de proveedores de atención de la salud, pacientes de cáncer avanzado y otras enfermedades terminales, así como familiares, priorizaron 3 destrezas de comunicación independientes que eran valiosas para la persona moribunda:[16]
- Comunicar las noticias desagradables con sensibilidad.
- Hablar sobre el morir.
- Reconocer el momento en que el paciente está listo para hablar sobre la muerte.
En conclusión, el momento apropiado de transición desde los tratamientos dirigidos a la enfermedad, hacia los cuidados paliativos terminales depende en gran parte de los objetivos y preferencias del paciente. Los hechos indican que las conversaciones sobre el cuidado terminal son difíciles pero muy beneficiosas para el paciente. Los oncólogos que posponen iniciar estas conversaciones importantes o que se comunican de forma ambigua o con un lenguaje difícil de comprender, no alcanzan a cumplir "la tarea principal del médico cuando cuida de un persona gravemente enferma, que es acompañar y guiar al paciente el cual, como es de esperarse, no se quiere morir; a través del camino de transición".[17]
Bibliografía
- OKEN D: What to tell cancer patients. A study of medical attitudes. JAMA 175: 1120-8, 1961. [PUBMED Abstract]
- Novack DH, Plumer R, Smith RL, et al.: Changes in physicians' attitudes toward telling the cancer patient. JAMA 241 (9): 897-900, 1979. [PUBMED Abstract]
- Eidinger RN, Schapira DV: Cancer patients' insight into their treatment, prognosis, and unconventional therapies. Cancer 53 (12): 2736-40, 1984. [PUBMED Abstract]
- Weeks JC, Catalano PJ, Cronin A, et al.: Patients' expectations about effects of chemotherapy for advanced cancer. N Engl J Med 367 (17): 1616-25, 2012. [PUBMED Abstract]
- Liu PH, Landrum MB, Weeks JC, et al.: Physicians' propensity to discuss prognosis is associated with patients' awareness of prognosis for metastatic cancers. J Palliat Med 17 (6): 673-82, 2014. [PUBMED Abstract]
- Craft PS, Burns CM, Smith WT, et al.: Knowledge of treatment intent among patients with advanced cancer: a longitudinal study. Eur J Cancer Care (Engl) 14 (5): 417-25, 2005. [PUBMED Abstract]
- Emanuel EJ, Emanuel LL: Four models of the physician-patient relationship. JAMA 267 (16): 2221-6, 1992 Apr 22-29. [PUBMED Abstract]
- McKneally MF, Martin DK: An entrustment model of consent for surgical treatment of life-threatening illness: perspective of patients requiring esophagectomy. J Thorac Cardiovasc Surg 120 (2): 264-9, 2000. [PUBMED Abstract]
- Schildmann J, Ritter P, Salloch S, et al.: 'One also needs a bit of trust in the doctor ... ': a qualitative interview study with pancreatic cancer patients about their perceptions and views on information and treatment decision-making. Ann Oncol 24 (9): 2444-9, 2013. [PUBMED Abstract]
- Epstein RM, Peters E: Beyond information: exploring patients' preferences. JAMA 302 (2): 195-7, 2009. [PUBMED Abstract]
- Agren Bolmsjö I, Nilstun T, Löfmark R: From cure to palliation: agreement, timing, and decision making within the staff. Am J Hosp Palliat Care 24 (5): 366-70, 2007 Oct-Nov. [PUBMED Abstract]
- Gramling R, Norton SA, Ladwig S, et al.: Direct observation of prognosis communication in palliative care: a descriptive study. J Pain Symptom Manage 45 (2): 202-12, 2013. [PUBMED Abstract]
- Matsuyama R, Reddy S, Smith TJ: Why do patients choose chemotherapy near the end of life? A review of the perspective of those facing death from cancer. J Clin Oncol 24 (21): 3490-6, 2006. [PUBMED Abstract]
- Pellegrino ED: Decisions to withdraw life-sustaining treatment: a moral algorithm. JAMA 283 (8): 1065-7, 2000. [PUBMED Abstract]
- Walling A, Lorenz KA, Dy SM, et al.: Evidence-based recommendations for information and care planning in cancer care. J Clin Oncol 26 (23): 3896-902, 2008. [PUBMED Abstract]
- Wenrich MD, Curtis JR, Shannon SE, et al.: Communicating with dying patients within the spectrum of medical care from terminal diagnosis to death. Arch Intern Med 161 (6): 868-74, 2001. [PUBMED Abstract]
- Finucane TE: How gravely ill becomes dying: a key to end-of-life care. JAMA 282 (17): 1670-2, 1999. [PUBMED Abstract]
Actualizaciones más recientes a este resumen (03/21/2025)
Los resúmenes del PDQ con información sobre el cáncer se revisan con regularidad y se actualizan a medida que se obtiene nueva información. Esta sección describe los cambios más recientes introducidos en este resumen a partir de la fecha arriba indicada.
Se actualizaron las estadísticas con el número estimado de defunciones para 2025 (se citó a la American Cancer Society como referencia 1).
Factores que influyen en las decisiones y los desenlaces en la etapa final de la vida
Se actualizó la American Cancer Society como referencia 7.
El Consejo editorial del PDQ sobre los cuidados médicos de apoyo y los cuidados paliativos es responsable de la redacción y actualización de este resumen y mantiene independencia editorial respecto del NCI. El resumen refleja una revisión independiente de la bibliografía médica y no representa las políticas del NCI ni de los NIH. Para obtener más información sobre las políticas relativas a los resúmenes y la función de los consejos editoriales del PDQ responsables de su actualización, consultar Información sobre este resumen del PDQ e Información del PDQ® sobre el cáncer dirigida a profesionales de la salud.
Información sobre este resumen del PDQ
Propósito de este resumen
Este resumen de información del PDQ sobre el cáncer dirigido a profesionales de la salud proporciona información integral revisada por expertos y basada en la evidencia sobre la planificación para la atención del cáncer avanzado en la etapa final de la vida. El objetivo es servir como fuente de información y ayuda para los profesionales clínicos durante la atención de pacientes. No ofrece pautas ni recomendaciones formales para tomar decisiones relacionadas con la atención sanitaria.
Revisores y actualizaciones
El consejo editorial del PDQ sobre los cuidados médicos de apoyo y los cuidados paliativos, que mantiene independencia editorial respecto del Instituto Nacional del Cáncer (NCI), revisa este resumen de manera periódica y, en caso necesario, lo actualiza. Este resumen es el resultado de una revisión bibliográfica independiente y no constituye una declaración de política del NCI ni de los Institutos Nacionales de la Salud (NIH).
Cada mes, los integrantes de este consejo revisan los artículos publicados recientemente para determinar lo siguiente:
- Si el artículo se debe analizar en una reunión del consejo.
- Si conviene añadir texto acerca del artículo.
- Si se debe reemplazar o actualizar un artículo que ya se citó.
Los cambios en los resúmenes se deciden mediante consenso de los integrantes del consejo después de evaluar la solidez de la evidencia de los artículos publicados y determinar la forma de incorporar el artículo en el resumen.
Los revisores principales del sumario sobre Planificar la transición para la atención del cáncer avanzado en la etapa final de la vida son:
- Larry D. Cripe, MD (Indiana University School of Medicine)
- Natalie Jacobowski, MD (Nationwide Children's Hospital)
- Jared R. Lowe, MD, HMDC (University of North Carolina School of Medicine)
- Maria Petzel, RD, CSO, LD, CNSC, FAND (University of TX MD Anderson Cancer Center)
- Joanna J. Sharpless, MD (University of California San Francisco)
Cualquier comentario o pregunta sobre el contenido de este resumen se debe enviar al Servicio de Información de Cáncer del Instituto Nacional del Cáncer. Por favor, no enviar preguntas o comentarios directamente a los integrantes del consejo, ya que no responderán consultas de manera individual.
Niveles de evidencia
Algunas de las referencias bibliográficas de este resumen se acompañan del nivel de evidencia. El propósito de esto es ayudar al lector a evaluar la solidez de la evidencia que respalda el uso de ciertas intervenciones o abordajes. El consejo editorial del PDQ sobre los cuidados médicos de apoyo y los cuidados paliativos emplea un sistema de jerarquización formal para asignar los niveles de evidencia científica.
Permisos para el uso de este resumen
PDQ (Physician Data Query) es una marca registrada. Se autoriza el uso del texto de los documentos del PDQ; sin embargo, no se podrá identificar como un resumen de información sobre cáncer del PDQ del NCI, salvo que el resumen se reproduzca en su totalidad y se actualice de manera periódica. Por otra parte, se permitirá que un autor escriba una oración como “En el resumen del PDQ del NCI de información sobre la prevención del cáncer de mama se describen, de manera concisa, los siguientes riesgos: [incluir fragmento del resumen]”.
Se sugiere citar la referencia bibliográfica de este resumen del PDQ de la siguiente forma:
PDQ® sobre los cuidados médicos de apoyo y los cuidados paliativos. PDQ Planificar la transición para la atención del cáncer avanzado en la etapa final de la vida. Bethesda, MD: National Cancer Institute. Actualización: <MM/DD/YYYY>. Disponible en: https://www.cancer.gov/espanol/cancer/cancer-avanzado/planes/etapa-final-pro-pdq. Fecha de acceso: <MM/DD/YYYY>.
Las imágenes en este resumen se reproducen con autorización del autor, el artista o la editorial para uso exclusivo en los resúmenes del PDQ. La utilización de las imágenes fuera del PDQ requiere la autorización del propietario, que el Instituto Nacional del Cáncer no puede otorgar. Para obtener más información sobre el uso de las ilustraciones de este resumen o de otras imágenes relacionadas con el cáncer, consultar Visuals Online, una colección de más de 2000 imágenes científicas.
Cláusula sobre el descargo de responsabilidad
La información en estos resúmenes no se debe utilizar para justificar decisiones sobre reembolsos de seguros. Para obtener más información sobre la cobertura de seguros, consultar la página Manejo de la atención del cáncer en Cancer.gov/espanol.
Comuníquese con el Instituto Nacional del Cáncer
Para obtener más información sobre las opciones para comunicarse con el NCI, incluso la dirección de correo electrónico, el número telefónico o el chat, consultar la página del Servicio de Información de Cáncer del Instituto Nacional del Cáncer.