Se aprueba el enfortumab vedotina para el cáncer de vejiga recidivante
, por el Equipo del NCI
El 18 de diciembre de 2019 la Administración de Alimentos y Medicamentos (FDA) otorgó la aprobación acelerada del enfortumab vedotina-ejfv (Padcev) para su uso en personas con cáncer de vejiga avanzado que progresó a pesar de que recibieron dos terapias anteriores.
El enfortumab vedotina fue el segundo medicamento dirigido que se aprobó en 2019 para tratar el cáncer de vejiga avanzado. A principios de este año, la FDA otorgó la aprobación acelerada del erdafitinib (Balversa). Sin embargo, solo es posible usar el erdafitnib para tratar cánceres con una alteración en uno de varios genes que se llaman FGFR. Solo alrededor de 20 % de los cánceres de vejiga presentan una alteración en FGFR.
"Hemos estado buscando por todos los medios una nueva opción de tratamiento para los pacientes" con enfermedad progresiva avanzada, manifestó Joaquim Bellmunt, doctor y licenciado en Medicina, que dirige el Programa de Cáncer de Vejiga del Centro Médico Beth Israel Deaconess de Boston.
La aprobación del enfortumab vedotina se fundamenta en los hallazgos de una cohorte de participantes en un estudio clínico pequeño llamado EV-201 que incluyó a personas con cáncer de vejiga metastásico. Como tratamiento inicial o de primera línea, los 125 participantes en la cohorte habían recibido quimioterapia con medicamentos a base de platino (como cisplatino y oxaliplatino). Cuando el cáncer progresó, se usó un inhibidor de puntos de control inmunitario como segunda línea de tratamiento.
Todos los pacientes en el estudio recibieron enfortumab vedotina. En general, en 55 participantes (44 %) los cánceres se achicaron o dejaron de crecer durante el tratamiento. En 15 de estos casos, los tumores desaparecieron en su totalidad; esto se conoce como respuesta completa. Las respuestas al tratamiento duraron una mediana de 7,6 meses. El estudio fue financiado por los fabricantes del medicamento, Seattle Genetics y Astellas Pharma.
En la actualidad, la tercera línea de tratamiento convencional para las personas con cáncer de vejiga metastásico es la quimioterapia con derivados del taxano, como paclitaxel y docetaxel.
"Menos del 10 % de nuestros pacientes presentan respuestas a estos regímenes", puntualizó el doctor Tian Zhang, de la Universidad Duke, que trabaja en otro estudio en curso sobre enfortumab vedotina. "Hemos observado respuestas excelentes [con enfortumab vedotina], y tengo bastante optimismo de que muchos de mis pacientes se beneficiarán de este medicamento".
Un blanco común
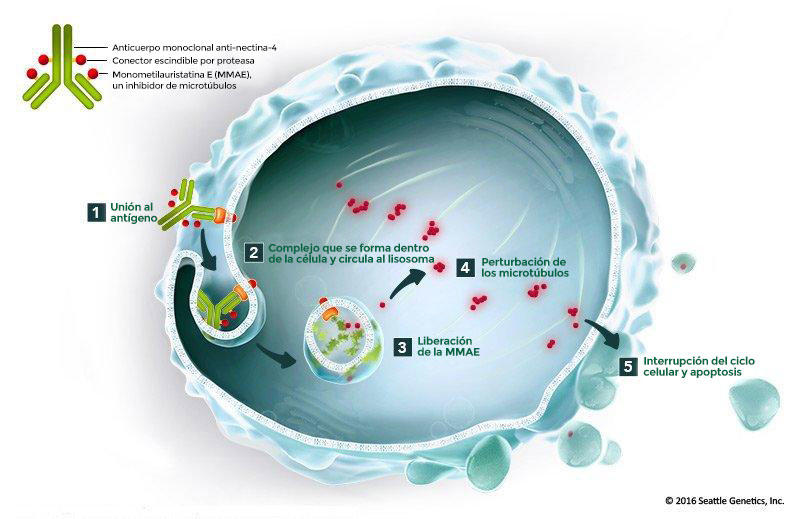
El enfortumab vedotina es un tipo de conjugado anticuerpo-fármaco que se usa en la terapia dirigida. Los conjugados anticuerpo-fármaco consisten en un anticuerpo monoclonal que se une químicamente a un fármaco.
La parte del anticuerpo monoclonal del enfortumab vedotina se une a una proteína llamada nectina-4 que se encuentra en la superficie de la mayoría de las células del cáncer de vejiga. El anticuerpo se une químicamente a la monometilauristatina E (MMAE), un tipo de medicamento quimioterapéutico llamado inhibidor de microtúbulos. Una vez que las células absorben el conjugado, este impide que se dividan y las destruye.
Como la nectina-4 está presente en la mayoría de los cánceres de vejiga, no se necesitan pruebas diagnósticas para determinar si los pacientes pueden recibir el tratamiento, explicó el doctor Bellmunt.
Los participantes inscritos en el estudio EV-201 recibieron infusiones del medicamento cerca de 3 veces al mes hasta que la enfermedad progresó o se presentaron efectos secundarios intolerables, o hasta que los pacientes decidieron dejar el estudio por cualquier motivo.
Los efectos secundarios más comunes incluyeron cansancio, caída del cabello, disminución del apetito, cambios en el sentido del gusto y neuropatía periférica. La neutropenia febril (fiebre y reducción en el número de glóbulos blancos) fue el efecto secundario grave más común del tratamiento.
Casi la mitad de los participantes tuvieron erupción cutánea por el tratamiento, pero casi siempre fue leve.
En general, los efectos secundarios llevaron a la reducción de la dosis de enfortumab vedotina en 32 % de los pacientes y a la interrupción del tratamiento en 12 % de los pacientes. La causa más común para la reducción de la dosis y el abandono del tratamiento fue la neuropatía periférica.
En el momento de la publicación de los resultados preliminares del estudio clínico, casi la mitad de los 55 pacientes que respondieron al medicamento seguían sin tener progresión del cáncer. Las respuestas duraron desde cerca de 3 meses hasta más de 11 meses.
Aunque el estudio clínico aún está en curso, los investigadores calcularon que la mediana de supervivencia sin progresión fue de 5,8 meses, y la mediana de supervivencia general fue de 11,7 meses.
Más estudios
Con las aprobaciones aceleradas, los fabricantes de medicamentos deben realizar más estudios y verificar el beneficio clínico de los tratamientos. En un estudio clínico en fase 3 en curso se está comparando el enfortumab vedotina con la quimioterapia a base de taxano como tercera línea de tratamiento.
En la actualidad, hay preguntas sin responder sobre cuáles medicamentos de tercera línea se deben administrar primero a las personas que tienen cáncer de vejiga con alteración en FGFR, que podrían también recibir erdafitinib.
El doctor Bellmunt explicó que "no sabemos si el orden [de administración de estos medicamentos] es importante porque [aún] no hay estudios clínicos ni datos".
Además, debido a que los índices de respuesta al tratamiento en el estudio EV-201 fueron tan altos (comparables a los que se observan en las terapias de primera línea), los investigadores ya comenzaron a probar el enfortumab vedotina más al comienzo del tratamiento, dijo el doctor Zhang.
Por ejemplo, en un estudio clínico en curso se está probando el enfortumab vedotina solo y en combinación con la inmunoterapia, la quimioterapia o ambas terapias, como tratamiento inicial para las personas con cáncer de vejiga avanzado.
Los resultados preliminares de uno de los grupos del estudio se presentaron en septiembre de 2019 en el congreso anual de la Sociedad Europea de Oncología Médica (ESMO). Según los datos, se observaron índices de respuesta de alrededor de 70 % con el uso combinado del enfortumab vedotina y el inhibidor de puntos de control inmunitario pembrolizumab (Keytruda) en pacientes que estaban demasiado enfermos para recibir quimioterapia a base de platino. Ese tipo de tasa de respuesta es "fenomenal" para las personas con cáncer de vejiga metastásico, explicó el doctor Zhang.
"El concepto es tratar realmente de administrar tratamientos activos más al inicio del proceso de la enfermedad", recalcó el doctor Zhang. "Deseamos [saber] más sobre el enfortumab vedotina, incluso potencialmente para [tratar] las enfermedades localizadas".