Se confirmó en un estudio que la terapia CAR-T beneficia a las personas con linfoma de crecimiento rápido
, por Sharon Reynolds
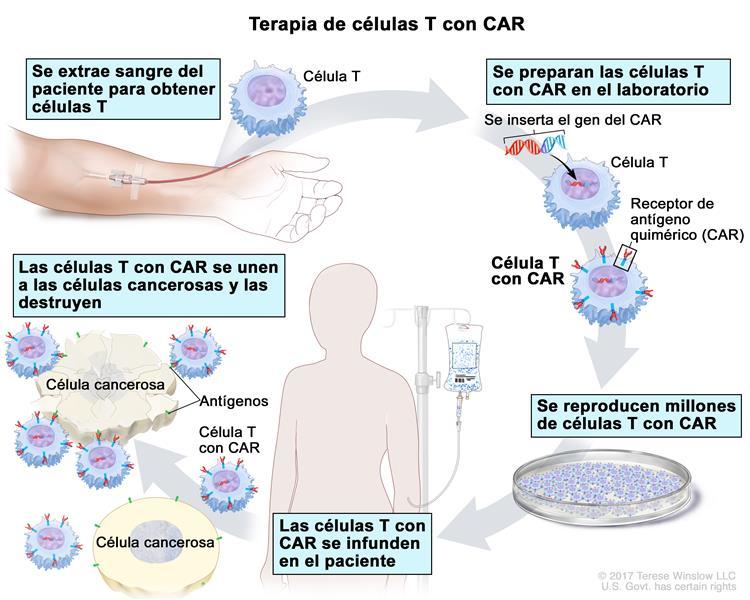
La terapia de células T con receptores quiméricos para antígenos (CAR-T), un tipo de inmunoterapia personalizada, ayuda a curar a algunas personas con linfoma no Hodgkin (LNH) de crecimiento rápido. Esto se señaló en los resultados actualizados de un estudio clínico aleatorizado grande de fase 3 de la terapia CAR-T con axicabtagén ciloleucel (Yescarta).
La mayoría de las personas con diagnóstico de linfoma difuso de células B grandes, la forma más común de LNH de crecimiento rápido, se curan con un tratamiento inicial de quimioterapia. Pero para quienes no se curan, las posibilidades hasta el momento eran dudosas en el mejor de los casos, incluso cuando se añaden la quimioterapia intensa y un trasplante de células madre.
Ahora, los nuevos datos del estudio clínico ZUMA-7 indican con solidez que la terapia CAR-T con axicabtagén ciloleucel ofrece una esperanza real para este último grupo de pacientes.
Los investigadores del estudio presentaron los hallazgos el 5 de junio en la reunión anual de la Sociedad Estadounidense de Oncología Clínica (ASCO). Según ellos, calculan que alrededor del 55 % de los pacientes seguirían vivos 4 años después de recibir axicabtagén ciloleucel, en comparación con el 46 % de quienes recibieron al comienzo el tratamiento estándar para la enfermedad en recaída.
“Este es el primer estudio en casi 30 años que mejora significativamente la supervivencia general de los pacientes con linfoma de células B grandes que no responden al tratamiento inicial o que recayeron”, destacó el doctor Jason Westin, del Centro Oncológico MD Anderson de la Universidad de Texas, que ayudó a dirigir el estudio.
Después de un seguimiento de los pacientes durante casi 4 años, es probable que quienes están vivos se hayan curado, agregó.
A partir de estos resultados, el axicabtagén ciloleucel es ahora el tratamiento preferido para las personas cuyo linfoma difuso de células B grandes recidivó muy rápido o fue resistente al tratamiento inicial estándar, explicó el doctor Christopher Melani, del Centro de Investigación Oncológica del NCI. Para futuros estudios, la terapia con el axicabtagén ciloleucel “es ahora el punto de referencia para mejorar los tratamientos futuros”, explicó el doctor Melani.
Una mejora clara de la supervivencia
Hasta hace poco, el único tratamiento con la posibilidad de eliminar el linfoma difuso de células B grandes recurrente o resistente al tratamiento era la quimioterapia adicional en dosis altas, seguida de un trasplante autólogo de células madre. Las células madre sanas formadoras de sangre de un paciente se obtienen de la sangre o la médula ósea antes del tratamiento y se devuelven al paciente después de administrar una quimioterapia intensiva de dosis altas.
Sin embargo, solo alrededor de la mitad de los pacientes están lo suficientemente sanos como para soportar este tratamiento. Y menos de una cuarta parte de los lo toleran se curan.
Este panorama comenzó a cambiar en 2021, cuando los resultados de dos estudios clínicos grandes mostraron que las células T con CAR podían mejorar el tiempo que las personas con linfoma de células B grandes recurrente o resistente al tratamiento vivían sin que el cáncer empeorara.
Los hallazgos anteriores del estudio ZUMA-7, que comenzó a inscribir pacientes en 2018, llevaron a que la Administración de Alimentos y Medicamentos (FDA) aprobara el axicabtagén ciloleucel en 2022 para los adultos con linfoma difuso de células B grandes que no se eliminó en el tratamiento inicial o que volvió dentro de los 12 meses de la quimioterapia inicial. Esa aprobación se basó en las mejoras observadas en la supervivencia sin complicaciones del LNH, una medida que incluye el tiempo que tarda en comenzar a empeorar la enfermedad después del tratamiento. Pero aún no quedaba en claro si el axicabtagén ciloleucel también mejoraría el tiempo de vida de los pacientes en general.
En el estudio ZUMA-7 se inscribió a personas que se consideraron sanas como para recibir quimioterapia adicional de dosis altas y, en algunos casos, un trasplante autógeno de células madre. Ahora se considera que esta combinación es el tratamiento estándar para el linfoma difuso de células B grandes resistente al tratamiento o en recaída.
Al igual que todas las terapias de CAR-T aprobadas hasta el momento, la terapia con axicabtagén ciloleucel es muy personalizada porque se crea con las propias células inmunitarias del paciente.
En el estudio ZUMA-7, que financió Kite Pharma, el fabricante del axicabtagén ciloleucel, los investigadores asignaron al azar a 180 personas para recibir axicabtagén ciloleucel y a 179 personas para recibir el tratamiento estándar. Las diferencias entre los grupos surgieron pronto. Mientras que el 94 % de las personas en el grupo de axicabtagén ciloleucel recibieron sus células T con CAR, solo el 36 % de las personas del grupo de tratamiento estándar pudieron recibir un trasplante de células madre porque en la mayoría de los casos la enfermedad continuó progresando a pesar de la quimioterapia, explicó el doctor Westin en la reunión de la ASCO.
Debido al rápido avance de la enfermedad, el 57 % de los participantes en el grupo de tratamiento estándar recibieron la terapia CAR-T (en la mayoría de los casos con axicabtagén ciloleucel) después de que empeoró la enfermedad.
La mejora sustancial en el tiempo de vida de las personas en el grupo de axicabtagén ciloleucel se mantuvo incluso cuando muchas personas en el grupo de tratamiento estándar pasaron enseguida a la terapia CAR-T, recalcó el doctor Westin.
La FDA otorgó la aprobación inicial del axicabtagén ciloleucel en 2017 como un tratamiento de tercera línea o posterior. Esto significa que solo se podía administrar a las personas cuya enfermedad seguía empeorando o volvía después de dos o más tipos de terapia, explicó el doctor Melani. Pero los hallazgos de ZUMA-7 indican que esperar tanto tiempo para usar el axicabtagén ciloleucel ya no es el mejor enfoque de tratamiento. “En los pacientes que recibieron quimioterapia primero, se observó que la supervivencia empeoró, incluso cuando la mayoría cambió de grupo para recibir las células T con CAR”, señaló. “Según este estudio, el axicabtagén ciloleucel sería el tratamiento de segunda línea preferido”.
Las terapias CAR-T, incluso las que usan el axicabtagén ciloleucel, a veces producen efectos secundarios graves a largo plazo diferentes a los que se observan después de la quimioterapia. A corto plazo, incluyen una reacción peligrosa del sistema inmunitario llamada síndrome de liberación de citocinas, efectos neurológicos y la reactivación de virus latentes en el cuerpo. A largo plazo, a veces incluyen la inmunodepresión, que tal vez conduzca a segundos cánceres.
En el momento del análisis de datos más reciente, murieron 82 pacientes del grupo de axicabtagén ciloleucel, en comparación con 95 en el grupo de tratamiento estándar. En el grupo de axicabtagén ciloleucel, murieron 7 personas por los efectos secundarios relacionados con el tratamiento, en comparación con 2 personas en el grupo de tratamiento estándar. Sin embargo, desde el análisis de los datos de ZUMA-7 que condujo a la aprobación más reciente de la FDA, no hubo más muertes relacionadas con el tratamiento con axicabtagén ciloleucel.
Aspectos de equidad y acceso
A pesar de que se demostró la eficacia de la terapia CAR-T en un número creciente de personas con cánceres de la sangre como el LNH, hubo problemas por la falta de acceso al tratamiento.
“Está en la letra chica [de la terapia CAR-T]”, mencionó el doctor Melani. “No todo el mundo va a poder conseguirla”.
Uno de los mayores problemas de las terapias CAR-T es el costo. Entre la producción, la hospitalización larga y el seguimiento necesario, “esta [terapia] puede costar medio millón de dólares o más”, indicó el doctor Melani.
“Debemos reducir los costos a… niveles accesibles”, señaló el doctor Asher Chanan-Khan, del Centro Oncológico de la Mayo Clinic, en la reunión de la ASCO. Algunos hospitales universitarios elaboran las células T con CAR en su propio establecimiento, explicó el doctor Melani, y esto podría reducir mucho el precio.
Pero también hay otros aspectos de la terapia CAR-T que afectan el acceso equitativo a este tratamiento, explicó la doctora Leyla Shune, del Centro Oncológico de la Universidad de Kansas, que planteó temas relacionados con la equidad y esta terapia en la reunión de la ASCO.
El manejo de los efectos secundarios únicos, y a menudo peligrosos, de la terapia CAR-T exige una capacitación amplia y práctica. Por lo tanto, en la actualidad, las terapias CAR-T solo se administran en algunos centros especializados, que suelen estar a cientos de millas de distancia de donde viven muchos pacientes, explicó la doctora Shune. Además, como la quimioterapia se administra antes de las terapias CAR-T y hace falta tiempo de recuperación después de recibirla, los pacientes quizás se ausenten del trabajo durante semanas o meses.
“Vivo en un estado donde solo hay dos centros que ofrecen la terapia CAR-T, y mis pacientes tienen que viajar [hasta] 8 horas para llegar aquí”, indicó la doctora Shune. En el futuro, para brindar un acceso más equitativo a la terapia CAR-T, es posible que los programas de asistencia al paciente deban incluir servicios como la asistencia para viajes y el alojamiento subsidiado, explicó.
Otras opciones en curso
Por ahora, las células T con CAR quizás sean un cambio revolucionario para muchas personas con linfoma difuso de células B grandes en recaída o resistente. Pero no son la única opción.
En los estudios clínicos también se está probando otro tipo de inmunoterapia con anticuerpos biespecíficos, que se llama BiTE, en personas con linfoma difuso de células B grandes en recaída o resistente al tratamiento, explicó el doctor Melani. Estos medicamentos se unen a las células inmunitarias y a las células cancerosas al mismo tiempo, lo que permite que las células inmunitarias encuentren y destruyan con facilidad a las células cancerosas al acercarlas.
Dos BiTE, glofitamab (Columvi) y epcoritamab (Epkinly), recibieron recién aprobación acelerada como tratamientos de tercera línea o posteriores para el linfoma difuso de células B grandes, y se están probando como tratamientos más tempranos en otros estudios.
A diferencia de las terapias CAR-T, los BiTE son medicamentos "listos para usar", o sea que no se tienen que elaborar para cada paciente. Es probable que esa característica haga que sean más accesibles para los pacientes porque se podrán administrar en los hospitales más pequeños, donde la mayoría de las personas con cáncer reciben tratamiento, recalcó el doctor Melani.
En otros estudios clínicos, como el ViPOR y el ViPOR-P que se realizan en el Centro Clínico de los NIH, se prueban cócteles de medicamentos dirigidos seleccionados para atacar los puntos débiles conocidos dentro de las células de linfoma.
“Es un momento emocionante en el [tratamiento del] linfoma de crecimiento rápido, con muchas más terapias nuevas que están ayudando a los pacientes a vivir más tiempo”, añadió el doctor Melani.