La aprobación de abemaciclib amplía las opciones iniciales de tratamiento para el cáncer avanzado de seno (mama)
, por Equipo del NCI
La Administración de Alimentos y Medicamentos (FDA) de los Estados Unidos amplió los usos aprobados del fármaco abemaciclib (Verzenio) en mujeres con cáncer de seno (mama).
El 26 de febrero, la dependencia aprobó la terapia dirigida como tratamiento inicial, o de primera línea, para mujeres posmenopáusicas con cáncer metastático o avanzado de seno con tumores con receptores de hormonas y sin HER2.
Según las normas de la aprobación, abemaciclib debe usarse en combinación con un inhibidor de aromatasa, un tipo de terapia hormonal.
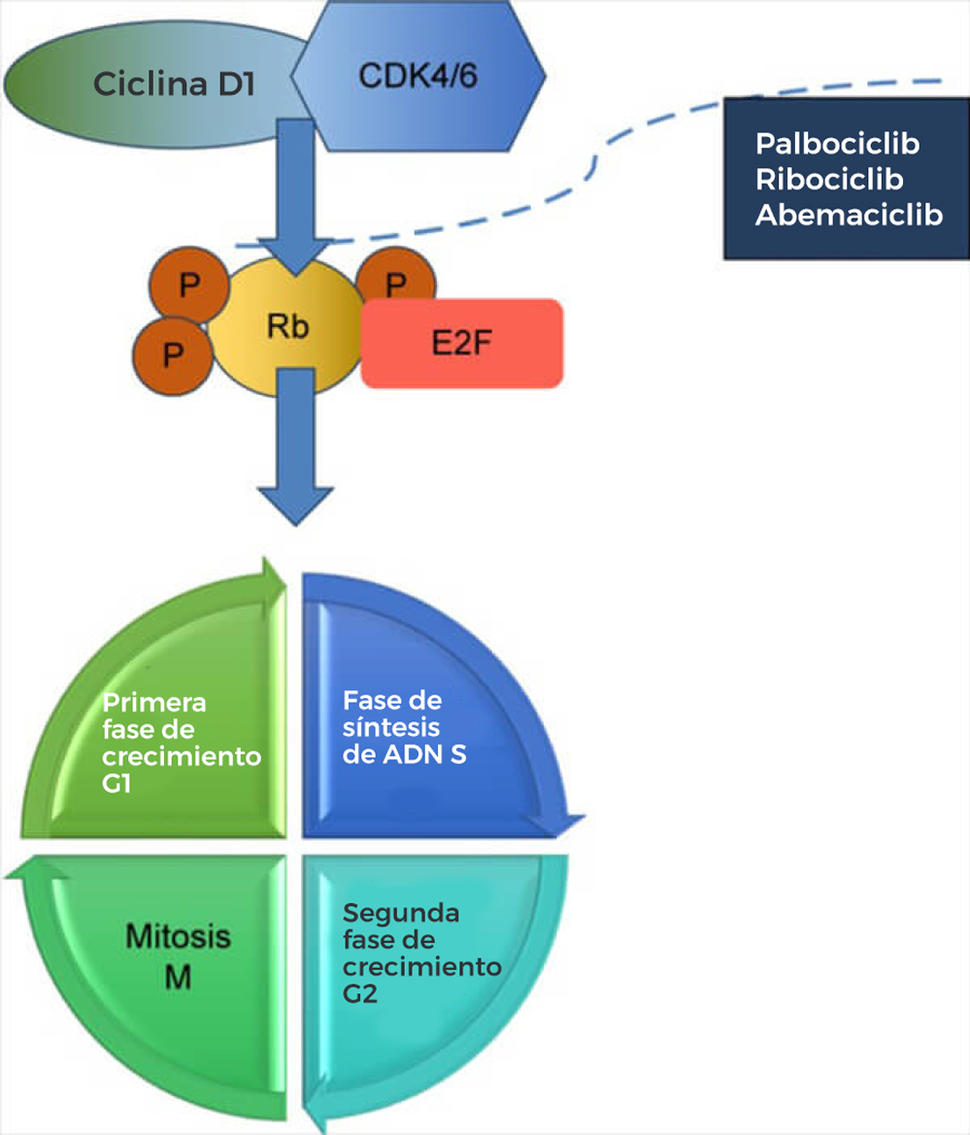
Abemaciclib pertenece a una clase de terapias dirigidas para el cáncer que bloquean la actividad de las proteínas CDK4 y CDK6 (CDK4/6). Estas proteínas pueden convertirse en una doble amenaza, en fomentar el avance de los tumores en el seno y en ayudar a hacerlos resistentes a los tratamientos usados frecuentemente, como los inhibidor de aromatasa.
Otros dos inhibidores de CDK4/6, ribociclib (Kisqali) y palbociclib (Ibrance), recibieron previamente la aprobación como tratamientos de primera línea para mujeres posmenopáusicas con cáncer metastático de seno con receptores de hormonas y sin HER2.
En el estudio clínico en fase 3, denominado MONARCH 3, que llevó a la aprobación de abemaciclib, el fármaco aumentó en forma considerable la vida de las mujeres sin avance de la enfermedad (supervivencia sin avance).
"La magnitud del efecto, al compararse con el uso de un solo inhibidor de aromatasa, es similar al efecto observado con los inhibidores de CDK4/6 aprobados previamente", explicó la doctora Alexandra Zimmer, de la Unidad de Malignidades en Mujeres en el Centro de Investigación Oncológica del NCI.
La aprobación, continuó la doctora Zimmer, "convierte a abemaciclib en otra opción de primera línea para estas pacientes".
Aumento de la supervivencia sin avance, pero con algunos efectos secundarios
La FDA aprobó inicialmente a abemaciclib en octubre de 2017 para mujeres con cáncer avanzado de seno con receptores de hormonas y sin HER2, cuya enfermedad había regresado después del tratamiento con inhibidores de aromatasa u otras terapias hormonales.
El estudio MONARCH 3 inscribió a casi 500 mujeres posmenopáusicas con cáncer avanzado de seno con receptores de hormonas y sin HER2, que no habían recibido previamente tratamiento para el cáncer avanzado. Las participantes del estudio fueron asignadas al azar para recibir abemaciclib o un placebo, en conjunto con uno o dos inhibidores de aromatasa, anastrozol (Arimidex) o letrozol (Femara). El estudio fue financiado por Eli Lilly, fabricante de abemaciclib.
Además de presentar un aumento de la supervivencia sin avance, más mujeres tratadas con abemaciclib y un inhibidor de aromatasa experimentaron al menos algo de reducción en el tamaño de sus tumores que las mujeres tratadas únicamente con un inhibidor de aromatasa: 59 % frente a 44 %.
Aproximadamente 20 % de las mujeres en el estudio tratadas con abemaciclib tuvieron que detener el tratamiento debido a los efectos secundarios, y más de 40 % tuvieron que reducir la dosis del fármaco.
Al igual que en otros estudios con abemaciclib, el efecto secundario grave más frecuente para quienes recibían el fármaco fue diarrea que se presentó en aproximadamente 80 % de los pacientes. En general, el efecto secundario fue controlable, informaron los directores del estudio, con más casos de diarrea tratada con medicamentos usados comúnmente y/o reducciones de la dosis de abemaciclib.
La fatiga leve y las náuseas fueron también frecuentes en mujeres tratadas con abemaciclib.
¿Cuál inhibidor de CDK4/6 para cuál paciente?
Los inhibidores de CDK4/6 aprobados, "han cambiado la manera en que controlamos el cáncer de seno con receptores de hormonas", dijo el doctor Andres Forero, quien dirige el Programa de Cáncer de Seno en la Facultad de Medicina Birmingham de la Universidad de Alabama.
El doctor Forero continuó diciendo que el gran desafío para los oncólogos en este momento es decidir cuál inhibidor de CDK4/6 es la mejor opción para cada paciente en particular. "Esa es la pregunta del millón", dijo el doctor.
A pesar de compartir el mismo blanco molecular en las células cancerosas, cada uno de los tres fármacos tiene diferentes efectos secundarios, dijo la doctora Zimmer. Además, esas diferencias podrían ayudar a identificar cuáles pacientes podrían beneficiarse más de recibir uno u otro fármaco.
Por ejemplo, la diarrea intensa es más común con abemaciclib que con palbociclib o ribociclib, señaló la doctora. Por otra parte, la reducción considerable de glóbulos blancos (neutropenia) es más común en pacientes tratados con palbociclib, y es más probable que los pacientes tratados con ribociclib presenten un tipo de cambio en el ritmo cardíaco denominado prolongación del QT.
El doctor Forero estuvo de acuerdo en que otros problemas de salud que pudieran exacerbarse con cada fármaco respectivo pueden ayudar a determinar las decisiones de tratamiento para cada paciente.
¿Qué será lo siguiente con los inhibidores de CDK4/6?
Una de las grandes preguntas actuales, dijo la doctora Zimmer, es si las mujeres tratadas con un inhibidor de CDK4/6 cuyos cánceres comienzan a avanzar deberían continuar el tratamiento junto con la adición de otra terapia.
Otra pregunta es si los inhibidores de CDK4/6 podrían mejorar los desenlaces de salud en mujeres con cánceres en estadio inicial. Los tres inhibidores de CDK4/6 aprobados por la FDA, de hecho, están siendo probados en estudios clínicos grandes en fase 3 de mujeres con cáncer de seno en estadio inicial con receptores de hormonas y sin HER2, tanto como tratamiento prequirúrgico (neoadyuvante) como posoperatorio (adyuvante)
En otros estudios también se están probando inhibidores de CDK4/6 en mujeres con cáncer de seno con HER2, usando los fármacos en combinación con terapias que actúan sobre HER2 como trastuzumab (Herceptin) y lapatinib (Tykerb), detalló el doctor Forero.
"Me parece que el próximo gran éxito para estos fármacos estará en los cánceres con HER2", opinó el doctor.