Darolutamida retrasa la diseminación de algunos cánceres de próstata
, por Equipo del NCI
El fármaco experimental darolutamida puede retrasar la diseminación de cáncer de próstata a otras partes del cuerpo en hombres con enfermedad no metastática resistente a la castración, de acuerdo con los resultados de un estudio clínico a gran escala. Además, parecería que el fármaco no produce alguno de los efectos secundarios observados con fármacos similares usados para tratar a hombres con esta forma de cáncer de próstata, según demostraron los resultados del estudio.
Hasta hace poco, no se contaba con opciones eficaces de tratamiento para pacientes con cáncer de próstata no metastático resistente a la castración. En estos casos, los tumores prostáticos siguen creciendo aún después de recibir terapia de privación androgénica (TPA), tratamiento que tiene el fin de mantener la concentración de andrógenos en el cuerpo extremadamente baja o no detectable.
Pero durante los últimos dos años, la Administración de Medicamentos y Alimentos (FDA) aprobó dos fármacos para tratar esta forma de la enfermedad, y algunos investigadores esperan que, basándose en los resultados de ese nuevo estudio clínico, probablemente darolutamida será el siguiente fármaco en recibir la aprobación.
Los hallazgos sobre darolutamida, provenientes de un análisis preliminar del estudio ARAMIS, fueron publicados en el New England Journal of Medicine y presentados el 14 de febrero en el Simposio sobre Cánceres Genitourinarios de la Sociedad Americana de Oncología Clínica en San Francisco.
La incidencia de efectos secundarios en general fue similar entre el grupo que recibió darolutamida y el grupo que recibió placebo, señaló el coautor del estudio doctor Karim Fizazi del Instituto Gustave Roussy, de la Universidad de París, quien presentó los resultados en San Francisco.
"Este fármaco tiene un perfil de seguridad muy favorable", dijo el doctor Fizazi. En comparación con el placebo, darolutamida no estaba asociada a un aumento en la incidencia de efectos secundarios como convulsiones, caídas, fracturas, cambios a nivel cognitivo o hipertensión, señaló el doctor.
Los resultados del estudio clínico ARAMIS "respaldan de manera contundente el uso de darolutamida" en pacientes con cáncer de próstata no metastático resistente a la castración, dijo el doctor William Dahut, director de la Sección de Investigación Clínica de Cáncer de Próstata del Centro de Investigación Oncológica del NCI.
"Tengo un optimismo moderado con respecto a que los efectos secundarios que afectan al sistema nervioso central serán menores de lo que son con otros fármacos en esta clase", agregó el doctor Dahut, quien no participó en el estudio.
Inhibición del receptor androgénico
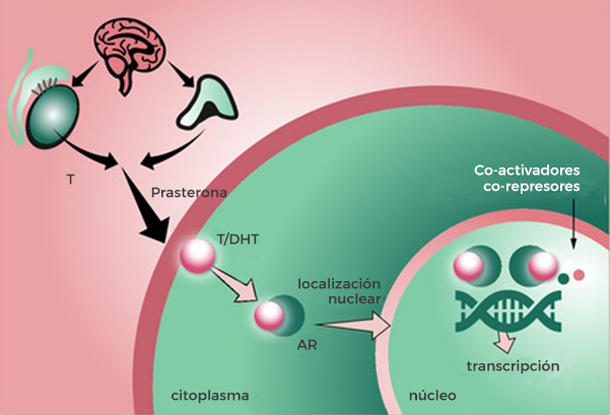
Darolutamida pertenece al tipo de fármacos denominados inhibidores del receptor androgénico. En el organismo, estas sustancias compiten con los andrógenos para unirse al receptor androgénico, lo cual reduce la capacidad de los andrógenos para promover el crecimiento de las células del cáncer de próstata.
En el año 2018, la Administración de Medicamentos y Alimentos (FDA) aprobó a apalutamida (Erleada) y a enzalutamida (Xtandi) para hombres con cáncer de próstata no metastático resistente a la castración.
En los estudios clínicos que llevaron a las aprobaciones, los fármacos demostraron mejorar la mediana de duración del tiempo entre que los pacientes son asignados al azar hasta que el tumor se disemina o hasta que el paciente muere (lo que se conoce como supervivencia sin metástasis) en hombres con esta forma de cáncer de próstata.
No obstante, el tratamiento con ambos fármacos se ha asociado a efectos secundarios que afectan al sistema nervioso central, incluidos fatiga, caídas y cambios cognitivos.
En ambos estudios, la supervivencia sin metástasis de los hombres que recibieron el tratamiento con los respectivos fármacos superó en más del doble a la de los pacientes que recibieron un placebo: 40 meses frente a 16 en el estudio de apalutamida y 36,6 meses frente a 14,7 en el estudio de enzalutamida.
El estudio ARAMIS
El estudio ARAMIS, patrocinado por Bayer y Orion Corporation (quienes crearon conjuntamente darolutamida) incluyó a hombres cuyas concentraciones del antígeno prostático específico (APE) aumentaban a un ritmo que se había asociado en estudios previos al incremento del riesgo de metástasis y muerte.
La supervivencia sin metástasis fue el criterio de valoración primario del estudio; los criterios de valoración secundarios fueron la supervivencia general y la cantidad de tiempo transcurrido hasta que empeoró el dolor del paciente.
El estudio de distribución al azar incluyó a más de 1500 hombres con cáncer de próstata no metastático resistente a la castración que se consideró presentaban un mayor riesgo de que la enfermedad se diseminara a otras partes del cuerpo. Todos los participantes recibieron TPA y darolutamida o TPA y un placebo.
Al cabo de una mediana de seguimiento de 17,9 meses, la mediana de supervivencia sin metástasis fue de 40,4 meses para los pacientes que recibieron darolutamida y TPA, en comparación con 18,4 meses para los pacientes que recibieron un placebo y TPA.
"El riesgo de metástasis o de muerte por cualquier causa se redujo en 59 %, y el beneficio fue sistemático en todos los subgrupos, incluido el subgrupo de pacientes con menor riesgo de padecer la enfermedad", escribieron los investigadores.
Al momento del análisis preliminar, habían muerto 78 hombres en el grupo que recibió darolutamida y 58 hombres en el grupo que recibió el placebo. Los índices de supervivencia general a 3 años fueron 83 % en el grupo que recibió darolutamida y 73 % en el grupo que recibió placebo, concluyeron los investigadores. Aún no se ha alcanzado la mediana de supervivencia general en el estudio.
La mediana de duración hasta que el dolor del paciente empeoró fue mayor en el grupo que recibió darolutamida que en el grupo que recibió el placebo (40,3 meses frente a 25,4 meses).
Una estructura química sin igual
Darolutamida tiene una estructura química diferente a la de apalutamida y la de enzalutamida, lo cual puede explicar por qué tiene menos efectos secundarios, según creen los autores del estudio.
“Básicamente, darolutamida no traspasa la barrera hematoencefálica, mientras que apalutamida y enzalutamida sí lo hacen¨, dijo el doctor Fizazi. La mayor parte de lo que se sabe sobre darolutamida y la barrera hematoencefálica proviene de estudios en roedores y no en seres humanos, agregó el doctor.
La baja incidencia de efectos secundarios relacionados con el sistema nervioso central observados en el estudio fue congruente con los estudios en roedores. Los efectos secundarios que probablemente están relacionados con los efectos del fármaco en el sistema nervioso central incluyen fatiga, mareos, dificultades cognitivas y convulsiones, de acuerdo con el doctor Fizazi.
No se detectaron diferencias en la incidencia de estos efectos secundarios entre los pacientes tratados con darolutamida y quienes recibieron un placebo, agregó el doctor, destacando que no se excluyeron del estudio a los pacientes con antecedentes de convulsiones.
En el estudio, la fatiga fue el único efecto secundario que se presentó en más de 10 % de los participantes en ambos grupos.
Una baja incidencia de efectos secundarios es particularmente importante para los hombres que no tienen síntomas de la enfermedad, señaló el doctor Fizazi. El porcentaje de participantes que dejaron de tomar cualquiera de los fármacos o el placebo debido a los efectos secundarios fue similar: alrededor de 9 %.
En los próximos años, investigadores y pacientes esperan obtener más información sobre las preferencias de los pacientes por darolutamida, enzalutamida y apalutamida.
Por ejemplo, un estudio clínico en curso compara dos de estos inhibidores del receptor androgénico (darolutamida y enzalutamida) en hombres con cáncer de próstata metastático resistente a la castración, a fin de determinar qué fármaco prefieren los pacientes basándose en sus respuestas a un cuestionario. Los pacientes primero tomarán un fármaco y luego el otro.
Entre tanto, Bayer y Orion presentaron ante la FDA una solicitud de aprobación para nuevos fármacos correspondiente a darolutamida.