Mapas de tumores a través del espacio y del tiempo con tecnologías avanzadas
, por Equipo del NCI
Cuando nos dirigimos a un destino completamente nuevo, en general consultamos un sitio web o aplicación que prediga la mejor ruta a seguir, usando mapas actualizados e información de circulación.
¿Qué pasaría si los oncólogos tuviesen un recurso similar que usara mapas altamente detallados del cáncer para predecir la mejor ruta a fin de tratar a una persona con cáncer o prevenir el cáncer en alguien que enfrenta un mayor riesgo?
La iniciativa Human Tumor Atlas Network (HTAN), un proyecto colaborativo de investigación financiado por el NCI, se estableció para lograr justamente eso: crear "mapas" detallados de una variedad de cánceres que puedan usarse para investigar cómo el cáncer puede crecer, diseminarse o responder al tratamiento.
Los mapas captarán las características moleculares del cáncer, de manera similar a lo que se ha hecho con otros "atlas" del cáncer. Sin embargo, el aspecto más exclusivo de la iniciativa HTAN es que las características del cáncer se localizarán a través del tiempo y del espacio.
Además, los investigadores de la iniciativa HTAN aprovecharán las últimas biotecnologías y enfoques informáticos para estudiar la biología del cáncer como nunca antes se ha hecho.
Por ejemplo, los mapas de HTAN incorporarán la ubicación tridimensional de las células individuales en un tumor, como si fueran la dirección de un edificio. Y de la misma forma como un mapa interactivo indica si un edificio es una residencia o un negocio, los mapas de HTAN estarán también caracterizados con información acerca del tipo de célula que se encuentra en cada "dirección".
Pero los tumores, al igual que la ciudades, cambian a través del tiempo, y un mapa obsoleto no es un recurso muy confiable. Como tal, los mapas de HTAN mostrarán los cambios en las características moleculares, celulares y espaciales de un tumor a medida que este avanza con el tiempo.
Con estos mapas altamente detallados, HTAN se propone generar una comprensión más integral del cáncer de lo que ha sido posible hasta ahora, dijeron los directores de la iniciativa.
"Un esfuerzo muy oportuno"
La idea de la iniciativa HTAN provino de la Misión contra el Cáncer (Cancer Moonshot℠), a través de una recomendación de su Panel Listón Azul.
"Es un esfuerzo que llega en un momento muy oportuno porque ha habido un verdadero auge de las tecnologías necesarias para analizar las células en profundidad, de una manera que no era posible hace 10 años", dijo la doctora Tracy Lively, codirectora de HTAN, de la División de Tratamiento y Diagnóstico Oncológico del NCI.
Y estas tecnologías se han vuelto disponibles recientemente "no solo para unos pocos laboratorios especializados, sino en forma tan amplia y suficiente que los laboratorios que tienen gran interés y experiencia en cáncer ahora pueden aprovecharlas", agregó la doctora.
La red consiste en 10 equipos de instituciones de investigación de todo el país. En la conferencia inaugural que se realizó en noviembre pasado, cada equipo describió cómo está generando los atlas de tumores usando una combinación diferente de tecnologías y enfoques.
"Cuando estamos tratando de comprender la biología subyacente [del cáncer], realmente necesitamos un enfoque altamente multifacético y debemos abordarlo desde muchas perspectivas diferentes", dijo el doctor Andrew Adey, científico financiado por HTAN, de la Universidad de Ciencias y Salud de Oregón.
Cada mapa representará a un tipo de cáncer al pasar por una transición específica. Por ejemplo, el equipo de la iniciativa HTAN del Hospital Infantil de Filadelfia está generando un mapa del glioma infantil de alto grado de malignidad, a medida que pasa por la transición desde que responde a los tratamientos convencionales hasta que presenta resistencia a los mismos.
Al llegar al nivel de la calle: análisis de células individuales
Si observamos una ciudad a vuelo de pájaro, esto puede revelar estructuras en líneas generales, como edificios y parques. Pero con una vista a nivel de la calle, pueden observarse detalles individuales de esos lugares, por ejemplo si un edificio es residencial o comercial.
En el pasado, era difícil para los investigadores lograr obtener un panorama de las células "a nivel de calle" porque, para la mayoría de las pruebas de laboratorio, una muestra de células está mezclada y se analiza como grupo.
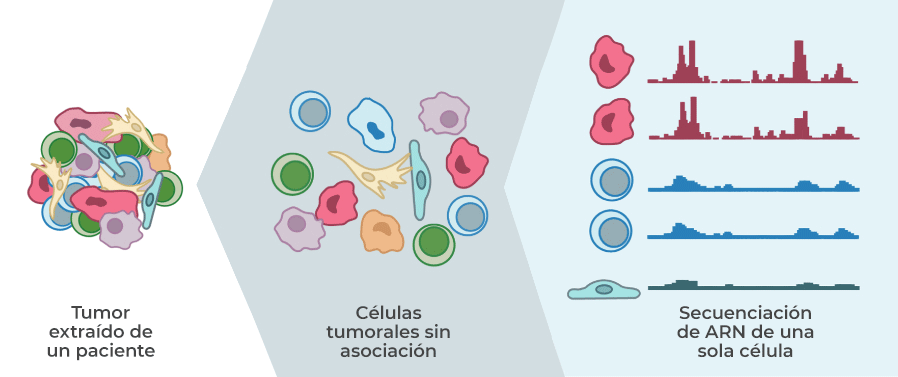
Es como si colocáramos una cantidad de células en una licuadora y observáramos el resultado, dijo la doctora Dana Pe’er, una directora del equipo de HTAN en el Centro Oncológico Memorial Sloan-Kettering (MSKCC). La doctora Pe’er explicó que con este enfoque "a granel" se pierden las diferencias individuales (lo que se llama heterogeneidad).
No obstante, los avances tecnológicos actualmente permiten a los investigadores analizar en forma rápida y económica las características moleculares de células individuales. Al combinar datos singulares de cientos o miles de células individuales de un tumor, los investigadores pueden comprender mejor su heterogeneidad.
Estas tecnologías dirigidas a células individuales están "abriendo un mundo completamente nuevo para el cáncer y la biomedicina", dijo la doctora Pe’er.
Cada equipo de la iniciativa HTAN usa diferentes tecnologías dirigidas a células individuales, pero su meta final es la misma: trazar un mapa de la ubicación y entender la función de cada tipo de célula en un tumor. Por ejemplo, los investigadores esperan diferenciar las células cancerosas y las células inmunitarias, además de determinar si esas células inmunitarias ayudan al cáncer a crecer o lo combaten.
"A fin de comprender no solo a las células tumorales sino también al microentorno circundante debemos utilizar tecnologías más modernas… para realmente analizar los diferentes grupos en un tumor", dijo la doctora Li Ding, una directora del equipo en la Universidad de Washington en St. Louis.
Más allá de los planos de ADN
Los planos de una ciudad pueden mostrar el esquema original de calles y carreteras, pero no pueden informar de los edificios y paisajes que han surgido a lo largo de esas calles, ni cómo se ha alterado el contorno a medida que la ciudad fue desarrollándose.
De manera similar, aunque no hay duda de que la secuencia del ADN (que a menudo se describe como el plano de una célula) revela claves acerca de la biología del cáncer, no nos permite conocer la historia completa.
Además de la secuenciación del ADN, los investigadores de la iniciativa HTAN están usando tecnologías dirigidas a las células individuales a fin de estudiar otras moléculas biológicas tales como el ARN y las proteínas, que pueden revelar importante información acerca de las células cancerosas.
Por ejemplo, el equipo MSKCC está estudiando las dinámicas de las metástasis por medio de la secuenciación del ARN de células individuales provenientes de tumores primarios en el pulmón y el páncreas, y de tumores metastáticos en el cerebro.
Con la secuenciación de células individuales del ARN, los investigadores pueden identificar de qué tipo de célula se trata y determinar sus características, como el potencial para formar metástasis, explicó la doctora Pe’er. Con sus mapas, esperan llegar a una mayor comprensión de los mecanismos de las metástasis y cómo se regulan.
Otros equipos están estudiando cómo cambian las modificaciones epigenéticas (alteraciones que controlan cuáles genes se encienden y se apagan sin cambiar la secuencia real del ADN) a medida que avanza el cáncer.
Por ejemplo, el equipo de la Universidad de Ciencias y Salud de Oregón está usando una tecnología denominada ATAC-seq a fin de analizar una clase de modificación epigenética. Esta tecnología es más eficaz y sencilla de usar que las pruebas epigenéticas previas, explicó el doctor Adey, miembro del equipo de Oregón.
El doctor y sus colegas adaptaron la tecnología ATAC-seq para analizar células individuales y están usando este enfoque para estudiar cambios epigenéticos que ocurren a medida que los tumores metastáticos de seno se vuelven resistentes a las terapias convencionales.
Múltiples estudios han indicado que ciertas alteraciones epigenéticas hacen que las células cancerosas se vuelvan resistentes a determinados tratamientos. El equipo espera que al profundizar en el estudio de estos cambios permitirá comprender mejor estos mecanismos de resistencia y, posiblemente, saber cómo subvertirlos.
Para crear estos mapas, el equipo de HTAN de la Universidad Washington está usando una nueva tecnología denominada nanoPOTS a fin de identificar cientos de proteínas en células individuales. Por medio del análisis de proteínas en las células obtenidas de tumores de seno, cerebro y páncreas durante y después del tratamiento, el equipo espera entender cómo los cambios en los tipos de células en un tumor se correlacionan con la respuesta del paciente al tratamiento.
Por ejemplo, este enfoque podría aclarar cómo cambian los tipos de células inmunitarias en un tumor durante y después del tratamiento, explicó la doctora Ding.
La expectativa es que, más adelante, los investigadores puedan usar los atlas de HTAN como recurso para encontrar respuestas sobre la biología del cáncer.
Por ejemplo, una manera en que los investigadores podrían usar los mapas es para "identificar biomarcadores para la estratificación de riesgo y la detección temprana del cáncer, e identificar blancos precisos para la prevención y la terapia", dijo el doctor Sudhir Srivastava, codirector de HTAN, de la División de Prevención del Cáncer del NCI.
Dichos marcadores y blancos podrían ayudar a los oncólogos a crear modelos que predigan cómo puede avanzar el cáncer de una persona y cómo puede responder al tratamiento, explicó el doctor.
El estudio del cáncer en contexto
Un mapa no nos ayudaría a llegar a destino si los componentes de la ciudad estuviesen dibujados en forma arbitraria en la página. Para llegar a su destino, es necesario saber cómo están organizados los edificios y las calles unos respecto de los otros.
De la misma manera, el atlas de un tumor debe transmitir cómo están organizados los componentes del microambiente tumoral (vasos sanguíneos, tejido conjuntivo, células inmunitarias y microorganismos) unos respecto de los otros y en relación a las células cancerosas.
Pero, en el pasado, de acuerdo con la doctora Lively, "muchas de las tecnologías usadas para observar las células requerían que separásemos al tumor", y así se perdían las relaciones espaciales entre estos componentes.
En la actualidad, las tecnologías por imágenes avanzadas permiten que los investigadores estudien en gran detalle el microambiente tumoral intacto. Uno de los principales objetivos de la iniciativa HTAN es usar estas tecnologías para conectar la información molecular con la espacial, puntualizó la doctora Lively.
Estos métodos "son increíblemente importantes porque permiten estudiar las células en contexto", señaló la doctora Pe’er. Por ejemplo, se pueden responder preguntas como, "¿en qué se diferencia el comportamiento de una célula cancerosa que se encuentra junto a una célula inmunitaria, del comportamiento de una que se encuentra en otro contexto?", dijo la doctora.
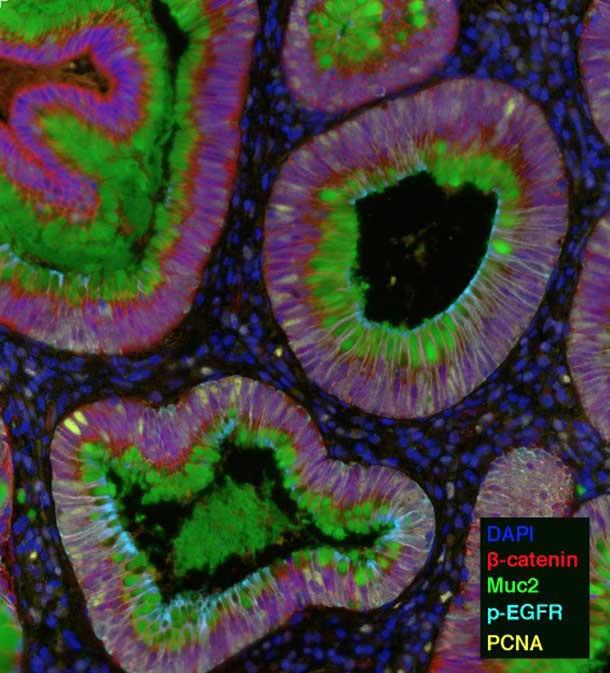
Los investigadores de la iniciativa HTAN usan varias técnicas de exploración con imágenes que permiten individualizar moléculas diferentes (a veces más de 100), resaltando cada una con un color diferente.
Por ejemplo, el equipo de la iniciativa HTAN de la Universidad de Vanderbilt está usando una técnica, denominada inmunofluorescencia multiplex (MxIF), que puede resaltar hasta 60 moléculas diferentes, incluidas proteínas, ARN y microbios. Están usando esa tecnología para estudiar cómo cambia el microambiente durante la formación de cáncer de colon.
"Los enfoques basados en exploración con imágenes, como la inmunofluorescencia multiplex, van a ser la clave de estas iniciativas", dijo el doctor Ken Lau, uno de los directores del equipo de Vanderbilt.
Los investigadores de Vanderbilt estudiarán combinaciones de proteínas y ARN a fin de delinear los tipos de células en muestras de crecimientos precancerosos en el colon y en tumores de colon completamente formados. Luego, analizarán cómo cambia la interacción y la organización de estas células durante la evolución del cáncer.
El equipo está usando también MxIF para estudiar microorganismos, porque ciertas especies bacterianas en los intestinos se vinculan a la formación y al avance del cáncer de colon.
"La flora microbiana se organiza en estructuras denominadas biopelículas", explicó el doctor Lau. "Es muy importante estudiar cómo están organizadas espacialmente estas biopelículas y dónde se encuentran exactamente los diferentes microbios", dijo el doctor. Por ejemplo, continuó, los microbios pueden establecerse encima del tumor de colon o pueden invadir el tumor por dentro, y eso puede cambiar el comportamiento del tumor.
Colaboración para responder a los nuevos desafíos
El proyecto HTAN es una enorme iniciativa y es el primer proyecto de atlas tridimensional enfocado exclusivamente en tumores, señaló la doctora Lively. Eso significa que surgirán varios problemas a solucionar, muchos de los cuales ya discutieron los científicos de la iniciativa HTAN en la conferencia inaugural.
El doctor Adey dijo que uno de los problemas será lograr aislar suficientes células para ensayos con células individuales. En ocasiones, grandes partes de la muestra tumoral mueren y se abren, lo cual hace difícil aislar células individuales, explicó el doctor.
Incluso una vez que se soluciona el problema, algunas de las tecnologías más recientes aún necesitan mejoras, dijo la doctora Pe’er. En la conferencia, los investigadores de la iniciativa HTAN estuvieron de acuerdo en que es necesario optimizar cada ensayo o prueba antes de que pueda usarse en grandes conjuntos de muestras.
La doctora Pe’er dijo que la computación e interpretación de grandes conjuntos de datos es otro cuello de botella importante. Parte del problema es que no contamos con suficientes biólogos informáticos, señaló la doctora.
Otro problema es lograr generar series de datos de una manera sistemática que permita comparar unos con otros, dijo la doctora Ding.
"Estamos tratando con un conjunto de tecnologías diferentes y debemos ser conscientes de la normalización. De no hacerlo así, será difícil poder sacar conclusiones", puntualizó la doctora.
Si bien existen problemas importantes, la experiencia combinada de la red es un excelente punto de partida para encontrar soluciones, dijo el doctor Adey. "Contar con esta red de pares para intercambiar ideas y experiencias tendrá un valor increíble", explicó el doctor.
La doctora Lively estuvo de acuerdo, y comentó: "creo que el valor real de poner en marcha una red como esta es que… será una oportunidad extraordinaria para compartir y aprender unos de otros".