Se aprueba Carvykti, la segunda terapia de células T con CAR para el mieloma múltiple
, por el Equipo del NCI
Los pacientes con mieloma múltiple avanzado ahora tienen una segunda opción para la terapia de células T con CAR, un tipo de inmunoterapia personalizada. El 28 de febrero, la Administración de Alimentos y Medicamentos (FDA) aprobó ciltacabtagén autoleucel (Carvykti) para adultos con mieloma múltiple que no responde (es resistente) al tratamiento o que regresó después del tratamiento (recaída).
Según las indicaciones de la aprobación de ciltacabtagén autoleucel, también llamado cilta-cel, el medicamento es para las personas que ya recibieron cuatro o más líneas de terapia, lo que incluye el tratamiento con tres de las clases principales de medicamentos para el mieloma múltiple (un modulador del sistema inmunitario, un inhibidor del proteasoma y un anticuerpo monoclonal anti-CD38).
La aprobación se basó en los resultados de un estudio clínico pequeño en el que cilta-cel redujo el cáncer en casi todos los participantes y, en muchos de ellos, mantuvo el cáncer bajo control durante más de 1 año. Al igual que la primera terapia de células T con CAR aprobada por la FDA para el mieloma múltiple, cilta-cel se dirige a una proteína en las células del mieloma llamada antígeno de maduración de célula B (BCMA).
"Si bien tenemos muchas opciones de tratamiento para el mieloma... en la mayoría de los pacientes, la enfermedad regresa" después de cada tratamiento, explicó la doctora Faith Davies, directora del Centro de Cánceres de la Sangre en el Centro Oncológico Perlmutter de la Universidad de Nueva York (NYU) en Langone. Una vez que se dan todos los tratamientos disponibles, en general los pacientes viven menos de 1 año.
"Por eso es tan importante contar con otro enfoque terapéutico disponible", agregó la doctora Davies. La terapia de células T con CAR "funciona de una manera completamente diferente que nuestros tratamientos estándar y, por lo tanto, ofrece otra manera de destruir las células del mieloma resistentes a los medicamentos, que es la clave", explicó la doctora.
No obstante, el costo, la disponibilidad y el tiempo que lleva producir el tratamiento son factores limitantes para la terapia de células T con CAR. El precio de venta de cilta-cel es $465 000 (dólares estadounidenses) por una sola infusión, aunque el costo final para los pacientes dependerá de la cobertura del seguro médico.
En la actualidad, cilta-cel está disponible solo en un número limitado de hospitales que tienen la certificación para ofrecer este tratamiento complejo. Según un comunicado de prensa de la empresa, se sumarán otros hospitales a medida que el fabricante, Janssen Pharmaceutical, aumente la producción.
Además, lleva alrededor de 1 mes elaborar el tratamiento personalizado, un tiempo de espera que quizá sea demasiado largo para algunos pacientes con cánceres muy agresivos.
Resultados impresionantes con cilta-cel
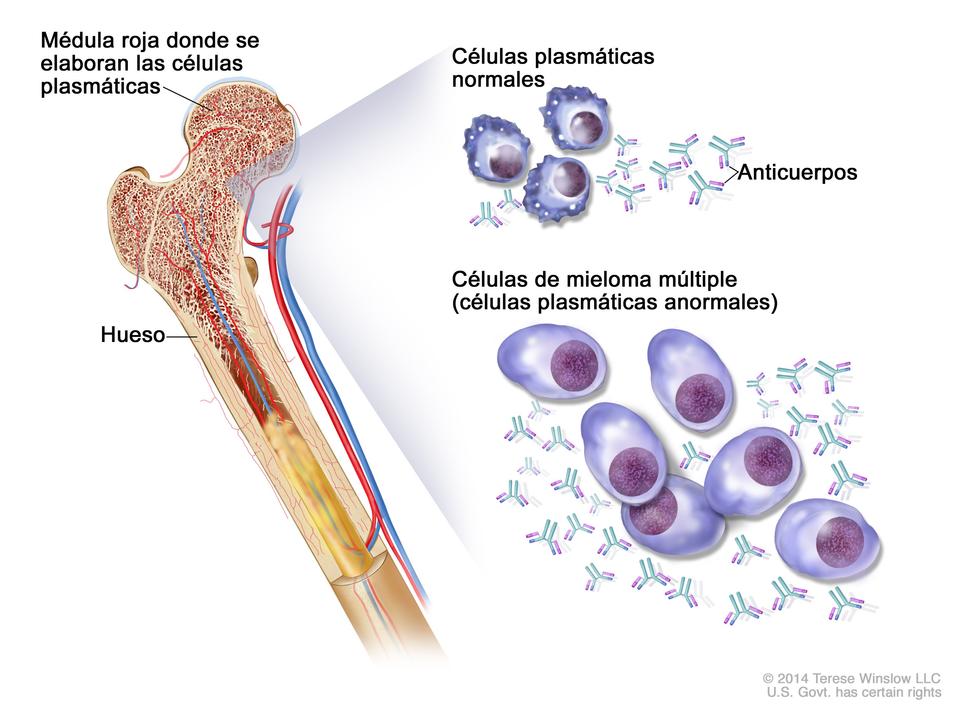
El mieloma múltiple es un cáncer de las células sanguíneas que producen anticuerpos. El cáncer puede formar tumores en los huesos y en otros órganos.
La aprobación de la FDA se basó en los resultados de CARTITUDE-1, un estudio clínico en curso que evalúa cilta-cel en personas con mieloma múltiple que ya recibieron varios tratamientos.
Los 97 participantes del estudio recibieron una sola infusión de cilta-cel. Casi todos (98 %) respondieron al tratamiento, lo que significa que disminuyó la cantidad del cáncer en el cuerpo, al menos en forma parcial. Para el 78 % de los participantes, no hubo signos de cáncer en la médula ósea o en la sangre según los resultados de pruebas sofisticadas, lo que se llama una remisión completa rigurosa. En general, las respuestas duraron una mediana de 22 meses.
"A modo de comparación, otros medicamentos que hasta la fecha tuvieron la aprobación [para el mieloma múltiple] dieron un resultado de alrededor del 30 %" en su tasa de respuesta, señaló el investigador principal del estudio, doctor Sundar Jagannath, del Instituto Oncológico Tisch en Nueva York.
Para los pacientes que ya habían recibido varias líneas de terapia, "presentar tasas de respuesta de casi el 100 % no tiene ningún precedente y es espectacular", puntualizó la doctora Davies. Además, tener respuestas que duraron casi 2 años "es muy impresionante", agregó la doctora.
El doctor Jagannath señaló que es importante destacar que los pacientes en general no necesitan otros tratamientos para el cáncer mientras se mantienen en remisión después de recibir cilta-cel.
"La mayoría ha estado en tratamiento de forma constante porque la terapia sin interrupción es importante para el mieloma", explicó el doctor. También mencionó que para muchos, el intervalo después de recibir el tratamiento con cilta-cel es el primer descanso verdadero de los tratamientos para el cáncer desde el diagnóstico, lo que mejora mucho la calidad de vida y el bienestar de los pacientes.
¿Cuáles son los efectos secundarios de cilta-cel?
Cilta-cel produjo los efectos secundarios que son típicos de la terapia de células T con CAR, por ejemplo, el síndrome de liberación de citocinas, infecciones y problemas nerviosos como dolores o sensación de hormigueo (neuropatía).
"No pareció producir ningún efecto secundario diferente en comparación con otras terapias de células T con CAR, lo cual es muy bueno", puntualizó la doctora Davies.
| Efecto secundario | Frecuencia |
|---|---|
| Síndrome de liberación de citocinas | 95 % |
| Infecciones | 59 % |
| Recuento bajo de plaquetas | 41 % |
| Recuento bajo de neutrófilos | 30 % |
| Problemas nerviosos | 26 % |
| Concentración baja de anticuerpos | 12 % |
Algunos efectos secundarios aparecieron días o semanas después de la infusión con cilta-cel. Además, se atribuyeron siete muertes al tratamiento.
El síndrome de liberación de citocinas se produce cuando las células T con CAR aceleradas depositan señales inflamatorias en la sangre, lo que produce síntomas similares a los de la gripe. Si bien casi todos los participantes del estudio presentaron el síndrome de liberación de citocinas, la mayoría de esos casos fueron leves y tratables con corticoesteroides u otros medicamentos.
"Todos hemos aprendido cómo manejar mejor el síndrome de liberación de citocinas. Con más experiencia, aumentó la seguridad", explicó el doctor Jagannath.
Cilta-cel incluye una etiqueta de advertencia sobre el riesgo de seis efectos secundarios mortales o potencialmente mortales. Por ejemplo, el síndrome de linfohistiocitosis hemofagocítica o de activación del macrófago (LHH/SAM), una afección que también se produce por las señales inflamatorias de las células T con CAR. La linfohistiocitosis hemofagocítica produce una disminución peligrosa de la presión sanguínea y disfunción de varios órganos, pero puede tratarse si se identifica en su inicio.
También tiene una etiqueta de advertencia sobre el riesgo del síndrome de Guillain-Barré y parkinsonismo, una afección con síntomas que son similares a los de la enfermedad de Parkinson, como temblores y movimientos lentos. El doctor Jagannath explicó que el equipo de investigación formuló un plan para atenuar el parkinsonismo, que parece ayudar a reducir la enfermedad en estudios en curso.
Las otras advertencias son para el síndrome de liberación de citocinas grave, períodos prolongados de recuentos sanguíneos bajos y el síndrome de neurotoxicidad asociado a las células efectoras inmunitarias (ICANS), un síndrome neurológico que produce alteraciones en la conciencia y problemas en el funcionamiento cerebral.
Dos opciones para la terapia de células T con CAR
Para producir cilta-cel, se obtienen las propias células inmunitarias del paciente y se modifican de forma genética para que puedan encontrar y destruir las células cancerosas. Las células inmunitarias mejoradas, llamadas células T con CAR, se dirigen a la BCMA, una proteína que se encuentra en grandes cantidades en las células del mieloma múltiple y en un subgrupo muy pequeño de células sanguíneas sanas.
Idecabtagén vicleucel (Abecma), o ide-cel, fue la primera terapia de células T con CAR que aprobó la FDA para el mieloma múltiple. Idecabtagén vicleucel también se dirige a la BCMA, pero cilta-cel tiene una pequeña diferencia: las células T con CAR se unen a dos secciones de la BCMA y no solo a una.
La doctora Davies señaló que ahora que ya hay dos opciones de terapia de células T con CAR, la gran pregunta que todo el mundo se está haciendo es, "¿cuáles son las diferencias y los posibles beneficios de una frente a la otra?".
Aún es muy temprano para saber la respuesta. Sin embargo, el doctor Jagannath dijo que lo más importante es que "ambas terapias de células T con CAR funcionan bien. Ambas sirven y ayudan a los pacientes".
Al momento, la decisión se basará en cuál está disponible, agregó la doctora Davies. "La demanda de idecabtagén vicleucel fue tan grande, que no pudimos abastecerla. Por eso es tan importante contar con otra terapia de células T con CAR", señaló la doctora.
¿Hay posibilidades de cura?
Según la doctora Davies, hay otra pregunta bien importante sobre la terapia de células T con CAR para el mieloma múltiple: Dado que las terapias funcionan bien para las personas que tuvieron cuatro o más tratamientos, ¿funcionarán aun mejor para las personas que no recibieron tratamiento o que tuvieron menos de cuatro?
"Estas terapias funcionan al usar el sistema inmunitario natural del paciente. En el caso del mieloma, para cuando los pacientes ya recibieron cuatro terapias, el sistema inmunitario está un tanto debilitado", explicó la doctora. Es probable que el sistema inmunitario de un paciente que recién recibió el diagnóstico y no tuvo ningún tratamiento esté en mejor forma, puntualizó la doctora.
Según el doctor Jagannath, otra posible ventaja de tratar pacientes con diagnóstico reciente con la terapia de células T con CAR es que la probabilidad de que tengan células cancerosas resistentes al tratamiento es menor.
La doctora Davies reflexionó que "hay muchas discusiones sobre qué pasaría si usáramos estas terapias en estadios tempranos de la enfermedad, ¿quizá los pacientes tendrían mejores respuestas o más prolongadas, o tal vez hasta se curarían?".