Dasatinib aprobado por la FDA para algunos niños con leucemia mielógena crónica
, por Equipo del NCI
El 9 de noviembre, la Administración de Medicamentos y Alimentos (FDA) aprobó dasatinib (Sprycel®) para el tratamiento de algunos niños con leucemia mielógena crónica (LMC). La aprobación es para niños con LMC cuyas células cancerosas presentan una alteración genética conocida como el cromosoma Filadelfia y en quienes la enfermedad se encuentra en una etapa relativamente temprana, la cual se conoce como fase crónica.
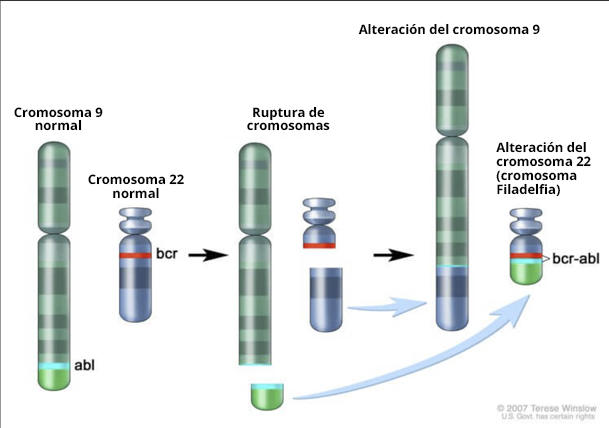
La mayoría de los casos de LMC son causados por el cromosoma Filadelfia, el cual se forma cuando se separan una parte del cromosoma 9 y una parte del cromosoma 22 e intercambian posiciones. El resultado de este cambio es la producción de una proteína de fusión, llamada BCR-ABL, la cual fomenta la producción de un exceso de glóbulos blancos, que es un rasgo característico de la enfermedad.
Dasatinib y un fármaco llamado imatinib (Gleevec®) inhiben a la BCR-ABL. Dasatinib podría ser eficaz para personas que dejaron de beneficiarse por la administración de imatinib o que no pueden recibir dicho fármaco debido a sus efectos secundarios.
La FDA basó la aprobación de dasatinib en los resultados de dos estudios clínicos en fase inicial (un estudio en fase 1 y un estudio en fase 2) en los que participaron un total de 97 niños con LMC. Los estudios fueron financiados por Bristol-Myers Squibb.
Cincuenta y uno de los 97 pacientes (todos en el estudio en fase 2) tenían un diagnóstico reciente de LMC. Los 46 pacientes restantes (17 del estudio en fase 1 y 29 del estudio en fase 2) no pudieron tolerar imatinib o su LMC era resistente a imatinib.
Después de 24 meses de tratamiento, 96,1 % de los pacientes con diagnóstico reciente de LMC y 82,6 % de los pacientes cuya LMC no podía tratarse con imatinib (Gleevec®) o había dejado de responder a ese fármaco, presentaron una respuesta completa.
En el estudio en fase 2, "las respuestas ocurrieron en forma relativamente rápida y los pacientes se beneficiaron con el tratamiento durante su permanencia en el estudio", dijo la doctora Lia Gore, coinvestigadora del estudio en el Anschutz Medical Campus de la Universidad de Colorado.
El hallazgo de que los pacientes que no pueden beneficiarse con imatinib quizá respondan a dasatinib fue importante también, puntualizó el doctor C. Michel Zwaan, coinvestigador del estudio en el Erasmus MC de los Países Bajos.
Por otra parte, continuó el doctor Zwaan, "el tratamiento fue extraordinariamente bien tolerado. Los efectos secundarios típicos que se presentan en adultos, como los derrames pleurales, apenas se produjeron en el grupo pediátrico”.
Los efectos secundarios notificados en más del 10 % de los pacientes fueron dolores de cabeza, náuseas, diarrea, erupciones cutáneas, vómitos, dolor en una extremidad, dolor abdominal, fatiga y dolor en articulaciones.
Después de una mediana de tiempo de seguimiento de 4,5 años en los pacientes con diagnóstico reciente y de 5,2 años en los pacientes que habían recibido tratamiento previo con imatinib, la enfermedad no empeoró en más de la mitad de los pacientes. Como consecuencia de ello, los investigadores aún no pueden calcular la mediana de duración de las respuestas completas.
Debido a que no todos los niños pueden pasar los comprimidos por su garganta (la presentación que se usó de dasatinib para los adultos), se usó la presentación líquida de dasatinib que puede tomarse una vez al día en una sola dosis.
El doctor Zwaan señaló que este grupo de pacientes podría tomar el fármaco durante décadas y que los investigadores deberán hacer seguimiento a los pacientes para comprender la seguridad del tratamiento a largo plazo.
“Siempre existe la preocupación sobre los efectos secundarios a largo plazo, en particular cuando se trata de niños que quizá necesiten un tratamiento muy prolongado”, agregó la doctora Gore. "Como comunidad, tendremos que continuar evaluando y haciendo el seguimiento de estos pacientes para garantizar el logro de un equilibrio óptimo entre riesgos y beneficios a corto y largo plazo".