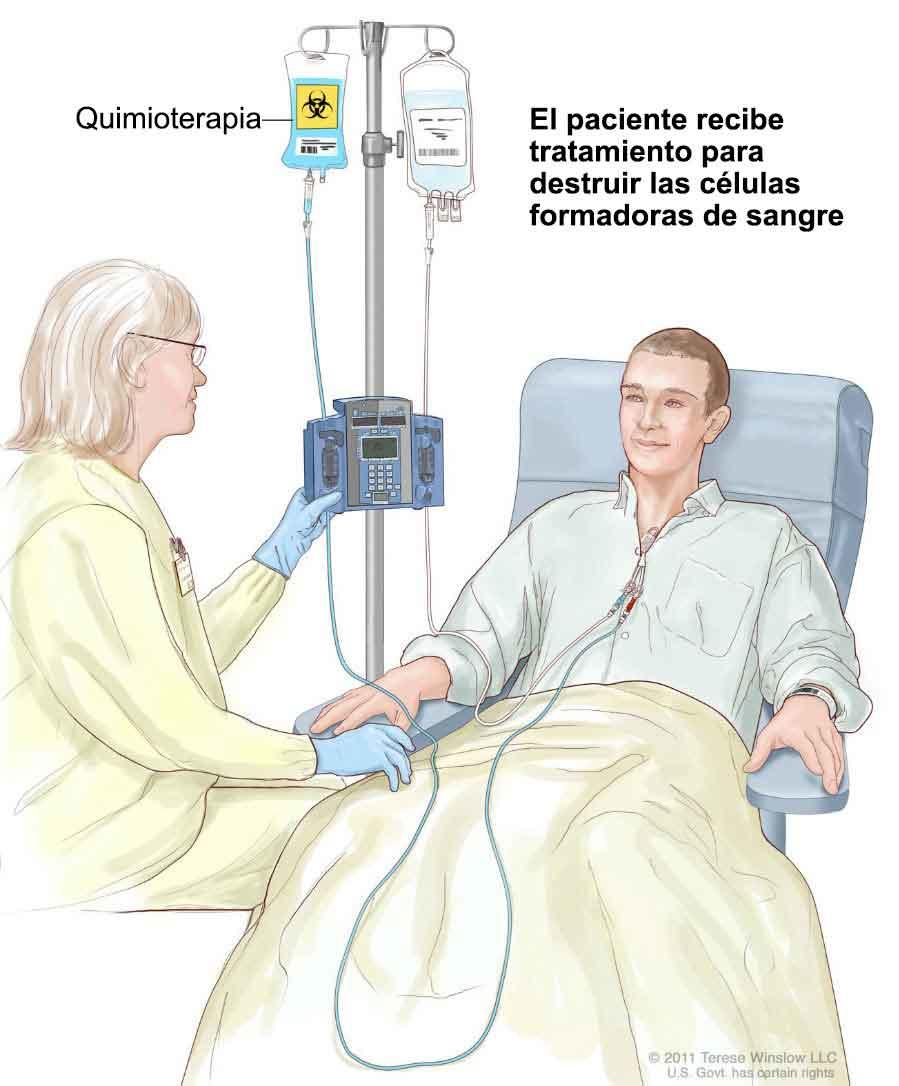
Planteamiento puede permitir trasplante de células madre sin radiación o quimioterapia
, por Equipo del NCI
En un estudio para probar un concepto en ratones, investigadores de la Escuela de Medicina de la Universidad de Stanford efectuaron con éxito trasplantes de células madre hematopoyéticas (también llamados trasplantes de médula ósea) sin usar primero radiación o quimioterapia.
En vez de estos esquemas tóxicos de acondicionamiento, los cuales se usan normalmente para eliminar las células madre existentes en la médula ósea antes del trasplante, los investigadores usaron dos sustancias biológicas que eliminan selectivamente las células madre hematopoyéticas en los ratones hospedadores pero dejaron intactos otros tejidos y órganos.
Si la técnica puede traducirse a humanos, “la terapia de células hematopoyéticas podría extenderse a quienes no pueden ahora tolerar sin peligro la terapia de preparación para trasplante de médula ósea”, incluso pacientes débiles o ancianos, dijo el doctor Richard Little, del Programa de Evaluación de Terapias del Cáncer del NCI, quien no participó en el estudio.
Los resultados fueron publicados el 10 de agosto en Science Translational Medicine.Despejar el camino para nuevas células madre
El trasplante de células madre puede ser un tratamiento de salvación para pacientes con algunos tipos de cáncer, principalmente cánceres de la sangre como leucemia y linfoma.
Sin embargo, el procedimiento es algunas veces agotador para pacientes y posiblemente peligroso. Antes del trasplante, los pacientes son tratados con frecuencia con radiación y con quimioterapia para destruir las células madre que existen en la médula ósea con el fin de que las células madre del donante trasplantadas tengan una acogida segura en la que crezcan y vuelvan a llenar el cuerpo con glóbulos sanos (proceso que se llama injerto). Y, en el caso de células madre hematopoyéticas de un donante similar genéticamente pero no idéntico (un trasplante alogénico), estos tratamientos de acondicionamiento ayudan a suprimir una respuesta inmunitaria contra las células trasplantadas.
Pero el esquema de acondicionamiento puede dañar las células sanas del paciente y tejidos así como sus células madre hematopoyéticas, lo que resulta en efectos secundarios, incluso infecciones, problemas respiratorios y daños a órganos que pueden ser fatales en un porcentaje reducido de pacientes.
Si la preparación para el trasplante pudiera hacerse menos tóxica para las células sanas, explicó la doctora Judith Shizuru, la autora principal del estudio, el procedimiento podría usarse no solo para cáncer sino también para otras indicaciones. Estas incluyen el tratamiento de enfermedades causadas por glóbulos y células inmunitarias que funcionen mal, incluso enfermedades autoinmunitarias y trastornos de la sangre marcados por hemoglobina anormal (como la anemia drepanocítica o talasemia), así como mejorar la terapia génica y el trasplante de órganos.
Investigación anterior, por el equipo de Stanford y otros, ha mostrado que las sustancias biológicas que se dirigen a la c-kit, una proteína que las células madre hematopoyéticas usan para muchas de sus funciones normales, pueden agotar las células madre hematopoyéticas en ratones a los que falta un sistema inmunitario que funcione. Sin embargo, en estudios anteriores, dirigirse a esta única proteína no agotó las células madre hematopoyéticas en ratones con un sistema inmunitario funcionando.
Entonces, los investigadores de Stanford probaron si al dirigirse a una segunda proteína, llamada CD47, además de la c-kit se podrían eliminar las células madre hematopoyéticas en ratones con un sistema inmunitario sano. La CD47 sirve como un “marcador propio” para células madre hematopoyéticas y algunos otros tipos de células, al decir al sistema inmunitario que no las ataque. Al bloquear la CD47 con una molécula especialmente diseñada, los investigadores esperaban hacer las células madre hematopoyéticas vulnerables al tratamiento con una sustancia que se apuntara a la c-kit.
La combinación funcionó. En ratones con sistemas inmunitarios sanos que fueron tratados con ambas sustancias, los investigadores vieron una reducción de 10 000 veces en las células madre hematopoyéticas atacadas, al punto que “ya no podíamos contarlas”, dijo la autora principal del estudio doctora Akanksha Chhabra.
En experimentos ulteriores, los ratones con sistemas inmunitarios sanos fueron tratados con ambas sustancias o con una sustancia que se dirigía a la c-kit sola y luego se sometieron a una forma modificada de trasplante autólogo de células madre. Los ratones que recibieron ambas sustancias mostraron cien veces más injerto de las células madre del donante en su médula ósea que los ratones tratados con la sustancia anti c-kit sola, y las células sanas derivadas de las células madre hematopoyéticas trasplantadas se encontraron en la sangre, en el bazo, la médula ósea y el timo.
Los investigadores probaron también si el planteamiento general funcionaría en un tipo de trasplante alogénico. Ellos trataron ratones con esquemas de acondicionamiento de dos sustancias y con otras sustancias biológicas para agotar las células inmunitarias (células T) para impedir que el sistema inmunitario atacara a las células trasplantadas. El trasplante tuvo éxito, al establecerse con éxito las células del donante en la médula ósea del recipiente y producir sangre sana y células inmunitarias.Hacia estudios humanos
Las sustancias que se dirigen a la c-kit y a la CD47 ya han sido evaluadas en estudios humanos en voluntarios sanos y en pacientes con cáncer, respectivamente, explicó la doctora Shizuru, y no se ha observado un efecto secundario importante. El equipo ha empezado recientemente a inscribir a pacientes en un estudio clínico que usa una sustancia que se dirige a la c-kit para niños con enfermedad de inmunodeficiencia combinada grave. En los ratones, añadió la doctora Chhabra, los investigadores han visto un poco de color gris en la piel y una caída de los recuentos de espermatozoides debida al anticuerpo del c-kit, pero “cuando terminó el tratamiento, los recuentos de espermatozoides volvieron a subir”, dijo ella. El estudio actual no se fijó en los efectos en la fecundidad por largo tiempo.
El siguiente paso es probar la combinación de fármacos como esquema de acondicionamiento para trasplante de células madre hematopoyéticas en primates no humanos, dijo la doctora Shizuru. Puesto que los fármacos ya han empezado estudios humanos de seguridad como sustancias solas, ella piensa que los estudios humanos iniciales de combinación para trasplante de células madre hematopoyéticas podrían empezar en los próximos 3 o 5 años.
“La meta de este estudio, y lo que esperamos haber mostrado, es que vamos a cambiar la forma como los trasplantes de sangre y de médula se harán en un futuro próximo”, dijo la doctora Shizuru. “Prevemos que los trasplantes se llevarán a cabo con más seguridad y que muchos más pacientes puedan ser tratados con esta terapia celular posiblemente curativa”.