Se amplió la aprobación de T-DM1 para incluir a algunas mujeres con cáncer de seno con HER2 en estadio inicial
, por Equipo del NCI
La Administración de Alimentos y Medicamentos (FDA) amplió el uso aprobado del fármaco ado-trastuzumab emtansina (Kadcyla) para tratar a algunas mujeres con cáncer de seno con HER2.
Ado-trastuzumab, llamado también T-DM1, recibió la aprobación inicial de la FDA hace más de seis años para el tratamiento de mujeres con cáncer metastático de seno con HER2. Con la presente ampliación, ahora se podrá usar cuando el cáncer está mucho menos avanzado: como tratamiento posoperatorio, o adyuvante, en mujeres con cáncer de seno con HER2 en estadio inicial. No obstante, a fin de poder recibir el fármaco para este uso recientemente aprobado, las mujeres deben haberse sometido en primer lugar a una terapia preoperatoria, o neoadyuvante, a fin de encoger los tumores y aún presentar algunos signos de cáncer invasor, denominado cáncer residual, en el seno o en los ganglios linfáticos adyacentes.
La nueva aprobación, anunciada el 3 de mayo, se basa en los resultados de un estudio clínico a gran escala llamado KATHERINE, que comparó al fármaco T-DM1 con trastuzumab (Herceptin) como tratamiento adyuvante. En el estudio, las mujeres tratadas con T-DM1 presentaron una reducción del 50 % del riesgo de que el cáncer retornara o de morir que las mujeres tratadas con trastuzumab.
Los efectos secundarios, entre los que se incluyen efectos secundarios graves, fueron más frecuentes en mujeres tratadas con T-DM1. Como consecuencia, el número de mujeres que no completaron todo el ciclo de tratamiento adyuvante entre las que recibieron T-DM1 (29 %), fue mayor que entre las que recibieron trastuzumab (19 %).
Pero muchas de estas mujeres no necesitaron interrumpir la toma del fármaco hasta que estuvieron cerca del final del periodo de tratamiento adyuvante, explicó el investigador principal del estudio, doctor Charles Geyer, Jr., del Centro Oncológico Massey de la Universidad de Virginia Commonwealth. El doctor Geyer dijo que, en general "la mayoría de las mujeres toleraron el fármaco bastante bien".
Los resultados del estudio, y la subsecuente aprobación de la FDA, ya han tenido un efecto importante en la atención de las pacientes, agregó el doctor.
"T-DM1 ahora se ha convertido en el tratamiento convencional después de la terapia neoadyuvante para mujeres con cáncer de seno con HER2 y con cáncer residual invasor, puntualizó el doctor.
Profundizar en avances anteriores
Trastuzumab, que es un anticuerpo monoclonal, fue de las primeras terapias dirigidas aprobadas por la FDA para combatir el cáncer, y se ha establecido desde hace mucho como terapia para el cáncer de seno con HER2. Trastuzumab se adhiere a las proteínas HER2 en la superficie de las células del cáncer de seno y previene que esta proteína estimule el crecimiento de células cancerosas.
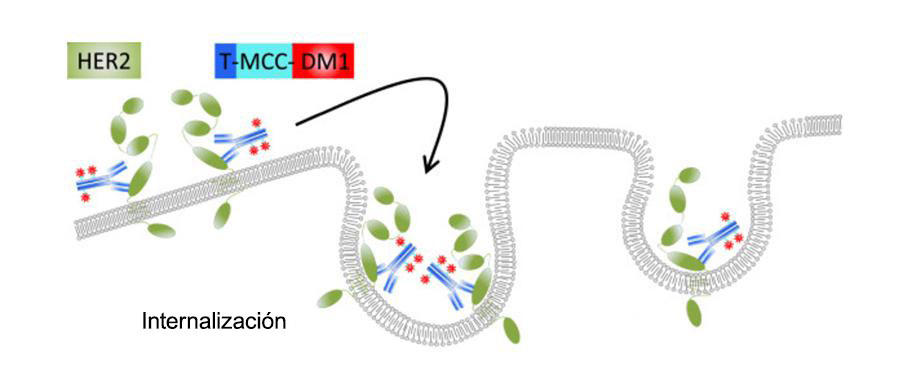
Conocido como conjugado de anticuerpo y de fármaco, T-DM1 vincula, a nivel químico, al anticuerpo trastuzumab con el fármaco quimioterapéutico emtansina (llamado también DM1).
La porción de anticuerpo de T-DM1, además de bloquear la actividad de la proteína HER2 en las células cancerosas, funciona como un mecanismo de asentamiento para emtansina. Cuando el anticuerpo se fija a HER2 en las células cancerosas, se libera emtansina dentro de las células.
Una vez demostrado que T-DM1 mejoró la supervivencia de mujeres con cáncer metastático de seno con HER2, los investigadores prosiguieron rápidamente a probar el fármaco en mujeres con el cáncer en estadio inicial. El estudio KATHERINE (financiado por el fabricante de T-DM1, Genentech) inscribió a aproximadamente 1500 mujeres con cáncer de seno con HER2 en estadio inicial, es decir, con cáncer confinado al seno y a los ganglios linfáticos axilares. Todas las mujeres en el estudio presentaron evidencia de enfermedad residual después de la terapia neoadyuvante, que consistió en la combinación de quimioterapia y trastuzumab. Casi el 20 % de las mujeres recibieron también pertuzumab (Perjeta) como parte de la terapia neoadyuvante.
El objetivo de la terapia neoadyuvante es eliminar la mayor cantidad posible de cáncer antes de la cirugía, por esa razón, muchas mujeres con cáncer de seno con HER2 en estadio inicial reciben terapia neoadyuvante, explicó la doctora Janice Lyons, quien es oncóloga radióloga del Centro Oncológico Integral Case en Cleveland y se especializa en el tratamiento de cáncer de seno. Algunas mujeres con cánceres muy pequeños, sin embargo, pueden someterse directamente a la cirugía, dijo la doctora.
En muchas mujeres, la quimioterapia neoadyuvante logrará eliminar todo rastro de la enfermedad residual, comentó el doctor Geyer. Los estudios han indicado de manera sistemática que las mujeres con cáncer de seno en estadio inicial (en particular quienes padecen cáncer triple negativo o con HER2) que no presentan enfermedad residual después de recibir quimioterapia neoadyuvante, sobreviven más tiempo sin que vuelva el cáncer, en comparación con mujeres que padecen cáncer residual invasor.
La terapia adyuvante con trastuzumab ha sido un tratamiento convencional para mujeres con cáncer de seno con HER2, independientemente de si tienen o no enfermedad residual.
Las participantes en el estudio KATHERINE fueron asignadas al azar para recibir terapia adyuvante con T-DM1 o con trastuzumab (en ciclos de tratamiento de tres semanas por un máximo de 14 ciclos).
Los investigadores que dirigieron el estudio estimaron que, a los 3 años de haber comenzado el tratamiento adyuvante, 88 % de las mujeres tratadas con T-DM1 estaban vivas y no tenían cáncer invasor, en comparación con 77 % de las mujeres tratadas con trastuzumab.
Se deberá hacer un seguimiento más prolongado para determinar si T-DM1 puede en última instancia mejorar la supervivencia general de las pacientes, enfatizó el doctor Geyer.
"Estos resultados son impactantes y tienen relevancia clínica", escribió el doctor Daniel F. Hayes, un experto en cáncer de seno del Centro Oncológico Rogel de la Universidad de Michigan, en un editorial que acompañó la publicación de los resultados del estudio KATHERINE en el pasado mes de diciembre en el New England Journal of Medicine. "El tratamiento posoperatorio con T-DM1 ofrece una oportunidad importante de mejorar resultados a largo plazo".
La doctora Lyons estuvo de acuerdo con que el tratamiento adyuvante con T-DM1 es el nuevo tratamiento convencional para mujeres con cáncer de seno con HER2 en estadio inicial que presentan cáncer residual invasor después de recibir quimioterapia neoadyuvante. La doctora comentó que el "resultado sorprendente" del estudio KATHERINE, es que todas las mujeres se benefician del fármaco T-DM1, "incluso quienes presentan cáncer residual escaso".
¿Cuál es el impacto de los efectos secundarios del tratamiento?
El doctor Hayes continuó diciendo que estas mejoras no se logran "sin pagar un precio", y destacó el aumento en los índices de efectos secundarios, algunos de ellos graves. Estos últimos incluyeron disminución considerable de la concentración de plaquetas y neuropatía periférica.
En general, 18 % de las mujeres en el grupo que recibió T-DM1 dejó de tomar el fármaco debido a efectos secundarios específicos, en comparación con 2 % de las mujeres en el grupo que recibió trastuzumab.
Es probable que el aumento de los efectos secundarios en las mujeres tratadas con T-DM1, puntualizó el doctor Geyer, haya sido un efecto acumulativo de los tratamientos previos y posteriores a la cirugía. "Emtansina es un fármaco quimioterapéutico y, como tal, se esperaba que produjera toxicidad en un nivel relativo comparado con tratamientos no quimioterapéuticos", agregó el doctor.
En algunos casos, la disminución de la dosis del fármaco alivió los efectos secundarios. Entre las participantes del estudio que en última instancia dejaron de tomar T-DM1, algunas cambiaron a trastuzumab por el resto de los 14 ciclos, como parte del plan del estudio.
La doctora Lyons señaló también que, en el estudio KATHERINE, hubo un riesgo levemente mayor de inflamación pulmonar (neumonitis) en mujeres que recibieron T-DM1, si bien los índices fueron en general bajos. Es probable que este efecto secundario esté vinculado a la radioterapia que recibieron las pacientes. La doctora recomendó a sus colegas "controlar con sumo cuidado" las dosis de todas las pacientes que reciben radioterapia como parte del tratamiento adyuvante con T-DM1.
El doctor Hayes no recomienda usar T-DM1 en mujeres sin enfermedad residual después de recibir terapia neoadyuvante ni en mujeres con cáncer en estadio I en el momento del diagnóstico; ya que estas pacientes "tienen un desenlace muy favorable" con la terapia convencional adyuvante de paclitaxel y trastuzumab, dijo el doctor.