La importancia de la investigación en el avance contra el cáncer infantil
En los Estados Unidos, el cáncer es la causa principal de muerte por enfermedad en los niños. Aunque en los últimos 50 años hubo avances considerables en el tratamiento de varios tipos de cáncer infantil, el avance fue limitado para algunos tipos de cáncer infantil. A veces, incluso cuando se logra la supervivencia a largo plazo, muchos sobrevivientes de cáncer infantil tienen efectos adversos por la enfermedad o el tratamiento.
Es evidente que hace falta más investigación para crear nuevos tratamientos que sean más eficaces y más seguros para el cáncer infantil. Además, se deben establecer una infraestructura y prácticas que permitan a los investigadores aprender de cada niño con cáncer.
El Instituto Nacional del Cáncer (NCI) tiene varios programas que se concentran en el cáncer infantil. Y muchos programas de investigación del NCI son aplicables a los niños aunque no sean diseñados para el estudio del cáncer infantil. El NCI financia investigación biomédica aplicable a esta población, que es amplia e incluye las siguientes áreas:
- Investigación básica para mejorar la comprensión sobre los mecanismos fundamentales del cáncer
- Investigación clínica para probar la seguridad y la eficacia de los tratamientos nuevos
- Investigación sobre la supervivencia para disminuir los efectos secundarios a largo plazo por el cáncer y el tratamiento
Desafíos en la investigación sobre el cáncer infantil
Un reto en la investigación sobre el cáncer infantil es que los cánceres en los niños y los adolescentes son bastante poco frecuentes. Los cánceres infantiles representan menos del 1 % de todos los casos nuevos que se diagnostican en los Estados Unidos cada año. Debido a que el número de niños con cáncer es pequeño y los pacientes reciben tratamiento en muchas instituciones distintas, es necesario colaborar para responder a preguntas biológicas complejas.
Cada vez más, la participación en los estudios clínicos se limita a pacientes que se definen por las características moleculares del tumor, en vez del lugar del cuerpo donde empezó el tumor. Para asegurar que se inscriban suficientes participantes y se obtengan resultados significativos, es esencial que los centros oncológicos infantiles colaboren y que el programa de investigación clínica nacional sea sólido.
Por otra parte, para acelerar el avance contra el cáncer infantil, es necesario crear formas más eficientes de seleccionar y compartir los conocimientos de investigación, desde datos genómicos a los desenlaces clínicos.
Hay otro desafío. Se cree que la mayoría de los cánceres en los niños (y en los adultos) surgen por cambios genéticos que llevan a la multiplicación celular descontrolada y luego al cáncer, pero no se conocen las causas de la mayoría de estos cambios genéticos en los niños. Un porcentaje bajo de cánceres infantiles se relaciona con los cambios genéticos heredados o la exposición a la radiación diagnóstica o terapéutica. Para la mayoría de los cánceres infantiles, no se han identificado causas ambientales. Por lo tanto, no es sencillo identificar formas de prevenir el cáncer infantil.
Además, los tipos de cáncer que presentan los niños y la biología de esos cánceres suelen ser distintos de los cánceres que se diagnostican en los adultos. Por ejemplo, los tumores que se inician en los órganos y tejidos (como los retinoblastomas en los ojos y los osteosarcomas en los huesos) son más comunes en los niños.
Es más, la mayoría de los cánceres infantiles presentan relativamente pocas alteraciones genéticas, así que es común que no haya cambios genéticos adonde apuntar el tratamiento, como los que se crearon y aprobaron para los cánceres que tienen los adultos. Es difícil usar en los niños aquellos medicamentos dirigidos a las vías de señalización activas presentes en algunos cánceres en los adultos. Esto es debido a que muchas de estas vías de señalización son esenciales para el desarrollo normal de los niños.
De hecho, los cambios genéticos que inician el cáncer en los niños suelen ser distintos de los cánceres en los adultos. Por ejemplo, la translocación de cromosomas, que fusiona partes de distintos genes y forman lo que se llama una oncoproteína de fusión, es común en el cáncer infantil. Aunque las oncoproteínas de fusión también aparecen en algunos cánceres en los adultos, las que se presentan en los niños son bastante difíciles de tratar. Otro factor que contribuye a que haya muy pocas terapias dirigidas para los cánceres infantiles es que, al ser enfermedades tan raras, hay pocos medicamentos en desarrollo comercial.
Crear tratamientos nuevos que sean menos dañinos y causen menos efectos adversos (agudos y tardíos) que los tratamientos en uso y diseñar intervenciones para atenuar los efectos adversos de los tratamientos actuales y futuros también son desafíos en la investigación del cáncer infantil. Los efectos tardíos de algunas terapias para el cáncer infantil tienen profundas repercusiones físicas, emocionales y de otro tipo para los sobrevivientes, que incluyen una esperanza de vida más corta. Encontrar formas de minimizar y responder a estos efectos tardíos para mejorar la supervivencia y la calidad de vida de los niños es una prioridad en la investigación.
También hace falta tener más información sobre la metabolización (cambios químicos) de los medicamentos oncológicos, que varía según la edad de desarrollo del niño, al igual que mejores modelos en el laboratorio y en animales para detectar el cáncer y probar medicamentos para el posible uso en los niños y adolescentes. Es necesario definir el uso óptimo de la radioterapia al tratar los cánceres infantiles para mantener o aumentar la eficacia al mismo tiempo que se disminuyen los efectos secundarios a largo plazo.
La investigación básica impulsa el avance contra el cáncer infantil
Casi todos los adelantos contra el cáncer en los niños y los adultos se originan en la investigación básica, en general, en áreas no relacionadas con la enfermedad.
Un ejemplo es el CRISPR-Cas9 que se usa para la edición genética, que ha revolucionado el estudio de los genes que controlan la multiplicación de las células cancerosas y la supervivencia al cáncer tanto en niños como adultos. El descubrimiento surgió de la investigación básica de microbiología para estudiar cómo las bacterias resistían las infecciones por virus.
Otro ejemplo con origen en la investigación básica es el estudio de proteínas llamadas histonas. Las histonas son proteínas que se unen al ADN, apoyan la estructura de los cromosomas y controlan la actividad de los genes. Los científicos investigaron durante muchos años la forma en que las histonas se modifican en del núcleo celular y la función de estos cambios en controlar cuándo y hasta qué punto se expresan los genes.
Los hallazgos de la investigación fueron de importancia inmediata para el glioma pontino intrínseco difuso (GPID), un tumor de encéfalo en los niños. Esto fue porque se descubrió que la mayoría de los tumores del GPID tienen una mutación en H3.3 (un cambio en el gen de una proteína llamada histona) que evita una modificación específica de la proteína. Se cree que esta mutación en H3.3 es oncoiniciadora (que inicia el cáncer) del GPID y se relaciona con la enfermedad de crecimiento rápido y una supervivencia menor.
Áreas prometedoras en la investigación sobre el cáncer infantil
Aunque en la última década aumentó muchísimo lo que entendemos sobre la biología del cáncer en los niños, todavía nos faltan conocimientos importantes. El NCI identificó varias áreas en las que hace falta más investigación, además de oportunidades para usar nuevas técnicas a fin de aprender más sobre los cánceres infantiles.
Inmunoterapias para el cáncer infantil
La inmunoterapia es un tratamiento en el que se restaura o mejora el sistema inmunitario para combatir el cáncer. La investigación sobre inmunoterapias produjo varios métodos nuevos para tratar el cáncer.
Un ejemplo es la terapia de células T con receptor de antígeno quimérico (CAR), que ahora se usa para tratar a algunos niños con leucemia linfoblástica aguda. Esta técnica terapéutica surgió de décadas de investigación sobre el funcionamiento del sistema inmunitario y la forma de manipularlo para obtener beneficios clínicos.
La División de Oncología Pediátrica (POB) del Centro de Investigación Oncológica del NCI lleva a cabo estudios clínicos de inmunoterapia en los que participan pacientes que son niños o adultos jóvenes, y el Grupo de Oncología Infantil (COG) y el Consorcio de Tumores de Encéfalo Infantiles (PBTC) evalúan tratamientos de inmunoterapia para algunos tipos de cáncer infantil. La Red de Estudios Clínicos de Inmunoterapias Oncológicas (CITN) tiene un componente que establece estudios clínicos de inmunoterapias para niños con cáncer.
Como parte de la Misión contra el Cáncer (Cancer Moonshot), el NCI estableció el Consorcio de Fusión de Oncoproteínas para Cánceres Infantiles (FusOnC2) y la Red de Descubrimiento y Desarrollo de Inmunoterapias Infantiles (PI-DDN).
Para obtener más información sobre la POB, el COG y los otros programas que se mencionan aquí, consulte Programas del Instituto Nacional del Cáncer importantes para el cáncer infantil.
Terapias moleculares dirigidas para tratar el cáncer infantil
Las terapias moleculares dirigidas son tratamientos con medicamentos u otras sustancias que destruyen células cancerosas al apuntar a moléculas específicas que las células cancerosas necesitan para formarse y diseminarse. Para estas terapias se usan inhibidores micromoleculares, anticuerpos monoclonales o conjugados anticuerpo-fármaco.
La POB lleva a cabo estudios clínicos de terapias dirigidas en los que participan pacientes que son niños o adultos jóvenes, y el COG y el PBTC evalúan terapias dirigidas para algunos tipos de cáncer infantil.
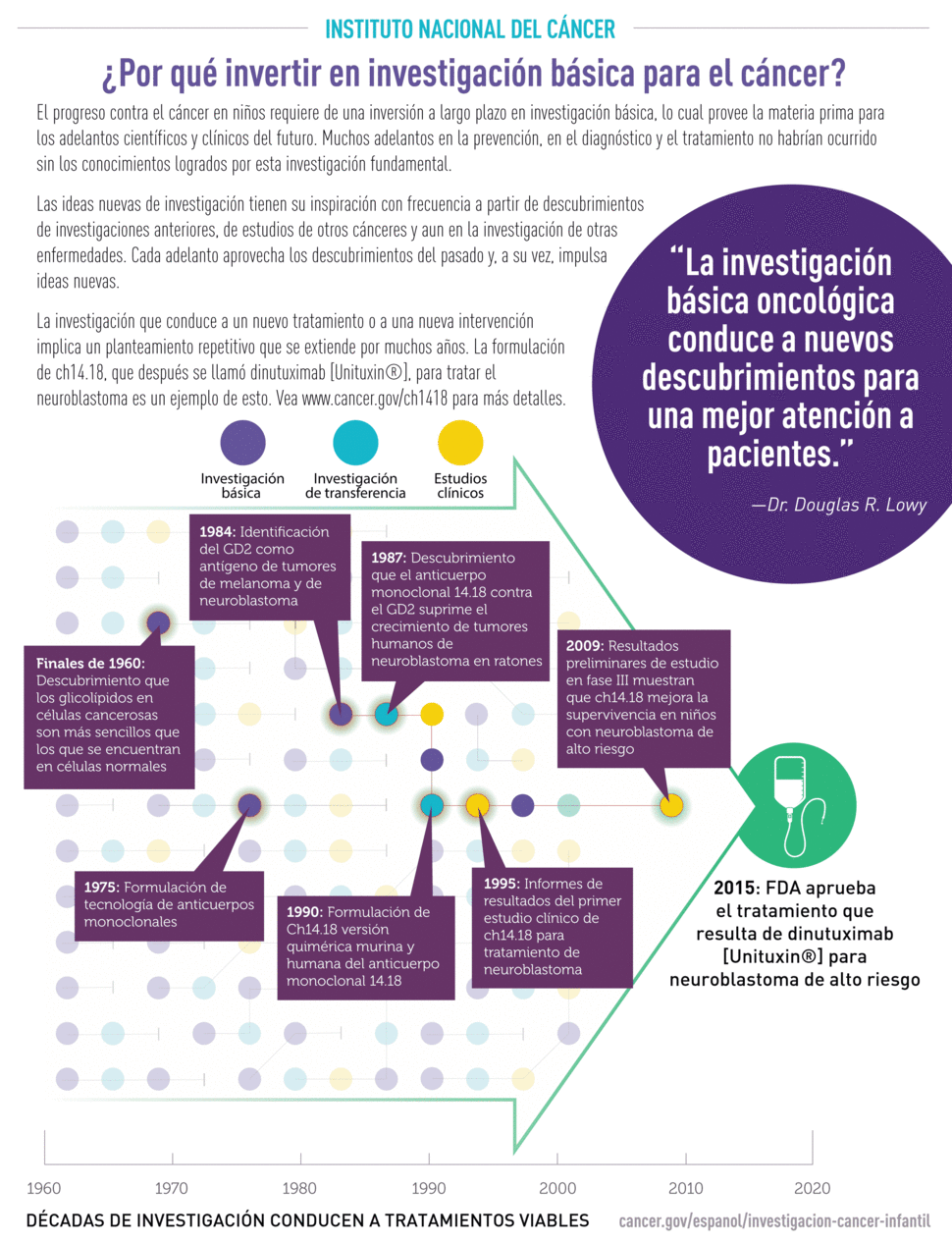
Por ejemplo, los resultados de un estudio clínico del COG patrocinado por el NCI y a cargo de la doctora y licenciada en Medicina Alice Yu, de la Universidad de California en San Diego, condujo a la aprobación del anticuerpo monoclonal dinutuximab (Unituxin) para tratar el neuroblastoma de riesgo alto.
Además, el PBTC estudió la terapia dirigida con selumetinib para tratar a niños con glioma de grado bajo recidivante o resistente al tratamiento. En la mayoría de los pacientes se observó un achicamiento del tamaño del tumor. A partir de estos resultados, los investigadores del COG evalúan el uso del selumetinib en estudios clínicos de fase 3 para niños con glioma de grado bajo de diagnóstico reciente.
En 2017, el NCI y el COG iniciaron el Análisis Molecular para Opciones de Terapia Infantil (Pediatric MATCH), un estudio clínico que evalúa el uso de terapias moleculares dirigidas en niños con tumores sólidos avanzados que no responden al tratamiento. Mediante la secuenciación del ADN tumoral, ahora se identifican a los niños cuyos cánceres presentan una anomalía genética para la que hay un medicamento dirigido que se evalúa en el estudio.
Programas del Instituto Nacional del Cáncer importantes para el cáncer infantil
El NCI reconoce que los niños no son solo adultos pequeños y que se necesitan tratamientos adaptados para los cánceres infantiles. El NCI participa junto con investigadores, profesionales clínicos, autoridades responsables, defensores de pacientes, y otros colaboradores para avanzar en esta área de investigación clave. El NCI respalda una gama de programas que se centran en avanzar la atención para el cáncer infantil y renovó numerosas financiaciones para estas iniciativas y programas. Algunos de estos programas son:
- La División de Oncología Pediátrica (POB) en el Centro de Investigación Oncológica del NCI lleva a cabo investigación básica, aplicable y clínica de alto riesgo y gran repercusión sobre el cáncer infantil. Por ejemplo, los investigadores de la POB estuvieron a cargo de un equipo de investigadores internacionales que analizaron datos de muchos pacientes con rabdomiosarcoma, un cáncer infantil raro que afecta los músculos y otros tejidos blandos, y hallaron mutaciones en varios genes asociados con el crecimiento más rápido de la enfermedad. Estas pistas genéticas del estudio podrían llevar al uso más amplio de las pruebas genéticas a fin de pronosticar si los niños con cáncer responderán a la terapia, además de crear terapias dirigidas para la enfermedad.
- La División de Epidemiología y Genética del Cáncer (DCEG) lleva a cabo estudios clínicos, genéticos, epidemiológicos y de patología molecular sobre niños con riesgo alto de tener cáncer. Por ejemplo, los investigadores de la DCEG dirigen un estudio de asociación de todo el genoma del sarcoma de Ewing para entender mejor la estructura genética de la enfermedad e identificar las regiones del genoma que causan un aumento del riesgo. Los investigadores de la DCEG también estudian el osteosarcoma para entender mejor la función que tiene la variación genética en el riesgo y el desenlace de los pacientes, además de identificar los genes o las regiones genómicas que son importantes en el osteosarcoma. En la DCEG también se estudian los síndromes de cáncer familiares, como el síndrome de Li-Fraumeni, el síndrome DICER1, la neurofibromatosis de tipo 1 (NF1), y los síndromes heredados de insuficiencia de la médula ósea (IBMFS), a fin de entender mejor estos trastornos e investigar los vínculos posibles entre el genotipo y el fenotipo que mejorarán el tratamiento clínico y ayudarán en la orientación genética.
- El programa Investigación Aplicable a Terapias para Generar Tratamientos Eficaces (TARGET) usa métodos genómicos para catalogar los cambios moleculares de varios tipos de cáncer infantil con el propósito de entender mejor los procesos causantes de la enfermedad, mejorar el diagnóstico y la clasificación, e identificar nuevas dianas moleculares (moléculas a las que se dirigen las terapias) para mejorar el tratamiento. Por ejemplo, los investigadores del TARGET hicieron un estudio sobre las alteraciones somáticas de varios tipos de cáncer en casi 1700 leucemias y tumores sólidos en niños y hallaron grandes diferencias genómicas al comprarlas con los cánceres en adultos. La Iniciativa de Caracterización del Genoma del Cáncer (CGCI) incluye estudios genómicos de varios cánceres infantiles que no suelen responder bien a los tratamientos.
- El Grupo de Oncología Infantil (COG), integrante de la Red Nacional de Estudios Clínicos (NCTN), establece y coordina estudios clínicos de cáncer infantil disponibles en más de 200 instituciones participantes, que incluyen centros oncológicos en los Estados Unidos y Canadá. Además de dirigir estudios clínicos de fases finales convencionales, el COG estableció la Red de Estudios Clínicos Pediátricos de Fases Iniciales (PEP-CTN) para realizar estudios de fase inicial y estudios pilotos a fin de que los medicamentos anticancerosos se usen en el tratamiento de cánceres infantiles con rapidez y eficacia. Los estudios clínicos que dirige el COG llevaron a tratamientos que son más eficaces y menos tóxicos, que evitan que los niños tengan efectos secundarios a corto y largo plazo.
- El Análisis Molecular para Opciones de Terapia Infantil (Pediatric MATCH) es un estudio nacional de medicina personalizada de precisión para investigar si las terapias dirigidas son eficaces para tratar a niños y adolescentes cuyos tumores sólidos con ciertas mutaciones genéticas progresaron durante el tratamiento estándar o después de este. El estudio que realiza el COG comenzó a inscribir pacientes en 2017 y recibe financiamiento del NCI. Todos los pacientes que participan reciben pruebas de línea germinal para evaluar si las anomalías genéticas identificadas en los tumores son hereditarias. Los datos genómicos obtenidos en el estudio serán muy valiosos para los investigadores que buscan entender los fundamentos genéticos del cáncer en la niñez.
- El Consorcio de Tumores de Encéfalo Pediátricos (PBTC) es una organización de investigación cooperativa multidisciplinaria dedicada a identificar las mejores estrategias de tratamiento para los niños con tumores de encéfalo primarios.
- El NCI participa en el Programa de Investigación Infantil Gabriella Miller Kids First, que recopila información para crear un recurso con muchos datos (patrocinado por los Institutos Nacionales de la Salud) con el propósito de aumentar los conocimientos sobre los cambios genéticos asociados con los cánceres infantiles y los defectos de nacimiento estructurales. Mediante el programa, las distintas comunidades de investigadores comparten datos y colaboran, además de promover nuevas formas de pensar sobre las enfermedades de la infancia.
- El NCI financia varios proyectos de investigación para niños, adolescentes y adultos jóvenes con cáncer, según se determinó en la Ley sobre la Supervivencia, Tratamiento, Acceso e Investigación Relacionada con el Cáncer Infantil (STAR). Esta ley faculta al NCI para mejorar la recolección de muestras biológicas, los bancos biológicos y otros recursos relacionados con el cáncer en niños, adolescentes y adultos jóvenes. La ley se enfoca en los tipos de cáncer, los subtipos y las recaídas cuyos tratamientos actuales son menos eficaces.
- El NCI dirige la Iniciativa de Datos sobre el Cáncer Infantil (CCDI) para recopilar, analizar y compartir datos a fin de aliviar la carga del cáncer en los niños, adolescentes y adultos jóvenes. La CCDI complementa y intensifica las actividades que se corresponden con la Ley STAR sobre Cáncer Infantil. Una de las iniciativas del CCDI, llamada Protocolo de Caracterización Molecular, facilitará la recolección y el análisis molecular del tejido tumoral de los niños con cáncer. Tendrán prioridad los cánceres para los que falten tejidos o no sean adecuados para la investigación, y los cánceres cuyos tratamientos existentes sean limitados o ineficaces. Los datos que se generen se almacenarán y estarán a disposición de la comunidad de investigadores y oncólogos mediante herramientas como los Datos Comunes Genómicos. Esto ayudará a inscribir a los niños en estudios clínicos de medicina personalizada de precisión y a orientar los tratamientos. La CCDI también inauguró el Registro Nacional del Cáncer Infantil (NCCR). Mediante este registro se recopilan y vinculan los datos sobre diagnóstico, desenlaces, tratamientos y efectos secundarios a largo plazo para casi todos los niños con cáncer en los Estados Unidos. El NCCR se basa en los registros de cáncer existentes que el NCI y los Centros para el Control y la Prevención de Enfermedades (CDC) financian y, además, los complementa.
- En el Estudio de Sobrevivientes de Cáncer Infantil (CCSS) se examinan los efectos adversos a largo plazo por el cáncer y por el tratamiento del cáncer en alrededor de 35 000 sobrevivientes de cáncer infantil que se diagnosticaron entre 1970 y 1999. El estudio se creó para obtener conocimientos nuevos sobre los efectos a largo plazo por el cáncer y por el tratamiento, además de educar a los sobrevivientes y a la comunidad médica sobre las repercusiones del diagnóstico y el tratamiento del cáncer. Los resultados obtenidos del CCSS se usarán en el diseño de protocolos e intervenciones de tratamiento que mejorarán la supervivencia y reducir al mínimo los daños de los efectos tardíos. Esta investigación también se usa para crear y ampliar programas para la detección y prevención de los efectos tardíos en los niños y adolescentes sobrevivientes de cáncer. Por ejemplo, para entender mejor el riesgo genético de segundos cánceres, los investigadores de la DCEG y el CCSS colaboran en estudios cuyo fin es identificar variantes genéticas comunes y raras que podrían asociarse con segundos cánceres u otros efectos adversos para sobrevivientes de cáncer infantil. En un estudio relacionado, los científicos de la DCEG también examinan la salud a largo plazo de los sobrevivientes de retinoblastoma, mediante el seguimiento de una cohorte de personas con enfermedades hereditarias o no hereditarias para entender la forma en que los tratamientos de retinoblastoma influyen en el riesgo de segundos cánceres y la mortalidad a largo plazo.
- El Consorcio de Nuevos Enfoques para la Terapia del Neuroblastoma (NANT) consta de un equipo multidisciplinario de científicos de laboratorio y clínicos que se concentran en mejorar los desenlaces para los pacientes con riesgo alto de neuroblastoma. El equipo se dedica a identificar los mecanismos que resisten la terapia, descubrir puntos débiles en los que genera resistencia y trasladar estos conocimientos a los estudios clínicos. El NANT trabaja de cerca con el COG para trasladar los hallazgos sobre terapias experimentales a los estudios clínicos de fase 3 del COG. Los hallazgos del NANT sobre el microambiente tumoral, la respuesta tumoral a la terapia y la aplicación de las terapias celulares a los tumores sólidos tienen aplicaciones que no se limitan al tratamiento del neuroblastoma.
- La Ley de Investigación para Acelerar las Curas y la Equidad (RACE) para los Niños, exige que todos los medicamentos de cáncer nuevos para adultos también se evalúen en los niños cuando las dianas moleculares son importantes para el cáncer infantil. El NCI inauguró el programa de Pruebas Preclínicas Infantiles in Vivo (PIVOT) para la evaluación sistemática de medicamentos nuevos en perfiles genómicos de cáncer infantil. La meta principal del programa de PIVOT es producir datos preclínicos de calidad alta para ayudar a los investigadores de cáncer infantil a identificar los medicamentos con mayor probabilidad de tener actividad significativa contra el cáncer cuando se prueban en la clínica para tratar determinados tipos de cáncer infantil. El NCI también colaborará con la Administración de Alimentos y Medicamentos (FDA), las instituciones académicas y las compañías farmacéuticas mediante la Alianza Pública-Privada de Pruebas Preclínicas Infantiles (PPTP3). La Fundación para los Institutos Nacionales de la Salud (FNIH) establecerá la PPTP3 para que las pruebas preclínicas infantiles de los medicamentos se lleven a cabo con rapidez y mayor alcance.
- El Inventario de Datos Genómicos Infantiles (PGDI) es un recurso de acceso libre que pone a disposición de los investigadores los datos de proyectos de secuenciación genómica de cánceres infantiles. En el inventario se incluyen listas de proyectos de secuenciación finalizados y en curso en los Estados Unidos y otros países. Para cada proyecto, se describe el tipo de cáncer estudiado, los datos de caracterización molecular disponibles y las personas contacto.
- Los Programas Especializados de Excelencia en Investigación (SPOREs) sobre la Hiperactividad del RAS se centran en idear mejores tratamientos para la neurofibromatosis de tipo 1 y cánceres relacionados en niños, adolescentes y adultos jóvenes.
- El Consorcio de Fusión de Oncoproteínas para Cánceres Infantiles (FusOnC2) es una red de colaboración multidisciplinaria de investigadores que estudian algunas oncoproteínas de fusión asociadas con cánceres infantiles cuyo riesgo de fracaso de tratamiento es alto y para los que se hubo poco avance para identificar medicamentos dirigidos.
- La Red de Descubrimiento y Desarrollo de Inmunoterapias Infantiles (PI-DDN) es una red de colaboración para promover e identificar oportunidades de investigación para la aplicación clínica de posibles inmunoterapias para niños y adolescentes con cáncer. Las metas principales de la PI-DDN son el descubrimiento y la identificación de dianas de inmunoterapia para los cánceres en niños y adolescentes, la creación de nuevos métodos de inmunoterapia y un mayor entendimiento del microambiente tumoral inmunodepresor que produzcan regímenes de tratamientos inmunitarios nuevos y más eficaces para los cánceres infantiles de riesgo alto.
- La Red del Atlas de Tumores Humanos (HTAN) es una red de colaboración que contruye varios atlas tumorales multidimensionales para documentar las alteraciones moleculares y celulares, y las interacciones dentro de los tumores, que registran la aparición y la evolución de los tumores. Los atlas representan una población diversa de pacientes, que incluyen a niños, y describen la dinámica del cáncer, concentrándose en la transición de los cambios precancerosos al cáncer, de la invasión local a la metástasis a distancia, y en las formas en que los tumores responden al tratamiento y se vuelven resistentes a los medicamentos.
- En la Red de Estudios sobre Inmunoterapias para el Cáncer Infantil (CITN Infantil), se usa la infraestructura de la CITN para realizar estudios clínicos de inmunoterapias que son de importancia particular para los niños y adolescentes con cáncer. Algunos ejemplos de tratamientos nuevos que investigará la CITN Infantil son las terapias celulares (como las células T con CAR dirigidas a antígenos en cánceres infantiles) y las terapias de anticuerpos, que incluyen los conjugados anticuerpo-fármaco, dirigidos a los antígenos en la superficie que se suelen expresar con más frecuencia en los cánceres infantiles.
- La Red de Tumores Raros en Niños y Adultos (MyPART) reúne a científicos, pacientes, familiares, defensores y profesionales de atención de la salud que trabajan juntos para encontrar tratamientos nuevos para tumores raros que no tienen cura en los niños, adolescentes y adultos jóvenes. Mediante la labor en equipo, los investigadores comparten datos y ayudan a diseñar experimentos y estudios clínicos, los defensores tratan temas que son importantes para los pacientes, y los médicos cuentan su experiencia en el tratamiento de cánceres raros. MyPART es un componente de la Red del NCI para la Participación de Pacientes con Tumores Raros.
- Los investigadores de la DCEG colaboran con el Consorcio Internacional de Cohortes de Cáncer Infantil (I4C) y el Consorcio Internacional de Leucemia Infantil (CLIC), para recopilar datos de estudios de cohorte de todo el mundo para responder a preguntas sobre los cánceres infantiles. El I4C reúne a equipos multidisciplinarios de epidemiólogos, especialistas en ciencias básicas y profesionales clínicos, para colaborar en investigaciones sobre el papel que tienen las exposiciones en etapas tempranas de la vida en el riesgo del cáncer. Las actividades del CLIC incluyen más de 30 estudios de casos y controles, además de la identificación de asociaciones entre la leucemia infantil y factores de riesgo ambientales.